1 . 阅读下列材料,按要求回答问题。
材料1 酒精、苯、CCl4都是有机溶剂,有机溶剂之间大多能互溶;
材料2 碘(I2)易溶于有机溶剂;
材料3 溴微溶于水,易溶于有机溶剂,其溶液呈橙红色。
在酒精、苯、CCl4、蒸馏水四种试剂中:
(1)能把碘单质从碘水中萃取出来的是___________ ,进行分液之后___________ (填“能”或“不能”)得到纯净的碘单质。
(2)能把溴从溴水中萃取出来,并在分液时使含溴液体从分液漏斗下口流出的是___________ 。
(3)CCl4___________ (填“能”或“不能”)把碘酒中的碘萃取出来,原因是___________ 。
材料1 酒精、苯、CCl4都是有机溶剂,有机溶剂之间大多能互溶;
材料2 碘(I2)易溶于有机溶剂;
材料3 溴微溶于水,易溶于有机溶剂,其溶液呈橙红色。
在酒精、苯、CCl4、蒸馏水四种试剂中:
(1)能把碘单质从碘水中萃取出来的是
(2)能把溴从溴水中萃取出来,并在分液时使含溴液体从分液漏斗下口流出的是
(3)CCl4
您最近一年使用:0次
名校
解题方法
2 . 分子式为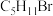 的烃,分子中含有3个甲基的同分异构体共有(不考虑立体异构)
的烃,分子中含有3个甲基的同分异构体共有(不考虑立体异构)
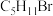 的烃,分子中含有3个甲基的同分异构体共有(不考虑立体异构)
的烃,分子中含有3个甲基的同分异构体共有(不考虑立体异构)| A.3种 | B.2种 | C.5种 | D.4种 |
您最近一年使用:0次
2024-05-08更新
|
104次组卷
|
8卷引用:江苏无锡市第三高级中学2023-2024学年高二上学期期中考试化学试卷
3 . 高锰酸钾溶液常用于物质的定性检验与定量分析。
(1)实验室用 固体来配制
固体来配制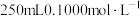 的
的 酸性溶液。
酸性溶液。
①需用的仪器有天平、药匙、烧杯、玻璃棒、量筒、胶头滴管、___________ 。
②计算所需 固体的质量为
固体的质量为___________ 克。
③下列关“容量瓶及其使用”的叙述中正确的是___________ (填序号)。
a.使用前必须检查是否漏水 b.能配制一定体积准确浓度的标准溶液
c.可用来长期贮存溶液 d.能用作溶解固体、稀释浓溶液的容器
④下列操作会导致溶液浓度偏高的是___________ (填序号)。
a.加水定容时俯视刻度线
b.未洗涤溶解后的烧杯和玻璃棒
c.颠倒摇匀后发现凹液面低于刻度线,没有加水补到刻度线
d. 溶解时放热,没有将溶液冷却即加水至刻度线
溶解时放热,没有将溶液冷却即加水至刻度线
(2)用 酸化的上述新配制的
酸化的上述新配制的 溶液10mL氧化并测定
溶液10mL氧化并测定 溶液中
溶液中 的物质的量浓度,消耗0.05mol/L的
的物质的量浓度,消耗0.05mol/L的 溶液100mL,则反应后锰元素的价态为
溶液100mL,则反应后锰元素的价态为___________ 。
(3)某同学利用 氧化
氧化 制备
制备 的装置如下图所示(夹持装置略):
的装置如下图所示(夹持装置略): )在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:
)在浓强碱溶液中可稳定存在,碱性减弱时易发生反应: ;
;
①装置A中a的作用是___________ ,装置A中制备 的化学方程式为
的化学方程式为___________ 。
②上述装置存在一处缺陷,会导致 产率降低,改进的方法是
产率降低,改进的方法是___________ 。
③装置C中发生反应的离子方程式为___________ 。
(1)实验室用
 固体来配制
固体来配制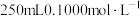 的
的 酸性溶液。
酸性溶液。①需用的仪器有天平、药匙、烧杯、玻璃棒、量筒、胶头滴管、
②计算所需
 固体的质量为
固体的质量为③下列关“容量瓶及其使用”的叙述中正确的是
a.使用前必须检查是否漏水 b.能配制一定体积准确浓度的标准溶液
c.可用来长期贮存溶液 d.能用作溶解固体、稀释浓溶液的容器
④下列操作会导致溶液浓度偏高的是
a.加水定容时俯视刻度线
b.未洗涤溶解后的烧杯和玻璃棒
c.颠倒摇匀后发现凹液面低于刻度线,没有加水补到刻度线
d.
 溶解时放热,没有将溶液冷却即加水至刻度线
溶解时放热,没有将溶液冷却即加水至刻度线(2)用
 酸化的上述新配制的
酸化的上述新配制的 溶液10mL氧化并测定
溶液10mL氧化并测定 溶液中
溶液中 的物质的量浓度,消耗0.05mol/L的
的物质的量浓度,消耗0.05mol/L的 溶液100mL,则反应后锰元素的价态为
溶液100mL,则反应后锰元素的价态为(3)某同学利用
 氧化
氧化 制备
制备 的装置如下图所示(夹持装置略):
的装置如下图所示(夹持装置略):
 )在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:
)在浓强碱溶液中可稳定存在,碱性减弱时易发生反应: ;
;①装置A中a的作用是
 的化学方程式为
的化学方程式为②上述装置存在一处缺陷,会导致
 产率降低,改进的方法是
产率降低,改进的方法是③装置C中发生反应的离子方程式为
您最近一年使用:0次
解题方法
4 . 按要求,回答下列问题:
(1)实验室用二氧化锰和浓盐酸反应制取氯气,反应的离子方程式是___________ 。
(2)氯气可用湿润的淀粉碘化钾试纸检验,请用化学方程式解释原因:___________ 。
(3)由于氯气贮存运输不方便,工业上常将氯气转化为漂白粉,工业上生产漂白粉的主要化学方程式是___________ 。
(4)家庭中使用漂白粉时,为了增强漂白能力,可加入少量的物质是___________。
(5)某同学在探究漂白粉溶液性质时,在漂白粉溶液中加入几滴无色酚酞溶液,发现溶液呈红色,随后溶液迅速褪色,说明漂白粉溶液呈___________ 性,并具有___________ 性。
(6)实验室也可用 固体和浓盐酸反应制氯气,反应方程式如下:
固体和浓盐酸反应制氯气,反应方程式如下: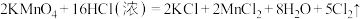 ,若反应中有0.5mol电子转移,被氧化HCl的物质的量为
,若反应中有0.5mol电子转移,被氧化HCl的物质的量为___________ 。
(1)实验室用二氧化锰和浓盐酸反应制取氯气,反应的离子方程式是
(2)氯气可用湿润的淀粉碘化钾试纸检验,请用化学方程式解释原因:
(3)由于氯气贮存运输不方便,工业上常将氯气转化为漂白粉,工业上生产漂白粉的主要化学方程式是
(4)家庭中使用漂白粉时,为了增强漂白能力,可加入少量的物质是___________。
| A.食醋 | B.食盐 | C.烧碱 | D.纯碱 |
(6)实验室也可用
 固体和浓盐酸反应制氯气,反应方程式如下:
固体和浓盐酸反应制氯气,反应方程式如下: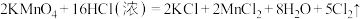 ,若反应中有0.5mol电子转移,被氧化HCl的物质的量为
,若反应中有0.5mol电子转移,被氧化HCl的物质的量为
您最近一年使用:0次
5 . 回答下列问题
(1)以下物质:①KCl晶体;②液态HCl;③食盐水;④熔融NaCl;⑤蔗糖;⑥铜;⑦ ;能导电的是
;能导电的是___________ (填序号,下同);属于电解质的是___________ ;属于非电解质的是___________ 。
(2)在离子 中,共有x个核外电子,R原子的质量数为A,氧原子的质子数为8,则R原子核内含有的中子数目是
中,共有x个核外电子,R原子的质量数为A,氧原子的质子数为8,则R原子核内含有的中子数目是___________ 。
(3)用___________ 方法将植物油和水的混合体系分离;用___________ 方法分离四氯化碳(沸点为76.75℃)和甲苯(沸点为110.6℃)的混合液体(四氯化碳和甲苯互溶)。
(4)胃液中含有盐酸,胃酸过多的人常有胃疼烧心的感觉,易吐酸水,服用适量的小苏打( ),能治疗胃酸过多,请写出其反应的离子方程式:
),能治疗胃酸过多,请写出其反应的离子方程式:___________ ;此时最好用含氢氧化铝的胃药(如胃舒平)离子方程式:___________ 。
(1)以下物质:①KCl晶体;②液态HCl;③食盐水;④熔融NaCl;⑤蔗糖;⑥铜;⑦
 ;能导电的是
;能导电的是(2)在离子
 中,共有x个核外电子,R原子的质量数为A,氧原子的质子数为8,则R原子核内含有的中子数目是
中,共有x个核外电子,R原子的质量数为A,氧原子的质子数为8,则R原子核内含有的中子数目是(3)用
(4)胃液中含有盐酸,胃酸过多的人常有胃疼烧心的感觉,易吐酸水,服用适量的小苏打(
 ),能治疗胃酸过多,请写出其反应的离子方程式:
),能治疗胃酸过多,请写出其反应的离子方程式:
您最近一年使用:0次
解题方法
6 . 汽车剧烈碰撞时,安全气囊中发生反应 。有关该反应,下列叙述正确的是
。有关该反应,下列叙述正确的是
 。有关该反应,下列叙述正确的是
。有关该反应,下列叙述正确的是A.上述反应中 是还原剂 是还原剂 |
B.每生成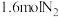 ,转移的电子为2mol ,转移的电子为2mol |
C. 中N的化合价为-3价 中N的化合价为-3价 |
| D.若被氧化的N原子的物质的量为3mol,则氧化产物比还原产物多1.4mol |
您最近一年使用:0次
解题方法
7 . 室温下进行下列实验,根据实验操作和现象所得出的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 某钠盐溶于盐酸,产生能使澄清石灰水变浑浊的无色无味气体 | 该钠盐是 |
| B | 向溶液X中先滴加稀硝酸,再滴加 溶液,出现白色沉淀 溶液,出现白色沉淀 | 溶液X中一定含有 |
| C | 向某溶液中滴入 溶液有白色沉淀产生 溶液有白色沉淀产生 | 溶液中一定含有 |
| D | 向CuSO4溶液中加入铁粉,有红色固体析出 |  的氧化性弱于 的氧化性弱于 的氧化性 的氧化性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
8 . 设 为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是
 为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是A.1mol氯气溶于水形成的新制氯水中,含有的 数为 数为 |
B.常温下,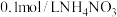 溶液中 溶液中 的数目为 的数目为 |
C.常温常压下, 和 和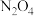 混合气体中含有的N原子数一定为 混合气体中含有的N原子数一定为 |
D.含有 个氦原子的氦气在标准状况下的体积约为11.2L 个氦原子的氦气在标准状况下的体积约为11.2L |
您最近一年使用:0次
解题方法
9 . 下列有关 说法正确的是
说法正确的是
 说法正确的是
说法正确的是A. 中阴阳离子的个数比为1:1 中阴阳离子的个数比为1:1 |
B. 体现强氧化性,可以用作呼吸面具的供氧剂 体现强氧化性,可以用作呼吸面具的供氧剂 |
C. 由钠在常温下与氧气反应得到 由钠在常温下与氧气反应得到 |
D. 与 与 反应,产生标准状况下 反应,产生标准状况下 ,转移 ,转移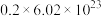 个电子 个电子 |
您最近一年使用:0次
解题方法
10 . 下列离子方程式书写正确的是
A.铁和盐酸溶液反应: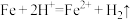 |
B.铜与硝酸银溶液反应: |
C.钠投入水中: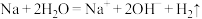 |
D.氢氧化钡溶液与稀 反应: 反应: |
您最近一年使用:0次



