1 . 在一定温度下,有a.盐酸 b.硫酸 c.醋酸三种酸:
(1)当三种酸物质的量浓度相同时,c(H+)由大到小的顺序是___________ (用字母表示,下同)。
(2)同体积、同物质的量浓度的三种酸,中和NaOH 的能力由大到小的顺序是___________ 。
(3)若三者pH相同时,物质的量浓度由大到小的顺序是___________ 。
(4)将pH相同且体积也相同的三种酸,分别与等浓度的NaOH稀溶液反应至pH=7,则消耗NaOH溶液的体积大小关系为___________ 。
(5)将pH相同的三种酸均加水稀释至原来的100倍后,pH由大到小的顺序是___________ 。
(1)当三种酸物质的量浓度相同时,c(H+)由大到小的顺序是
(2)同体积、同物质的量浓度的三种酸,中和NaOH 的能力由大到小的顺序是
(3)若三者pH相同时,物质的量浓度由大到小的顺序是
(4)将pH相同且体积也相同的三种酸,分别与等浓度的NaOH稀溶液反应至pH=7,则消耗NaOH溶液的体积大小关系为
(5)将pH相同的三种酸均加水稀释至原来的100倍后,pH由大到小的顺序是
您最近一年使用:0次
2 . 尿素[CO(NH2)2][s]是首个由无机物人工合成的有机物。
(1)在尿素合成塔中发生的反应可表示为2NH3(g)+CO2(g) NH2COONH4(l)
NH2COONH4(l)  H1=-119.2 kJ∙mol-1;NH2COONH4(l)
H1=-119.2 kJ∙mol-1;NH2COONH4(l) CO(NH2)2(s)+H2O(g)
CO(NH2)2(s)+H2O(g)  H2=+15.5kJ∙mol-1,已知第一步反应为快速反应,第二步反应为慢速反应,则2NH3(g)+CO2(g)
H2=+15.5kJ∙mol-1,已知第一步反应为快速反应,第二步反应为慢速反应,则2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g)
CO(NH2)2(s)+H2O(g)  H3=
H3=___________ kJ∙mol-1,下列图象能表示尿素合成塔中发生反应的能量变化历程的是___________ (填标号)。
A .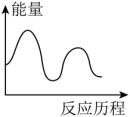 B.
B. 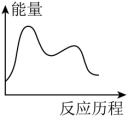 C.
C. 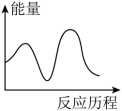 D.
D.
(2)T℃,在2L的密闭容器中,通入2molNH3和1molCO2,保持体积不变,发生反应,2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g),10min时反应刚好达到平衡。测得起始压强为平衡时压强的1.5倍,则:
CO(NH2)2(s)+H2O(g),10min时反应刚好达到平衡。测得起始压强为平衡时压强的1.5倍,则:
①NH3的平衡转化率为___________ 。
②能说明上述反应达到平衡状态的是___________ (填标号)。
A.n(CO2):n(NH3)=1:2
B.混合气体的密度不再发生变化
C.CO2的体积分数在混合气体中保持不变
D.单位时间内消耗2molNH3,同时生成1molH2O
(3)一定温度下,某恒容密闭容器中发生反应2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g),若原料气中
CO(NH2)2(s)+H2O(g),若原料气中 =m,测得m与CO2的平衡转化率(α)的关系如图所示:
=m,测得m与CO2的平衡转化率(α)的关系如图所示:
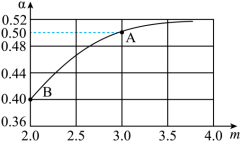
若平衡时A点容器内总压强为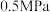 ,则上述反应的平衡常数Kp=
,则上述反应的平衡常数Kp=___________  。(用平衡分压代平衡浓度计算,分压=总压×物质的量分数)
。(用平衡分压代平衡浓度计算,分压=总压×物质的量分数)
(1)在尿素合成塔中发生的反应可表示为2NH3(g)+CO2(g)
 NH2COONH4(l)
NH2COONH4(l)  H1=-119.2 kJ∙mol-1;NH2COONH4(l)
H1=-119.2 kJ∙mol-1;NH2COONH4(l) CO(NH2)2(s)+H2O(g)
CO(NH2)2(s)+H2O(g)  H2=+15.5kJ∙mol-1,已知第一步反应为快速反应,第二步反应为慢速反应,则2NH3(g)+CO2(g)
H2=+15.5kJ∙mol-1,已知第一步反应为快速反应,第二步反应为慢速反应,则2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g)
CO(NH2)2(s)+H2O(g)  H3=
H3=A .
 B.
B.  C.
C.  D.
D.
(2)T℃,在2L的密闭容器中,通入2molNH3和1molCO2,保持体积不变,发生反应,2NH3(g)+CO2(g)
 CO(NH2)2(s)+H2O(g),10min时反应刚好达到平衡。测得起始压强为平衡时压强的1.5倍,则:
CO(NH2)2(s)+H2O(g),10min时反应刚好达到平衡。测得起始压强为平衡时压强的1.5倍,则:①NH3的平衡转化率为
②能说明上述反应达到平衡状态的是
A.n(CO2):n(NH3)=1:2
B.混合气体的密度不再发生变化
C.CO2的体积分数在混合气体中保持不变
D.单位时间内消耗2molNH3,同时生成1molH2O
(3)一定温度下,某恒容密闭容器中发生反应2NH3(g)+CO2(g)
 CO(NH2)2(s)+H2O(g),若原料气中
CO(NH2)2(s)+H2O(g),若原料气中 =m,测得m与CO2的平衡转化率(α)的关系如图所示:
=m,测得m与CO2的平衡转化率(α)的关系如图所示:
若平衡时A点容器内总压强为
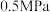 ,则上述反应的平衡常数Kp=
,则上述反应的平衡常数Kp= 。(用平衡分压代平衡浓度计算,分压=总压×物质的量分数)
。(用平衡分压代平衡浓度计算,分压=总压×物质的量分数)
您最近一年使用:0次
3 . 在T℃条件下,向1L固定体积的密闭容器M中加入2 mol X和1 mol Y,发生如下反应:2X(g) + Y(g) a Z(g) + W(g)
a Z(g) + W(g)  H = -Q kJ·mol-1 (Q>0)。当反应达到平衡后,反应放出的热量为Q1 kJ,物质X的转化率为α;若平衡后再升高温度,混合气体的平均相对分子质量减小,则
H = -Q kJ·mol-1 (Q>0)。当反应达到平衡后,反应放出的热量为Q1 kJ,物质X的转化率为α;若平衡后再升高温度,混合气体的平均相对分子质量减小,则
(1)化学计量数a的值为___________ ;此反应的逆反应 S
S___________ 0 (填﹤,﹥,﹦)。
(2)下列说法中能说明该反应达到了化学平衡状态的是___________ 。
A.容器内压强一定
B.v(X)正=2 v (Y)逆
C.容器内Z分子数一定
D.容器内气体的质量一定
E.容器内气体的密度一定
F.X、Y、Z、W的浓度之比为2∶1∶a∶1
(3)维持温度不变,若起始时向容器中加入4mol X和6 mol Y,若达平衡时容器内的压强减小到开始时的85%,则反应中放出的热量为___________ kJ。
(4)已知:该反应的平衡常数随温度的变化如下表:
若在某温度下,2 mol X和1 mol Y在该容器中反应达平衡,X的平衡转化率为50%,则该温度为___________ ℃。
 a Z(g) + W(g)
a Z(g) + W(g)  H = -Q kJ·mol-1 (Q>0)。当反应达到平衡后,反应放出的热量为Q1 kJ,物质X的转化率为α;若平衡后再升高温度,混合气体的平均相对分子质量减小,则
H = -Q kJ·mol-1 (Q>0)。当反应达到平衡后,反应放出的热量为Q1 kJ,物质X的转化率为α;若平衡后再升高温度,混合气体的平均相对分子质量减小,则(1)化学计量数a的值为
 S
S(2)下列说法中能说明该反应达到了化学平衡状态的是
A.容器内压强一定
B.v(X)正=2 v (Y)逆
C.容器内Z分子数一定
D.容器内气体的质量一定
E.容器内气体的密度一定
F.X、Y、Z、W的浓度之比为2∶1∶a∶1
(3)维持温度不变,若起始时向容器中加入4mol X和6 mol Y,若达平衡时容器内的压强减小到开始时的85%,则反应中放出的热量为
(4)已知:该反应的平衡常数随温度的变化如下表:
| 温度/℃ | 150 | 200 | 250 | 300 | 350 |
| 平衡常数K | 9.94 | 5.2 | 1 | 0.5 | 0.21 |
您最近一年使用:0次
4 . 回答下列问题。
(1)溶液酸化时,K2MnO4转变为MnO2固体和KMnO4的离子方程式是___________ 。
(2)常温下,某种饮品pH=4,其中c(OH-)=___________ 。
(3)将0.025 mol·L-1的H2SO4溶液和0.075 mol·L-1的H2SO4溶液等体积混合,混合溶液的pH=___________ 。
(4)常温下,pH=13的氢氧化钡溶液,c[Ba(OH)2]=___________ 。
(5)当H2S浓度较低时常用纯碱溶液进行吸收。表为H2S、H2CO3 的电离平衡常数。
纯碱溶液吸收少量H2S的离子方程式为___________ 。
(1)溶液酸化时,K2MnO4转变为MnO2固体和KMnO4的离子方程式是
(2)常温下,某种饮品pH=4,其中c(OH-)=
(3)将0.025 mol·L-1的H2SO4溶液和0.075 mol·L-1的H2SO4溶液等体积混合,混合溶液的pH=
(4)常温下,pH=13的氢氧化钡溶液,c[Ba(OH)2]=
(5)当H2S浓度较低时常用纯碱溶液进行吸收。表为H2S、H2CO3 的电离平衡常数。
| 电离平衡常数 | Kal | Ka2 |
| H2S | 9.1×10-8 | 1.1×10-12 |
| H2CO3 | 4.3×10-7 | 5.61×10-11 |
您最近一年使用:0次
名校
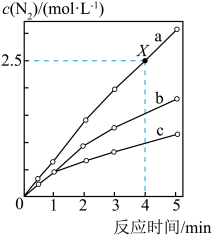
5 . 相同条件下,在固定容积的密闭容器中选用不同的催化剂(a、b、c)发生反应:4NH3(g)+6NO(g) 5N2(g)+6H2O(g),反应产生N2的物质的量浓度随时间变化如图所示。下列说法错误的是
5N2(g)+6H2O(g),反应产生N2的物质的量浓度随时间变化如图所示。下列说法错误的是
 5N2(g)+6H2O(g),反应产生N2的物质的量浓度随时间变化如图所示。下列说法错误的是
5N2(g)+6H2O(g),反应产生N2的物质的量浓度随时间变化如图所示。下列说法错误的是
| A.催化剂的催化效率:a>b>c |
| B.X点时,NH3的化学反应速率为0.5 mol·L-1·min-1 |
| C.使用催化剂a、b、c达到平衡时NO的转化率相等 |
| D.若在恒容绝热的密闭容器中发生该反应,当K值不变时,说明反应已经达到平衡 |
您最近一年使用:0次
2024-04-26更新
|
58次组卷
|
2卷引用:甘肃省白银市会宁县第三中学2023-2024学年高二上学期期中考试化学试题
名校
解题方法
6 . 已知温度T时水的离子积常数为Kw,该温度下,将浓度为a mol/L的一元酸HA与b mol/L的一元碱BOH等体积混合,可判断溶液呈中性的依据是
| A.a=b | B.混合溶液中,c(H+)+c(B+)=c(OH﹣)+c(A﹣) |
C.混合溶液中,c(H+)=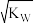 | D.混合溶液的pH=7 |
您最近一年使用:0次
2024-04-26更新
|
30次组卷
|
2卷引用:甘肃省白银市会宁县第三中学2023-2024学年高二上学期期中考试化学试题
7 . 完成下列问题。
(1)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。Zn、C、O电负性由大至小的顺序是___________
(2)①基态Cu原子有___________ 种不同能级的电子。位于在周期表___________ 区(填s、p、d或ds)。Cu+的价电子排布式为___________ 。
②N原子中最高能级的电子的电子云轮廓图为___________ 。
③在空气中FeO稳定性小于Fe2O3,从电子排布的角度分析,其主要原因是___________ 。
(3)由于Be与Al处于对角线位置,性质具有相似性,根据“对角线规则”,写出Be(OH)2与NaOH反应的化学方程式:___________ 。
(4)高锰酸钾是一种重要的化学试剂,实验室常常利用高锰酸钾溶液测定草酸晶体(H2C2O4·xH2O)中 的值,高锰酸钾溶液需用
的值,高锰酸钾溶液需用___________ 盛装(填 酸式滴定管 或 碱式滴定管)滴定终点溶液的判断是___________ 颜色变化为由无色变为浅红色。
(1)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。Zn、C、O电负性由大至小的顺序是
(2)①基态Cu原子有
②N原子中最高能级的电子的电子云轮廓图为
③在空气中FeO稳定性小于Fe2O3,从电子排布的角度分析,其主要原因是
(3)由于Be与Al处于对角线位置,性质具有相似性,根据“对角线规则”,写出Be(OH)2与NaOH反应的化学方程式:
(4)高锰酸钾是一种重要的化学试剂,实验室常常利用高锰酸钾溶液测定草酸晶体(H2C2O4·xH2O)中
 的值,高锰酸钾溶液需用
的值,高锰酸钾溶液需用
您最近一年使用:0次
8 . (1)已知25℃时,醋酸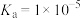 ,0.1mol/L的醋酸溶液的pH=
,0.1mol/L的醋酸溶液的pH=___________ 。
(2)相同物质的量浓度的五种溶液:①(NH4)2SO4 ②氨水③NH4HSO4 ④NH4Cl⑤(NH4)2Fe(SO4)2,c(NH4+)由大到小顺序是___________ (用序号表示)。
(3)可溶性铝盐常用作净水剂的原因:___________ (用离子方程式表示)。
(4)将等体积等物质的量浓度的CH3COONa和NaF溶液混合:c(CH3COOH)+c(HF)___________ c(OH-)-c(H+)(填 > 或 < 或 =)
(5)某温度下,测得的0.001mol/LHCl溶液中,由水电离出来的 。求此温度下,水离子积常数为
。求此温度下,水离子积常数为___________ 。在此温度下,将 的HCl溶液和
的HCl溶液和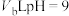 的
的 溶液混合均匀,测得溶液的pH=7,则
溶液混合均匀,测得溶液的pH=7,则
___________ 。
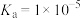 ,0.1mol/L的醋酸溶液的pH=
,0.1mol/L的醋酸溶液的pH=(2)相同物质的量浓度的五种溶液:①(NH4)2SO4 ②氨水③NH4HSO4 ④NH4Cl⑤(NH4)2Fe(SO4)2,c(NH4+)由大到小顺序是
(3)可溶性铝盐常用作净水剂的原因:
(4)将等体积等物质的量浓度的CH3COONa和NaF溶液混合:c(CH3COOH)+c(HF)
(5)某温度下,测得的0.001mol/LHCl溶液中,由水电离出来的
 。求此温度下,水离子积常数为
。求此温度下,水离子积常数为 的HCl溶液和
的HCl溶液和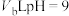 的
的 溶液混合均匀,测得溶液的pH=7,则
溶液混合均匀,测得溶液的pH=7,则
您最近一年使用:0次
9 . NA表示阿伏加德罗常数的值,下列说法正确的是
A.0.1mol/L的NH4Cl溶液中 浓度小于0.1NA 浓度小于0.1NA |
B.室温下,等体积的pH=1的 溶液和pH=1的 溶液和pH=1的 溶液,所含有的 溶液,所含有的 的个数均为0.1NA 的个数均为0.1NA |
| C.3.2gCH4中所含σ键数目为0.8NA |
| D.1mol基态Al原子位于p能级上的电子数为3NA |
您最近一年使用:0次
10 . N2H4、N2O4常用作火箭发射的推进剂。火箭推进剂发生的反应为:2N2H4(1)+N2O4(1)=3N2(g)+4H2O(g)。下列有关说法正确的是
A.充有N2O4的密闭容器中存在:N2O4(g) 2NO2(g),当c(N2O4)=c(NO2)时,该可逆反应到达限度 2NO2(g),当c(N2O4)=c(NO2)时,该可逆反应到达限度 |
| B.碱性N2H4-空气燃料电池工作时,负极电极反应式为N2H4+4e-+4OH-=N2+4H2O |
| C.反应每生成0.9molN2,转移电子的数目为2.4×6.02×1023 |
D.N2H4的水溶液中存在:N2H4+H2O  +OH-,向稀溶液中加水稀释, +OH-,向稀溶液中加水稀释,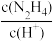 值变大 值变大 |
您最近一年使用:0次



