名校
解题方法
1 . 一种超导材料(仅由Cs、Ag、F三种元素组成)的长方体晶胞结构如图所示(已知 ,用
,用 表示阿伏加德罗常数的值):
表示阿伏加德罗常数的值):
 ,用
,用 表示阿伏加德罗常数的值):
表示阿伏加德罗常数的值):
A.基态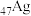 失去4d能级上的一个电子转化为 失去4d能级上的一个电子转化为 |
B.若N点原子分数坐标为(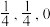 ),则P点原子分数坐标为( ),则P点原子分数坐标为(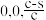 ) ) |
C.M、N之间的距离为 |
D.晶体的密度为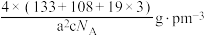 |
您最近一年使用:0次
7日内更新
|
7次组卷
|
6卷引用:河南省信阳高级中学2023-2024学年高三上学期11月一模考试化学试题
名校
解题方法
2 . 分子式为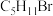 的烃,分子中含有3个甲基的同分异构体共有(不考虑立体异构)
的烃,分子中含有3个甲基的同分异构体共有(不考虑立体异构)
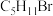 的烃,分子中含有3个甲基的同分异构体共有(不考虑立体异构)
的烃,分子中含有3个甲基的同分异构体共有(不考虑立体异构)| A.3种 | B.2种 | C.5种 | D.4种 |
您最近一年使用:0次
2024-05-08更新
|
102次组卷
|
8卷引用:河南省安阳市新乡鹤壁2022-2023学年高二下学期5月份联考化学试题
3 . 回答下列问题。
(1)镍元素基态原子的核外电子排布式为___________ ,3d能级上的未成对电子数为___________ 。
(2)基态Ge原子的价层电子排布式为___________ ,有___________ 个未成对电子。
(3)Zn2+基态核外电子排布式为___________ 。
(4)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用___________ 形象化描述。在基态 14C原子中,核外存在___________ 对自旋相反的电子。
(5)基态Fe原子有___________ 个未成对电子。Fe3+的电子排布式为___________ 。
(1)镍元素基态原子的核外电子排布式为
(2)基态Ge原子的价层电子排布式为
(3)Zn2+基态核外电子排布式为
(4)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用
(5)基态Fe原子有
您最近一年使用:0次
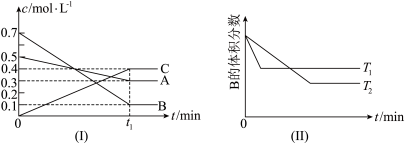
4 . I.T℃时,A气体与B气体反应生成C气体,反应过程中A、B、C浓度变化如图(Ⅰ)所示,若保持其他条件不变,温度分别为T1和T2时,B的体积分数与时间的关系如(Ⅱ)所示:
(1)反应的化学方程式为___________ 。
(2)当反应达到平衡后升高平衡体系的温度(保持体积不变),混合气体的平均相对分子质量___________ (填“变大”、“变小”或“不变”)。
Ⅱ.在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g) CO(g)+H2O(g)
CO(g)+H2O(g)
其化学平衡常数K和温度t的关系如下表:
回答下列问题:
(3)一般说化学平衡常数数值K___________ ,通常认为该反应进行较完全。
(4)该反应为___________ 反应(填“吸热”或“放热”)。
(5)能判断该反应是否达到化学平衡状态的依据是___________。
(6)某温度下,在2L的密闭容器中,加入1molCO2和1molH2充分反应达平衡时,CO平衡浓度为0.25mol/L,试判断此时的温度为___________ 。
(1)反应的化学方程式为
(2)当反应达到平衡后升高平衡体系的温度(保持体积不变),混合气体的平均相对分子质量
Ⅱ.在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)
 CO(g)+H2O(g)
CO(g)+H2O(g)其化学平衡常数K和温度t的关系如下表:
| t/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(3)一般说化学平衡常数数值K
(4)该反应为
(5)能判断该反应是否达到化学平衡状态的依据是___________。
| A.v正(H2) = v逆(H2O) | B.反应停止,正、逆反应速率都等于零 |
| C.容器中压强不再发生变化 | D.混合气体中c(CO2)不变 |
(6)某温度下,在2L的密闭容器中,加入1molCO2和1molH2充分反应达平衡时,CO平衡浓度为0.25mol/L,试判断此时的温度为
您最近一年使用:0次
5 . 硫代硫酸钠晶体(Na2S2O3·5H2O,M=248g/mol)可用作定影剂、还原剂。回答下列问题:
(1)已知: 难溶于水,BaS2O3微溶于水。市售硫代硫酸钠中常含有硫酸根杂质,请完成相应实验步骤和现象:
难溶于水,BaS2O3微溶于水。市售硫代硫酸钠中常含有硫酸根杂质,请完成相应实验步骤和现象:
①取少量样品,加入煮沸后冷却的蒸馏水,固体完全溶解得无色澄清溶液;
②加入过量稀盐酸,有刺激性气体产生,溶液中出现___________ (填“白色”或“淡黄色”)浑浊;
③静置,吸取___________ (填“上层”或“下层”)清液,滴入___________ (填“ ”或“
”或“ ”)溶液,产生
”)溶液,产生___________ (填“白色”或“淡黄色”)沉淀,则证明含有硫酸根杂质。
(2)利用 标准溶液定量测定硫代硫酸钠的纯度,补充相应测定步骤和结论:
标准溶液定量测定硫代硫酸钠的纯度,补充相应测定步骤和结论:
①溶液配制:称取1.2000g某硫代硫酸钠晶体样品,用新煮沸并冷却的蒸馏水在___________ 中溶解,完全溶解后,全部转移至100mL的___________ 中,加蒸馏水至刻度;
②滴定:取0.00950mol/L的 标准溶液
标准溶液 ,硫酸酸化后加入过量KI,发生反应:Cr2O
,硫酸酸化后加入过量KI,发生反应:Cr2O +6I—+14H+=3I2+2Cr3++7H2O,然后用硫代硫酸钠样品溶液滴定至淡黄绿色,发生反应:I2+2S2O
+6I—+14H+=3I2+2Cr3++7H2O,然后用硫代硫酸钠样品溶液滴定至淡黄绿色,发生反应:I2+2S2O =S4O
=S4O +2I—,加入
+2I—,加入___________ 溶液作为指示剂,继续滴定,当溶液___________ ,且半分钟内不恢复,即为终点;
③平行滴定3次,样品溶液的用量数据记录如下表:
则样品纯度为___________ %(保留1位小数)。
(1)已知:
 难溶于水,BaS2O3微溶于水。市售硫代硫酸钠中常含有硫酸根杂质,请完成相应实验步骤和现象:
难溶于水,BaS2O3微溶于水。市售硫代硫酸钠中常含有硫酸根杂质,请完成相应实验步骤和现象:①取少量样品,加入煮沸后冷却的蒸馏水,固体完全溶解得无色澄清溶液;
②加入过量稀盐酸,有刺激性气体产生,溶液中出现
③静置,吸取
 ”或“
”或“ ”)溶液,产生
”)溶液,产生(2)利用
 标准溶液定量测定硫代硫酸钠的纯度,补充相应测定步骤和结论:
标准溶液定量测定硫代硫酸钠的纯度,补充相应测定步骤和结论:①溶液配制:称取1.2000g某硫代硫酸钠晶体样品,用新煮沸并冷却的蒸馏水在
②滴定:取0.00950mol/L的
 标准溶液
标准溶液 ,硫酸酸化后加入过量KI,发生反应:Cr2O
,硫酸酸化后加入过量KI,发生反应:Cr2O +6I—+14H+=3I2+2Cr3++7H2O,然后用硫代硫酸钠样品溶液滴定至淡黄绿色,发生反应:I2+2S2O
+6I—+14H+=3I2+2Cr3++7H2O,然后用硫代硫酸钠样品溶液滴定至淡黄绿色,发生反应:I2+2S2O =S4O
=S4O +2I—,加入
+2I—,加入③平行滴定3次,样品溶液的用量数据记录如下表:
| 平行滴定/次序 | 1 | 2 | 3 |
| 样品溶液的用量/mL | 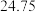 | 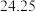 | 24.85 |
您最近一年使用:0次
解题方法
6 .  在室温下为无色液体,易挥发,有强烈的刺激性气味,遇水强烈水解,并放出大量的热,可用
在室温下为无色液体,易挥发,有强烈的刺激性气味,遇水强烈水解,并放出大量的热,可用 与
与 和
和 在加热的条件下来制备。
在加热的条件下来制备。
(1)用所给仪器和药品制备 ,仪器各接口的连接顺序是
,仪器各接口的连接顺序是_________ (填标号)。
(2)当________ 时,点燃装置 处的酒精灯来制备
处的酒精灯来制备 ;装置
;装置 的作用为
的作用为__________ 。
(3)写出装置E的硬质玻璃管中反应的化学方程式:_________ ;装置 水槽中盛放的是
水槽中盛放的是______ (填“冷水”或“热水”)。
(4)该制备 的装置有一定的缺陷,其改进措施是
的装置有一定的缺陷,其改进措施是_________ 。
(5)氮化硅 是一种高温结构陶瓷材料,
是一种高温结构陶瓷材料, 可以在高温条件下由
可以在高温条件下由 蒸气与
蒸气与 反应得到,写出该反应的化学方程式:
反应得到,写出该反应的化学方程式:_________ 。
 在室温下为无色液体,易挥发,有强烈的刺激性气味,遇水强烈水解,并放出大量的热,可用
在室温下为无色液体,易挥发,有强烈的刺激性气味,遇水强烈水解,并放出大量的热,可用 与
与 和
和 在加热的条件下来制备。
在加热的条件下来制备。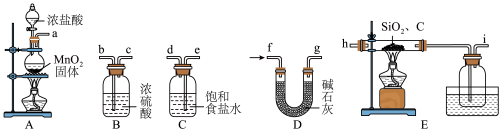
(1)用所给仪器和药品制备
 ,仪器各接口的连接顺序是
,仪器各接口的连接顺序是(2)当
 处的酒精灯来制备
处的酒精灯来制备 ;装置
;装置 的作用为
的作用为(3)写出装置E的硬质玻璃管中反应的化学方程式:
 水槽中盛放的是
水槽中盛放的是(4)该制备
 的装置有一定的缺陷,其改进措施是
的装置有一定的缺陷,其改进措施是(5)氮化硅
 是一种高温结构陶瓷材料,
是一种高温结构陶瓷材料, 可以在高温条件下由
可以在高温条件下由 蒸气与
蒸气与 反应得到,写出该反应的化学方程式:
反应得到,写出该反应的化学方程式:
您最近一年使用:0次
解题方法
7 . 某化学兴趣小组对钠和钠的化合物进行了一系列的实验探究,请回答下列问题。
实验Ⅰ:探究二氧化碳与过氧化钠的反应是否有氧气生成,设计了如图所示的实验装置。_______ ,作用是_______ 。
(2)指出装置 中的错误之处:
中的错误之处:_______ 。
(3)取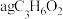 在氧气中完全燃烧,将其产物与足量
在氧气中完全燃烧,将其产物与足量 固体完全反应,反应后固体质量的增加量
固体完全反应,反应后固体质量的增加量_______ (填“大于”“等于”或“小于”) 。
。
实验Ⅱ:利用如图所示装置(省略夹持装置)模拟工业级 的制备。
的制备。 。
。
(4)装置 中盛放的药品为
中盛放的药品为_______ 。
(5)实验中使用油浴加热而不使用水浴加热的原因是_______ 。
(6)氨气与熔融钠反应生成 的化学方程式为
的化学方程式为_______ 。
实验Ⅰ:探究二氧化碳与过氧化钠的反应是否有氧气生成,设计了如图所示的实验装置。
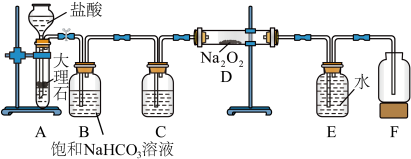
(2)指出装置
 中的错误之处:
中的错误之处:(3)取
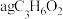 在氧气中完全燃烧,将其产物与足量
在氧气中完全燃烧,将其产物与足量 固体完全反应,反应后固体质量的增加量
固体完全反应,反应后固体质量的增加量 。
。实验Ⅱ:利用如图所示装置(省略夹持装置)模拟工业级
 的制备。
的制备。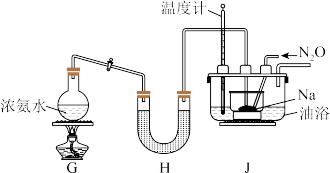
 。
。(4)装置
 中盛放的药品为
中盛放的药品为(5)实验中使用油浴加热而不使用水浴加热的原因是
(6)氨气与熔融钠反应生成
 的化学方程式为
的化学方程式为
您最近一年使用:0次
解题方法
8 . 空气质量日报中涉及的污染物主要是 和可吸入颗粒物。
和可吸入颗粒物。
Ⅰ.汽车尾气是城市大气氮氧化物的主要来源之一。治理方法之一是在汽车排气管上加装“催化转化器”,使 和
和 反应生成可参与大气生态环境循环的无毒气体。
反应生成可参与大气生态环境循环的无毒气体。
(1)以 为例写出反应的化学方程式:
为例写出反应的化学方程式:_________ 。
Ⅱ.SO2的排放是造成酸雨的主要因素,形成酸雨的原理之一可简单表示为:
______________ (填“>”“<”或“=”)5.6。
(3)反应 的化学方程式为
的化学方程式为______________ 。
(4)用足量的氨水吸收 ,其离子方程式为
,其离子方程式为________ 。
(5) 溶液可以吸收含
溶液可以吸收含 的烟气,若
的烟气,若 溶液与
溶液与 恰好反应完全,检验反应后的溶液中是否含有
恰好反应完全,检验反应后的溶液中是否含有 的方法为
的方法为_____________ 。
Ⅲ.利用溶液吸收尾气(主要含 及少量
及少量 )中的氮氧化物,实验装置如图所示.已知:
)中的氮氧化物,实验装置如图所示.已知: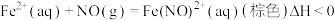
______ 时,说明 中
中 溶液需要更换。
溶液需要更换。
(7)若尾气体积为 (标准状况),用
(标准状况),用 溶液滴定a中溶液,消耗
溶液滴定a中溶液,消耗 溶液体积为
溶液体积为 ,尾气中
,尾气中 的体积分数为
的体积分数为_________ 。
 和可吸入颗粒物。
和可吸入颗粒物。Ⅰ.汽车尾气是城市大气氮氧化物的主要来源之一。治理方法之一是在汽车排气管上加装“催化转化器”,使
 和
和 反应生成可参与大气生态环境循环的无毒气体。
反应生成可参与大气生态环境循环的无毒气体。(1)以
 为例写出反应的化学方程式:
为例写出反应的化学方程式:Ⅱ.SO2的排放是造成酸雨的主要因素,形成酸雨的原理之一可简单表示为:


(3)反应
 的化学方程式为
的化学方程式为(4)用足量的氨水吸收
 ,其离子方程式为
,其离子方程式为(5)
 溶液可以吸收含
溶液可以吸收含 的烟气,若
的烟气,若 溶液与
溶液与 恰好反应完全,检验反应后的溶液中是否含有
恰好反应完全,检验反应后的溶液中是否含有 的方法为
的方法为Ⅲ.利用溶液吸收尾气(主要含
 及少量
及少量 )中的氮氧化物,实验装置如图所示.已知:
)中的氮氧化物,实验装置如图所示.已知: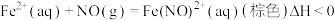

 中
中 溶液需要更换。
溶液需要更换。(7)若尾气体积为
 (标准状况),用
(标准状况),用 溶液滴定a中溶液,消耗
溶液滴定a中溶液,消耗 溶液体积为
溶液体积为 ,尾气中
,尾气中 的体积分数为
的体积分数为
您最近一年使用:0次
解题方法
9 . Ⅰ.过氧化氢是用途很广的绿色氧化剂,常用于消毒、杀菌、漂白等.试回答下列问题:
(1)写出酸性高锰酸钾溶液和 反应的离子方程式:
反应的离子方程式:______________ 。
(2)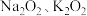 以及
以及 都可与酸作用生成过氧化氢,目前实验室制取过氧化氢可通过上述某种过氧化物与适量稀硫酸作用,然后过滤.则上述最适合的过氧化物是
都可与酸作用生成过氧化氢,目前实验室制取过氧化氢可通过上述某种过氧化物与适量稀硫酸作用,然后过滤.则上述最适合的过氧化物是______________ 。
Ⅱ.某工厂废水中含 ,其浓度为
,其浓度为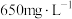 ,现用氯氧化法处理,发生如下反应(化合物中
,现用氯氧化法处理,发生如下反应(化合物中 的化合价均为-3价):
的化合价均为-3价):
(3)反应 中被氧化的元素是
中被氧化的元素是______________ 。
(4)通入过量氯气,可将萻酸盐进一步氧化为氮气,请配平下列化学方程式:_____________ 。
(1)写出酸性高锰酸钾溶液和
 反应的离子方程式:
反应的离子方程式:(2)
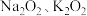 以及
以及 都可与酸作用生成过氧化氢,目前实验室制取过氧化氢可通过上述某种过氧化物与适量稀硫酸作用,然后过滤.则上述最适合的过氧化物是
都可与酸作用生成过氧化氢,目前实验室制取过氧化氢可通过上述某种过氧化物与适量稀硫酸作用,然后过滤.则上述最适合的过氧化物是Ⅱ.某工厂废水中含
 ,其浓度为
,其浓度为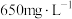 ,现用氯氧化法处理,发生如下反应(化合物中
,现用氯氧化法处理,发生如下反应(化合物中 的化合价均为-3价):
的化合价均为-3价):(3)反应
 中被氧化的元素是
中被氧化的元素是(4)通入过量氯气,可将萻酸盐进一步氧化为氮气,请配平下列化学方程式:

您最近一年使用:0次
10 . 下列各组离子在给定条件下一定能大量共存的是
A. 的溶液中: 的溶液中: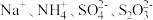 |
B.含大量 的溶液中: 的溶液中: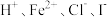 |
C.与 反应放出 反应放出 的溶液中: 的溶液中: |
D.能使紫色石荵试液变蓝色的溶液中: |
您最近一年使用:0次



