名校
解题方法
1 . 分子式为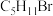 的烃,分子中含有3个甲基的同分异构体共有(不考虑立体异构)
的烃,分子中含有3个甲基的同分异构体共有(不考虑立体异构)
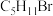 的烃,分子中含有3个甲基的同分异构体共有(不考虑立体异构)
的烃,分子中含有3个甲基的同分异构体共有(不考虑立体异构)| A.3种 | B.2种 | C.5种 | D.4种 |
您最近一年使用:0次
2024-05-08更新
|
102次组卷
|
8卷引用:黑龙江省鸡西实验中学2022-2023学年高二下学期7月期末考试化学试题
2 . 下列各图所示的能量转化形式主要是化学能转化为热能的是
| 选项 | A.钻木取火 | B.电器取暖 | C.蜡烛燃烧 | D.燃煤发电 |
| 图片 |
|
|
|
|
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
3 . 醋酸是常见的一元弱酸。请运用化学反应原理回答下列问题:
(1)室温下,pH=2的醋酸中,水电离出的c(H+)=___________ mol·L-1该醋酸和pH=2的盐酸溶液相比,导电性___________ (填“相同”“不同”或“无法判断”)。
(2)pH相同的盐酸和醋酸分别与足量的锌粒反应,生成等量的H2时所需时间较短的是___________ 。
(3)向 醋酸溶液中滴入
醋酸溶液中滴入 溶液,下列浓度大小顺序不可能出现的是
溶液,下列浓度大小顺序不可能出现的是___________ (填字母)。
a.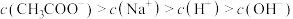
b.
c.
d.
(4)常温下,将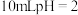 的醋酸溶液稀释至
的醋酸溶液稀释至 ,溶液的
,溶液的
___________ (填“>”“<”或“=”)4;在醋酸稀释过程中下列数值变大的是___________ 。
A. B.
B. C.
C. D.
D.
(5)醋酸中存在平衡: ,下列措施可使醋酸的
,下列措施可使醋酸的 增大,并且电离平衡向右移动的是___________。
增大,并且电离平衡向右移动的是___________。
(1)室温下,pH=2的醋酸中,水电离出的c(H+)=
(2)pH相同的盐酸和醋酸分别与足量的锌粒反应,生成等量的H2时所需时间较短的是
(3)向
 醋酸溶液中滴入
醋酸溶液中滴入 溶液,下列浓度大小顺序不可能出现的是
溶液,下列浓度大小顺序不可能出现的是a.
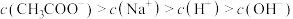
b.

c.

d.

(4)常温下,将
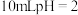 的醋酸溶液稀释至
的醋酸溶液稀释至 ,溶液的
,溶液的
A.
 B.
B. C.
C. D.
D.
(5)醋酸中存在平衡:
 ,下列措施可使醋酸的
,下列措施可使醋酸的 增大,并且电离平衡向右移动的是___________。
增大,并且电离平衡向右移动的是___________。A.加入 溶液 溶液 | B.加入盐酸 | C.加水稀释 | D.对醋酸溶液加热 |
您最近一年使用:0次
4 . 已知 时,几种弱酸的电离平衡常数如下:
时,几种弱酸的电离平衡常数如下: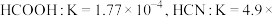
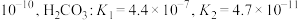 ,则以下反应不能自发进行的是
,则以下反应不能自发进行的是
 时,几种弱酸的电离平衡常数如下:
时,几种弱酸的电离平衡常数如下: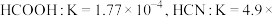
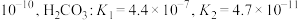 ,则以下反应不能自发进行的是
,则以下反应不能自发进行的是A. |
B.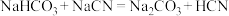 |
C.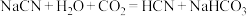 |
D.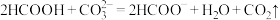 |
您最近一年使用:0次
5 . Ⅰ.下表是生活生产中常见的物质,表中列出了它们的一种主要成分(其中加碘盐是氯化钠中添加适量的 ,其他成分未列出)
,其他成分未列出)
(1)请你对表中①~⑦的主要成分进行分类,是电解质的是______ ,是非电解质的是______ 。(填序号)
(2)写出④在水中的电离方程式____________ 。
(3)写出用④治疗胃酸(主要成分为盐酸)过多涉及的化学方程式:______________ 。
Ⅱ.铁的化学性质比较活泼,常温下铁可以与稀硝酸发生反应,反应的化学方程式为
(4)反应中氧化剂与还原剂的个数之比为______ ,其中 反应中显出来的性质是
反应中显出来的性质是______ 。
(5)该反应中的氧化产物为______ ,每生成11.2L(标准状况下)的NO,转移的电子个数为______ 。
 ,其他成分未列出)
,其他成分未列出)名称 | 天然气 | 白酒 | 醋酸 | 小苏打 |
主要成分 | ① | ② | ③ | ④ |
名称 | 熟石灰 | 铜线 | 加碘盐 | |
主要成分 | ⑤ | ⑥Cu | ⑦NaCl和 |
(2)写出④在水中的电离方程式
(3)写出用④治疗胃酸(主要成分为盐酸)过多涉及的化学方程式:
Ⅱ.铁的化学性质比较活泼,常温下铁可以与稀硝酸发生反应,反应的化学方程式为

(4)反应中氧化剂与还原剂的个数之比为
 反应中显出来的性质是
反应中显出来的性质是(5)该反应中的氧化产物为
您最近一年使用:0次
解题方法
6 . 有A、B两种常见化合物,其焰色试验均呈黄色,C是一种单质气体,相互转化关系如图所示(其他物质均已略去)。回答下列问题:______ 。
(2)B加热产生D的化学方程式:____________ 。
(3)请用化学方程式表示A在潜水艇中的一种重要用途:____________ 。
(4)A、B在密闭装置中加热,充分反应后,若只得到一种固体化合物E,其化学式为______ 。
(5)写出一种将E转化为B的化学方程式:____________ 。

(2)B加热产生D的化学方程式:
(3)请用化学方程式表示A在潜水艇中的一种重要用途:
(4)A、B在密闭装置中加热,充分反应后,若只得到一种固体化合物E,其化学式为
(5)写出一种将E转化为B的化学方程式:
您最近一年使用:0次
7 . 下列电离方程式中正确的是
A. | B. |
C.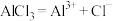 | D. |
您最近一年使用:0次
8 . 常温下,几种弱酸的电离平衡常数如表所示,下列说法正确的是
| 化学式 | HCOOH | H2CO3 | HCN |
| 电离平衡常数 | K=1.8×10﹣4 | K1=4.3×10﹣7 K2=5.6×10﹣11 | K=4.9×10﹣10 |
A.结合H+的能力由大到小:CO >CN﹣>HCO >CN﹣>HCO >HCOO﹣ >HCOO﹣ |
| B.等物质的量浓度的 HCOONa溶液和NaCN溶液,pH大小顺序:HCOONa>NaCN |
| C.加水稀释 HCOOH溶液,其电离平衡常数将减小 |
D.H2CO3溶液和NaCN溶液反应的离子方程式为H2CO3+2CN﹣=2HCN+CO |
您最近一年使用:0次
9 . 铁在一定条件下能够和水反应,最近科学家利用常见金属铁研发了一种新型可充电池,简易装置如图。下列说法错误的是

| A.该电池不能在低温环境下使用 |
| B.充电时,石墨烯a应连接电源的负极 |
| C.放电时,电池内部O2﹣向石墨烯b移动 |
| D.充电时,石墨烯b极发生反应:FeOx+2xe﹣=Fe+xO2﹣ |
您最近一年使用:0次
解题方法
10 . Ⅰ.按要求回答下列问题:
(1)某粒子有1个原子核、核中有17个质子、20个中子,核外有18个电子,该粒子的化学符号是___________ 。
(2)写出下列物质的电子式:
NaOH___________ Cl2 ___________ NH4I ___________ 。
(3)用电子式表示下列化合物的形成过程:
Na2S___________ 。
H2O___________ 。
Ⅱ. 如图为元素周期表的一部分,列出了10种元素在元素周期表中的位置,试回答下列问题:___________ 。(填化学式)。
(5)10种元素中,原子半径最小的是___________ (填序号)。
(6)元素⑦的简单氢化物与元素⑧的单质反应的离子方程式为___________ 。
(7)元素②和⑤的最高价氧化物对应水化物相互反应的化学方程式为___________ 。
(8)元素⑩的原子序数为___________ 。
(9)元素⑨的单质易溶于元素⑥与⑧形成的化合物中,所得溶液颜色为___________ 色。
(1)某粒子有1个原子核、核中有17个质子、20个中子,核外有18个电子,该粒子的化学符号是
(2)写出下列物质的电子式:
NaOH
(3)用电子式表示下列化合物的形成过程:
Na2S
H2O
Ⅱ. 如图为元素周期表的一部分,列出了10种元素在元素周期表中的位置,试回答下列问题:
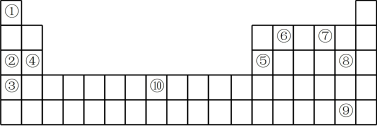
(5)10种元素中,原子半径最小的是
(6)元素⑦的简单氢化物与元素⑧的单质反应的离子方程式为
(7)元素②和⑤的最高价氧化物对应水化物相互反应的化学方程式为
(8)元素⑩的原子序数为
(9)元素⑨的单质易溶于元素⑥与⑧形成的化合物中,所得溶液颜色为
您最近一年使用:0次












