名校
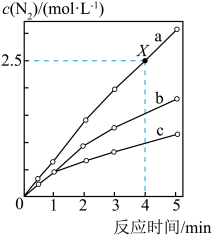
1 . 相同条件下,在固定容积的密闭容器中选用不同的催化剂(a、b、c)发生反应:4NH3(g)+6NO(g) 5N2(g)+6H2O(g),反应产生N2的物质的量浓度随时间变化如图所示。下列说法错误的是
5N2(g)+6H2O(g),反应产生N2的物质的量浓度随时间变化如图所示。下列说法错误的是
 5N2(g)+6H2O(g),反应产生N2的物质的量浓度随时间变化如图所示。下列说法错误的是
5N2(g)+6H2O(g),反应产生N2的物质的量浓度随时间变化如图所示。下列说法错误的是
| A.催化剂的催化效率:a>b>c |
| B.X点时,NH3的化学反应速率为0.5 mol·L-1·min-1 |
| C.使用催化剂a、b、c达到平衡时NO的转化率相等 |
| D.若在恒容绝热的密闭容器中发生该反应,当K值不变时,说明反应已经达到平衡 |
您最近一年使用:0次
2024-04-26更新
|
44次组卷
|
2卷引用:甘肃省白银市会宁县第三中学2023-2024学年高二上学期期中考试化学试题
2 . 完成下列问题。
(1)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。Zn、C、O电负性由大至小的顺序是___________
(2)①基态Cu原子有___________ 种不同能级的电子。位于在周期表___________ 区(填s、p、d或ds)。Cu+的价电子排布式为___________ 。
②N原子中最高能级的电子的电子云轮廓图为___________ 。
③在空气中FeO稳定性小于Fe2O3,从电子排布的角度分析,其主要原因是___________ 。
(3)由于Be与Al处于对角线位置,性质具有相似性,根据“对角线规则”,写出Be(OH)2与NaOH反应的化学方程式:___________ 。
(4)高锰酸钾是一种重要的化学试剂,实验室常常利用高锰酸钾溶液测定草酸晶体(H2C2O4·xH2O)中 的值,高锰酸钾溶液需用
的值,高锰酸钾溶液需用___________ 盛装(填 酸式滴定管 或 碱式滴定管)滴定终点溶液的判断是___________ 颜色变化为由无色变为浅红色。
(1)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。Zn、C、O电负性由大至小的顺序是
(2)①基态Cu原子有
②N原子中最高能级的电子的电子云轮廓图为
③在空气中FeO稳定性小于Fe2O3,从电子排布的角度分析,其主要原因是
(3)由于Be与Al处于对角线位置,性质具有相似性,根据“对角线规则”,写出Be(OH)2与NaOH反应的化学方程式:
(4)高锰酸钾是一种重要的化学试剂,实验室常常利用高锰酸钾溶液测定草酸晶体(H2C2O4·xH2O)中
 的值,高锰酸钾溶液需用
的值,高锰酸钾溶液需用
您最近一年使用:0次
3 . A、B、C、D是钠及其重要化合物,有着广泛的用途。已知B是常见的供氧剂,其相互转化关系如图所示(部分反应条件省略)。红热的铁能与水蒸气发生置换反应。回答下列问题:___________ 。
(2)B→C的化学方程式为___________ 。
(3)D→C的化学方程式为___________ 。
(4)若A为金属钠, 完全转化成D(涉及的其它反应物均足量),则生成D的质量为
完全转化成D(涉及的其它反应物均足量),则生成D的质量为___________ g。
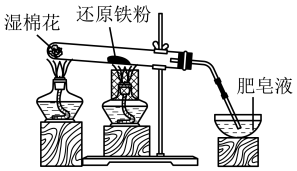
(5)某同学探究铁与水蒸气的反应,进行了如下实验:___________ (填标号)。
A.先点燃湿棉花处的酒精灯,一段时间后再点燃还原铁粉处的酒精灯
B.先点燃还原铁粉处的酒精灯,一段时间后再点燃湿棉花处的酒精灯
C.同时点燃湿棉花处和还原铁粉处的酒精灯
②能否根据肥皂液冒气泡来证明铁与水蒸气发生了反应?___________ (填“能”或“不能”)。
③实验结束恢复到室温后,能否用磁铁将未参加反应的铁粉从反应后的固体中分离出来?___________ (填“能”或“不能”)。

(2)B→C的化学方程式为
(3)D→C的化学方程式为
(4)若A为金属钠,
 完全转化成D(涉及的其它反应物均足量),则生成D的质量为
完全转化成D(涉及的其它反应物均足量),则生成D的质量为(5)某同学探究铁与水蒸气的反应,进行了如下实验:
A.先点燃湿棉花处的酒精灯,一段时间后再点燃还原铁粉处的酒精灯
B.先点燃还原铁粉处的酒精灯,一段时间后再点燃湿棉花处的酒精灯
C.同时点燃湿棉花处和还原铁粉处的酒精灯
②能否根据肥皂液冒气泡来证明铁与水蒸气发生了反应?
③实验结束恢复到室温后,能否用磁铁将未参加反应的铁粉从反应后的固体中分离出来?
您最近一年使用:0次
解题方法
4 .  在现代工业生产中应用广泛,查阅资料得:无水
在现代工业生产中应用广泛,查阅资料得:无水 在空气中易潮解,加热易升华。
在空气中易潮解,加热易升华。
(1)用丁达尔效应鉴别 胶体和
胶体和 溶液的操作是
溶液的操作是____________ (写出具体实验操作、结论)。
(2)电子工业中用 溶液腐蚀敷在绝缘板上的铜,从而制造印刷电路板,写出
溶液腐蚀敷在绝缘板上的铜,从而制造印刷电路板,写出 溶液与铜反应的离子方程式:
溶液与铜反应的离子方程式:__________________ 。该反应的还原剂是______ 。
(3)硫化氢( )是一种有毒的气体,可用
)是一种有毒的气体,可用 溶液吸收,生成单质硫(S)沉淀。
溶液吸收,生成单质硫(S)沉淀。 溶液与
溶液与 反应的离子方程式为
反应的离子方程式为____________ 。该反应中氧化产物与还原产物的物质的量之比为______ 。
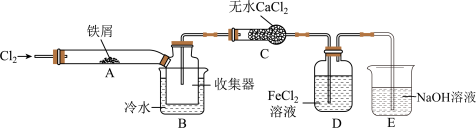
(4)某小组同学设计了制备无水) 的实验方案,装置示意图(加热及夹持装置略去)及操作步骤如下:
的实验方案,装置示意图(加热及夹持装置略去)及操作步骤如下:
步骤Ⅰ.检验装置的气密性;
步骤Ⅱ.通入干燥的 ,赶尽装置中的空气;
,赶尽装置中的空气;
步骤Ⅲ.用酒精灯在铁屑下方加热至反应完成;
步骤Ⅳ.体系冷却后,停止通入 ,并用干燥的
,并用干燥的 赶尽
赶尽 ,将收集器密封。
,将收集器密封。
①装置A中发生反应的化学方程式为__________________ 。
②装置B中冷水浴的作用为____________ 。
 在现代工业生产中应用广泛,查阅资料得:无水
在现代工业生产中应用广泛,查阅资料得:无水 在空气中易潮解,加热易升华。
在空气中易潮解,加热易升华。(1)用丁达尔效应鉴别
 胶体和
胶体和 溶液的操作是
溶液的操作是(2)电子工业中用
 溶液腐蚀敷在绝缘板上的铜,从而制造印刷电路板,写出
溶液腐蚀敷在绝缘板上的铜,从而制造印刷电路板,写出 溶液与铜反应的离子方程式:
溶液与铜反应的离子方程式:(3)硫化氢(
 )是一种有毒的气体,可用
)是一种有毒的气体,可用 溶液吸收,生成单质硫(S)沉淀。
溶液吸收,生成单质硫(S)沉淀。 溶液与
溶液与 反应的离子方程式为
反应的离子方程式为(4)某小组同学设计了制备无水)
 的实验方案,装置示意图(加热及夹持装置略去)及操作步骤如下:
的实验方案,装置示意图(加热及夹持装置略去)及操作步骤如下:
步骤Ⅰ.检验装置的气密性;
步骤Ⅱ.通入干燥的
 ,赶尽装置中的空气;
,赶尽装置中的空气;步骤Ⅲ.用酒精灯在铁屑下方加热至反应完成;
步骤Ⅳ.体系冷却后,停止通入
 ,并用干燥的
,并用干燥的 赶尽
赶尽 ,将收集器密封。
,将收集器密封。①装置A中发生反应的化学方程式为
②装置B中冷水浴的作用为
您最近一年使用:0次
解题方法
5 . 含镍废水对环境和人体健康均会造成巨大的影响。某化学小组在实验室设计了以下装置模拟工业含镍废水处理,图中电极均为惰性电极。错误 的是
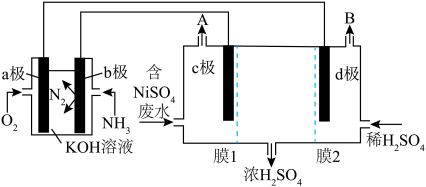
A.a极为正极, 极为阴极 极为阴极 |
B. 极的电极反应为2H2O-4e-=O2+4H+↑ 极的电极反应为2H2O-4e-=O2+4H+↑ |
| C.膜1为阴离子交换膜 |
D.b极消耗22.4LNH3,理论上 极上析出88.5gNi单质 极上析出88.5gNi单质 |
您最近一年使用:0次
名校
解题方法
6 . 《周礼》中记载:涑帛,以栏为灰,渥淳其帛,实诸泽器,淫之以蜃,清其灰而盝之。这介绍了古代精炼丝绸的步骤:
Ⅰ.丝绸放在光滑的容器里要用草木灰水浸润透;
Ⅱ.将一定量蚌壳灼烧成的蚌壳灰加入上述容器中一起浸泡。
上述方法生成的用于精炼丝绸的物质是
Ⅰ.丝绸放在光滑的容器里要用草木灰水浸润透;
Ⅱ.将一定量蚌壳灼烧成的蚌壳灰加入上述容器中一起浸泡。
上述方法生成的用于精炼丝绸的物质是
A. | B. | C. | D. |
您最近一年使用:0次
2024-01-21更新
|
56次组卷
|
2卷引用:甘肃省靖远县第一中学2023-2024学年高一上学期12月期末考试化学试题
名校
7 . 写出下列反应的方程式:
(1)氢氧化亚铁沉淀在空气中迅速变为灰绿色,最终变成红褐色对应的化学方程式___________ 。
(2)工业用氯化铁溶液腐蚀铜印刷电路板的离子方程式___________ 。
(3)漂白粉在空气中生效的化学方程式___________ 。
(4)请写出次氯酸光照分解的离子方程式___________ 。
(5) 中的少量
中的少量 ,可以利用加入酸性
,可以利用加入酸性 溶液进行检验,请写出离子方程式
溶液进行检验,请写出离子方程式______ 。
(1)氢氧化亚铁沉淀在空气中迅速变为灰绿色,最终变成红褐色对应的化学方程式
(2)工业用氯化铁溶液腐蚀铜印刷电路板的离子方程式
(3)漂白粉在空气中生效的化学方程式
(4)请写出次氯酸光照分解的离子方程式
(5)
 中的少量
中的少量 ,可以利用加入酸性
,可以利用加入酸性 溶液进行检验,请写出离子方程式
溶液进行检验,请写出离子方程式
您最近一年使用:0次
名校
8 . I.下图是一个电化学过程的装置示意图。请回答下列问题:

(1)甲池中通入O2的电极作___________ 极,该电池的负极反应式为___________ 。
(2)乙池中总反应的离子方程式为___________ ,假设乙池中溶液的体积为200mL且反应后溶液体积不变,当向甲池中通入112mL(标准状况)O₂(假设完全反应)时,乙池溶液的pH为___________ 。
(3)电解一段时间后丙池中阴极附近会观察到的现象是___________ 。
Ⅱ.回收并利用CO₂一直是科研人员研究的热点。一种聚合物锂电池通过充、放电可实现“大气固碳”(工作原理如图所示)。

(4)该电池在充电时,通过催化剂的选择性控制,只有 发生氧化释放出
发生氧化释放出 和
和 。图中
。图中 的移动方向是
的移动方向是___________ (填“充电”或“放电”)时的移动方向;充电时,阳极的电极反应式为___________ ;该电池每循环充、放电子各 ,理论上可固定
,理论上可固定
___________ L(标准状况)。

(1)甲池中通入O2的电极作
(2)乙池中总反应的离子方程式为
(3)电解一段时间后丙池中阴极附近会观察到的现象是
Ⅱ.回收并利用CO₂一直是科研人员研究的热点。一种聚合物锂电池通过充、放电可实现“大气固碳”(工作原理如图所示)。

(4)该电池在充电时,通过催化剂的选择性控制,只有
 发生氧化释放出
发生氧化释放出 和
和 。图中
。图中 的移动方向是
的移动方向是 ,理论上可固定
,理论上可固定
您最近一年使用:0次
9 . 化学定量分析法是以测定物质中各种成分的含量以及成分之间的定量关系的分析方法,化学定量分析在研究物质性质及其变化中的应用十分广泛。
I.酸碱中和滴定法测定市售白醋的总酸量( )
)
(1)食用白醋的主要化学成分是 ,
, 的电离方程式为
的电离方程式为___________ 。用___________ (填仪器名称)量取10.00mL的食用白醋,在烧杯中用蒸馏水稀释后转移到100mL容量瓶中定容,摇匀即得到待测的白醋溶液。
(2)量取待测的白醋溶液20.00mL于锥形瓶中,向其中滴加2滴指示剂,用浓度为 的NaOH标准液对待测白醋溶液进行滴定(已知白醋中其他成分不与NaOH反应);滴定实验过程中消耗的NaOH溶液的体积如下表:
的NaOH标准液对待测白醋溶液进行滴定(已知白醋中其他成分不与NaOH反应);滴定实验过程中消耗的NaOH溶液的体积如下表:
①滴定时所加的指示剂为___________ (填指示剂的名称)。滴定达到滴定终点的现象为___________ 。
②按上表中正确的数据处理,可计算出c(市售白醋)=___________  ,市售白醋的总酸量=
,市售白醋的总酸量=___________ ( )。
)。
③在滴定过程中下列操作或结果正确的是___________ (填序号)。
A.碱式滴定管在滴定时先用水洗,再用标准NaOH溶液润洗
B.锥形瓶先用水洗,再用待测的白醋溶液润洗
C.滴定读数时,应该单手持滴定管上端并保持其自然垂直
D.滴定时剧烈摇动锥形瓶,有少量液体溅出可导致测定结果偏大
II.用pH计探究浓度对醋酸电离程度的影响。
取25℃时不同浓度的醋酸,分别用pH计测定其pH,测定结果如下:
(3)根据表中的数据可以得出醋酸是弱电解质,得出该结论的依据是___________ 。
(4)根据表中的数据,还可以得出另一结论:随着醋酸浓度的减小,醋酸的电离程度逐渐___________ (填“增大”“减小”或“不变”)。
I.酸碱中和滴定法测定市售白醋的总酸量(
 )
)(1)食用白醋的主要化学成分是
 ,
, 的电离方程式为
的电离方程式为(2)量取待测的白醋溶液20.00mL于锥形瓶中,向其中滴加2滴指示剂,用浓度为
 的NaOH标准液对待测白醋溶液进行滴定(已知白醋中其他成分不与NaOH反应);滴定实验过程中消耗的NaOH溶液的体积如下表:
的NaOH标准液对待测白醋溶液进行滴定(已知白醋中其他成分不与NaOH反应);滴定实验过程中消耗的NaOH溶液的体积如下表:| 实验序号 | 1 | 2 | 3 | 4 |
| 消耗NaOH溶液的体积mL | 15.95 | 15.00 | 15.05 | 14.95 |
②按上表中正确的数据处理,可计算出c(市售白醋)=
 ,市售白醋的总酸量=
,市售白醋的总酸量= )。
)。③在滴定过程中下列操作或结果正确的是
A.碱式滴定管在滴定时先用水洗,再用标准NaOH溶液润洗
B.锥形瓶先用水洗,再用待测的白醋溶液润洗
C.滴定读数时,应该单手持滴定管上端并保持其自然垂直
D.滴定时剧烈摇动锥形瓶,有少量液体溅出可导致测定结果偏大
II.用pH计探究浓度对醋酸电离程度的影响。
取25℃时不同浓度的醋酸,分别用pH计测定其pH,测定结果如下:
醋酸的浓度( ) ) | 0.0010 | 0.0100 | 0.0200 | 0.1000 | 0.2000 |
| pH | 3.88 | 3.38 | 3.23 | 2.88 | 2.73 |
(4)根据表中的数据,还可以得出另一结论:随着醋酸浓度的减小,醋酸的电离程度逐渐
您最近一年使用:0次
10 . 对于反应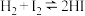 ,下列有关说法错误的是
,下列有关说法错误的是
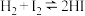 ,下列有关说法错误的是
,下列有关说法错误的是A.该反应同时向生成HI和生成 的方向进行 的方向进行 |
B.该反应的 与HI不可能同时存在同一个反应体系中 与HI不可能同时存在同一个反应体系中 |
C.该反应中生成HI的反应与生成 的反应的条件相同 的反应的条件相同 |
D.该反应中 不可能全部转化为H1 不可能全部转化为H1 |
您最近一年使用:0次
2024-01-11更新
|
310次组卷
|
3卷引用:甘肃省部分学校2023-2024学年高二上学期期末学业质量监测化学试题



