解题方法
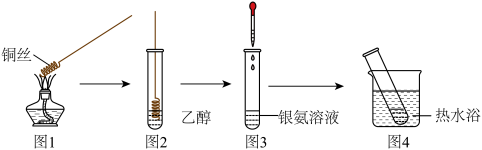
1 . 探究乙醇的氧化反应,并检验其产物,观察思考并回答下列问题 黑
黑 红”可推测,铜丝的作用是
红”可推测,铜丝的作用是_______ 。
(2)图2实验中乙醇的氧化产物是_______ 。
(3)为检验乙醇的氧化产物,需配置银氨溶液,具体操作如下:取洁净的试管,加入1mL____ (填序号,下同),一边振荡试管,一边逐滴加入____ ,直到最初产生的沉淀恰好溶解为止,得到银氨溶液。①氨水,②2%AgNO3溶液
(4)图4中水浴加热的优点是_______ 。
(5)图4试管壁出现光亮的银镜,实验结束后,可选用_______洗去银镜。
 黑
黑 红”可推测,铜丝的作用是
红”可推测,铜丝的作用是(2)图2实验中乙醇的氧化产物是
(3)为检验乙醇的氧化产物,需配置银氨溶液,具体操作如下:取洁净的试管,加入1mL
(4)图4中水浴加热的优点是
(5)图4试管壁出现光亮的银镜,实验结束后,可选用_______洗去银镜。
| A.盐酸 | B.稀硝酸 | C.氨水 | D.氨氧化钠溶液 |
您最近一年使用:0次
解题方法
2 . 下列说法不正确 的是
|
|
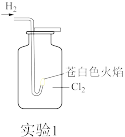
| A.实验1可推测Cl2具有助燃性 | B.实验2可推测Na2O2与H2O反应生成O2 |
|
|
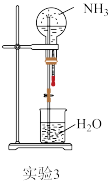
| C.实验3可推测NH3具有强碱性 | D.实验4光照后可观察到试管内液面上升 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
3 . 摄入人体内的淀粉在酶的催化作用下可发生如下转化过程。
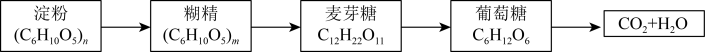
| A.n>m |
| B.上述转化过程均为水解反应 |
C.葡萄糖转化为CO2和H2O的过程中能量转化:热能 化学能 化学能 |
| D.纤维素在人体内也可按上述转化过程最终水解成葡萄糖 |
您最近一年使用:0次
解题方法
4 . 制作豆腐过程一般有如图步操作,其中操作⑤CaSO4或MgCl2作凝固剂根据图示,下列说法不正确的是

| A.操作①与操作②的目的是为了更多的蛋白质溶解于水 |
| B.操作③属于固液分离,取其袋子内的固体作为操作④的原料 |
| C.在适宜温度下,操作⑤用MgCl2,作凝固剂可使蛋白质沉淀 |
| D.操作⑥使豆腐“成形”,此过程主要发生的是物理变化 |
您最近一年使用:0次
解题方法
5 . 工业上以黄铁矿为原料制备硫酸的原理示意图如下。
(1)黄铁矿主要成分的化学式是_______ 。
(2)SO2使品红溶液褪色,体现SO2具有_______ 性。
(3)步骤Ⅲ的化学方程式是_______ 。
(4)下列说法不正确 的是_______。

(1)黄铁矿主要成分的化学式是
(2)SO2使品红溶液褪色,体现SO2具有
(3)步骤Ⅲ的化学方程式是
(4)下列说法
| A.步骤Ⅰ前需将黄铁矿粉碎,目的是增大接触面积,加快反应速率 |
| B.步骤Ⅱ中使用催化剂,能使SO2的转化率达到100% |
| C.步骤Ⅲ中选用98.3%的浓硫酸作吸收剂 |
| D.图中每一步含硫物质均发生氧化反应 |
您最近一年使用:0次
解题方法
6 . 食品包装中的铁系脱氧剂由还原铁粉、氯化钠和炭粉等组成,利用铁的吸氧腐蚀除去氧气,主要反应有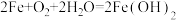 ,
,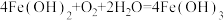 。已知某脱氧剂中含有2.24g还原铁粉,请计算:
。已知某脱氧剂中含有2.24g还原铁粉,请计算:
(1)还原铁粉的物质的量是_______ mol。
(2)若还原铁粉完全转化为Fe(OH)3,则转移电子的物质的量是_______ mol。
(3)在25 和101kPa的条作下,气体摩尔体积约为24.5L/mol,空气中氧气的体积分数约为21%,则该脱氧剂理论上最多能处理
和101kPa的条作下,气体摩尔体积约为24.5L/mol,空气中氧气的体积分数约为21%,则该脱氧剂理论上最多能处理_______ mL包装盒中的空气。
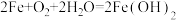 ,
,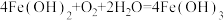 。已知某脱氧剂中含有2.24g还原铁粉,请计算:
。已知某脱氧剂中含有2.24g还原铁粉,请计算:(1)还原铁粉的物质的量是
(2)若还原铁粉完全转化为Fe(OH)3,则转移电子的物质的量是
(3)在25
 和101kPa的条作下,气体摩尔体积约为24.5L/mol,空气中氧气的体积分数约为21%,则该脱氧剂理论上最多能处理
和101kPa的条作下,气体摩尔体积约为24.5L/mol,空气中氧气的体积分数约为21%,则该脱氧剂理论上最多能处理
您最近一年使用:0次
7 . 下表中"方法导引”与“示例"对应关系不正确的是
| 选项 | 方法导引 | 示例 |
| A | 分类 | 实验室中制取气体装置的连接顺序一般为:发生装置 除杂装置 除杂装置 收集装置 收集装置 尾气处理装置 尾气处理装置 |
| B | 预测 | 钠、钾能与水反应,铷与钠、钾都属于IA族元素,则可预测铷也能与水反应 |
| C | 变量控制 | 探究催化剂对化学反应速率的影响时,需要控制温度、浓度和他影响因素保持不变 |
| D | 认识有机化合物的一般思路 | 先分析有机物的碳骨架和官能团,再认识它的类别、性质和用途 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
8 . 进行化学实验时,为保护眼睛需要佩戴的的防护用具是
| A.护目镜 | B.口罩 | C.实验服 | D.手套 |
您最近一年使用:0次
9 . 常温下,将某一元酸HA(甲、乙、丙、丁代表不同的一元酸)和NaOH溶液等体积混合(溶液混合体积变化忽略不计),两种溶液的物质的量浓度和混合溶液的pH如下表所示:
(1)从甲组情况分析,如何判断HA是强酸还是弱酸?___________ 。
(2)根据乙组数据,可计算得出此温度下HA的电离常数为___________ (计算结果要求化简)。
(3)从丙组实验结果分析,该混合溶液中离子浓度由大到小的顺序是___________ 。此溶液c(A-)+c(HA)=___________ 。(写精确值)
(4)据丁组实验数据,写出该混合溶液中下列算式的列式结果:
c(Na+)-c(A-)=___________ mol/L。
(5)现用0.1000mol/LNaOH溶液滴定未知浓度的HA溶液,
①在滴定步骤前,要进行一系列操作,按正确顺序排列___________ 。
a.向碱式滴定管中装入标准液至“0”刻度以上2~3mL处
b.用蒸馏水洗涤滴定管
c.将滴定管内装满水,直立于滴定管夹上约2min
d.用标准溶液润洗滴定管
e.将滴定管直立于滴定管夹上,静置1min左右,准确读取读数
f.将滴定管垂直固定在滴定管夹上,右手将乳胶管弯曲,并挤压玻璃球
②在滴定过程中,下列实验中,由于错误操作导致滴定实验结果一定偏高的是___________ 。
A.配制NaOH标准溶液定容时仰视刻度线,用此溶液去滴定HA溶液
B.滴定时盛放待测液的锥形瓶没有干燥,所测得待测液的浓度
C.选用甲基橙作指示剂
D.滴定管(装标准溶液)滴定前尖嘴处有气泡,滴定后无气泡
| 实验编号 | c(HA)/mol·L-1 | c([NaOH)/mol·L-1 | 混合溶液的pH |
| 甲 | 0.1 | 0.1 | =m |
| 乙 | 0.12 | 0.1 | =7 |
| 丙 | 0.2 | 0.1 | <7 |
| 丁 | 0.1 | 0.1 | =11 |
(2)根据乙组数据,可计算得出此温度下HA的电离常数为
(3)从丙组实验结果分析,该混合溶液中离子浓度由大到小的顺序是
(4)据丁组实验数据,写出该混合溶液中下列算式的列式结果:
c(Na+)-c(A-)=
(5)现用0.1000mol/LNaOH溶液滴定未知浓度的HA溶液,
①在滴定步骤前,要进行一系列操作,按正确顺序排列
a.向碱式滴定管中装入标准液至“0”刻度以上2~3mL处
b.用蒸馏水洗涤滴定管
c.将滴定管内装满水,直立于滴定管夹上约2min
d.用标准溶液润洗滴定管
e.将滴定管直立于滴定管夹上,静置1min左右,准确读取读数
f.将滴定管垂直固定在滴定管夹上,右手将乳胶管弯曲,并挤压玻璃球
②在滴定过程中,下列实验中,由于错误操作导致滴定实验结果一定偏高的是
A.配制NaOH标准溶液定容时仰视刻度线,用此溶液去滴定HA溶液
B.滴定时盛放待测液的锥形瓶没有干燥,所测得待测液的浓度
C.选用甲基橙作指示剂
D.滴定管(装标准溶液)滴定前尖嘴处有气泡,滴定后无气泡
您最近一年使用:0次
解题方法
10 . 下表为长式元素周期表的主要部分。①~⑬代表13种元素,⑭表示元素周期表中某一区域。
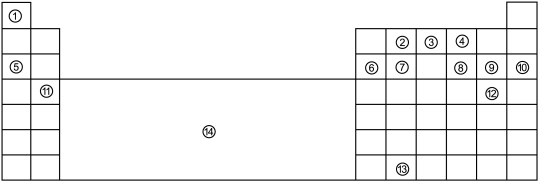
请回答:
(1)①、②、④的原子半径从大到小排列的顺序是______ 。(填化学式)
(2)①与③组成的含10个电子的阳离子的化学式是______ 。
(3)有些族的元素有特别的名称,⑨所在主族的元素叫做______ 元素。
(4)⑩的元素符号是______ 。
(5)⑪的元素名称是______ 。
(6)⑫的原子结构示意图是______ 。
(7)⑬在元素周期表中的位置是______ 。
(8)下列说法不正确 的是______ 。
A. ②的原子所含原子数即
②的原子所含原子数即 任何粒子的粒子数
任何粒子的粒子数
B.⑥、⑦的氧化物均能与⑤的最高价氧化物对应水化物反应
C.⑧的某种氧化物进入大气会形成酸雨
D.⑨的某种氧化物可用于自来水消毒
E.⑭所示区域内的元素常见于农药中
(9)⑥的单质与 溶液反应的化学方程式是
溶液反应的化学方程式是______ 。

请回答:
(1)①、②、④的原子半径从大到小排列的顺序是
(2)①与③组成的含10个电子的阳离子的化学式是
(3)有些族的元素有特别的名称,⑨所在主族的元素叫做
(4)⑩的元素符号是
(5)⑪的元素名称是
(6)⑫的原子结构示意图是
(7)⑬在元素周期表中的位置是
(8)下列说法
A.
 ②的原子所含原子数即
②的原子所含原子数即 任何粒子的粒子数
任何粒子的粒子数B.⑥、⑦的氧化物均能与⑤的最高价氧化物对应水化物反应
C.⑧的某种氧化物进入大气会形成酸雨
D.⑨的某种氧化物可用于自来水消毒
E.⑭所示区域内的元素常见于农药中
(9)⑥的单质与
 溶液反应的化学方程式是
溶液反应的化学方程式是
您最近一年使用:0次