1 . 铬酰氯( )可在有机合成中作氯化剂。某兴趣小组用
)可在有机合成中作氯化剂。某兴趣小组用 与HCl反应制备液态
与HCl反应制备液态 ,实验装置如图。
,实验装置如图。
① 的沸点是117℃,易挥发、易水解。
的沸点是117℃,易挥发、易水解。
② 水解反应:
水解反应: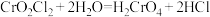
请回答:
(1)仪器X的名称是___________ 。
(2)完善虚框内的装置排序:____ 。
____→C→____→____→____→尾气处理装置
(3)尾气处理装置中最合理的是___________ 。___________ 。
(5)下列说法正确的是___________
(6)取1.60g 产品,控制pH值为6.5-10.5,滴加
产品,控制pH值为6.5-10.5,滴加 溶液至沉淀出现砖红色时,停止滴加,将沉淀经过滤、洗涤、干燥后称量为2.87g。产品的纯度为
溶液至沉淀出现砖红色时,停止滴加,将沉淀经过滤、洗涤、干燥后称量为2.87g。产品的纯度为___________ 。(结果保留3位有效数字)。
 )可在有机合成中作氯化剂。某兴趣小组用
)可在有机合成中作氯化剂。某兴趣小组用 与HCl反应制备液态
与HCl反应制备液态 ,实验装置如图。
,实验装置如图。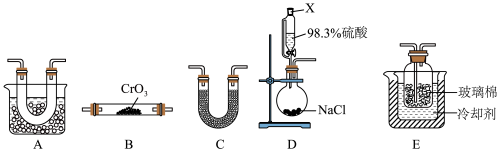
①
 的沸点是117℃,易挥发、易水解。
的沸点是117℃,易挥发、易水解。②
 水解反应:
水解反应: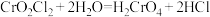
请回答:
(1)仪器X的名称是
(2)完善虚框内的装置排序:
____→C→____→____→____→尾气处理装置
(3)尾气处理装置中最合理的是
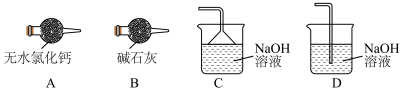
(5)下列说法正确的是___________
| A.该实验操作须在通风橱中进行 |
| B.浓硫酸在反应前可预冷却至0℃左右,以防止反应速率过快 |
| C.加入过量NaCl固体,有利于产生过量的氯化氢,可以提高铬酰氯的产率 |
| D.装置C中可盛放碱石灰 |
(6)取1.60g
 产品,控制pH值为6.5-10.5,滴加
产品,控制pH值为6.5-10.5,滴加 溶液至沉淀出现砖红色时,停止滴加,将沉淀经过滤、洗涤、干燥后称量为2.87g。产品的纯度为
溶液至沉淀出现砖红色时,停止滴加,将沉淀经过滤、洗涤、干燥后称量为2.87g。产品的纯度为
您最近一年使用:0次
名校
解题方法
2 . 科学家通过对过渡金属尖晶石氧化物(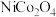 )进行氧化和还原性能优化,成功实现高性能长寿命锌—空气二次电池。
)进行氧化和还原性能优化,成功实现高性能长寿命锌—空气二次电池。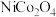 的晶胞结构如图Ⅲ,它由A、B两种小晶格交替拼接而成。已知Ni和Co的常见价态为+2、+3价,且在该物质中均只有一种化合价。
的晶胞结构如图Ⅲ,它由A、B两种小晶格交替拼接而成。已知Ni和Co的常见价态为+2、+3价,且在该物质中均只有一种化合价。
(1)写出该物质中镍离子的价电子排布图___________ ,“●”代表的元素是___________
(2)下列说法正确的是___________
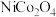 )进行氧化和还原性能优化,成功实现高性能长寿命锌—空气二次电池。
)进行氧化和还原性能优化,成功实现高性能长寿命锌—空气二次电池。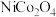 的晶胞结构如图Ⅲ,它由A、B两种小晶格交替拼接而成。已知Ni和Co的常见价态为+2、+3价,且在该物质中均只有一种化合价。
的晶胞结构如图Ⅲ,它由A、B两种小晶格交替拼接而成。已知Ni和Co的常见价态为+2、+3价,且在该物质中均只有一种化合价。
(1)写出该物质中镍离子的价电子排布图
(2)下列说法正确的是___________
| A.A和B也可以作为单独的晶胞存在 |
| B.基态原子第二电离能Cu>Zn |
C. 、 、 、 、 中S、C、Si原子杂化类型各不相同 中S、C、Si原子杂化类型各不相同 |
D.氧原子的一种激发态的价电子排布式: |
您最近一年使用:0次
3 .  是重要的化工原料,可以按如下流程充分利用
是重要的化工原料,可以按如下流程充分利用
① 具有较强的还原性
具有较强的还原性
②水溶液中, 可与
可与 反应生成
反应生成 ;
; 是一种溶于稀硝酸的白色沉淀
是一种溶于稀硝酸的白色沉淀
(1)物质A的化学式为___________ 。
(2) 是离子化合物,各原子均满足8电子稳定结构。写出
是离子化合物,各原子均满足8电子稳定结构。写出 的电子式
的电子式___________ 。
(3)写出途径Ⅰ的化学反应方程式___________ 。
(4)下列说法不正确的是___________
(5)途径Ⅱ除生成B外,另一种产物为HF,设计实验验证化合物B中含有Cl元素___________ 。写出实验过程中涉及的第一个反应的离子方程式___________ 。
 是重要的化工原料,可以按如下流程充分利用
是重要的化工原料,可以按如下流程充分利用
①
 具有较强的还原性
具有较强的还原性②水溶液中,
 可与
可与 反应生成
反应生成 ;
; 是一种溶于稀硝酸的白色沉淀
是一种溶于稀硝酸的白色沉淀(1)物质A的化学式为
(2)
 是离子化合物,各原子均满足8电子稳定结构。写出
是离子化合物,各原子均满足8电子稳定结构。写出 的电子式
的电子式(3)写出途径Ⅰ的化学反应方程式
(4)下列说法不正确的是___________
A.工业上制备硝酸时,应该将 与纯 与纯 混合反应 混合反应 |
B.结合 能力: 能力: |
C.物质A发生水解反应后可以得到 溶液 溶液 |
D.途径Ⅰ可以采用将氨水滴入NaClO溶液中的方法制备 |
(5)途径Ⅱ除生成B外,另一种产物为HF,设计实验验证化合物B中含有Cl元素
您最近一年使用:0次
名校
解题方法
4 . 工业上高炉炼铁产生的CO和CO2可以按如下流程脱除或利用。___________ 。
(2)煅烧产生的尾气可通过途径Ⅱ转化为CO2.。2分子氨和1分子CO2生产A,最终转化为尿素[CO(NH2)2];可通过途径Ⅲ转为b。
①下列说法正确的是___________ 。
A.黄铁(FeS2)可作为高炉炼铁的铁源
B.途径Ⅱ可通过实现反应转化MnO2+CO→CO2+Mn2O3
C.化合物A是一种盐
D.化合物B为CH3COONa
②尿素[CO(NH2)2]在较高温度下可以聚合成环状化合物三聚氰胺(C3H6N6),写出该反应的化学方程式___________ 。
(3)设计实验验证化合物A中含有N元素___________ ;写出实验过程中涉及的反应方程式___________ 。

已知: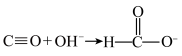 。请回答:
。请回答:
(2)煅烧产生的尾气可通过途径Ⅱ转化为CO2.。2分子氨和1分子CO2生产A,最终转化为尿素[CO(NH2)2];可通过途径Ⅲ转为b。
①下列说法正确的是
A.黄铁(FeS2)可作为高炉炼铁的铁源
B.途径Ⅱ可通过实现反应转化MnO2+CO→CO2+Mn2O3
C.化合物A是一种盐
D.化合物B为CH3COONa
②尿素[CO(NH2)2]在较高温度下可以聚合成环状化合物三聚氰胺(C3H6N6),写出该反应的化学方程式
(3)设计实验验证化合物A中含有N元素
您最近一年使用:0次
解题方法
5 . 醛酮在酸或碱的催化下生成偕二醇的反应历程如下:
下列说法不正确的是
酸催化历程: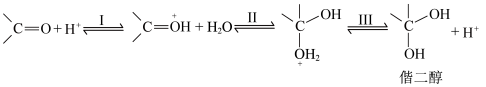
碱催化历程: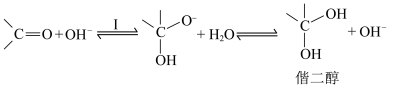
| 羰基化合物 |  |  |  |
| 平衡常数K | 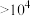 | 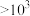 | 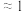 |
A.酸催化历程的步骤I中 与羰基中的O结合,增大了碳氧双键的极性 与羰基中的O结合,增大了碳氧双键的极性 |
B.对比酸和碱的催化历程可知,与羰基反应的活性: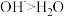 |
C.无论酸或碱催化,生成偕二醇的平衡常数: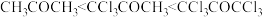 |
D.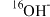 催化下, 催化下,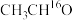 的 的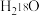 溶液中无法生成 溶液中无法生成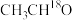 |
您最近一年使用:0次
6 . Au溶于食盐和硝酸混合液发生反应: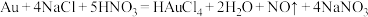 ,(已知:
,(已知: ),下列说法
),下列说法不正确 的是
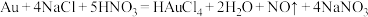 ,(已知:
,(已知: ),下列说法
),下列说法| A.Au是还原剂,HNO3是氧化剂 |
| B. HAuCl4是氧化产物,NO是还原产物 |
| C.Au消耗0.5mol得到1.5mol电子 |
| D.Au也能溶于王水(浓硝酸和浓盐酸体积比1∶3) |
您最近一年使用:0次
名校
解题方法
7 . 硫酸是重要的化工原料,属于大宗化学品。下列说法正确的是
| A.S是第三周期第ⅣA族元素 |
B.工业上用稀硫酸吸收 制备硫酸 制备硫酸 |
| C.98%浓硫酸滴在pH试纸上,先变红后变白 |
| D.酸雨中含有硫酸和亚硫酸,露置一段时间酸性变强 |
您最近一年使用:0次
8 . 7下表是醋酸电离常数与温度的关系。下列说法不正确 的是
| 温度/℃ | 0 | 30 | 50 |
 | 1.65 | 1.75 | 1.63 |
A.醋酸在水中的电离方程式: |
| B.0.1mol/L醋酸中加水稀释,醋酸和水的电离程度均增加 |
| C.醋酸溶液升温中可能涉及共价键和氢键断裂、离子水合的过程 |
| D.0~30℃电离总过程是放热的,30~50℃电离总过程是吸热的 |
您最近一年使用:0次
解题方法
9 . 一种新型短路膜电池分离 装置如下图所示。
装置如下图所示。
 装置如下图所示。
装置如下图所示。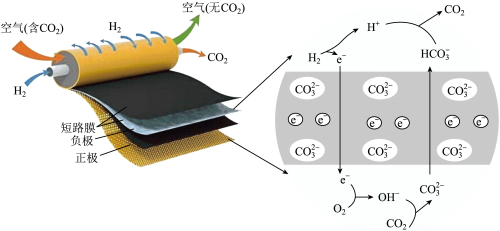
| A.短路膜既能传递阴离子,也能传递电子 |
B.电池工作过程中,正极 增大,工作结束后,短路膜中 增大,工作结束后,短路膜中 减小 减小 |
C.标准状况下,每分离出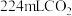 ,进出短路膜前后空气的体积差为 ,进出短路膜前后空气的体积差为 |
D.空气(含 )的流速越快, )的流速越快, 的去除率不一定越高 的去除率不一定越高 |
您最近一年使用:0次
10 .  发生如下转化。
发生如下转化。 是一种拟卤素,性质与卤素相似;
是一种拟卤素,性质与卤素相似; 和
和 均位于
均位于 族。请回答:
族。请回答:
(1) 和
和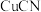 中热稳定性更好的是
中热稳定性更好的是___________ 。写出溶液A中的所有的阴离子___________ 。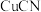 转化为
转化为 的过程中,需适当控制反应温度,反应温度不能过高,原因是
的过程中,需适当控制反应温度,反应温度不能过高,原因是___________ 。
(2)下列说法正确的是___________。
(3)设计实验检验白色沉淀C中的组成元素___________ 。写出检验白色沉淀C中的金属元素所发生的离子方程式___________ 。
 发生如下转化。
发生如下转化。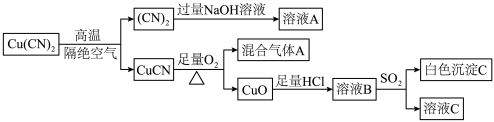
 是一种拟卤素,性质与卤素相似;
是一种拟卤素,性质与卤素相似; 和
和 均位于
均位于 族。请回答:
族。请回答:(1)
 和
和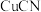 中热稳定性更好的是
中热稳定性更好的是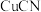 转化为
转化为 的过程中,需适当控制反应温度,反应温度不能过高,原因是
的过程中,需适当控制反应温度,反应温度不能过高,原因是(2)下列说法正确的是___________。
A. 的空间构型为直线形 的空间构型为直线形 | B.白色沉淀C可能溶于氨水 |
C. 在混合气体A中燃烧生成三种固体 在混合气体A中燃烧生成三种固体 | D.溶液B的颜色一定呈蓝色 |
(3)设计实验检验白色沉淀C中的组成元素
您最近一年使用:0次



