1 . 某钒制品厂钙法提钒工艺产生的酸性废水中MnSO4和CaSO4的含量较高,且含有少量的Al3+。以下是采用化学沉淀法处理钙法提钒废水并制备高纯MnCO3的生产工艺流程。请回答下列问题:
(1)滤渣I为___________ 。
(2)步骤2中加少量CaC2O4的目的是___________ ,有利于滤渣Ⅱ的析出。加入的试剂X最合理的是___________ (填标号)。
A.H2C2O4 B.NH4HC2O4 C.(NH4)2C2O4
(3)步骤3中溶液pH、反应时间与MnCO3的产率的关系如图所示。___________ 。
②请从平衡移动原理角度解释:pH过小导致MnCO3产率降低的原因___________ 。
③最佳pH条件下,保持溶液中 ,此时溶液中
,此时溶液中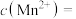
___________ mol/L。[25℃时, ,
, ,
, 。]
。]
(4)碳酸锰在不同条件下煅烧可制得不同锰的氧化物晶体。某种MnOx晶体的晶胞如下图所示,碳酸锰煅烧生成该晶体的化学方程式为___________ 。已知该晶胞底面是边长为acm的正方形,以晶胞参数为单位长度建立坐标系,A、B、C处的原子坐标参数分别为(0,0,0)、 、
、 ,则Mn与O形成化学键的键长为
,则Mn与O形成化学键的键长为___________ cm(用含a、m的代数式表示)。

(1)滤渣I为
(2)步骤2中加少量CaC2O4的目的是
A.H2C2O4 B.NH4HC2O4 C.(NH4)2C2O4
(3)步骤3中溶液pH、反应时间与MnCO3的产率的关系如图所示。

②请从平衡移动原理角度解释:pH过小导致MnCO3产率降低的原因
③最佳pH条件下,保持溶液中
 ,此时溶液中
,此时溶液中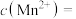
 ,
, ,
, 。]
。](4)碳酸锰在不同条件下煅烧可制得不同锰的氧化物晶体。某种MnOx晶体的晶胞如下图所示,碳酸锰煅烧生成该晶体的化学方程式为
 、
、 ,则Mn与O形成化学键的键长为
,则Mn与O形成化学键的键长为
您最近一年使用:0次
名校
2 . 某化学兴趣小组在阴暗的地方用如图所示装置探究CH4与Cl2的反应,灯泡接通电源后,开始实验。下列说法错误的是

| A.软管内会发生取代反应,生成物可能有5种 |
| B.透明软管内气体颜色会逐渐变浅,透明软管的体积会缩小直至完全凹瘪 |
| C.软管内会有油状液滴产生 |
| D.充分反应后,打开K1,导管口可能会有白雾出现 |
您最近一年使用:0次
今日更新
|
224次组卷
|
3卷引用:期末押题卷01-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(辽宁专用)
(已下线)期末押题卷01-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(辽宁专用)河北省保定市部分示范性高中2023-2024学年高一下学期5月期中考试化学试题河北省保定市定州市第二中学2023-2024学年高一下学期5月月考化学试题
名校
3 . 利用介孔限域催化温室气体 加氢制甲醇,再通过甲醇制备燃料和化工原料等,是解决能源问题与实现双碳目标的主要技术之一,反应如下:
加氢制甲醇,再通过甲醇制备燃料和化工原料等,是解决能源问题与实现双碳目标的主要技术之一,反应如下:
i.
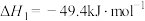
ii.

(1)稳定单质的焓(H)为0,有关物质的焓如表所示,

___________  。
。
(2)在5.0MPa下,将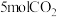 和
和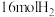 在
在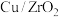 催化剂作用下进行反应i和ii.平衡时
催化剂作用下进行反应i和ii.平衡时 和CO选择性S[S(
和CO选择性S[S( 或CO)
或CO)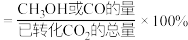 ]及
]及 的转化率a随温度的变化如图所示。
的转化率a随温度的变化如图所示。 的转化率的曲线是
的转化率的曲线是___________ (填“x”“y”或“z”)。
②250℃时,平衡体系共有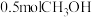 ,则
,则 的平衡转化率=
的平衡转化率=___________ ,反应i的
___________ (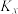 是以组分体积分数代替物质的量浓度表示的平衡常数,列计算式)。
是以组分体积分数代替物质的量浓度表示的平衡常数,列计算式)。
③p、q两点反应i的正反应速率大小:
___________ 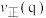 。(填“>”“=”或“<”)
。(填“>”“=”或“<”)
(3)若只发生反应ii,反应的速率方程为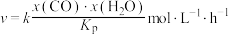 ,其中x表示相应气体的物质的量分数,
,其中x表示相应气体的物质的量分数, 为平衡常数(用平衡分压代替平衡浓度计算),k为反应的速率常数。已知平衡后
为平衡常数(用平衡分压代替平衡浓度计算),k为反应的速率常数。已知平衡后 ,此时反应ii的速率
,此时反应ii的速率
___________  (用含k的代数式表示)。
(用含k的代数式表示)。
(4)我国科学者又进一步研究了在 催化剂上
催化剂上 加氢制甲醇的机理;其主反应历程如图所示
加氢制甲醇的机理;其主反应历程如图所示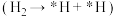 。下列说法正确的是___________(填字母)。
。下列说法正确的是___________(填字母)。
 加氢制甲醇,再通过甲醇制备燃料和化工原料等,是解决能源问题与实现双碳目标的主要技术之一,反应如下:
加氢制甲醇,再通过甲醇制备燃料和化工原料等,是解决能源问题与实现双碳目标的主要技术之一,反应如下:i.

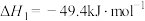
ii.


(1)稳定单质的焓(H)为0,有关物质的焓如表所示,
| 物质 |  |  |  |
焓 | -394 | -111 | -242 |

 。
。(2)在5.0MPa下,将
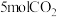 和
和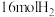 在
在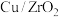 催化剂作用下进行反应i和ii.平衡时
催化剂作用下进行反应i和ii.平衡时 和CO选择性S[S(
和CO选择性S[S( 或CO)
或CO)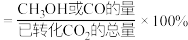 ]及
]及 的转化率a随温度的变化如图所示。
的转化率a随温度的变化如图所示。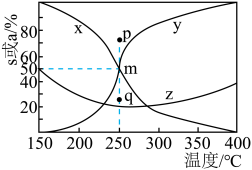
 的转化率的曲线是
的转化率的曲线是②250℃时,平衡体系共有
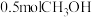 ,则
,则 的平衡转化率=
的平衡转化率=
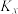 是以组分体积分数代替物质的量浓度表示的平衡常数,列计算式)。
是以组分体积分数代替物质的量浓度表示的平衡常数,列计算式)。③p、q两点反应i的正反应速率大小:

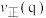 。(填“>”“=”或“<”)
。(填“>”“=”或“<”)(3)若只发生反应ii,反应的速率方程为
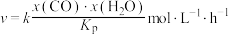 ,其中x表示相应气体的物质的量分数,
,其中x表示相应气体的物质的量分数, 为平衡常数(用平衡分压代替平衡浓度计算),k为反应的速率常数。已知平衡后
为平衡常数(用平衡分压代替平衡浓度计算),k为反应的速率常数。已知平衡后 ,此时反应ii的速率
,此时反应ii的速率
 (用含k的代数式表示)。
(用含k的代数式表示)。(4)我国科学者又进一步研究了在
 催化剂上
催化剂上 加氢制甲醇的机理;其主反应历程如图所示
加氢制甲醇的机理;其主反应历程如图所示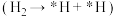 。下列说法正确的是___________(填字母)。
。下列说法正确的是___________(填字母)。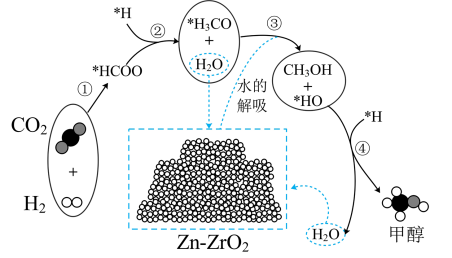
| A.二氧化碳加氢制甲醇的过程中原子利用率达100% |
| B.带*标记的物质是该反应历程中的中间产物 |
C.第④步的反应式为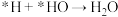 |
D.反应历程中只有 键断裂,没有 键断裂,没有 键断裂 键断裂 |
您最近一年使用:0次
昨日更新
|
242次组卷
|
4卷引用:辽宁省协作校2023-2024学年高三下学期三模化学试题
4 . 硫酸钴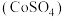 主要用于电镀、碱性电池、生产含钴颜料和其他钴产品,可利用
主要用于电镀、碱性电池、生产含钴颜料和其他钴产品,可利用 与葡萄糖制备,反应的化学方程式为
与葡萄糖制备,反应的化学方程式为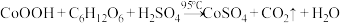 (未配平)。设
(未配平)。设 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是
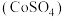 主要用于电镀、碱性电池、生产含钴颜料和其他钴产品,可利用
主要用于电镀、碱性电池、生产含钴颜料和其他钴产品,可利用 与葡萄糖制备,反应的化学方程式为
与葡萄糖制备,反应的化学方程式为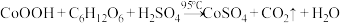 (未配平)。设
(未配平)。设 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是A.氧化性: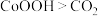 |
B.氧化剂与还原剂的物质的量之比为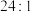 |
C.生成 (标准状况) (标准状况) 时,转移电子数为 时,转移电子数为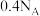 |
D. 葡萄糖中含有 葡萄糖中含有 键的数目为 键的数目为 |
您最近一年使用:0次
5 . X、Y、Z、M为原子序数依次增大的前四周期元素。X、Y、Z位于同一周期,X的基态原子含有3个能级,且每个能级所含的电子数相同,Y的第一电离能大于Z的第一电离能,M的合金是我国使用最早的合金。下列说法错误的是
| A.Y与Z能形成五种化合物 |
B.简单氢化物的键角: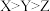 |
| C.X的最高价氧化物为非极性分子 |
| D.基态M原子的未成对电子所在轨道的电子云轮廓图为球形 |
您最近一年使用:0次
6 . 米酒是一种传统的风味小吃。下列说法错误的是
| A.酿米酒的原材料的主要成分是淀粉 |
| B.酿米酒过程只发生了水解反应 |
| C.酿米酒需要添加酒曲作催化剂 |
D.米酒存放时间越长, 越低 越低 |
您最近一年使用:0次
7 . 化学与生产、生活息息相关。下列说法错误的是
| A.推广使用可在自然界降解的聚乳酸作食品外包装材料 |
| B.鼓励分类回收、再利用生活垃圾和废弃物 |
C.开发高效催化剂有利于环氧乙烷和 发生缩聚反应合成高分子材料 发生缩聚反应合成高分子材料 |
| D.推广使用新能源汽车可有效减少碳排放 |
您最近一年使用:0次
8 . 物质结构决定其性质。下列有关物质结构和性质的比较中正确的是
A.键角: 中 中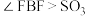 中 中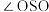 |
B. 和 和 的 的 模型名称都是正四面体形 模型名称都是正四面体形 |
| C.沸点:邻羟基苯甲胺>对羟基苯甲胺 |
D.杂化轨道中s所占百分率: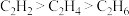 |
您最近一年使用:0次
名校
解题方法
9 . 为实现“碳中和”“碳达峰”,碳的循环利用是重要措施。利用氢气和CO反应生成甲烷,涉及的反应如下:
i.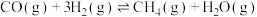

ii.

iii.

回答下列问题:
(1)在25℃和101kPa下, 转变为
转变为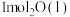 时放出44.0kJ热量,
时放出44.0kJ热量, 的燃烧热为
的燃烧热为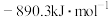 ,CO的燃烧热为
,CO的燃烧热为 ,
, 的燃烧热为
的燃烧热为 ,则
,则
________  。
。
(2)一定温度下,在恒容的密闭容器中进行上述反应,平衡时CO的转化率及 的选择性随
的选择性随 变化的情况如图所示[已知
变化的情况如图所示[已知 的选择性
的选择性 ]。
]。 选择性变化的曲线是
选择性变化的曲线是________ (填“甲”或“乙”),保持 不变,曲线甲由B点达到A点需要的条件为
不变,曲线甲由B点达到A点需要的条件为________ 。
②相同温度下,向恒容容器内加入 和1molCO,初始压强为10MPa,平衡时
和1molCO,初始压强为10MPa,平衡时 的物质的量为
的物质的量为________ mol,反应ii的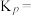
________ (保留小数点后一位)。
(3) 催化加氢制甲醇也是碳循环的重要途径。
催化加氢制甲醇也是碳循环的重要途径。 在某催化剂表面与氢气作用制备甲醇的反应机理如图所示。催化循环中产生的中间体微粒共
在某催化剂表面与氢气作用制备甲醇的反应机理如图所示。催化循环中产生的中间体微粒共________ 种, 催化加氢制甲醇总反应的化学方程式为
催化加氢制甲醇总反应的化学方程式为________ 。
i.
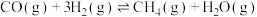

ii.


iii.


回答下列问题:
(1)在25℃和101kPa下,
 转变为
转变为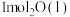 时放出44.0kJ热量,
时放出44.0kJ热量, 的燃烧热为
的燃烧热为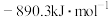 ,CO的燃烧热为
,CO的燃烧热为 ,
, 的燃烧热为
的燃烧热为 ,则
,则
 。
。(2)一定温度下,在恒容的密闭容器中进行上述反应,平衡时CO的转化率及
 的选择性随
的选择性随 变化的情况如图所示[已知
变化的情况如图所示[已知 的选择性
的选择性 ]。
]。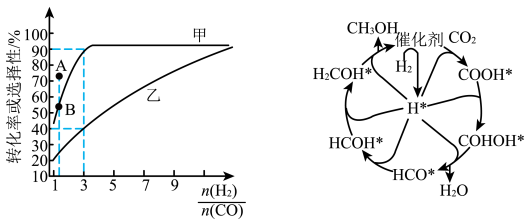
 选择性变化的曲线是
选择性变化的曲线是 不变,曲线甲由B点达到A点需要的条件为
不变,曲线甲由B点达到A点需要的条件为②相同温度下,向恒容容器内加入
 和1molCO,初始压强为10MPa,平衡时
和1molCO,初始压强为10MPa,平衡时 的物质的量为
的物质的量为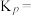
(3)
 催化加氢制甲醇也是碳循环的重要途径。
催化加氢制甲醇也是碳循环的重要途径。 在某催化剂表面与氢气作用制备甲醇的反应机理如图所示。催化循环中产生的中间体微粒共
在某催化剂表面与氢气作用制备甲醇的反应机理如图所示。催化循环中产生的中间体微粒共 催化加氢制甲醇总反应的化学方程式为
催化加氢制甲醇总反应的化学方程式为
您最近一年使用:0次
名校
10 . 电石渣的主要成分为 ,含少量的
,含少量的 、
、 和C等杂质。从中回收制备高纯碳酸钙的工艺流程如下。已知:浸出液的金属阳离子只有
和C等杂质。从中回收制备高纯碳酸钙的工艺流程如下。已知:浸出液的金属阳离子只有 。
。
 ,含少量的
,含少量的 、
、 和C等杂质。从中回收制备高纯碳酸钙的工艺流程如下。已知:浸出液的金属阳离子只有
和C等杂质。从中回收制备高纯碳酸钙的工艺流程如下。已知:浸出液的金属阳离子只有 。
。
| A.本流程中可以循环使用的物质是氨气和氯化铵 |
| B.系列操作为洗涤和干燥 |
C.已知: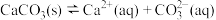 ,则 ,则 属于弱电解质 属于弱电解质 |
D.滤渣1的成分为 、 、 和C 和C |
您最近一年使用:0次
7日内更新
|
126次组卷
|
2卷引用:辽宁省大连市2023-2024学年高三下学期第二次模拟考试化学试卷



