解题方法
1 . 现代社会的一切活动都离不开能量,化学反应在发生物质变化的同时伴随能量的变化。回答下列问题:
(1)下列反应中,属于放热反应的是___________(填字母)。
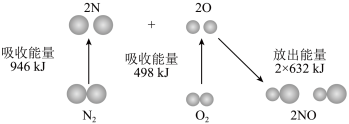
(2)下图为1molN2(g)和1molO2(g)充分反应生成2molNO(g)的能量变化图。若断裂1molNO分子中的化学键,需要吸收___________ 能量。该反应中反应物所具有的总能量___________ (填“高于”“低于”或“等于”)生成物所具有的总能量。
(3)某实验小组为了探究化学能与热能的转化,设计了如图所示的三套实验装置:
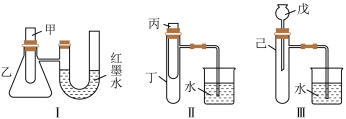
①某同学选用装置I进行实验(实验前U形管里液面左右相平),在甲试管中加入了适量Ba(OH)2溶液与稀硫酸,U形管中可观察到的现象是___________ 。
②上述3个装置中,能探究“铜与浓硝酸的反应是吸热反应还是放热反应”的装置是_______ (填装置序号)。
(1)下列反应中,属于放热反应的是___________(填字母)。
| A.盐酸与NaHCO3 |
| B.Ba(OH)2·8H2O晶体和NH4Cl晶体反应 |
| C.Zn和稀硫酸反应 |
| D.KOH溶液和稀硝酸反应 |
(2)下图为1molN2(g)和1molO2(g)充分反应生成2molNO(g)的能量变化图。若断裂1molNO分子中的化学键,需要吸收

(3)某实验小组为了探究化学能与热能的转化,设计了如图所示的三套实验装置:

①某同学选用装置I进行实验(实验前U形管里液面左右相平),在甲试管中加入了适量Ba(OH)2溶液与稀硫酸,U形管中可观察到的现象是
②上述3个装置中,能探究“铜与浓硝酸的反应是吸热反应还是放热反应”的装置是
您最近一年使用:0次
解题方法
2 . 将铁片和银片用导线连接置于同一稀盐酸溶液中,经过一段时间后,下列各项叙述正确的是
| A.负极有Cl2逸出,正极有H2逸出 | B.负极附近Cl-的浓度减小 |
| C.正极附近Cl-浓度逐渐增大 | D.溶液中Cl-的浓度基本不变 |
您最近一年使用:0次
3 . 已知氨可以与灼热的氧化铜反应得到氮气和金属铜,用如图中的装置可以实现该反应。实验时C中粉末逐渐变为红色,D中出现无色液体。下列有关说法正确的是
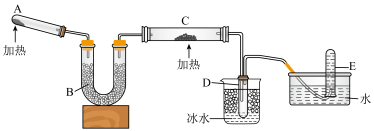

| A.C中氧化剂和还原剂的物质的量之比为3∶2 |
| B.B中加入的物质可以是碱石灰或无水氯化钙 |
| C.D中液体可以使干燥的红色石蕊试纸变蓝 |
| D.A中加入的固体,可以是NH4HCO3或NH4Cl |
您最近一年使用:0次
4 . N2O俗称“笑气”,早期被用于牙科手术的麻醉,是人类最早应用于医疗的麻醉剂之一、反应:3CO+2NO2=3CO2+N2O能产生N2O。下列关于N2O的说法一定正确的是
| A.上述反应中,每消耗2molNO2,就会生成22.4LN2O(标准状况下测定) |
| B.N2O有氧化性,且为HNO2的酸性氧化物 |
| C.当生成3molCO2时,转移的电子数为6NA |
| D.N2O使用时必须少量,否则会与人体血红蛋白结合,使人中毒 |
您最近一年使用:0次
解题方法
5 . 甲醇、氧气和强碱溶液作电解质的手机电池中存在反应2CH3OH+3O2+4OH- 2
2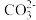 +6H2O,有关说法正确的是
+6H2O,有关说法正确的是
 2
2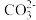 +6H2O,有关说法正确的是
+6H2O,有关说法正确的是A.放电时,负极电极反应式:CH3OH+8OH--6e-= +6H2O +6H2O |
| B.放电时,CH3OH参与反应的电极为正极 |
| C.标准状况下,通入5.6L完全反应有1mol电子转移 |
| D.充电时,电解质溶液的酸性逐渐增强 |
您最近一年使用:0次
6 . 由粗SiO2制备纯SiO2的流程如图所示,下列说法不正确的是
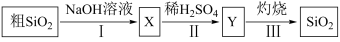

| A.X应存放在玻璃塞试剂瓶中 |
| B.步骤II的反应是Na2SiO3+H2SO4=H2SiO3↓+Na2SO4 |
| C.步骤II中的稀硫酸可用CO2替代 |
| D.若在实验室中完成步骤III,一般在蒸发皿中进行 |
您最近一年使用:0次
7 . 甲、乙两个研究小组决定用实验探究的方法证明化学反应具有一定的限度,在一定条件下会达到“平衡状态”。
I.甲组:取5mL0.1mol·L-1的KI溶液于试管中,滴加0.1mol·L-1的FeCl3溶液2mL,发生如下反应:2I-+2Fe3+=2Fe2++I2.为了证明该反应具有一定的限度,他们设计了如下实验:①取少量反应液,滴加AgNO3溶液,发现有少量的黄色沉淀(AgI)生成,证明反应物没有反应完全;②再取少量反应液,加入少量CCl4,振荡,发现CCl4显浅紫色,证明萃取到了I2,即有I2生成。结合①②的结论,他们得出结论:该反应具有一定的可逆性,在一定条件下会达到反应限度。
(1)指导老师指出上述实验中①不合理,你认为原因是___________ ,改进的方法是___________ 。
(2)有人认为步骤②适合检验生成I2较多的情况,还有一种简单的方法可以灵敏地检验是否生成了I2,这种方法是___________ 。
II.乙组:取4mL1mol·L-1的CaCl2溶液于试管中,发现滴入1mol·L-1的Na2SO4溶液6mL后已经观察不到有白色沉淀产生了,发生的反应是Na2SO4+CaCl2=CaSO4↓+2NaCl。
(3)请设计一个简单的实验,确认上述反应具有可逆性和反应限度,简要列出实验步骤和结论:___________ 。
I.甲组:取5mL0.1mol·L-1的KI溶液于试管中,滴加0.1mol·L-1的FeCl3溶液2mL,发生如下反应:2I-+2Fe3+=2Fe2++I2.为了证明该反应具有一定的限度,他们设计了如下实验:①取少量反应液,滴加AgNO3溶液,发现有少量的黄色沉淀(AgI)生成,证明反应物没有反应完全;②再取少量反应液,加入少量CCl4,振荡,发现CCl4显浅紫色,证明萃取到了I2,即有I2生成。结合①②的结论,他们得出结论:该反应具有一定的可逆性,在一定条件下会达到反应限度。
(1)指导老师指出上述实验中①不合理,你认为原因是
(2)有人认为步骤②适合检验生成I2较多的情况,还有一种简单的方法可以灵敏地检验是否生成了I2,这种方法是
II.乙组:取4mL1mol·L-1的CaCl2溶液于试管中,发现滴入1mol·L-1的Na2SO4溶液6mL后已经观察不到有白色沉淀产生了,发生的反应是Na2SO4+CaCl2=CaSO4↓+2NaCl。
(3)请设计一个简单的实验,确认上述反应具有可逆性和反应限度,简要列出实验步骤和结论:
您最近一年使用:0次
解题方法
8 . 下列关于氢硫酸、亚硫酸、硫酸的叙述正确的是
| A.它们都是酸,因此彼此不发生反应 |
| B.只有亚硫酸可以露置在空气中,其他酸不可以 |
| C.鉴别三种酸溶液时,只要分别滴加BaCl2溶液即可 |
| D.它们都是二元酸,酸性:H2S<H2SO3<H2SO4 |
您最近一年使用:0次
解题方法
9 . 为了说明影响化学反应快慢的因素,甲、乙、丙、丁四位学生分别设计了如下A~D四个实验,你认为结论不正确的是
| A.相同温度下,将大小、形状相同的镁条和铝条与相同浓度的稀盐酸反应时,两者速率一样大 |
| B.在相同条件下,等质量的大理石块和大理石粉与相同的盐酸反应,大理石粉反应快 |
| C.将浓硝酸分别放在冷暗处和强光照射下,会发现光照可以加快浓硝酸的分解 |
| D.两支试管中分别加入相同质量的氯酸钾,其中一支试管中再加入少量二氧化锰,同时加热,产生氧气的快慢不同 |
您最近一年使用:0次
10 . 如下反应条件的控制中,不恰当的是
| A.为增大H2O2的分解速率而增大H2O2的浓度 |
| B.为防止火灾,在面粉厂、加油站等场所要严禁烟火 |
| C.为增大KClO3的分解速率而加入MnO2 |
| D.为增大H2O2的分解速率而把反应容器放到冷水中冷却 |
您最近一年使用:0次



