解题方法
1 . 配制一定物质的量浓度的NaCl溶液过程的部分示意图如下:
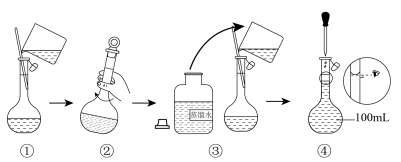
| A.操作①中用玻璃棒引流将NaCl溶液注入100mL容量瓶 |
| B.操作②轻轻摇动容量瓶,使溶液混合均匀 |
| C.操作③用蒸馏水洗涤烧杯内壁和玻璃棒2~3次,并将洗涤液注入容量瓶 |
| D.操作④若仰视容量瓶上的刻度线,最后配成的溶液中溶质的实际浓度偏大 |
您最近一年使用:0次
解题方法
2 . 下列事实不能用“组成和结构决定性质”来解释的是
| A.常见的一些合金的硬度比其成分金属的大 |
| B.高碳钢、中碳钢和低碳钢的性能有很大差别 |
| C.测试工程师依据组成元素及含量确定不锈钢等级 |
| D.铝和铁是地壳中含量最多的二种金属元素 |
您最近一年使用:0次
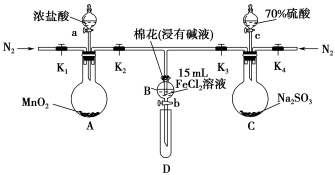
3 . 某化学兴趣小组为验证Cl2、Fe3+、SO2三者氧化性强弱顺序,按照如图所示的装置(夹持装置和A中加热装置已省略)进行探究。
 .打开止水夹K1、K2、K3、K4,通入N2一段时间,关闭K1、K3、K4,向B中加入15 mL新制FeCl2溶液。
.打开止水夹K1、K2、K3、K4,通入N2一段时间,关闭K1、K3、K4,向B中加入15 mL新制FeCl2溶液。
 .打开活塞a,向容器A中滴加适量浓盐酸,加热A,当B中溶液变黄时,停止加热,关闭K2。
.打开活塞a,向容器A中滴加适量浓盐酸,加热A,当B中溶液变黄时,停止加热,关闭K2。
 .打开活塞b,待约2 mL溶液流入D试管,关闭活塞b,检验D试管溶液中的阳离子。
.打开活塞b,待约2 mL溶液流入D试管,关闭活塞b,检验D试管溶液中的阳离子。
 .打开K3和活塞c,向C中滴加70%硫酸,一段时间后关闭K3。
.打开K3和活塞c,向C中滴加70%硫酸,一段时间后关闭K3。
 .另取试管E,打开活塞b,待约2 mL溶液流入E试管,关闭活塞b,检验E试管溶液中的阴离子。
.另取试管E,打开活塞b,待约2 mL溶液流入E试管,关闭活塞b,检验E试管溶液中的阴离子。
回答下列问题:
(1)实验开始前需进行的操作是___________ 。
(2)步骤 中通入N2的目的是
中通入N2的目的是___________ 。
(3)步骤 中溶液变黄的原因是
中溶液变黄的原因是___________ 。
(4)步骤 ,检验D试管溶液中是否含有Fe2+,不能选用酸性KMnO4溶液的理由
,检验D试管溶液中是否含有Fe2+,不能选用酸性KMnO4溶液的理由___________ (请用离子方程式表示)。
(5)步骤 和步骤
和步骤 的检验结果如下:
的检验结果如下:
则Cl2、Fe3+、SO2三者氧化性强弱顺序为 ___________ 。
(6)请设计实验方案检验E试管溶液中的SO :
:___________ 。
 .打开止水夹K1、K2、K3、K4,通入N2一段时间,关闭K1、K3、K4,向B中加入15 mL新制FeCl2溶液。
.打开止水夹K1、K2、K3、K4,通入N2一段时间,关闭K1、K3、K4,向B中加入15 mL新制FeCl2溶液。 .打开活塞a,向容器A中滴加适量浓盐酸,加热A,当B中溶液变黄时,停止加热,关闭K2。
.打开活塞a,向容器A中滴加适量浓盐酸,加热A,当B中溶液变黄时,停止加热,关闭K2。 .打开活塞b,待约2 mL溶液流入D试管,关闭活塞b,检验D试管溶液中的阳离子。
.打开活塞b,待约2 mL溶液流入D试管,关闭活塞b,检验D试管溶液中的阳离子。 .打开K3和活塞c,向C中滴加70%硫酸,一段时间后关闭K3。
.打开K3和活塞c,向C中滴加70%硫酸,一段时间后关闭K3。 .另取试管E,打开活塞b,待约2 mL溶液流入E试管,关闭活塞b,检验E试管溶液中的阴离子。
.另取试管E,打开活塞b,待约2 mL溶液流入E试管,关闭活塞b,检验E试管溶液中的阴离子。回答下列问题:
(1)实验开始前需进行的操作是
(2)步骤
 中通入N2的目的是
中通入N2的目的是(3)步骤
 中溶液变黄的原因是
中溶液变黄的原因是(4)步骤
 ,检验D试管溶液中是否含有Fe2+,不能选用酸性KMnO4溶液的理由
,检验D试管溶液中是否含有Fe2+,不能选用酸性KMnO4溶液的理由(5)步骤
 和步骤
和步骤 的检验结果如下:
的检验结果如下:步骤 ,D试管溶液中含有的阳离子 ,D试管溶液中含有的阳离子 | 既有Fe3+,又有Fe2+ |
步骤 ,E试管溶液中含有的阴离子 ,E试管溶液中含有的阴离子 | 有SO |
(6)请设计实验方案检验E试管溶液中的SO
 :
:
您最近一年使用:0次
名校
解题方法
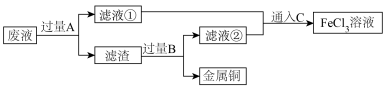
4 . 电子工业常用30%的氯化铁溶液腐蚀覆在绝缘板上的铜箔,制作印刷电路板。为了使用后的“废液(主要成份为FeCl3、FeCl2和CuCl2)”得到充分利用,设计如下的实验方案:___________ ,B的物质为___________ 。
(2)加入过量A发生的主要反应化学方程式:___________ 、___________ 。
(3)通入C发生反应的离子方程式为___________ 。
(2)加入过量A发生的主要反应化学方程式:
(3)通入C发生反应的离子方程式为
您最近一年使用:0次
7日内更新
|
17次组卷
|
2卷引用:浙江省丽水市2023-2024学年高一上学期期末检测化学试题
5 . 下图为元素周期表的一部分,请参考元素①~⑥在表中的位置,请回答:
(1)元素①的符号___________ ,在周期表中的位置是___________ 。
(2)元素②和③的最高价氧化物的水化物相互反应的化学方程式___________ 。
(3)元素④和⑤的最高价氧化物的水化物酸性由强到弱的顺序为___________ (填化学式)。
(4)写出能证明元素金属性⑥>②的实验事实:___________ (写出一种即可)。
| 族 周期 |  A A | 0 | ||||||
| 1 |  A A |  A A |  A A |  A A |  A A |  A A | ||
| 2 | ① | |||||||
| 3 | ② | ③ | ④ | ⑤ | ||||
| 4 | ⑥ | |||||||
(2)元素②和③的最高价氧化物的水化物相互反应的化学方程式
(3)元素④和⑤的最高价氧化物的水化物酸性由强到弱的顺序为
(4)写出能证明元素金属性⑥>②的实验事实:
您最近一年使用:0次
解题方法
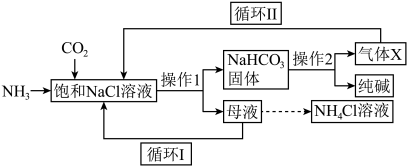
6 . 我国化学家侯德榜先生提出的联合制碱法得到世界各国的认可,主要工业流程可简要表示如图:
(1)“操作1”的名称:___________ 。
(2)“循环 ”的物质为:
”的物质为:___________ 。
(3)“操作2”的化学反应方程式:___________ 。
(4)流程中产生NaHCO3固体的化学方程式:___________ 。
(5)下列说法不正确的是___________。
(1)“操作1”的名称:
(2)“循环
 ”的物质为:
”的物质为:(3)“操作2”的化学反应方程式:
(4)流程中产生NaHCO3固体的化学方程式:
(5)下列说法不正确的是___________。
| A.由“操作1”可知,在相同温度下碳酸氢钠溶解度比NaCl大 |
| B.侯德榜联合制碱法得到的主要产品是烧碱,副产物是NH4Cl |
| C.应该向“饱和NaCl溶液”中先通入足量NH3,再通入足量CO2 |
D.使原料氯化钠的利用率从70%提高到90%以上,主要设计了“循环 ” ” |
您最近一年使用:0次
7 . 按要求完成下列问题:
(1)CuSO4·5H2O的俗名:___________ ;硫黄的化学式:___________ 。
(2)NaHSO4在水溶液中的电离方程式___________ 。
(3)钠与水反应的离子方程式___________ 。
(1)CuSO4·5H2O的俗名:
(2)NaHSO4在水溶液中的电离方程式
(3)钠与水反应的离子方程式
您最近一年使用:0次
解题方法
8 . 下列实验操作、现象、结论都正确的是
| 选项 | 实验操作与现象 | 结论 |
| A | 把温度计插入滴加了几滴水的碳酸氢钠固体中,温度计读数下降 | 碳酸氢钠溶解放热 |
| B | 用玻璃棒蘸取新制氯水点在pH试纸上,试纸变白 | Cl2分子具有漂白性 |
| C | 向分别装有盐酸和氢氧化钠溶液的两支试管中,各加入一小块铝片,两支试管均产生气泡 | 铝片与酸、碱都能反应 |
| D | 向二氧化硫的水溶液中滴入1~2滴品红溶液,振荡,溶液变为无色 | 二氧化硫有强氧化性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
9 . 高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用离子方程式表示为:2Fe3++3ClO-+10OH-=2FeO +3Cl-+5H2O,对于该反应下列说法正确的是
+3Cl-+5H2O,对于该反应下列说法正确的是
 +3Cl-+5H2O,对于该反应下列说法正确的是
+3Cl-+5H2O,对于该反应下列说法正确的是| A.该反应利用了ClO-的还原性 |
| B.该反应中Fe3+被还原 |
| C.氧化剂与还原剂的物质的量之比为2:3 |
| D.制备0.1mol Na2FeO4,转移的电子数为0.3NA |
您最近一年使用:0次
10 . 某合金15 g与足量稀硫酸完全反应,产生标准状况下的H2 11.2 L,此合金的主要组成可能为
| A.Mg和Al | B.Fe和Cu | C.Fe和Al | D.Fe和C |
您最近一年使用:0次



