解题方法
1 . 回答下列问题。
(1)基态N原子的电子排布式为___________ 。基态P原子中,电子占据的最高能级原子轨道形状为___________ 。
(2)H2O中心原子杂化轨道类型为___________ ,说明H2O沸点大于H2S的原因___________ 。
(3)基态Ca原子价层电子由4s2状态变化为4s14p1状态所得原子光谱为___________ (填“发射”或“吸收”)光谱。
(4)下列氧原子电子排布图表示的状态中,能量最高的是___________ (填标号,下同),能量最低的是___________ 。
A.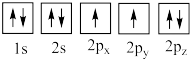 B.
B.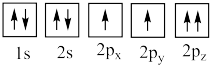
C. D.
D.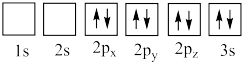
(1)基态N原子的电子排布式为
(2)H2O中心原子杂化轨道类型为
(3)基态Ca原子价层电子由4s2状态变化为4s14p1状态所得原子光谱为
(4)下列氧原子电子排布图表示的状态中,能量最高的是
A.
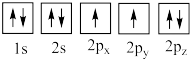 B.
B.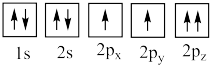
C.
 D.
D.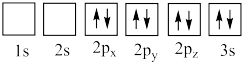
您最近一年使用:0次
2024-03-22更新
|
486次组卷
|
2卷引用:海南中学白沙学校2022-2023学年高二下学期期末考试化学试题
2 . A、B、C、D、E、F、G均为有机物,其中A是用来衡量一个国家石油化工发展水平的标志性物质,它们之间有下图转化关系。已知醛基在氧气中容易被氧化成羧基,请回答下列问题
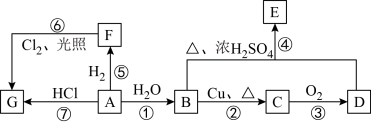
(1)A的结构简式为___________ ,D中官能团名称是___________ 。
(2)F→G的反应类型为___________ ,A发生加聚反应产物的名称是___________ 。
(3)写出下列编号对应的化学方程式:
②___________ 。
④___________ 。
(4)与B互为同分异构体的结构简式为___________ 。
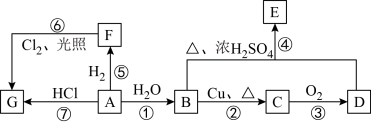
(1)A的结构简式为
(2)F→G的反应类型为
(3)写出下列编号对应的化学方程式:
②
④
(4)与B互为同分异构体的结构简式为
您最近一年使用:0次
3 . 铁、铜及其化合物在日常生产、生活中有着广泛的应用。回答下列问题:
(1)基态Fe原子的价层电子的电子排布图为___________ 。
(2)三氯化铁常温下为固体,熔点282℃,沸点315℃,在300℃以上易升华。易溶于水,也易溶于乙醚、丙酮等有机溶剂。在蒸气中也容易双聚,据此判断三氯化铁晶体为___________ (填“分子晶体”或“离子晶体”)。
(3)(NH4)2Fe(SO4)2∙6H2O俗称摩尔盐,其阴离子 的空间构型为
的空间构型为___________ 。
(4)Fe(CO)5可用作催化剂、汽油抗爆剂等,其分子中σ键和π键的数目之比为___________ 。CO的沸点高于N2的原因是___________ 。
(5)CuCl2和CuCl是铜的两种氯化物。
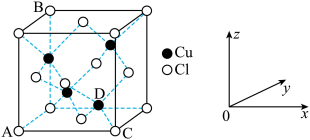
①图中表示的是___________ (填“CuCl2”或“CuCl”)的晶胞。
②原子坐标参数可用来表示晶胞内各原子的相对位置,图中各原子坐标参数A为 (0,0,0);B为(0,1,1);C为(1,0,0);则D原子的坐标参数为___________ 。
(1)基态Fe原子的价层电子的电子排布图为
(2)三氯化铁常温下为固体,熔点282℃,沸点315℃,在300℃以上易升华。易溶于水,也易溶于乙醚、丙酮等有机溶剂。在蒸气中也容易双聚,据此判断三氯化铁晶体为
(3)(NH4)2Fe(SO4)2∙6H2O俗称摩尔盐,其阴离子
 的空间构型为
的空间构型为(4)Fe(CO)5可用作催化剂、汽油抗爆剂等,其分子中σ键和π键的数目之比为
(5)CuCl2和CuCl是铜的两种氯化物。

①图中表示的是
②原子坐标参数可用来表示晶胞内各原子的相对位置,图中各原子坐标参数A为 (0,0,0);B为(0,1,1);C为(1,0,0);则D原子的坐标参数为
您最近一年使用:0次
4 . 1-溴丁烷常用作稀有元素萃取剂、烃化剂及合成染料和香料的有机原料。实验室制备1-溴丁烷的反应、主要装置和有关数据如下:
NaBr+H2SO4 NaHSO4+HBr↑、CH3CH2CH2CH2OH+HBr
NaHSO4+HBr↑、CH3CH2CH2CH2OH+HBr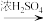 CH3CH2CH2CH2Br+H2O。
CH3CH2CH2CH2Br+H2O。
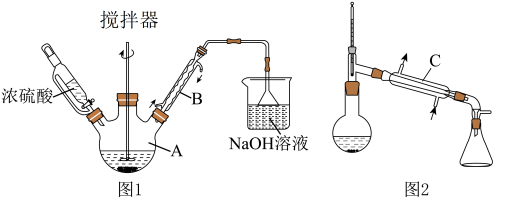
实验步骤:在仪器A中加入10mL水,边搅拌边缓慢滴加20mL过量的浓硫酸,冷却至室温。再依次加入7.4g正丁醇、16.5g研细的溴化钠和几粒沸石。在不断搅拌下,用图1所示装置小火加热回流90min,得到粗品。将粗品依次用15mL水、7mL浓硫酸、10mL水、10mL饱和碳酸氢钠溶液、10mL水洗涤并分液,分出的产物用无水氯化钙充分干燥,滤除氯化钙固体,用图2所示装置加热蒸馏,收集99~103℃的馏分,得纯净1-溴丁烷9.3g。
回答下列问题:
(1)仪器B的名称是___________ 。仪器B与仪器C___________ (填“能”或“不能”)交换使用。
(2)在用浓硫酸洗涤、分液的操作中,待液体分层后,产物应从分液漏斗的___________ (填“上口倒出”或“下口放出”)。
(3)本实验最可能产生两种有机副产物,任写其中一种副产物的结构简式___________ 。
(4)本实验中,1-溴丁烷的产率为___________ (保留三位有效数字)。
NaBr+H2SO4
 NaHSO4+HBr↑、CH3CH2CH2CH2OH+HBr
NaHSO4+HBr↑、CH3CH2CH2CH2OH+HBr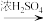 CH3CH2CH2CH2Br+H2O。
CH3CH2CH2CH2Br+H2O。
| 相对分子质量 | 熔点/℃ | 沸点/℃ | 密度(g/cm3) | 溶解性 | |
| 正丁醇 | 74 | -89.8 | 117.7 | 0.81 | 微溶于水,易溶于浓 硫酸和有机溶剂 |
| 1-溴丁烷 | 137 | -112.4 | 101.6 | 1.28 | 不溶于水,易溶于醇、 醚等有机溶剂 |
| 浓硫酸 | 98 | 10.3 | 338 | 1.84 | 易溶于水 |
回答下列问题:
(1)仪器B的名称是
(2)在用浓硫酸洗涤、分液的操作中,待液体分层后,产物应从分液漏斗的
(3)本实验最可能产生两种有机副产物,任写其中一种副产物的结构简式
(4)本实验中,1-溴丁烷的产率为
您最近一年使用:0次
解题方法
5 . 用辉铜矿(主要成分为Cu2S,含少量Fe2O3、SiO2等杂质)制备难溶于水的碱式碳酸铜的流程如下:
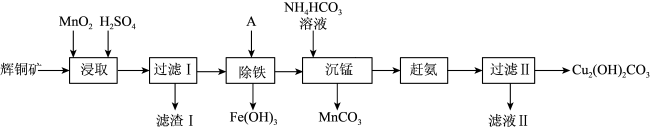
(1)下列措施能加快浸取速率的是___________ 。(填字母)
A.适当增大硫酸浓度 B.将辉铜矿粉碎 C.延长浸取时间
(2)滤渣I中的主要成分是MnO2、S、SiO2,写出“浸取”反应中生成S的离子方程式:___________ 。
(3)“除铁”的方法是通过调节溶液pH,使Fe3+转化为Fe(OH)3,则加入的试剂A最好是___________。
(4)“沉锰”(除Mn2+)过程中有关反应的离子方程式为___________ 。
(5)滤液Ⅱ所含溶质主要是___________ (填化学式)。

(1)下列措施能加快浸取速率的是
A.适当增大硫酸浓度 B.将辉铜矿粉碎 C.延长浸取时间
(2)滤渣I中的主要成分是MnO2、S、SiO2,写出“浸取”反应中生成S的离子方程式:
(3)“除铁”的方法是通过调节溶液pH,使Fe3+转化为Fe(OH)3,则加入的试剂A最好是___________。
| A.CO2 | B.CuO | C.氨水 | D.HCl |
(4)“沉锰”(除Mn2+)过程中有关反应的离子方程式为
(5)滤液Ⅱ所含溶质主要是
您最近一年使用:0次
23-24高二下·全国·课后作业
6 . 1869年俄国科学家门捷列夫绘制出了第一张元素周期表,成为化学史上的里程碑之一,且大大地促进了化学学科的快速发展。下表是现代元素周期表的一部分,请据表回答下列问题:
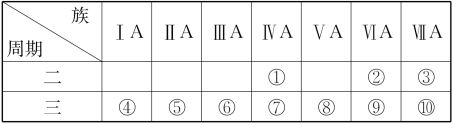
(1)元素③的名称是___________ ,金属性最强的元素是___________ (填元素符号)。
(2)①②⑤三种元素原子半径由大到小的顺序为___________ (填序号)。
(3)元素⑦的单质的一种用途是___________ (填写“制造玻璃”或“制造计算机芯片”)。
(4)元素⑧⑨⑩最高价氧化物的水化物中酸性最强的是___________ (填化学式)。

(1)元素③的名称是
(2)①②⑤三种元素原子半径由大到小的顺序为
(3)元素⑦的单质的一种用途是
(4)元素⑧⑨⑩最高价氧化物的水化物中酸性最强的是
您最近一年使用:0次
解题方法
7 . 已知下列物质的转化过程如下,D为含氧强酸:
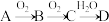
(1)若A是非金属固体单质,则A、C的化学式分别是___________ 、___________ ,D的浓溶液与铜反应的化学方程式为___________ 。
(2)若A是气态氢化物,C是红棕色气体,则A、C的化学式分别是___________ 、___________ ,C→D的反应方程式是___________ 。
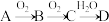
(1)若A是非金属固体单质,则A、C的化学式分别是
(2)若A是气态氢化物,C是红棕色气体,则A、C的化学式分别是
您最近一年使用:0次
解题方法
8 . 下列离子方程式书写不正确 的是
A.稀硝酸与铜:3Cu+8H++2NO =3Cu2++2NO↑+4H2O =3Cu2++2NO↑+4H2O |
| B.金属铁加入稀硫酸:2Fe+6H+=2Fe3++3H2↑ |
C.BaCl2溶液加入Na2SO4溶液:Ba2++SO =BaSO4↓ =BaSO4↓ |
D.NaOH溶液与NH4Cl溶液混合加热:NH +OH- +OH- NH3·H2O NH3·H2O |
您最近一年使用:0次
解题方法
9 . 下列说法不正确 的是
| A.烷烃分子中所有的化学键都是单键 |
| B.二氯甲烷只有一种结构说明甲烷是正四面体 |
| C.丙烯分子中所有原子都在同一平面 |
| D.烷烃同系物的熔沸点随碳原子数的增加逐渐升高 |
您最近一年使用:0次
10 . 下列叙述中,正确的是
| A.氨水是混合物,NH3·H2O是纯净物 |
| B.糖类、蛋白质均为天然高分子化合物 |
| C.工业上电解饱和氯化钠溶液制取金属钠 |
| D.铵态氮肥与草木灰混用会降低肥效 |
您最近一年使用:0次



