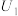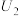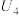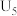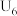名校
1 . 某小组在实验室用NaClO溶液和NH3反应制备N2H4,并进行相关的性质探究实验。
(1)制备N2H4
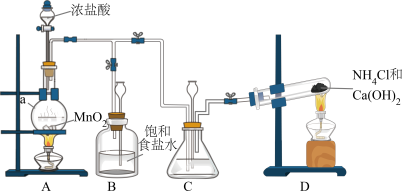
制备N2H4的离子方程式为___________ 。
Ⅱ.测定产品中水合肼(N2H4 · H2O)的含量
称取产品6.0 g,加入适量NaHCO3固体(滴定过程中,调节溶液的pH保持在6.5左右), 加水配成250 mL溶液,移取25.00 mL置于锥形瓶中,并滴加2 ~ 3滴淀粉溶液,用 0.3000 mol • L-1的碘标准溶液滴定(已知:N2H4·H2O+2I2 =N2↑ +4HI+H2O)。
(2)滴定到达终点的现象是___________ 。
(3)实验测得消耗碘标准溶液的平均值为20.00 mL,产品中水合肼的质量分数为___________ 。
Ⅲ.探究肼的性质。
(4)写出肼的电子式___________ ,肼为___________ 分子。(填“极性”或“非极性”)。
(5)预设肼可能具有___________ (a.氧化性 b.还原性 c.酸性 d.碱性)。
将制得的肼分离提纯后,进行如图实验探究。
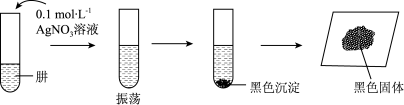
【查阅资料]AgOH在溶液中不稳定,易分解生成黑色的Ag2O,Ag2O可溶于氨水。
【提出假设】黑色固体可能是Ag、Ag2O中的一种或两种。
【实验验证】设计如下方案,进行实验。
(6)请完成表中的空白部分:①___________ ;②___________ 。
(7)实验表明,黑色固体主要成分是Ag,还有少量氧化银,请解释原因:___________ 。
(1)制备N2H4

制备N2H4的离子方程式为
Ⅱ.测定产品中水合肼(N2H4 · H2O)的含量
称取产品6.0 g,加入适量NaHCO3固体(滴定过程中,调节溶液的pH保持在6.5左右), 加水配成250 mL溶液,移取25.00 mL置于锥形瓶中,并滴加2 ~ 3滴淀粉溶液,用 0.3000 mol • L-1的碘标准溶液滴定(已知:N2H4·H2O+2I2 =N2↑ +4HI+H2O)。
(2)滴定到达终点的现象是
(3)实验测得消耗碘标准溶液的平均值为20.00 mL,产品中水合肼的质量分数为
Ⅲ.探究肼的性质。
(4)写出肼的电子式
(5)预设肼可能具有
将制得的肼分离提纯后,进行如图实验探究。

【查阅资料]AgOH在溶液中不稳定,易分解生成黑色的Ag2O,Ag2O可溶于氨水。
【提出假设】黑色固体可能是Ag、Ag2O中的一种或两种。
【实验验证】设计如下方案,进行实验。
| 操作 | 现象 | 实验结论 |
| i.取少量黑色固体于试管中,加入适量①___________ | 黑色固体部分溶解 | 黑色固体有Ag2O |
| ii.取少量黑色固体于试管中加入足量稀硝酸,振荡 | ②___________ | 黑色固体是Ag和Ag2O |
(7)实验表明,黑色固体主要成分是Ag,还有少量氧化银,请解释原因:
您最近一年使用:0次
名校
解题方法
2 . 在处理NO废气的过程中,催化剂[Co(NH3)6]2+会逐渐失活变为[Co(NH3)6]3+。某小组为解决这一问题,实验研究 和
和 之间的相互转化。
之间的相互转化。
资料:i.Ksp[Co(OH)2]=5.9×10-15,Ksp[Co(OH)3]=1.6×10-44
ii.Co2++6NH3 [Co(NH3)6]2+K1=1.3×105
[Co(NH3)6]2+K1=1.3×105
Co3++6NH3 [Co(NH3)6]3+K2=2×1035
[Co(NH3)6]3+K2=2×1035
iii.[Co(NH3)6]2+和[Co(NH3)6]3+在酸性条件下均能生成NH
(1)探究 的还原性
的还原性
实验I.粉红色的CoCl2溶液或CoSO4溶液在空气中久置,无明显变化。
实验II.向0.1mol/LCoCl2溶液中滴入2滴酸性KMnO4溶液,无明显变化。
实验III.按如图装置进行实验,观察到电压表指针偏转。
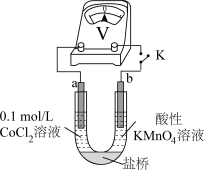
①甲同学根据实验III得出结论:Co2+可以被酸性KMnO4溶液氧化。
乙同学补充实验IV,____ (补全实验操作及现象),否定了该观点。
②探究碱性条件下 的还原性,进行实验。
的还原性,进行实验。
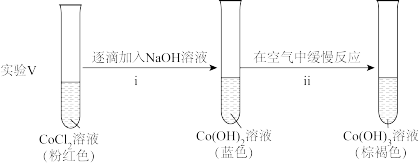
ii中反应的化学方程式是____ 。
③根据氧化还原反应规律解释:还原性Co(OH)2>Co2+:Co2+-e-=Co3+在碱性条件下,OH-与Co2+、Co3+反应,使c(Co2+)和c(Co3+)均降低,但____ 降低的程度更大,还原剂的还原性增强。
(2)探究 的氧化性
的氧化性
①根据实验III和IV推测氧化性:Co3+>Cl2,设计实验证明:向V中得到的棕褐色沉淀中,____ (补全实验操作及现象),反应的离子方程式是____ 。
②向V中得到的棕褐色沉淀中滴加H2SO4溶液,加入催化剂,产生无色气泡,该气体是____ 。
(3)催化剂[Co(NH3)6]2+的失活与再生
①结合数据解释[Co(NH3)6]2+能被氧化为[Co(NH3)6]3+而失活的原因:____ 。
②根据以上实验,设计物质转化流程图实现[Co(NH3)6]2+的再生:____ 。
示例:Co CoCl2
CoCl2 Co(OH)2
Co(OH)2
 和
和 之间的相互转化。
之间的相互转化。资料:i.Ksp[Co(OH)2]=5.9×10-15,Ksp[Co(OH)3]=1.6×10-44
ii.Co2++6NH3
 [Co(NH3)6]2+K1=1.3×105
[Co(NH3)6]2+K1=1.3×105Co3++6NH3
 [Co(NH3)6]3+K2=2×1035
[Co(NH3)6]3+K2=2×1035iii.[Co(NH3)6]2+和[Co(NH3)6]3+在酸性条件下均能生成NH

(1)探究
 的还原性
的还原性实验I.粉红色的CoCl2溶液或CoSO4溶液在空气中久置,无明显变化。
实验II.向0.1mol/LCoCl2溶液中滴入2滴酸性KMnO4溶液,无明显变化。
实验III.按如图装置进行实验,观察到电压表指针偏转。

①甲同学根据实验III得出结论:Co2+可以被酸性KMnO4溶液氧化。
乙同学补充实验IV,
②探究碱性条件下
 的还原性,进行实验。
的还原性,进行实验。
ii中反应的化学方程式是
③根据氧化还原反应规律解释:还原性Co(OH)2>Co2+:Co2+-e-=Co3+在碱性条件下,OH-与Co2+、Co3+反应,使c(Co2+)和c(Co3+)均降低,但
(2)探究
 的氧化性
的氧化性①根据实验III和IV推测氧化性:Co3+>Cl2,设计实验证明:向V中得到的棕褐色沉淀中,
②向V中得到的棕褐色沉淀中滴加H2SO4溶液,加入催化剂,产生无色气泡,该气体是
(3)催化剂[Co(NH3)6]2+的失活与再生
①结合数据解释[Co(NH3)6]2+能被氧化为[Co(NH3)6]3+而失活的原因:
②根据以上实验,设计物质转化流程图实现[Co(NH3)6]2+的再生:
示例:Co
 CoCl2
CoCl2 Co(OH)2
Co(OH)2
您最近一年使用:0次
2022-05-08更新
|
1354次组卷
|
9卷引用:热点1物质性质探究类实验
名校
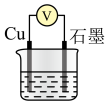
3 . 某学习小组将Cu与 的反应设计为原电池,并进行相关实验探究。回答下列问题:
的反应设计为原电池,并进行相关实验探究。回答下列问题:
I.实验准备
(1)稀硫酸的配制
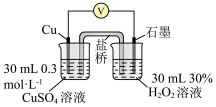
①配制 的
的 溶液,需
溶液,需 溶液的体积为
溶液的体积为______ mL。
②在实验室配制上述溶液的过程中,下图所示仪器,需要用到的是__________ (填仪器名称)。
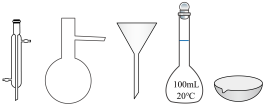
(2)Cu与 在酸性条件下反应的离子方程式为
在酸性条件下反应的离子方程式为__________ 。
II.实验探究
【实验任务】利用相关原电池装置进行实验,探究物质氧化性或还原性的影响因素。
【查阅资料】其他条件相同时,参与原电池反应的氧化剂(或还原剂)的氧化性(或还原性)越强,原电池的电压越大。
【进行实验】
(3)利用下表所示装置进行实验1~4,记录数据。
已知:本实验条件下, 对电压的影响可忽略。
对电压的影响可忽略。
①根据表中信息,补充数据:
__________ 。
②由实验2和4可知,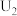
______ 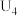 (填“大于”或“小于”或“等于”),说明其他条件相同时,
(填“大于”或“小于”或“等于”),说明其他条件相同时, 溶液的浓度越大,其氧化性越强。
溶液的浓度越大,其氧化性越强。
(4)由(3)中实验结果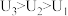 ,小组同学对“电压随pH减小而增大”可能的原因,提出了以下两种猜想:
,小组同学对“电压随pH减小而增大”可能的原因,提出了以下两种猜想:
猜想1:酸性条件下, 的氧化性随pH减小而增强。
的氧化性随pH减小而增强。
猜想2:酸性条件下,Cu的还原性随pH减小而增强。
为验证猜想,小组同学在(3)中实验1~4的基础上,利用下表装置进行实验5~-7,并记录数据。
②实验结果为: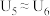 、
、______ ,说明猜想2不成立,猜想1成立。
(5)已知Cu与 反应时,加入氨水可形成深蓝色的
反应时,加入氨水可形成深蓝色的 。小组同学利用(4)中实验5的装置继续探究,向左侧烧杯中滴加5.0mL一定浓度的氨水,相比实验5,电压表读数增大,分析该电压表读数增大的原因:
。小组同学利用(4)中实验5的装置继续探究,向左侧烧杯中滴加5.0mL一定浓度的氨水,相比实验5,电压表读数增大,分析该电压表读数增大的原因:__________ 。
【实验结论】物质的氧化性(或还原性)强弱与其浓度、pH等因素有关。
 的反应设计为原电池,并进行相关实验探究。回答下列问题:
的反应设计为原电池,并进行相关实验探究。回答下列问题:I.实验准备
(1)稀硫酸的配制
①配制
 的
的 溶液,需
溶液,需 溶液的体积为
溶液的体积为②在实验室配制上述溶液的过程中,下图所示仪器,需要用到的是

(2)Cu与
 在酸性条件下反应的离子方程式为
在酸性条件下反应的离子方程式为II.实验探究
【实验任务】利用相关原电池装置进行实验,探究物质氧化性或还原性的影响因素。
【查阅资料】其他条件相同时,参与原电池反应的氧化剂(或还原剂)的氧化性(或还原性)越强,原电池的电压越大。
【进行实验】
(3)利用下表所示装置进行实验1~4,记录数据。
装置 | 实验 序号 | 烧杯中所加试剂 | 电压表 读数 | ||
| 30% |
|
| ||
|
|
| |||
1 | 30.0 | / | 10.0 |
| |
2 | 30.0 | 1.0 | 9.0 |
| |
3 | 30.0 | 2.0 | 8.0 |
| |
4 | 35.0 | 1.0 |
|
| |
 对电压的影响可忽略。
对电压的影响可忽略。①根据表中信息,补充数据:

②由实验2和4可知,
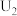
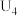 (填“大于”或“小于”或“等于”),说明其他条件相同时,
(填“大于”或“小于”或“等于”),说明其他条件相同时, 溶液的浓度越大,其氧化性越强。
溶液的浓度越大,其氧化性越强。(4)由(3)中实验结果
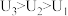 ,小组同学对“电压随pH减小而增大”可能的原因,提出了以下两种猜想:
,小组同学对“电压随pH减小而增大”可能的原因,提出了以下两种猜想:猜想1:酸性条件下,
 的氧化性随pH减小而增强。
的氧化性随pH减小而增强。猜想2:酸性条件下,Cu的还原性随pH减小而增强。
为验证猜想,小组同学在(3)中实验1~4的基础上,利用下表装置进行实验5~-7,并记录数据。
装置 | 实验 序号 | 操作 | 电压表 读数 |
| 5 | / |
|
6 | ①向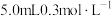  溶液。 溶液。 |
| |
7 | 向另一侧烧杯中滴加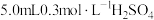 溶液 溶液 |
|
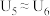 、
、(5)已知Cu与
 反应时,加入氨水可形成深蓝色的
反应时,加入氨水可形成深蓝色的 。小组同学利用(4)中实验5的装置继续探究,向左侧烧杯中滴加5.0mL一定浓度的氨水,相比实验5,电压表读数增大,分析该电压表读数增大的原因:
。小组同学利用(4)中实验5的装置继续探究,向左侧烧杯中滴加5.0mL一定浓度的氨水,相比实验5,电压表读数增大,分析该电压表读数增大的原因:【实验结论】物质的氧化性(或还原性)强弱与其浓度、pH等因素有关。
您最近一年使用:0次
2023-02-19更新
|
1814次组卷
|
4卷引用:广东省深圳市2022-2023学年高三第一次调研考试变式题(实验综合题)
(已下线)广东省深圳市2022-2023学年高三第一次调研考试变式题(实验综合题)(已下线)专题19 实验综合题广东省深圳市2022-2023学年高三第一次调研考试化学试题福建省泉州市泉港区第一中学、厦门外国语学校石狮分校2023-2024学年高二上学期期中考试化学试题
名校
解题方法
4 . 某小组探究 和
和 的反应的氧化还原反应,从电极反应角度分析物质氧化性和还原性的变化规律。
的反应的氧化还原反应,从电极反应角度分析物质氧化性和还原性的变化规律。
【实验探究】
实验i:向装有0.5g 的烧杯中加入20mL30%
的烧杯中加入20mL30% 溶液,一段时间内无明显现象,10小时后,溶液中有少量蓝色浑浊,
溶液,一段时间内无明显现象,10小时后,溶液中有少量蓝色浑浊, 片表面附着少量蓝色固体。
片表面附着少量蓝色固体。
(1)写出该反应的化学方程式:_______ 。
【继续探究】
针对该反应速率较慢,小组同学查阅资料,设计并完成了下列实验。
(2)实验ii中:溶液变蓝的原因是_______ (用离子反应方程式表示);经检验产生的气体为氧气,产生氧气的原因是_______ 。
(3)对比实验i和iii,为探究氨水对 的还原性或
的还原性或 氧化性的影响,该同学利用如图装置继续实验。
氧化性的影响,该同学利用如图装置继续实验。
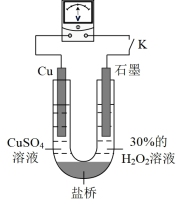
已知:电压大小反映了物质氧化还原性强弱的差异;物质氧化性与还原性强弱差异越大,电压越大。
a.K闭合时,电压为x。
b.向U型管右侧溶液中滴加氨水后,电压不变。
c.继续向U型管左侧溶液中滴加氨水后,电压增大了y。
①利用电极反应解释该实验的结论:_______ 。
②利用该方法也可证明酸性增强可提高 的氧化性,与上述实验操作不同的是
的氧化性,与上述实验操作不同的是_______ 。
(4)总结:物质氧化性和还原性变化的一般规律是_______ 。
(5)应用: 分别与
分别与 的盐酸、氢溴酸、氢碘酸混合,
的盐酸、氢溴酸、氢碘酸混合, 只与氢碘酸发生置换反应,试解释原因
只与氢碘酸发生置换反应,试解释原因_______ 。
 和
和 的反应的氧化还原反应,从电极反应角度分析物质氧化性和还原性的变化规律。
的反应的氧化还原反应,从电极反应角度分析物质氧化性和还原性的变化规律。【实验探究】
实验i:向装有0.5g
 的烧杯中加入20mL30%
的烧杯中加入20mL30% 溶液,一段时间内无明显现象,10小时后,溶液中有少量蓝色浑浊,
溶液,一段时间内无明显现象,10小时后,溶液中有少量蓝色浑浊, 片表面附着少量蓝色固体。
片表面附着少量蓝色固体。(1)写出该反应的化学方程式:
【继续探究】
针对该反应速率较慢,小组同学查阅资料,设计并完成了下列实验。
| 装置 | 序号 | 试剂a | 现象 |
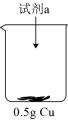 | ii | 20mL30% 与4mL 与4mL5mol/L  混合液 混合液 |  表面很快生产少量气泡,溶液逐渐变蓝,产生较多气泡 表面很快生产少量气泡,溶液逐渐变蓝,产生较多气泡 |
| iii | 20mL30% 与4mL 与4mL5mol/L氨水混合液 | 溶液立即变为深蓝色,产生大量气泡, 表面有少量蓝色不溶物 表面有少量蓝色不溶物 |
(3)对比实验i和iii,为探究氨水对
 的还原性或
的还原性或 氧化性的影响,该同学利用如图装置继续实验。
氧化性的影响,该同学利用如图装置继续实验。
已知:电压大小反映了物质氧化还原性强弱的差异;物质氧化性与还原性强弱差异越大,电压越大。
a.K闭合时,电压为x。
b.向U型管右侧溶液中滴加氨水后,电压不变。
c.继续向U型管左侧溶液中滴加氨水后,电压增大了y。
①利用电极反应解释该实验的结论:
②利用该方法也可证明酸性增强可提高
 的氧化性,与上述实验操作不同的是
的氧化性,与上述实验操作不同的是(4)总结:物质氧化性和还原性变化的一般规律是
(5)应用:
 分别与
分别与 的盐酸、氢溴酸、氢碘酸混合,
的盐酸、氢溴酸、氢碘酸混合, 只与氢碘酸发生置换反应,试解释原因
只与氢碘酸发生置换反应,试解释原因
您最近一年使用:0次
2022-06-03更新
|
544次组卷
|
4卷引用:微专题 物质性质综合实验探究
(已下线)微专题 物质性质综合实验探究(已下线)易错点21 化学反应速率-备战2023年高考化学考试易错题北京市东直门中学2023-2024学年高三上学期12月阶段测试化学试题北京市和平街第一中学2021-2022学年高三下学期保温化学试题
名校
5 . 某兴趣小组为探究浓硫酸与铜的反应,设计了如下装置。_______ 。
(2)为验证品红被 漂白的产物不稳定,简述操作步骤及现象
漂白的产物不稳定,简述操作步骤及现象_______ 。
(3)浸NaOH溶液的棉团作用是_______ 。
(4)为进一步探究 的还原性,将过量的
的还原性,将过量的 通入到200mL1.0mol/L的
通入到200mL1.0mol/L的 和过量
和过量 混合溶液中,观察到装置中产生了白色沉淀。装置如图所示。
混合溶液中,观察到装置中产生了白色沉淀。装置如图所示。 产生的原因进行探究(不考虑溶液中
产生的原因进行探究(不考虑溶液中 的影响)
的影响)
①查阅资料 不同浓度的 被还原的产物不同且产物不单一、不同pH时,
被还原的产物不同且产物不单一、不同pH时, 的氧化性不同。1.0mol/L的
的氧化性不同。1.0mol/L的 的
的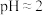 。
。
②提出猜想 猜想1: 被
被 氧化
氧化
猜想2: 在酸性条件下被
在酸性条件下被 氧化
氧化
猜想3:_______
③设计实验、验证猜想
限选实验试剂:0.01mol/LHCl、0.02mol/LHCl、3.0mol/LHNO3、6.0mol/LHNO3、3.0mol/LNaNO3、6.0mol/LNaNO3、0.1mol/LKSCN、 和
和 固体
固体
④交流讨论 小组同学认为,综合上述两个实验不足以证明猜想3成立。
⑤优化实验 若要证明猜想3成立,还要进行实验3。
实验3:_______ (只需提供设计思路,不需要写出具体操作步骤)。

(2)为验证品红被
 漂白的产物不稳定,简述操作步骤及现象
漂白的产物不稳定,简述操作步骤及现象(3)浸NaOH溶液的棉团作用是
(4)为进一步探究
 的还原性,将过量的
的还原性,将过量的 通入到200mL1.0mol/L的
通入到200mL1.0mol/L的 和过量
和过量 混合溶液中,观察到装置中产生了白色沉淀。装置如图所示。
混合溶液中,观察到装置中产生了白色沉淀。装置如图所示。
 产生的原因进行探究(不考虑溶液中
产生的原因进行探究(不考虑溶液中 的影响)
的影响)①查阅资料 不同浓度的
 被还原的产物不同且产物不单一、不同pH时,
被还原的产物不同且产物不单一、不同pH时, 的氧化性不同。1.0mol/L的
的氧化性不同。1.0mol/L的 的
的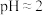 。
。②提出猜想 猜想1:
 被
被 氧化
氧化猜想2:
 在酸性条件下被
在酸性条件下被 氧化
氧化猜想3:
③设计实验、验证猜想
限选实验试剂:0.01mol/LHCl、0.02mol/LHCl、3.0mol/LHNO3、6.0mol/LHNO3、3.0mol/LNaNO3、6.0mol/LNaNO3、0.1mol/LKSCN、
 和
和 固体
固体| 实验步骤 | 实验现象和结论 |
| 实验1:取少量反应后的上层清液于试管中,滴入少量 | 出现 与 与 发生的离子方程式为 发生的离子方程式为 |
实验2:往图中的装置中加入100mL 固体,再通入过量 固体,再通入过量 。 。 | 出现白色沉淀,说明猜想2成立。 |
⑤优化实验 若要证明猜想3成立,还要进行实验3。
实验3:
您最近一年使用:0次
2022-04-29更新
|
1052次组卷
|
7卷引用:热点1实验方案设计
热点1实验方案设计(已下线)专项14 化学实验综合题-备战2022年高考化学阶段性新题精选专项特训(全国卷)(5月期)四川省泸州市古蔺县金兰高级中学校2022-2023学年高二下学期第一次月考化学试题(已下线)化学-2023年高考押题预测卷03(广东卷)(含考试版、全解全析、参考答案、答题卡)广东省粤港澳大湾区普通高中2022届高三第二次模拟考试化学试题湖南省郴州市永兴县第一中学2021-2022学年高三下学期期中考试化学试题2024届四川省攀枝花市第十五中学校高三上学期12月第7次半月考理科综合试题-高中化学
6 . 亚硫酸钠(Na2SO3)是一种重要的化工产品,常用作防腐剂、漂白剂、脱氯剂等。为探究 Na2SO3的性质,进行了如下实验。
【性质预测】
(1)Na2SO3中硫元素的化合价是_______ ,属于S元素的中间价态,既具有氧化性,又具有还原性。
【实验验证】
资料:酸性条件下,KMnO4 被还原为无色的 Mn2+。
【分析解释】
(2)实验ⅰ中,反应的离子方程式是_______ 。
(3)实验ⅱ中,能说明 Na2S 在酸性条件下被氧化的实验现象是_______ 。
【继续探究】
(4)甲同学认为实验ⅱ的现象不能直接得出“Na2SO3 具有氧化性”。
①对淡黄色浑浊产生的原因作出如下假设:
假设 a:酸性溶液中的 SO 具有氧化性,可产生 S;
具有氧化性,可产生 S;
假设 b:空气中存在 O2,在酸性条件下,由于_______ (用离子方程式表示),可产生 S;
假设 c:酸性溶液中的 SO 具有氧化性,可产生 S。
具有氧化性,可产生 S。
②设计实验 iii 证实了假设 a和b不是产生 S 的主要原因。
实验 iii:向 Na2S溶液中加入_______ (填试剂名称),产生有臭鸡蛋气味的气体,离子方程式为_______ ,溶液未变浑浊。
(5)结合实验 ii 和 iii,用离子方程式解释实验ⅱ中产生淡黄色浑浊的原因:_______ 。
【性质预测】
(1)Na2SO3中硫元素的化合价是
【实验验证】
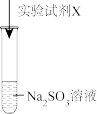 | 实验序号 | 实验试剂X | 实验现象 |
| ⅰ | KMnO4溶液、稀硫酸 | 紫色褪去,变为无色 | |
| ⅱ | Na2S 溶液、稀硫酸 | 加入Na2S溶液,无明显现象;再加入稀硫酸,产生淡黄色浑浊。 |
【分析解释】
(2)实验ⅰ中,反应的离子方程式是
(3)实验ⅱ中,能说明 Na2S 在酸性条件下被氧化的实验现象是
【继续探究】
(4)甲同学认为实验ⅱ的现象不能直接得出“Na2SO3 具有氧化性”。
①对淡黄色浑浊产生的原因作出如下假设:
假设 a:酸性溶液中的 SO
 具有氧化性,可产生 S;
具有氧化性,可产生 S;假设 b:空气中存在 O2,在酸性条件下,由于
假设 c:酸性溶液中的 SO
 具有氧化性,可产生 S。
具有氧化性,可产生 S。②设计实验 iii 证实了假设 a和b不是产生 S 的主要原因。
实验 iii:向 Na2S溶液中加入
(5)结合实验 ii 和 iii,用离子方程式解释实验ⅱ中产生淡黄色浑浊的原因:
您最近一年使用:0次
名校
解题方法
7 . 某校实验小组欲探究 溶液与
溶液与 的反应。
的反应。
Ⅰ.配制 溶液。
溶液。
(1)由 固体配制
固体配制 溶液,下列仪器中需要使用的有
溶液,下列仪器中需要使用的有_______ (写出名称)。
Ⅱ.探究 溶液与
溶液与 的反应。
的反应。
经查阅资料,该实验小组设计了如下实验,结合实验现象回答下列问题:
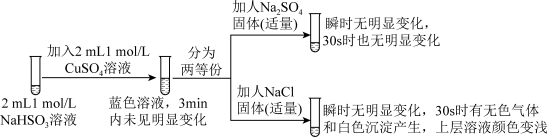
已知: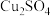 易溶于水;CuCl为白色难溶于水的固体。
易溶于水;CuCl为白色难溶于水的固体。
(2)若试管d中发生了氧化还原反应,写出该反应的离子方程式_______ 。
(3)该实验小组对试管d中加入NaCl固体后产生白色沉淀的原因提出了如下猜想:
猜想1: 改变了
改变了 的还原性。
的还原性。
猜想2: 改变了
改变了 的氧化性。
的氧化性。
为进一步证实上述猜想,该实验小组利用原电池原理设计了如下实验:
通过分析上表中对比实验现象可知_______ (填“猜想1”或“猜想2”)不合理。
(4)为证明猜想2的合理性,对实验1的装置做了如下改进:
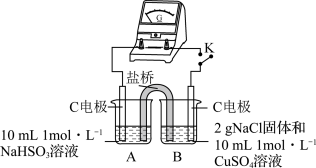
①烧杯B中的石墨电极是原电池的_______ 极,电极反应式为_______ 。
②闭合开关K,若_______ (描述实验现象),说明猜想2合理。
③请从化学反应原理的角度解释原因_______ ,使 与
与 的反应能够进行完全。
的反应能够进行完全。
 溶液与
溶液与 的反应。
的反应。Ⅰ.配制
 溶液。
溶液。(1)由
 固体配制
固体配制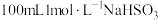 溶液,下列仪器中需要使用的有
溶液,下列仪器中需要使用的有
Ⅱ.探究
 溶液与
溶液与 的反应。
的反应。经查阅资料,该实验小组设计了如下实验,结合实验现象回答下列问题:

已知:
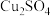 易溶于水;CuCl为白色难溶于水的固体。
易溶于水;CuCl为白色难溶于水的固体。(2)若试管d中发生了氧化还原反应,写出该反应的离子方程式
(3)该实验小组对试管d中加入NaCl固体后产生白色沉淀的原因提出了如下猜想:
猜想1:
 改变了
改变了 的还原性。
的还原性。猜想2:
 改变了
改变了 的氧化性。
的氧化性。为进一步证实上述猜想,该实验小组利用原电池原理设计了如下实验:
| 编号 | 实验1 | 实验2 |
| 实验装置 | 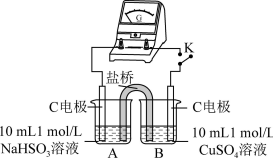 | 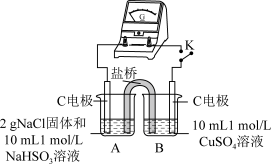 |
| 实验现象 | 闭合开关K,电流计指针发生微小偏转,烧杯中未见明显现象 | 闭合开关K,电流计指针发生微小偏转,烧杯中未见明显现象 |
(4)为证明猜想2的合理性,对实验1的装置做了如下改进:

①烧杯B中的石墨电极是原电池的
②闭合开关K,若
③请从化学反应原理的角度解释原因
 与
与 的反应能够进行完全。
的反应能够进行完全。
您最近一年使用:0次
2023-02-07更新
|
526次组卷
|
3卷引用:广东省深圳市2022-2023学年高三第一次调研考试变式题(实验综合题)
(已下线)广东省深圳市2022-2023学年高三第一次调研考试变式题(实验综合题)福建省漳州市2023届高三毕业班1月教学质量检测化学试题湖南省永州市第一中学2022-2023学年高三下学期3月月考化学试题
解题方法
8 . 工业上可用过氧化氢为氧化剂浸取废旧线路板中的铜,某兴趣小组采取不同方案进行实验并研究可行性。
方案1
(1)实验结果表明,双氧水与铜可以缓慢的反应,其电极反应式可表示为
i.还原反应
ii.氧化反应_______
(2)根据电极反应式,有同学设想可以通过以下方式加快反应。
i.增大 ,增强
,增强 的氧化性
的氧化性
ii.降低_______ ,增强Cu的还原性
(3)以此为依据设计了方案2与方案3
方案2与方案3均在一定程度上加快了反应。
①方案2中,生成气体明显更剧烈的原因是_______ 。
②方案3中发生主要反应的离子方程式为_______ 。
③试评价方案2在回收铜过程的优缺点_______ 。
(4)方案3中生成沉淀会降低铜的回收率并会阻碍反应进行,进一步改进方案获得了良好效果。
试分析 的作用
的作用_______ 。
(5)小组同学通过进一步探究发现,含有 和氨水的混合溶液能继续浸取单质铜。资料:
和氨水的混合溶液能继续浸取单质铜。资料: 在水溶液中不稳定,Cu(I)在溶液中能以
在水溶液中不稳定,Cu(I)在溶液中能以 等形式稳定存在。
等形式稳定存在。
①用离子方程式表示上述反应原理_______ 。
②通常条件下,含 的溶液不能与Cu发生反应,请从氧化还原角度分析此反应能够发生的原因
的溶液不能与Cu发生反应,请从氧化还原角度分析此反应能够发生的原因_____ 。
方案1
| 实验装置 | 加入液体试剂 | 反应现象 |
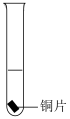 | 10mL 30%  溶液(pH约为4) 溶液(pH约为4) | 开始无明显现象,静置10小时后,溶液变为浅蓝色,铜片上有少量蓝色沉淀,之后不再有明显变化 |
i.还原反应

ii.氧化反应
(2)根据电极反应式,有同学设想可以通过以下方式加快反应。
i.增大
 ,增强
,增强 的氧化性
的氧化性ii.降低
(3)以此为依据设计了方案2与方案3
| 编号 | 加入液体试剂 | 反应现象 |
| 方案2 | 10mL30%  溶液和2mL 5mol/L 溶液和2mL 5mol/L  溶液 溶液 | 开始产生少量气泡,溶液变为蓝色,片刻后,反应越来越剧烈,甚至形成大量泡沫涌出(经检测,生成气体可使带火星木条复燃),反应后剩余铜片表面光亮 |
| 方案3 | 10mL 30%  溶液和2mL 5mol/L 氨水 溶液和2mL 5mol/L 氨水 | 生成较多气泡,溶液变为深蓝色。一段时间后,反应逐渐变慢,此时铜片上覆盖少量蓝色沉淀物。 |
①方案2中,生成气体明显更剧烈的原因是
②方案3中发生主要反应的离子方程式为
③试评价方案2在回收铜过程的优缺点
(4)方案3中生成沉淀会降低铜的回收率并会阻碍反应进行,进一步改进方案获得了良好效果。
| 编号 | 加入液体试剂 | 反应现象 |
| 方案4 | 10mL 30%  溶液 溶液2mL 5mol/L氨水 同时加入少量固体  | 生成较多气泡,溶液变为深蓝色。反应后铜片变薄且表面光亮。 |
 的作用
的作用(5)小组同学通过进一步探究发现,含有
 和氨水的混合溶液能继续浸取单质铜。资料:
和氨水的混合溶液能继续浸取单质铜。资料: 在水溶液中不稳定,Cu(I)在溶液中能以
在水溶液中不稳定,Cu(I)在溶液中能以 等形式稳定存在。
等形式稳定存在。①用离子方程式表示上述反应原理
②通常条件下,含
 的溶液不能与Cu发生反应,请从氧化还原角度分析此反应能够发生的原因
的溶液不能与Cu发生反应,请从氧化还原角度分析此反应能够发生的原因
您最近一年使用:0次
名校
解题方法
9 . 二氧化硫(化学式:SO2)广泛地用于葡萄酒的酿造工艺中,具有抗氧化和杀菌的作用。
(1)实验室常用亚硫酸钠固体和浓硫酸反应制备SO2,其化学方程式为_____________ 。
(2)如图是有关二氧化硫部分性质的实验装置图:
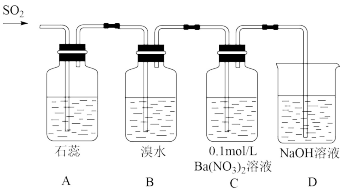
A装置中的现象证明SO2有_____ (填序号),B装置中的现象证明SO2有____ (填序号)。
a、漂白性 b、酸性氧化物性质 c、还原性 d、氧化性
(3)一段时间后C装置中会出现白色沉淀,为确定其成分,某学习小组进行了以下实验探究。
①查阅资料:25℃时,H2SO3电离常数Ka1=1.54×10-2,Ka2=1.02×10-7;Ksp(BaSO3)=5.3×10-7;饱和亚硫酸溶液的pH约为1,其中c(H2SO3)约为1.25mol/L。
小组同学通过计算排除了白色沉淀为BaSO3可能性,计算过程的关键数据如下:
饱和亚硫酸溶液中c(SO2)=_________ (保留2位有效数字);
Q(BaSO3)_______ Ksp(BaSO3) (填“>”“<”或“=”)。
②判断并检验,确定该沉淀为BaSO4
③为进一步探究C装置的溶液中什么微粒将SO2氧化,小组同学提出以下猜想:
猜想a:溶液中有氧气,将SO2氧化,继而生成BaSO4。
猜想b:____________________________________ (用离子方程式表示)
设计实验、验证猜想。
实验过程:
实验1、实验2中煮沸、油覆的目的是_______________________
④实验数据如下:

小组同学通过对比实验1、2、4三组实验的pH变化图像,得出结论:_______________________ 。综合以上pH变化数据,你还可得出什么结论?____________________________ 。
(1)实验室常用亚硫酸钠固体和浓硫酸反应制备SO2,其化学方程式为
(2)如图是有关二氧化硫部分性质的实验装置图:

A装置中的现象证明SO2有
a、漂白性 b、酸性氧化物性质 c、还原性 d、氧化性
(3)一段时间后C装置中会出现白色沉淀,为确定其成分,某学习小组进行了以下实验探究。
①查阅资料:25℃时,H2SO3电离常数Ka1=1.54×10-2,Ka2=1.02×10-7;Ksp(BaSO3)=5.3×10-7;饱和亚硫酸溶液的pH约为1,其中c(H2SO3)约为1.25mol/L。
小组同学通过计算排除了白色沉淀为BaSO3可能性,计算过程的关键数据如下:
饱和亚硫酸溶液中c(SO2)=
Q(BaSO3)
②判断并检验,确定该沉淀为BaSO4
③为进一步探究C装置的溶液中什么微粒将SO2氧化,小组同学提出以下猜想:
猜想a:溶液中有氧气,将SO2氧化,继而生成BaSO4。
猜想b:
设计实验、验证猜想。
实验过程:
实验1 | 实验2 | 实验3 | 实验4 | |
步 骤 | 在a烧杯中加入煮沸的25ml 0.1mol/L BaCl2溶液,再加入食用油覆盖,冷却至室温 | 在b烧杯中加入煮沸的25ml 0.1mol/L Ba(NO3)2溶液,再加入食用油覆盖,冷却至室温 | 在c烧杯中加入未煮沸的25ml 0.1mol/L BaCl2溶液 | 在d烧杯中加入未煮沸的25ml 0.1mol/L Ba(NO3)2溶液 |
| 在a、b、c、d四个烧杯中均放入pH传感器,然后通入纯净的SO2气体 | ||||
④实验数据如下:

小组同学通过对比实验1、2、4三组实验的pH变化图像,得出结论:
您最近一年使用:0次
解题方法
10 . 小组同学探究+3价铬元素和+6价铬元素的相互转化。
资料: (绿色)、
(绿色)、 (灰绿色,不溶于水)、
(灰绿色,不溶于水)、 (橙色)、
(橙色)、 (黄色)、
(黄色)、 (砖红色,难溶于水)
(砖红色,难溶于水)
实验Ⅰ:向2mL0.1mol/L 溶液中滴入2mL3%
溶液中滴入2mL3% 溶液,无明显变化,得到溶液a.取少量溶液a,加入
溶液,无明显变化,得到溶液a.取少量溶液a,加入 溶液,未观察到砖红色沉淀。
溶液,未观察到砖红色沉淀。
实验Ⅱ:向溶液a中加入2mL10%NaOH溶液,产生少量气泡,水浴加热,有大量气泡产生,经检验气体为 ,溶液最终变为黄色。取少量黄色溶液,加入稀硫酸调节溶液的pH约为3,再加入
,溶液最终变为黄色。取少量黄色溶液,加入稀硫酸调节溶液的pH约为3,再加入 溶液,有砖红色沉淀生成。
溶液,有砖红色沉淀生成。
(1)实验Ⅱ中加入稀硫酸的目的是___________ 。
(2)甲同学认为实验Ⅱ中溶液变黄生成 的原因是
的原因是 将+3价铬元素氧化为
将+3价铬元素氧化为 ,乙同学认为该说法不严谨。
,乙同学认为该说法不严谨。
①乙的理由是___________ 。
②设计实验否定了乙的猜想,___________ (填操作),溶液未变成黄色。
(3)对比实验I和Ⅱ,小组同学研究碱性环境对+3价铬元素或 性质的影响。
性质的影响。
①提出假设:
假设a:碱性增强, 的氧化性增强
的氧化性增强
假设b:___________ 。
② 参与的电极反应式是
参与的电极反应式是___________ ,据此分析,假设a不成立。
③设计实验证实假设b,画出实验装置图(注明试剂)并写出实验操作和现象___________ 。
实验Ⅲ:向实验Ⅱ中的黄色溶液中加入稀硫酸,溶液变为橙色,再加入3% 溶液,溶液最终变为绿色,有气泡生成。
溶液,溶液最终变为绿色,有气泡生成。
(4)实验Ⅲ中溶液由橙色变为绿色的离子方程式是___________ 。
(5)综上, 在+3价铬元素和+6价铬元素相互转化中的作用是
在+3价铬元素和+6价铬元素相互转化中的作用是___________ 。
资料:
 (绿色)、
(绿色)、 (灰绿色,不溶于水)、
(灰绿色,不溶于水)、 (橙色)、
(橙色)、 (黄色)、
(黄色)、 (砖红色,难溶于水)
(砖红色,难溶于水)实验Ⅰ:向2mL0.1mol/L
 溶液中滴入2mL3%
溶液中滴入2mL3% 溶液,无明显变化,得到溶液a.取少量溶液a,加入
溶液,无明显变化,得到溶液a.取少量溶液a,加入 溶液,未观察到砖红色沉淀。
溶液,未观察到砖红色沉淀。实验Ⅱ:向溶液a中加入2mL10%NaOH溶液,产生少量气泡,水浴加热,有大量气泡产生,经检验气体为
 ,溶液最终变为黄色。取少量黄色溶液,加入稀硫酸调节溶液的pH约为3,再加入
,溶液最终变为黄色。取少量黄色溶液,加入稀硫酸调节溶液的pH约为3,再加入 溶液,有砖红色沉淀生成。
溶液,有砖红色沉淀生成。(1)实验Ⅱ中加入稀硫酸的目的是
(2)甲同学认为实验Ⅱ中溶液变黄生成
 的原因是
的原因是 将+3价铬元素氧化为
将+3价铬元素氧化为 ,乙同学认为该说法不严谨。
,乙同学认为该说法不严谨。①乙的理由是
②设计实验否定了乙的猜想,
(3)对比实验I和Ⅱ,小组同学研究碱性环境对+3价铬元素或
 性质的影响。
性质的影响。①提出假设:
假设a:碱性增强,
 的氧化性增强
的氧化性增强假设b:
②
 参与的电极反应式是
参与的电极反应式是③设计实验证实假设b,画出实验装置图(注明试剂)并写出实验操作和现象
实验Ⅲ:向实验Ⅱ中的黄色溶液中加入稀硫酸,溶液变为橙色,再加入3%
 溶液,溶液最终变为绿色,有气泡生成。
溶液,溶液最终变为绿色,有气泡生成。(4)实验Ⅲ中溶液由橙色变为绿色的离子方程式是
(5)综上,
 在+3价铬元素和+6价铬元素相互转化中的作用是
在+3价铬元素和+6价铬元素相互转化中的作用是
您最近一年使用:0次