名校
解题方法
1 . 如图所示为原电池装置,下列说法不正确的是
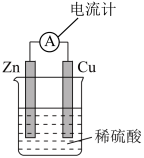
A.负极附近 浓度逐渐增大 浓度逐渐增大 | B. 为负极,发生还原反应 为负极,发生还原反应 |
| C.电子由锌片经过导线流向铜片 | D. 为正极,在铜片处有气泡产生 为正极,在铜片处有气泡产生 |
您最近一年使用:0次
名校
解题方法
2 . 碳在地壳中的含量很低,但是含有碳元素的有机物却分布极广。
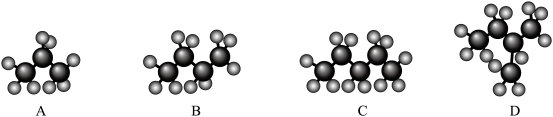
(1)观察下面几种烷烃的球棍模型:______________ (填字母,下同),与C互为同分异构体的是______________ .
(2)写出下列链状烷烃的分子式:
①含有30个氢原子的烷烃的分子式为______________ .
②假如某烷烃的相对分子质量为142,则该烷烃的分子式为______________ .
(3)利用甲烷与氯气发生取代反应制取副产品盐酸的设想在工业上已成为现实.某化学兴趣小组在实验室模拟上述过程,其设计的模拟装置如图.
①装置B有三种功能:a.控制气流速度;b.均匀混合气体;c.______________ .
②设 ,若理论上欲获得最多的氯化氢,则x值应
,若理论上欲获得最多的氯化氢,则x值应______________ .
③装置D的石棉中均匀混有 粉末,其作用是
粉末,其作用是__________________________________________ .
④装置E的作用是______________ (填序号).
A.收集气体 B.吸收氯气 C.防止倒吸 D.吸收氯化氢
(1)观察下面几种烷烃的球棍模型:
(2)写出下列链状烷烃的分子式:
①含有30个氢原子的烷烃的分子式为
②假如某烷烃的相对分子质量为142,则该烷烃的分子式为
(3)利用甲烷与氯气发生取代反应制取副产品盐酸的设想在工业上已成为现实.某化学兴趣小组在实验室模拟上述过程,其设计的模拟装置如图.
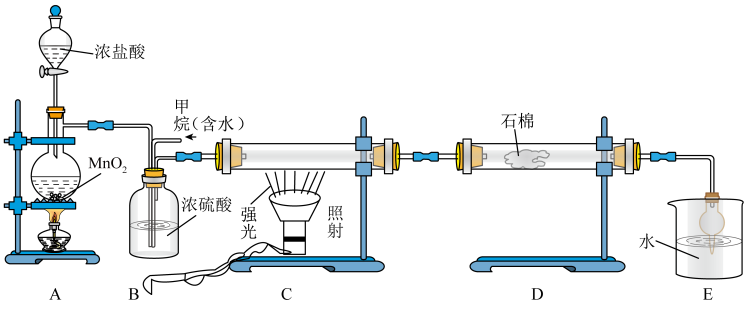
①装置B有三种功能:a.控制气流速度;b.均匀混合气体;c.
②设
 ,若理论上欲获得最多的氯化氢,则x值应
,若理论上欲获得最多的氯化氢,则x值应③装置D的石棉中均匀混有
 粉末,其作用是
粉末,其作用是④装置E的作用是
A.收集气体 B.吸收氯气 C.防止倒吸 D.吸收氯化氢
您最近一年使用:0次
名校
3 . 下列关于有机物的说法不正确的是
A.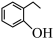 和 和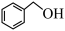 互为同系物 互为同系物 |
B. 可由 可由 制得, 制得, 可萃取碘水中的碘 可萃取碘水中的碘 |
| C.CH≡CH分子中所有原子共直线 |
D.乙醇和二甲醚的分子式均为 ,二者属于官能团异构 ,二者属于官能团异构 |
您最近一年使用:0次
名校
4 . 我国科学家将聚酰亚胺(组成元素为H、C、N、O等)介电聚合物与高绝缘纳米氧化镁(MgO)填料混合,成功制得聚酰亚胺/纳米氧化镁复合材料。该复合材料特点为具有高击穿强度、宽温度范围和低介电损耗。结合所学知识,回答下列问题。
(1)基态Mg原子的电子排布式为_________ 。
(2)C、N、O第一电离能由大到小的顺序为_________ ;C、N、O电负性由大到小的顺序为_________ ,理由是________________ 。
(3) 三种分子的空间结构和相应的键角如图1所示。
三种分子的空间结构和相应的键角如图1所示。 中O的未成对电子所在原子轨道的形状为
中O的未成对电子所在原子轨道的形状为_________ ; 的沸点比
的沸点比 的高,其主要原因是
的高,其主要原因是__________ ; 的键角大于
的键角大于 的键角,其原因是
的键角,其原因是________ 。
(1)基态Mg原子的电子排布式为
(2)C、N、O第一电离能由大到小的顺序为
(3)
 三种分子的空间结构和相应的键角如图1所示。
三种分子的空间结构和相应的键角如图1所示。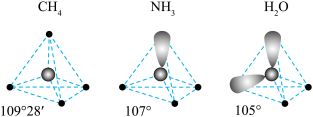
 中O的未成对电子所在原子轨道的形状为
中O的未成对电子所在原子轨道的形状为 的沸点比
的沸点比 的高,其主要原因是
的高,其主要原因是 的键角大于
的键角大于 的键角,其原因是
的键角,其原因是
您最近一年使用:0次
名校
5 . 回答下列问题
(1)利用 与
与 反应可制得碳化硅晶体,其晶胞结构如图,硅原子位于立方体的顶点和面心,碳原子位于立方体的内部。
反应可制得碳化硅晶体,其晶胞结构如图,硅原子位于立方体的顶点和面心,碳原子位于立方体的内部。
________ (填“大于”“小于”或“等于”) 。
。
②碳化硅晶体中每个Si原子周围距离最近的C原子数目为________ 。
③碳化硅的晶胞参数为a pm,晶胞密度为 ,则阿伏加德罗常数
,则阿伏加德罗常数
_______ (用含a和ρ的计算式表示)
④碳化硅的硬度_________ (填“大于”“小于”或“等于”)氮化硅的硬度,原因是_____________ 。
(2)氮化碳比氮化硅的硬度更大,其中β—氮化碳硬度超过金刚石晶体,成为首屈一指的超硬新材料,已知氮化碳的二维晶体结构如图,图中线框内表示晶胞结构。______________ 晶体。
②氮化碳的化学式为______________ 。
(3)三氧化铼 晶胞如图所示,其中O原子的配位数为
晶胞如图所示,其中O原子的配位数为________ ,已知该晶胞的密度为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则Re与O的最近距离为
,则Re与O的最近距离为________ cm。
(1)利用
 与
与 反应可制得碳化硅晶体,其晶胞结构如图,硅原子位于立方体的顶点和面心,碳原子位于立方体的内部。
反应可制得碳化硅晶体,其晶胞结构如图,硅原子位于立方体的顶点和面心,碳原子位于立方体的内部。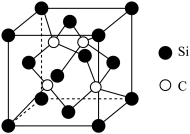

 。
。②碳化硅晶体中每个Si原子周围距离最近的C原子数目为
③碳化硅的晶胞参数为a pm,晶胞密度为
 ,则阿伏加德罗常数
,则阿伏加德罗常数
④碳化硅的硬度
(2)氮化碳比氮化硅的硬度更大,其中β—氮化碳硬度超过金刚石晶体,成为首屈一指的超硬新材料,已知氮化碳的二维晶体结构如图,图中线框内表示晶胞结构。
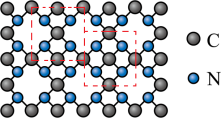
②氮化碳的化学式为
(3)三氧化铼
 晶胞如图所示,其中O原子的配位数为
晶胞如图所示,其中O原子的配位数为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则Re与O的最近距离为
,则Re与O的最近距离为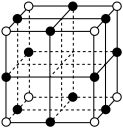
您最近一年使用:0次
7日内更新
|
70次组卷
|
2卷引用:甘肃省酒泉市四校联考2023-2024学年高二下学期5月期中考试化学试题
名校
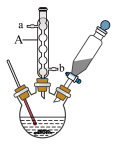
6 . 苯甲酸是一种重要原料。实验室可以用甲苯与高锰酸钾反应制得苯甲酸,反应装置图和有关数据如下:
合成步骤如下:
①在三颈烧瓶中加入5.4mL甲苯和30mL稀硫酸,放入碎瓷片,加热至沸腾时再迅速加入12.8g高锰酸钾固体,继续加热到甲苯层消失,过滤;
②反应后的溶液仍呈紫色,在容器中加入适量亚硫酸氢钠溶液,振荡,直到溶液变为无色,搅拌下向容器中加入足量浓盐酸;待反应完全后,将反应容器放在冰水浴中冷却,析出晶体,过滤,洗涤,干燥,称量。
(1)仪器A的名称是____________ ,它的作用是____________ 。
(2)加入碎瓷片的作用是____________ 。
(3)加入亚硫酸氢钠溶液使紫色褪去时发生反应的离子方程式为________________________ 。
(4)若得到的苯甲酸晶体产品不纯,则采用____________ 方法可得到纯度更高的产品。
(5)下列有关苯甲酸重结晶实验的说法正确的是_________ (填字母)。
A.粗苯甲酸溶解过程中,加热、玻璃棒搅拌均能提高苯甲酸的溶解度
B.在苯甲酸重结晶实验中,粗苯甲酸加热溶解后还需加少量蒸馏水
C.冷却结晶时,温度过低将析出杂质,故此时温度不是越低越好
(6)若最后得到纯净的苯甲酸质量为4.0g,则该反应的产率是____________ (保留一位小数)。
物质 | 熔点/℃ | 沸点/℃ | 水中溶解度/g(25℃) | 相对分子质量 | 密度/( |
甲苯 |
| 110.6 | 难溶 | 92 | 0.85 |
苯甲酸 | 122.13 | 249 | 0.344 | 122 | 1.27 |
①在三颈烧瓶中加入5.4mL甲苯和30mL稀硫酸,放入碎瓷片,加热至沸腾时再迅速加入12.8g高锰酸钾固体,继续加热到甲苯层消失,过滤;
②反应后的溶液仍呈紫色,在容器中加入适量亚硫酸氢钠溶液,振荡,直到溶液变为无色,搅拌下向容器中加入足量浓盐酸;待反应完全后,将反应容器放在冰水浴中冷却,析出晶体,过滤,洗涤,干燥,称量。
已知: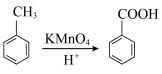 。
。
(1)仪器A的名称是
(2)加入碎瓷片的作用是
(3)加入亚硫酸氢钠溶液使紫色褪去时发生反应的离子方程式为
(4)若得到的苯甲酸晶体产品不纯,则采用
(5)下列有关苯甲酸重结晶实验的说法正确的是
A.粗苯甲酸溶解过程中,加热、玻璃棒搅拌均能提高苯甲酸的溶解度
B.在苯甲酸重结晶实验中,粗苯甲酸加热溶解后还需加少量蒸馏水
C.冷却结晶时,温度过低将析出杂质,故此时温度不是越低越好
(6)若最后得到纯净的苯甲酸质量为4.0g,则该反应的产率是
您最近一年使用:0次
名校
7 . 下列有关二氧化碳的描述错误的是
| A.含有非极性键 | B.是直线形分子 |
| C.属于非极性分子 | D.结构式为 |
您最近一年使用:0次
8 . 下列关于晶体的说法不正确的是
| A.具有各向异性的固体可能是晶体 |
| B.液晶是物质的一种聚集状态 |
| C.晶体类型一定是纯粹的,不存在过渡晶体 |
| D.由晶体X射线衍射图经过计算,可以获得晶胞的形状、大小以及微粒在晶胞里的位置 |
您最近一年使用:0次
名校
解题方法
9 . 研究人员研制出一种锂水电池,可作为鱼类和潜艇的储备电源.该电池以金属锂和钢板为电极材料,以 为电解质,使用时加入水即可放电.关于该电池的说法,不正确的是
为电解质,使用时加入水即可放电.关于该电池的说法,不正确的是
 为电解质,使用时加入水即可放电.关于该电池的说法,不正确的是
为电解质,使用时加入水即可放电.关于该电池的说法,不正确的是| A.水既是氧化剂又是溶剂 | B.放电时 向正极移动 向正极移动 |
C.放电时正极上有 生成 生成 | D.总反应为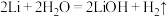 |
您最近一年使用:0次
名校
解题方法
10 . 某化学兴趣小组的同学为了探究铝电极在电池中的作用,设计并进行了以下实验,实验结果记录如下:
根据表中的实验现象回答下列问题.
(1)实验1和实验2中 所作的电极
所作的电极______________ (填“相同”或“不相同”);
(2)对实验3完成下列填空.
①铝为_________ 极,电极反应式为__________________ ;
②石墨为__________ 极,电极反应式为_______________________ ;
③电池总反应的化学方程式为__________ ;
(3)实验4中铝作_________ 极,理由是__________ ;铝电极的电极反应式为__________ ;
(4)解释实验5中电流表指针偏向铝的原因:__________ ;
(5)根据实验结果总结影响铝在原电池中作正极或负极的因素:__________ 。
编号 | 电极材料 | 电解质溶液 | 电流表指针偏转方向 |
1 |
| 稀盐酸 | 偏向 |
2 |
| 稀盐酸 | 偏向 |
3 |
| 稀盐酸 | 偏向石墨 |
4 |
|
| 偏向 |
5 |
| 浓硝酸 | 偏向 |
(1)实验1和实验2中
 所作的电极
所作的电极(2)对实验3完成下列填空.
①铝为
②石墨为
③电池总反应的化学方程式为
(3)实验4中铝作
(4)解释实验5中电流表指针偏向铝的原因:
(5)根据实验结果总结影响铝在原电池中作正极或负极的因素:
您最近一年使用:0次

 )
)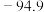
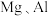
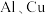
 溶液
溶液