1 . 下列离子方程式书写错误的是
A.过氧化钠溶于硫酸铜溶液中: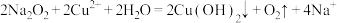 |
B.向 溶液中通入少量 溶液中通入少量 气体: 气体: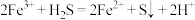 |
C.向碳酸氢钠溶液中滴加盐酸: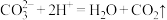 |
D.向次氯酸钠溶液中通入少量 : :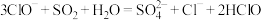 |
您最近一年使用:0次
名校
2 .  为阿伏加德罗常数的值。下列叙述错误的是
为阿伏加德罗常数的值。下列叙述错误的是
 为阿伏加德罗常数的值。下列叙述错误的是
为阿伏加德罗常数的值。下列叙述错误的是A.1mol 中 中 键的个数为 键的个数为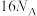 |
B.46g 中 中 杂化的碳原子数为 杂化的碳原子数为 |
C.1L 的HCN溶液中, 的HCN溶液中,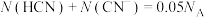 |
D.1mol 晶体中含有 晶体中含有 共价键 共价键 |
您最近一年使用:0次
3 . 氯化钠(NaCl)是生活中常用的化学品,也是重要的化工生产原料。
Ⅰ.实验室研究氯化钠的性质及制备
(1)下图表示NaCl在水中溶解过程的微观状态示意图。___________ 。
a.干燥的NaCl固体不导电,是由于其中不存在Na+和Cl-
b.由上图可知,水分子在形成自由移动的Na+和Cl-中起到了至关重要的作用
c.NaCl溶液能导电,是由于在电流作用下,其可解离出自由移动的Na+和Cl-
(2)某同学用含钠元素的不同类别物质制备NaCl。化学反应方程式如下:
a.2Na + Cl2 2NaCl
2NaCl
b.NaOH + HCl = NaCl + H2O
c.Na2O + 2HCl = 2NaCl + H2O
d.___________。
① 反应d可为某物质与HCl反应来制得氯化钠,该物质的化学式为___________ 。
② 反应d也可为两种盐溶液相互反应获得氯化钠,该反应的化学方程式为___________ 。
③ 反应c中的原料Na2O的物质类别是碱性氧化物,请依据其类别通性,再列举2个能与Na2O反应的其他物质(用化学式表示)___________ 。
Ⅱ.工业生产中氯化钠的制备
我国食盐的来源主要为海盐、湖盐、井矿盐。粗食盐中除了含泥沙等难溶性杂质外,还含有Ca2+、Mg2+、SO 等可溶性杂质。为得到精制食盐,某同学设计如下除杂流程,向粗盐中依次加入:过量BaCl2溶液、过量Na2CO3溶液、过量NaOH溶液,然后过滤,再在滤液中加入适量盐酸后加热蒸发结晶得纯净的NaCl。
等可溶性杂质。为得到精制食盐,某同学设计如下除杂流程,向粗盐中依次加入:过量BaCl2溶液、过量Na2CO3溶液、过量NaOH溶液,然后过滤,再在滤液中加入适量盐酸后加热蒸发结晶得纯净的NaCl。
(3)①过滤操作中所用到的玻璃仪器有烧杯、漏斗和___________ 。
②用离子方程式表示加入过量Na2CO3溶液的作用Ca2++CO =CaCO3↓和
=CaCO3↓和___________ 。
③ 用离子方程式表示盐酸的作用H+ + OH-=H2O 和___________ 。
Ⅰ.实验室研究氯化钠的性质及制备
(1)下图表示NaCl在水中溶解过程的微观状态示意图。

a.干燥的NaCl固体不导电,是由于其中不存在Na+和Cl-
b.由上图可知,水分子在形成自由移动的Na+和Cl-中起到了至关重要的作用
c.NaCl溶液能导电,是由于在电流作用下,其可解离出自由移动的Na+和Cl-
(2)某同学用含钠元素的不同类别物质制备NaCl。化学反应方程式如下:
a.2Na + Cl2
 2NaCl
2NaCl b.NaOH + HCl = NaCl + H2O
c.Na2O + 2HCl = 2NaCl + H2O
d.___________。
① 反应d可为某物质与HCl反应来制得氯化钠,该物质的化学式为
② 反应d也可为两种盐溶液相互反应获得氯化钠,该反应的化学方程式为
③ 反应c中的原料Na2O的物质类别是碱性氧化物,请依据其类别通性,再列举2个能与Na2O反应的其他物质(用化学式表示)
Ⅱ.工业生产中氯化钠的制备
我国食盐的来源主要为海盐、湖盐、井矿盐。粗食盐中除了含泥沙等难溶性杂质外,还含有Ca2+、Mg2+、SO
 等可溶性杂质。为得到精制食盐,某同学设计如下除杂流程,向粗盐中依次加入:过量BaCl2溶液、过量Na2CO3溶液、过量NaOH溶液,然后过滤,再在滤液中加入适量盐酸后加热蒸发结晶得纯净的NaCl。
等可溶性杂质。为得到精制食盐,某同学设计如下除杂流程,向粗盐中依次加入:过量BaCl2溶液、过量Na2CO3溶液、过量NaOH溶液,然后过滤,再在滤液中加入适量盐酸后加热蒸发结晶得纯净的NaCl。(3)①过滤操作中所用到的玻璃仪器有烧杯、漏斗和
②用离子方程式表示加入过量Na2CO3溶液的作用Ca2++CO
 =CaCO3↓和
=CaCO3↓和③ 用离子方程式表示盐酸的作用H+ + OH-=H2O 和
您最近一年使用:0次
4 . 下表列出了①~⑥六种元素在周期表中的位置。
回答下列问题(用化学用语填空):
(1)元素①的一种核素中,含有1个质子和1个中子,表示该核素组成的符号是___________ 。
(2)上述元素中,原子半径最大的是___________ (填元素符号)。
(3)由元素①、⑥组成的化合物的电子式为___________ 。
(4)元素⑤和⑥最高价氧化物对应的水化物酸性由强到弱的顺序是___________ (填化学式)。
(5)金属性:③___________ ④(填“>”或“<”),它们的最高价氧化物对应的水化物反应的离子方程式为___________ 。
(6)下列说法正确的是___________ (填序号)。
a.元素②、③组成的化合物只有一种
b.元素②的气态氢化物稳定性高于元素⑤的气态氢化物
c.元素⑥在化合物中呈现的最高化合价为+7价
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | |||||||
| 3 | ③ | ④ | ⑤ | ⑥ |
(1)元素①的一种核素中,含有1个质子和1个中子,表示该核素组成的符号是
(2)上述元素中,原子半径最大的是
(3)由元素①、⑥组成的化合物的电子式为
(4)元素⑤和⑥最高价氧化物对应的水化物酸性由强到弱的顺序是
(5)金属性:③
(6)下列说法正确的是
a.元素②、③组成的化合物只有一种
b.元素②的气态氢化物稳定性高于元素⑤的气态氢化物
c.元素⑥在化合物中呈现的最高化合价为+7价
您最近一年使用:0次
解题方法
5 . Ⅰ.某小组同学探究Na2CO3的性质。
(1)用Na2CO3固体配制100 mL 0.200 mol·L-1Na2CO3溶液。
①用到的仪器有:天平、药匙、量筒、烧杯、玻璃棒、胶头滴管和___________ 。
②计算需要Na2CO3固体的质量是___________ g。
③下列情况中,会使所配溶液浓度偏高的是___________ (填字母)。
a.转移时,没有洗涤烧杯和玻璃棒
b.定容时,眼睛俯视刻度线
c.摇匀后,发现液面低于刻度线,继续加水至液面与刻度线相切
(2)探究Na2CO3与盐酸的反应。向0.200 mol·L-1Na2CO3溶液中滴加稀盐酸,开始无气泡,继续滴加,产生气泡,反应的离子方程式为: +H+=
+H+= 、
、___________ 。
Ⅱ.某化学兴趣小组设计如下实验探究KMnO4固体与草酸(H2C2O4,具有还原性)反应的产物,以其产物为原料制备氯气:
室温下,取KMnO4固体于锥形瓶中,加入适量的草酸(H2C2O4)溶液,振荡,充分反应,可以观察到有黑色沉淀产生,溶液变为无色,同时生成无色无味的气体M,将燃着的木条靠近锥形瓶瓶口时木条熄灭。
分析实验并回答相应问题。
(3)M的化学式是___________ 。
(4)将充分反应后的混合物过滤,检验滤液中金属阳离子的方法及现象为___________ 、___________ 。向滤液中加入盐酸时又产生无色无味气体。
(5)将滤渣加入浓盐酸中加热,产生黄绿色气体,该反应的离子方程式为___________ 。
(1)用Na2CO3固体配制100 mL 0.200 mol·L-1Na2CO3溶液。
①用到的仪器有:天平、药匙、量筒、烧杯、玻璃棒、胶头滴管和
②计算需要Na2CO3固体的质量是
③下列情况中,会使所配溶液浓度偏高的是
a.转移时,没有洗涤烧杯和玻璃棒
b.定容时,眼睛俯视刻度线
c.摇匀后,发现液面低于刻度线,继续加水至液面与刻度线相切
(2)探究Na2CO3与盐酸的反应。向0.200 mol·L-1Na2CO3溶液中滴加稀盐酸,开始无气泡,继续滴加,产生气泡,反应的离子方程式为:
 +H+=
+H+= 、
、Ⅱ.某化学兴趣小组设计如下实验探究KMnO4固体与草酸(H2C2O4,具有还原性)反应的产物,以其产物为原料制备氯气:
室温下,取KMnO4固体于锥形瓶中,加入适量的草酸(H2C2O4)溶液,振荡,充分反应,可以观察到有黑色沉淀产生,溶液变为无色,同时生成无色无味的气体M,将燃着的木条靠近锥形瓶瓶口时木条熄灭。
分析实验并回答相应问题。
(3)M的化学式是
(4)将充分反应后的混合物过滤,检验滤液中金属阳离子的方法及现象为
(5)将滤渣加入浓盐酸中加热,产生黄绿色气体,该反应的离子方程式为
您最近一年使用:0次
6 . A和B两支试管所盛的溶液中共含有K+、Ag+、Mg2+、Cl−、OH−、 六种离子,向试管A的溶液中滴入酚酞溶液,溶液呈红色。请回答下列问题:
六种离子,向试管A的溶液中滴入酚酞溶液,溶液呈红色。请回答下列问题:
(1)若向某试管中滴入稀盐酸产生沉淀,则该试管为___________ (填“A”或“B”)。
(2)若向试管B的溶液中加入合适的药品,过滤后可以得到相应的金属和仅含一种溶质的溶液,则加入的药品是___________ (填化学式)。
(3)若将试管A和试管B中的溶液按一定体积比混合后过滤,蒸干所得滤液可得到一种纯净物,该物质为___________ ( 写化学式),则混合过程中发生反应的离子方程式为Ag++Cl-=AgCl↓与___________ (不考虑Ag+与OH−的反应)。
(4)按如图所示操作,充分反应后:___________ 。
②结合Ⅰ、Ⅱ实验现象可知 、
、 、
、 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为___________ 。
(5)已知 可发生反应:
可发生反应:
①该反应中氧化剂是___________ (填化学式)。
②用双线桥法标出电子转移的数目和方向:___________ 。
 六种离子,向试管A的溶液中滴入酚酞溶液,溶液呈红色。请回答下列问题:
六种离子,向试管A的溶液中滴入酚酞溶液,溶液呈红色。请回答下列问题:(1)若向某试管中滴入稀盐酸产生沉淀,则该试管为
(2)若向试管B的溶液中加入合适的药品,过滤后可以得到相应的金属和仅含一种溶质的溶液,则加入的药品是
(3)若将试管A和试管B中的溶液按一定体积比混合后过滤,蒸干所得滤液可得到一种纯净物,该物质为
(4)按如图所示操作,充分反应后:
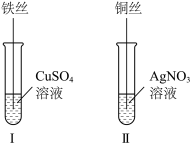
②结合Ⅰ、Ⅱ实验现象可知
 、
、 、
、 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为(5)已知
 可发生反应:
可发生反应:
①该反应中氧化剂是
②用双线桥法标出电子转移的数目和方向:
您最近一年使用:0次
7 . 研究物质性质及物质转化具有重要的价值,根据所学知识回答下列问题:
(1)下图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示置换反应的是___________ (填字母)。
①下列应用或事实与胶体的性质有关系的是___________ 。
A.在 溶液中滴加
溶液中滴加 溶液出现红褐色沉淀
溶液出现红褐色沉淀
B.在河流入海处易形成三角洲
C.用石膏或盐卤点制豆腐
②提纯明胶的水溶液和 溶液装置是下列中的
溶液装置是下列中的___________ (填序号)。___________ (填化学式),若该反应生成标准状况下的气体为8.96L,则该反应中转移电子的数目为___________ 。
(4)中国古代著作中有“银针验毒”的记录,其原理为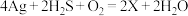 ,则X的化学式是
,则X的化学式是___________ ,其中 在该反应中
在该反应中___________ (填标号)。
A.作氧化剂 B.作还原剂
C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂
(1)下图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示置换反应的是

①下列应用或事实与胶体的性质有关系的是
A.在
 溶液中滴加
溶液中滴加 溶液出现红褐色沉淀
溶液出现红褐色沉淀B.在河流入海处易形成三角洲
C.用石膏或盐卤点制豆腐
②提纯明胶的水溶液和
 溶液装置是下列中的
溶液装置是下列中的A. B.
B. 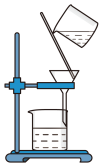 C.
C.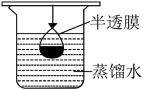
(4)中国古代著作中有“银针验毒”的记录,其原理为
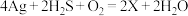 ,则X的化学式是
,则X的化学式是 在该反应中
在该反应中A.作氧化剂 B.作还原剂
C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂
您最近一年使用:0次
名校
解题方法
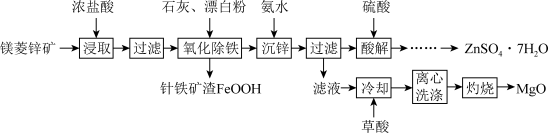
8 . 镁菱锌矿(主要成分为ZnCO3、MgCO3等,含有少量FeCO3、CaCO3等杂质)可用于生产媒染剂、防腐剂ZnSO4•7H2O以及耐火材料MgO。制备工艺流程如图:
回答下列有关问题:
(1)浓盐酸浸取矿石时,保持较大液固体积比(如3:1),目的是_______ 。
(2)“氧化除铁”在90℃,控制溶液pH在4.0~5.0,得到针铁矿渣的离子方程式为_______ 。
(3)“沉锌”时,加入氨水调节pH的范围是_______ 。
(4)“酸解”后获得ZnSO4•7H2O的操作依次经过蒸发浓缩、_______ 制得的ZnSO4•7H2O在烘干时需减压烘干的原因是_______ 。
(5)“滤液”中加入H2C2O4饱和溶液产生MgC2O4沉淀,若“灼烧”时产生两种气体,则该反应的化学方程式为:_______ 。
| 阳离子 | Fe3+ | Fe2+ | Zn2+ | Mg2+ | Ca2+ |
| 开始沉淀 | 2.7 | 7.6 | 6.2 | 9.4 | 13 |
| 完全沉淀 | 3.7 | 9.6 | 8.2 | 12.4 | _______ |
(1)浓盐酸浸取矿石时,保持较大液固体积比(如3:1),目的是
(2)“氧化除铁”在90℃,控制溶液pH在4.0~5.0,得到针铁矿渣的离子方程式为
(3)“沉锌”时,加入氨水调节pH的范围是
(4)“酸解”后获得ZnSO4•7H2O的操作依次经过蒸发浓缩、
(5)“滤液”中加入H2C2O4饱和溶液产生MgC2O4沉淀,若“灼烧”时产生两种气体,则该反应的化学方程式为:
您最近一年使用:0次
9 . 某温度下将氯气通入过量KOH溶液中,反应后得到KCl、KClO和KClO3的混合溶液,若所得溶液中ClO-和ClO 的物质的量之比为2:1,则该反应中被氧化和被还原氯元素的质量比为
的物质的量之比为2:1,则该反应中被氧化和被还原氯元素的质量比为
 的物质的量之比为2:1,则该反应中被氧化和被还原氯元素的质量比为
的物质的量之比为2:1,则该反应中被氧化和被还原氯元素的质量比为| A.3:7 | B.7:3 | C.1:1 | D.3:11 |
您最近一年使用:0次
10 . 下列反应的离子方程式或电离方程式正确的是
A.氧化铜与稀硫酸反应: |
B.向 NaHSO4溶液中滴加 Ba(OH)2溶液至SO 恰好沉淀完全: 恰好沉淀完全: |
C.盐酸和足量碳酸钠反应:  |
D.硫酸氢钠溶于水的电离方程式: |
您最近一年使用:0次



