1 . 设 为阿伏加德罗常数的值,下列叙述正确的是
为阿伏加德罗常数的值,下列叙述正确的是
 为阿伏加德罗常数的值,下列叙述正确的是
为阿伏加德罗常数的值,下列叙述正确的是A.标准状况下,2.24LCl2溶于足量水中可得到HClO分子的数目是 |
B.一定量氨水中通入0.1molHCl后溶液恰好呈中性,则中性溶液中 的数目为 的数目为 |
C.56g铁粉与足量水蒸气在高温下充分反应,转移的电子数为 |
D.常温下,pH=10的Na2CO3溶液中,水电离出的OH-数为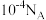 |
您最近半年使用:0次
2 . 硫代硫酸钠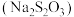 主要用于照相时作定影剂,也可用作氰化物的解毒剂,下列离子方程式书写错误的是
主要用于照相时作定影剂,也可用作氰化物的解毒剂,下列离子方程式书写错误的是
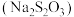 主要用于照相时作定影剂,也可用作氰化物的解毒剂,下列离子方程式书写错误的是
主要用于照相时作定影剂,也可用作氰化物的解毒剂,下列离子方程式书写错误的是A.用过量的 溶液除去底片上的 溶液除去底片上的 时有 时有 生成: 生成: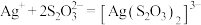 |
B.久置空气中的 溶液变质: 溶液变质: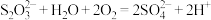 |
C.用 溶液吸收工业尾气中足是的 溶液吸收工业尾气中足是的 : : |
D.向 溶液中滴加稀硫酸: 溶液中滴加稀硫酸: |
您最近半年使用:0次
今日更新
|
197次组卷
|
2卷引用:河北省邢台市2024届高三下学期质量检测一模化学试题
3 . 亚氨基化硫(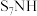 )的制备原理:
)的制备原理: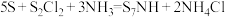 。下列化学用语表述正确的是
。下列化学用语表述正确的是
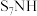 )的制备原理:
)的制备原理: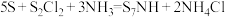 。下列化学用语表述正确的是
。下列化学用语表述正确的是A.基态S原子的价层电子排布式: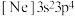 |
B. 的VSEPR模型: 的VSEPR模型: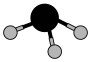 |
C. 的电子式: 的电子式: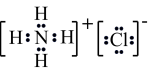 |
D. 的结构式: 的结构式: |
您最近半年使用:0次
解题方法
4 . 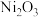 可用于制备镉镍碱性电池。镍废料中含有Ni、Cu、Fe、Ca、Mg等的化合物及难溶性杂质,以镍废料为原料制备高纯
可用于制备镉镍碱性电池。镍废料中含有Ni、Cu、Fe、Ca、Mg等的化合物及难溶性杂质,以镍废料为原料制备高纯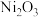 的工艺流程如图所示。
的工艺流程如图所示。 存在;
存在;
②常温下,部分物质溶度积如下:
回答下列问题:
(1)常温下,为提高酸浸效率,通常采用的措施是___________ (举2例)。
(2)加入碳酸钙调pH=4的目的是___________ ,此时 (0.10mol/L)是否会沉淀
(0.10mol/L)是否会沉淀___________ (通过计算说明)。
(3)“沉渣3”的主要成分是___________ (填化学式)。“滤液4”中除含 、
、 、
、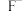 、
、 外,还含有较多的
外,还含有较多的___________ (填离子符号)。
(4)向“酸溶”后的溶液中加入NaOH和NaClO,发生反应的化学方程式是___________ 。
(5)工艺流程中使用 去除
去除 。研究表明,也可在加热条件下使用
。研究表明,也可在加热条件下使用 去除
去除 ,生成等物质的量的
,生成等物质的量的 、S混合沉淀以及
、S混合沉淀以及 ,该反应的离子方程式是
,该反应的离子方程式是___________ 。
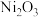 可用于制备镉镍碱性电池。镍废料中含有Ni、Cu、Fe、Ca、Mg等的化合物及难溶性杂质,以镍废料为原料制备高纯
可用于制备镉镍碱性电池。镍废料中含有Ni、Cu、Fe、Ca、Mg等的化合物及难溶性杂质,以镍废料为原料制备高纯 的工艺流程如图所示。
的工艺流程如图所示。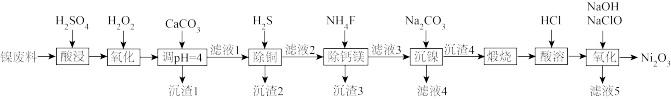
 存在;
存在;②常温下,部分物质溶度积如下:
 |  |  |  | |
 |  |  | 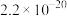 | 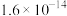 |
(1)常温下,为提高酸浸效率,通常采用的措施是
(2)加入碳酸钙调pH=4的目的是
 (0.10mol/L)是否会沉淀
(0.10mol/L)是否会沉淀(3)“沉渣3”的主要成分是
 、
、 、
、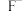 、
、 外,还含有较多的
外,还含有较多的(4)向“酸溶”后的溶液中加入NaOH和NaClO,发生反应的化学方程式是
(5)工艺流程中使用
 去除
去除 。研究表明,也可在加热条件下使用
。研究表明,也可在加热条件下使用 去除
去除 ,生成等物质的量的
,生成等物质的量的 、S混合沉淀以及
、S混合沉淀以及 ,该反应的离子方程式是
,该反应的离子方程式是
您最近半年使用:0次
解题方法
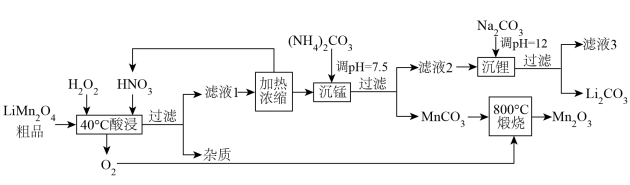
5 . 利用硝酸、过氧化氢对废弃锂电池中的正极材料LiMn2O4进行处理,回收Li、Mn元素,工艺流程如下:
(1)通过仪器分析可知LiMn2O4晶体中锰元素由 、
、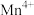 构成,它们的个数比为
构成,它们的个数比为___________ 。
(2)为了提高“酸浸”的效率,可采取的方法有___________ (答出2条)。“滤液1”的主要溶质有LiNO3、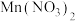 ,写出“酸浸”时发生反应的离子方程式
,写出“酸浸”时发生反应的离子方程式___________ 。
(3)在“酸浸”时,若用盐酸替代硝酸,可能产生的不良影响是___________ ,请评价若流程中缺少“加热浓缩”步骤后工艺的优缺点___________ (优点和缺点各写一条)。
(4)“沉锂”试剂不选用 的原因可能是
的原因可能是___________ (写出一条)。
(5)写出“800℃煅烧” 时发生反应的化学方程式
时发生反应的化学方程式___________ 。
(6)若“沉锂”前“滤液2”中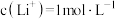 ,取1L该溶液加入等体积Na2CO3溶液充分反应后溶液中
,取1L该溶液加入等体积Na2CO3溶液充分反应后溶液中 ,则该实验中锂离子的沉淀率为
,则该实验中锂离子的沉淀率为___________ %(已知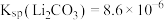 ,混合后溶液体积变化忽略不计)。
,混合后溶液体积变化忽略不计)。
(1)通过仪器分析可知LiMn2O4晶体中锰元素由
 、
、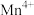 构成,它们的个数比为
构成,它们的个数比为(2)为了提高“酸浸”的效率,可采取的方法有
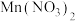 ,写出“酸浸”时发生反应的离子方程式
,写出“酸浸”时发生反应的离子方程式(3)在“酸浸”时,若用盐酸替代硝酸,可能产生的不良影响是
(4)“沉锂”试剂不选用
 的原因可能是
的原因可能是(5)写出“800℃煅烧”
 时发生反应的化学方程式
时发生反应的化学方程式(6)若“沉锂”前“滤液2”中
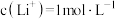 ,取1L该溶液加入等体积Na2CO3溶液充分反应后溶液中
,取1L该溶液加入等体积Na2CO3溶液充分反应后溶液中 ,则该实验中锂离子的沉淀率为
,则该实验中锂离子的沉淀率为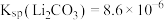 ,混合后溶液体积变化忽略不计)。
,混合后溶液体积变化忽略不计)。
您最近半年使用:0次
6 . 化学与科技、生产、生活密切相关,下列说法正确的是
| A.“碳中和”就是利用中和反应减少二氧化碳的排放 |
| B.醋酸除水垢,纯碱去油污都发生了化学变化 |
| C.汽车尾气处理是把氮的氧化物催化氧化为氮气 |
D.利用 合成了脂肪酸,实现了无机小分子向有机高分子的转变 合成了脂肪酸,实现了无机小分子向有机高分子的转变 |
您最近半年使用:0次
解题方法
7 . 以辉铜矿(主要成分为Cu2S,含少量SiO2)为原料制备草酸铜(CuC2O4)的流程如图所示:
(1)滤渣中含有单质S和___________ (填化学式),写出“浸取”时反应的化学方程式:___________ 。
(2)“还原”时除生成Cu外,还有N2生成,写出该反应的离子方程式:___________ 。
(3)“氧化溶解”时,也可以直接用稀硝酸溶解Cu,但没有采用此法,考虑的主要原因是___________ 。
(4)向滤液1中加入(或通入)___________(填字母),可得到一种可循环利用的物质。
(5)“制备”时 过多会导致
过多会导致 与
与 生成环状结构的配离子
生成环状结构的配离子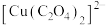 ,该配离子的结构式为
,该配离子的结构式为___________ (不考虑立体异构)。
(6)将一定质量的CuC2O4置于Ar气中热解,测得剩余固体的质量与原始固体的质量的比值随温度变化的曲线如图1所示。350~400℃下剩余固体的化学式为___________ 。 为
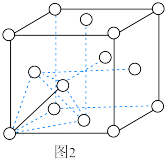
为___________  (已知该晶胞的晶胞参数为anm,阿伏加德罗常数的值为
(已知该晶胞的晶胞参数为anm,阿伏加德罗常数的值为 )。
)。

(1)滤渣中含有单质S和
(2)“还原”时除生成Cu外,还有N2生成,写出该反应的离子方程式:
(3)“氧化溶解”时,也可以直接用稀硝酸溶解Cu,但没有采用此法,考虑的主要原因是
(4)向滤液1中加入(或通入)___________(填字母),可得到一种可循环利用的物质。
| A.铁 | B.氯气 | C.高锰酸钾 | D.氯化氢 |
(5)“制备”时
 过多会导致
过多会导致 与
与 生成环状结构的配离子
生成环状结构的配离子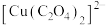 ,该配离子的结构式为
,该配离子的结构式为(6)将一定质量的CuC2O4置于Ar气中热解,测得剩余固体的质量与原始固体的质量的比值随温度变化的曲线如图1所示。350~400℃下剩余固体的化学式为
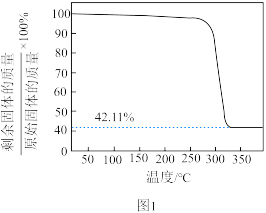
 为
为 (已知该晶胞的晶胞参数为anm,阿伏加德罗常数的值为
(已知该晶胞的晶胞参数为anm,阿伏加德罗常数的值为 )。
)。
您最近半年使用:0次
8 .  磁材料应用广泛,制备流程如图。下列说法错误的是
磁材料应用广泛,制备流程如图。下列说法错误的是
 磁材料应用广泛,制备流程如图。下列说法错误的是
磁材料应用广泛,制备流程如图。下列说法错误的是
| A.“产物1”需要密封保存防止氧化 |
B.“釜B”中主要反应的化学方程式为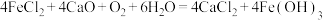 |
C.“产物1”与“产物2”中参与生成 反应的物质的物质的量之比为2:1 反应的物质的物质的量之比为2:1 |
| D.“分散剂”可破坏形成的胶体来促进氧化 |
您最近半年使用:0次
名校
9 . 三氯三(四氢呋喃)合铬(Ⅲ) 可催化烯烃加聚,制备的方法加下。
可催化烯烃加聚,制备的方法加下。
已知:① 易潮解,易升华,高温下易被氧气氧化。
易潮解,易升华,高温下易被氧气氧化。
② 气体有毒,遇水发生水解产生两种酸性气体。
气体有毒,遇水发生水解产生两种酸性气体。
Ⅰ.制备无水 :
:
某化学小组用 (沸点76.8℃)和
(沸点76.8℃)和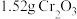 在高温下制备无水
在高温下制备无水 ,同时生成
,同时生成 气体,实验装置如图所示:
气体,实验装置如图所示: ,实验装置合理的连接顺序为A→G-→F→
,实验装置合理的连接顺序为A→G-→F→_______ →B(填装置字母标号,可重复使用)。
(2)装置乙名称为_______ ,装置D中粗导管的作用是_______ 。
(3)尾气处理时发生反应的离子方程式:_______ 。
Ⅱ.合成 :
: 原理为:
原理为:
实验操作:按如图组装仪器,将步骤Ⅰ所得无水 和
和 锌粉放入滤纸套筒内,双颈烧瓶中加入
锌粉放入滤纸套筒内,双颈烧瓶中加入 无水四氢呋喃(THF),通
无水四氢呋喃(THF),通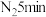 后关闭,接通冷却水,加热四氢呋喃至沸腾,在索氏提取器中发生反应,回流
后关闭,接通冷却水,加热四氢呋喃至沸腾,在索氏提取器中发生反应,回流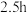 后再通入
后再通入 冷却至室温;取下双颈烧瓶,在通风橱中蒸发至有较多固体析出,冷却、抽滤、干燥后称量即得产品
冷却至室温;取下双颈烧瓶,在通风橱中蒸发至有较多固体析出,冷却、抽滤、干燥后称量即得产品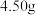 。
。_______ 。
(5)产品沿索氏提取器的管_______ (2或3)流回双颈烧瓶。
(6)已知Cr(Ⅱ)对该反应有催化作用,推断加入Zn粉发生反应的化学方程式为:_______ 。
(7)实验所用的四氢呋喃需进行无水处理,下列可以除去四氢呋喃中少量水分的试剂是_______ 。
A.金属钠 B.浓硫酸 C.具有吸水能力的分子筛
(8)产品产率为____ %(结果保留小数点后一位)[已知: 的摩尔质量为
的摩尔质量为 ;
; 的摩尔质量为
的摩尔质量为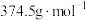 ]。
]。
 可催化烯烃加聚,制备的方法加下。
可催化烯烃加聚,制备的方法加下。已知:①
 易潮解,易升华,高温下易被氧气氧化。
易潮解,易升华,高温下易被氧气氧化。②
 气体有毒,遇水发生水解产生两种酸性气体。
气体有毒,遇水发生水解产生两种酸性气体。Ⅰ.制备无水
 :
:某化学小组用
 (沸点76.8℃)和
(沸点76.8℃)和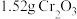 在高温下制备无水
在高温下制备无水 ,同时生成
,同时生成 气体,实验装置如图所示:
气体,实验装置如图所示: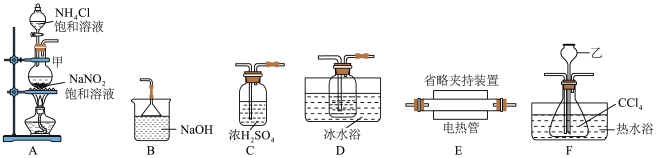
 ,实验装置合理的连接顺序为A→G-→F→
,实验装置合理的连接顺序为A→G-→F→(2)装置乙名称为
(3)尾气处理时发生反应的离子方程式:
Ⅱ.合成
 :
:①四氢呋喃(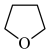 THF)为常见的有机溶剂,沸点66℃,易燃。
THF)为常见的有机溶剂,沸点66℃,易燃。
 原理为:
原理为:
实验操作:按如图组装仪器,将步骤Ⅰ所得无水
 和
和 锌粉放入滤纸套筒内,双颈烧瓶中加入
锌粉放入滤纸套筒内,双颈烧瓶中加入 无水四氢呋喃(THF),通
无水四氢呋喃(THF),通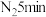 后关闭,接通冷却水,加热四氢呋喃至沸腾,在索氏提取器中发生反应,回流
后关闭,接通冷却水,加热四氢呋喃至沸腾,在索氏提取器中发生反应,回流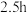 后再通入
后再通入 冷却至室温;取下双颈烧瓶,在通风橱中蒸发至有较多固体析出,冷却、抽滤、干燥后称量即得产品
冷却至室温;取下双颈烧瓶,在通风橱中蒸发至有较多固体析出,冷却、抽滤、干燥后称量即得产品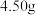 。
。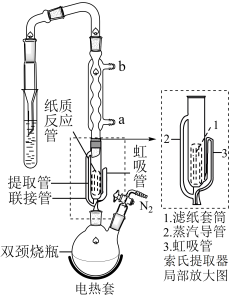
(5)产品沿索氏提取器的管
(6)已知Cr(Ⅱ)对该反应有催化作用,推断加入Zn粉发生反应的化学方程式为:
(7)实验所用的四氢呋喃需进行无水处理,下列可以除去四氢呋喃中少量水分的试剂是
A.金属钠 B.浓硫酸 C.具有吸水能力的分子筛
(8)产品产率为
 的摩尔质量为
的摩尔质量为 ;
; 的摩尔质量为
的摩尔质量为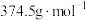 ]。
]。
您最近半年使用:0次
名校
10 . 下列实验方案设计现象和结论都正确的是
| 选项 | 实验方案 | 现象 | 结论 |
| A | 将 溶于水,进行导电性实验 溶于水,进行导电性实验 |  溶液可导电 溶液可导电 | 由此可证明 中含有离子键 中含有离子键 |
| B | 在试管中仅加入 无水乙醇和 无水乙醇和 冰醋酸,混合后,酒精灯缓缓加热,将产生的蒸汽经导管通入到饱和碳酸钠溶液中,反应结束后充分振荡盛有饱和碳酸钠溶液的试管 冰醋酸,混合后,酒精灯缓缓加热,将产生的蒸汽经导管通入到饱和碳酸钠溶液中,反应结束后充分振荡盛有饱和碳酸钠溶液的试管 | 溶液分层 | 制备获得乙酸乙酯 |
| C | 加热铜与浓硫酸的混合物,充分反应后冷却,将试管里的物质慢慢倒入盛水的烧杯中 | 试管底部有灰白色固体,稀释后溶液变蓝 | 浓硫酸具有氧化性,与铜反应生成硫酸铜 |
| D | 用pH试纸分别测定等物质的量浓度的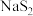 和 和 溶液的pH 溶液的pH | 前者pH大 | 非金属性:S<Cl |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次



