解题方法
1 . 下列反应的离子方程式正确的是
A.向硫化钠溶液中通入足量二氧化硫: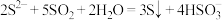 |
B.向 溶液中加入足量烧碱溶液: 溶液中加入足量烧碱溶液: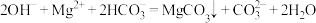 |
C.向次氯酸钙溶液中通入过量二氧化碳: |
D.向 溶液中通入少量 溶液中通入少量 : :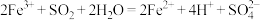 |
您最近一年使用:0次
昨日更新
|
91次组卷
|
2卷引用:湖南省2024届普通高中高三下学期学业水平选择性考试临考预测押题密卷化学试题(B卷)
名校
解题方法
2 . 工业上由含铜废料((含有Cu、CuS、CuSO4等)制备硝酸铜晶体的流程如图。
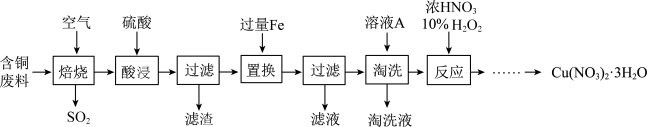
| A.“焙烧”时可以通过将大颗粒固体研成粉末的方式,加快反应速率 |
| B.“酸浸”目的是将氧化铜转化为Cu2+ |
| C.“反应”过程中无红棕色气体生成,理论上消耗HNO3和H2O2的物质的量之比为2:1 |
| D.“滤液”中含有的阳离子主要为Fe2+,“淘洗”所用的溶液A可选用稀硝酸 |
您最近一年使用:0次
名校
3 . 以绿茶为主要原料合成生物炭负载纳米铁(CT-FeNPs/BC)
步骤1:绿茶提取液及生物炭的制备。按如图1流程实验:
 溶液和生物炭。
溶液和生物炭。
②通一段时间 后,将绿茶提取液以2mL·
后,将绿茶提取液以2mL·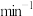 的速度全部滴入三颈烧瓶中,持续磁力搅拌1h,得黑色悬浊液。
的速度全部滴入三颈烧瓶中,持续磁力搅拌1h,得黑色悬浊液。
③离心分离,依次用乙醇和蒸馏水洗涤,真空干燥,产品密封备用。
回答下列问题:
(1)操作(b)中,应采用___________ 进行加热。
(2)图2中,盛装绿茶提取液的仪器名称为___________ ,加入绿茶提取液的目的是___________ 。
(3)离心分离后,用乙醇洗涤的作用是___________ 。
(4)判断产品洗涤干净的实验操作为___________ 。
(5)GT-FeNPs/BC可高效去除含铬强酸性废水中的六价铬(以 表示),反应过程如图3。
表示),反应过程如图3。 和
和 共同生成沉淀
共同生成沉淀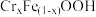 的离子方程式:
的离子方程式:___________ 。
②研究表明,GT-FeNPs/BC和 均可用于降解含
均可用于降解含 的废水。为探究两者降解效果,进行了如下实验,相同时间内得到如下实验结果:
的废水。为探究两者降解效果,进行了如下实验,相同时间内得到如下实验结果:
结合图3分析,实验3降解 效率显著增大的原因是
效率显著增大的原因是___________ 。
步骤1:绿茶提取液及生物炭的制备。按如图1流程实验:
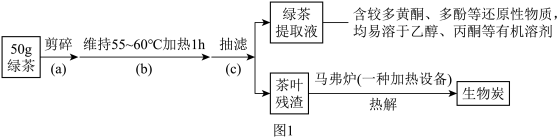


 溶液和生物炭。
溶液和生物炭。②通一段时间
 后,将绿茶提取液以2mL·
后,将绿茶提取液以2mL·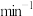 的速度全部滴入三颈烧瓶中,持续磁力搅拌1h,得黑色悬浊液。
的速度全部滴入三颈烧瓶中,持续磁力搅拌1h,得黑色悬浊液。③离心分离,依次用乙醇和蒸馏水洗涤,真空干燥,产品密封备用。
回答下列问题:
(1)操作(b)中,应采用
(2)图2中,盛装绿茶提取液的仪器名称为
(3)离心分离后,用乙醇洗涤的作用是
(4)判断产品洗涤干净的实验操作为
(5)GT-FeNPs/BC可高效去除含铬强酸性废水中的六价铬(以
 表示),反应过程如图3。
表示),反应过程如图3。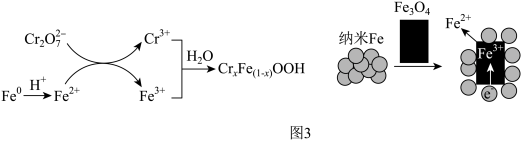
 和
和 共同生成沉淀
共同生成沉淀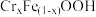 的离子方程式:
的离子方程式:②研究表明,GT-FeNPs/BC和
 均可用于降解含
均可用于降解含 的废水。为探究两者降解效果,进行了如下实验,相同时间内得到如下实验结果:
的废水。为探究两者降解效果,进行了如下实验,相同时间内得到如下实验结果:| 实验编号 | GT-FeNPs/BC(g/L) |  (g/L) (g/L) |  实际降解率 实际降解率 |
| 1 | 0.05 | 0 | 51.4% |
| 2 | 0 | 2 | 7.12% |
| 3 | 0.05 | 2 | 86.67% |
 效率显著增大的原因是
效率显著增大的原因是
您最近一年使用:0次
名校
解题方法
4 . 工业上采用酸性高浓度含砷废水主要以亚砷酸(H3AsO3)形式存在,提取As2O3的工艺流程如下:
Ⅰ.As2S3与过量的 存在以下反应:
存在以下反应: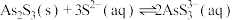 ;
;
Ⅱ.亚砷酸盐的溶解性大于相应砷酸盐。
回答下列问题:
(1)沉砷中FeSO4的作用是___________ :
(2)H2O2的作用是___________ ;滤渣I中含有FeAsO4、 、
、 和
和___________ (填化学式)。
(3)加生石灰和过氧化氢过程中,也可将砷元素转化为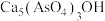 沉淀,发生的主要反应有:
沉淀,发生的主要反应有:
A.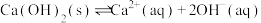

B.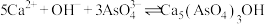

资料表明:“沉砷”的最佳温度是85℃,温度高于85℃,随温度升高沉淀率下降,从平衡移动角度分析其原因是___________ 。
(4)调节pH=0时,由Na3AsO4制备As2O3的离子方程式为___________ 。
(5)常温下,用NaOH溶液滴定H3AsO3时,各种微粒的物质的量分数随pH的变化曲线如图所示:___________ 。
(6)已知 的
的 ,含砷污染物允许排放标准为不大于0.5mg⋅L-1。若低浓度含砷废水(假设砷均以
,含砷污染物允许排放标准为不大于0.5mg⋅L-1。若低浓度含砷废水(假设砷均以 形式存在)中Fe3+的浓度为
形式存在)中Fe3+的浓度为 ,则低浓度含砷废水中
,则低浓度含砷废水中 的浓度为
的浓度为___________ mg⋅L-1,___________ (填“符合”或“不符合”)排放标准。

Ⅰ.As2S3与过量的
 存在以下反应:
存在以下反应: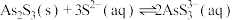 ;
;Ⅱ.亚砷酸盐的溶解性大于相应砷酸盐。
回答下列问题:
(1)沉砷中FeSO4的作用是
(2)H2O2的作用是
 、
、 和
和(3)加生石灰和过氧化氢过程中,也可将砷元素转化为
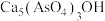 沉淀,发生的主要反应有:
沉淀,发生的主要反应有:A.
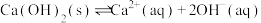

B.
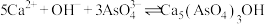

资料表明:“沉砷”的最佳温度是85℃,温度高于85℃,随温度升高沉淀率下降,从平衡移动角度分析其原因是
(4)调节pH=0时,由Na3AsO4制备As2O3的离子方程式为
(5)常温下,用NaOH溶液滴定H3AsO3时,各种微粒的物质的量分数随pH的变化曲线如图所示:

(6)已知
 的
的 ,含砷污染物允许排放标准为不大于0.5mg⋅L-1。若低浓度含砷废水(假设砷均以
,含砷污染物允许排放标准为不大于0.5mg⋅L-1。若低浓度含砷废水(假设砷均以 形式存在)中Fe3+的浓度为
形式存在)中Fe3+的浓度为 ,则低浓度含砷废水中
,则低浓度含砷废水中 的浓度为
的浓度为
您最近一年使用:0次
名校
解题方法
5 . 研究实验发现硝酸的浓度越稀,硝酸发生氧化还原反应时,对应还原产物中氮元素的化合价越低。现有一定量的铝粉和铁粉的混合物与一定量很稀的硝酸充分反应,反应过程中无气体放出,在反应结束后的溶液中逐滴加入5mol/LNaOH溶液,所加NaOH溶液的体积与产生沉淀的物质的量关系如图所示,下列说法不正确的是
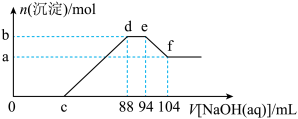
| A.该稀硝酸与铝粉、铁粉反应,其还原产物为硝酸铵 |
| B.c点对应NaOH溶液的体积为40mL |
| C.b点与a点的差值为0.03mol |
| D.样品中铝粉和铁粉的物质的量之比为5∶3 |
您最近一年使用:0次
名校
解题方法
6 . 在酸性溶液中,下列各组离子能在水溶液中大量共存的是
A. 、 、 、 、 、 、 | B. 、 、 、 、 、 、 |
C. 、 、 、 、 、 、 | D. 、 、 、 、 、 、 |
您最近一年使用:0次
名校
解题方法
7 . 研究人员拟设计黄铜矿(主要含 )制备硝酸铜和绿矾晶体的流程如下:
)制备硝酸铜和绿矾晶体的流程如下:
(1) 中铁元素的化合价为
中铁元素的化合价为_______ 价,已知“焙烧”生成 、CuO和
、CuO和 则其化学反应方程式为
则其化学反应方程式为_______ 。
(2)“置换”步骤中发生的所有反应的离子方程式有
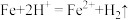 、
、_______ 。
(3)流程中“操作A”所需的玻璃仪器有烧杯、玻璃棒、_______ 。
(4)“浸洗”步骤中加入用于分离Cu、Fe的溶液A是_______ (填“稀 ”或“稀
”或“稀 ”)。
”)。
(5)“反应”步骤中,10% 为氧化剂,20%
为氧化剂,20% 提供
提供 ,可以避免污染性气体的产生,写出该“反应”的离子方程式:
,可以避免污染性气体的产生,写出该“反应”的离子方程式:_______ 。
(6)绿矾晶体( )在空气中极易变质;验证绿矾晶体已变质可选择的试剂为
)在空气中极易变质;验证绿矾晶体已变质可选择的试剂为_______ 。
 )制备硝酸铜和绿矾晶体的流程如下:
)制备硝酸铜和绿矾晶体的流程如下: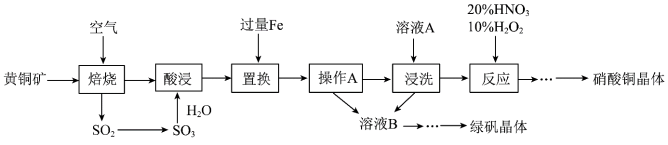
(1)
 中铁元素的化合价为
中铁元素的化合价为 、CuO和
、CuO和 则其化学反应方程式为
则其化学反应方程式为(2)“置换”步骤中发生的所有反应的离子方程式有

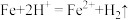 、
、(3)流程中“操作A”所需的玻璃仪器有烧杯、玻璃棒、
(4)“浸洗”步骤中加入用于分离Cu、Fe的溶液A是
 ”或“稀
”或“稀 ”)。
”)。(5)“反应”步骤中,10%
 为氧化剂,20%
为氧化剂,20% 提供
提供 ,可以避免污染性气体的产生,写出该“反应”的离子方程式:
,可以避免污染性气体的产生,写出该“反应”的离子方程式:(6)绿矾晶体(
 )在空气中极易变质;验证绿矾晶体已变质可选择的试剂为
)在空气中极易变质;验证绿矾晶体已变质可选择的试剂为
您最近一年使用:0次
名校
解题方法
8 . 氮的氧化物( )是大气污染物之一,含有氮氧化物的尾气需处理后才能排放。回答下列问题:
)是大气污染物之一,含有氮氧化物的尾气需处理后才能排放。回答下列问题:
(1)工业上在一定温度和催化剂条件下用 将
将 还原生成
还原生成 。
。
①如果选择图中A作为氨气的发生装置,对应反应的化学方程式为:_______ 。_______ :a→d→c→_______→_______→d→c→i。(按气流方向,用小写字母表示),F中倒置漏斗的作用是_______ 。
③若用通式 表示氮氧化物,则
表示氮氧化物,则_______ mol氨气(用含x表示)可将1mol的 转化为
转化为 。
。
(2)NO和 可用NaOH溶液吸收,主要反应:
可用NaOH溶液吸收,主要反应: ,
,

①下列措施能提高尾气中NO和 去除率的有
去除率的有_______ (填标号)。
A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气过程中定期补加适量NaOH溶液
②将NO、 通入石灰乳中可制备重要的工业原料
通入石灰乳中可制备重要的工业原料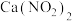 。该工艺需控制NO和
。该工艺需控制NO和 物质的量之比接近1:1,每生成
物质的量之比接近1:1,每生成 ,该反应转移的电子数为
,该反应转移的电子数为_______ (NA表示阿伏伽德罗常数)。若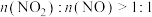 ,则会导致
,则会导致_______ 。
 )是大气污染物之一,含有氮氧化物的尾气需处理后才能排放。回答下列问题:
)是大气污染物之一,含有氮氧化物的尾气需处理后才能排放。回答下列问题:(1)工业上在一定温度和催化剂条件下用
 将
将 还原生成
还原生成 。
。①如果选择图中A作为氨气的发生装置,对应反应的化学方程式为:

③若用通式
 表示氮氧化物,则
表示氮氧化物,则 转化为
转化为 。
。(2)NO和
 可用NaOH溶液吸收,主要反应:
可用NaOH溶液吸收,主要反应: ,
,
①下列措施能提高尾气中NO和
 去除率的有
去除率的有A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气过程中定期补加适量NaOH溶液
②将NO、
 通入石灰乳中可制备重要的工业原料
通入石灰乳中可制备重要的工业原料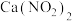 。该工艺需控制NO和
。该工艺需控制NO和 物质的量之比接近1:1,每生成
物质的量之比接近1:1,每生成 ,该反应转移的电子数为
,该反应转移的电子数为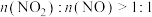 ,则会导致
,则会导致
您最近一年使用:0次
名校
解题方法
9 . 设NA表示阿伏加德罗常数的值,下列叙述正确的是
A.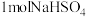 熔融态时含有NA个 熔融态时含有NA个 离子 离子 |
B. 气体中氧原子总数为3NA 气体中氧原子总数为3NA |
C.氧原子总数为0.2NA的 和 和 的混合气体,其体积为2.24L 的混合气体,其体积为2.24L |
D.1mol/L的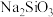 水溶液中含有的氧原子数为3 NA 水溶液中含有的氧原子数为3 NA |
您最近一年使用:0次
名校
解题方法
10 . 微生物在电子供体的作用下可将 (存在形式为
(存在形式为 )还原为更易被去除的
)还原为更易被去除的 ,根据电子供体的不同可分为自养还原和异养还原。为去除水中锑(+5)酸盐,某大学建立升流式硫自养固定床生物反应器,其反应机理如图所示。下列说法正确的是
,根据电子供体的不同可分为自养还原和异养还原。为去除水中锑(+5)酸盐,某大学建立升流式硫自养固定床生物反应器,其反应机理如图所示。下列说法正确的是
 (存在形式为
(存在形式为 )还原为更易被去除的
)还原为更易被去除的 ,根据电子供体的不同可分为自养还原和异养还原。为去除水中锑(+5)酸盐,某大学建立升流式硫自养固定床生物反应器,其反应机理如图所示。下列说法正确的是
,根据电子供体的不同可分为自养还原和异养还原。为去除水中锑(+5)酸盐,某大学建立升流式硫自养固定床生物反应器,其反应机理如图所示。下列说法正确的是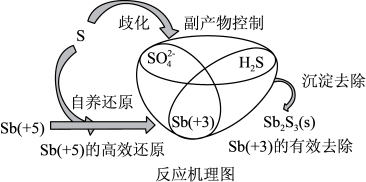
| A.在生物反应器中可以实现S单质的循环利用 |
B.自养还原过程的离子方程式为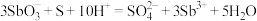 |
C.歧化过程中,氧化产物与还原产物的物质的量之比为 |
D. 的沉淀去除过程发生了氧化还原反应 的沉淀去除过程发生了氧化还原反应 |
您最近一年使用:0次



