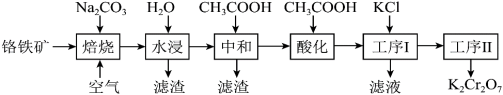
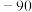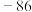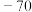1 . 重铬酸钾(K2Cr2O7)是一种重要的化工原料,可用于制铬矾、火柴、铬颜料,并供鞣革、电镀、有机合成等。工业上以铬铁矿[主要成分为Fe(CrO2)2,质量分数为67.2%,杂质主要为硅、铁、铝的氧化物]为原料制备重铬酸钾的工艺流程如图所示:
①焙烧时Fe(CrO2)2中的Fe元素转化为NaFeO2,Cr元素转化为Na2CrO4;铝的氧化物转化为NaAlO2。
②Fe(CrO2)2的摩尔质量为224g/mol,K2Cr2O7的摩尔质量为294g/mol。
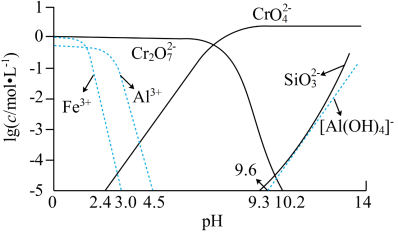
③矿物中相关元素可溶性组分物质的量浓度c(mol•L-1)的对数值与pH的关系如图所示。
请回答下列问题:
(1)写出“焙烧”过程中发生的主要反应的化学方程式:______ 。
(2)“水浸”所得滤渣1的主要成分是Fe(OH)3,写出生成此滤渣的离子方程式:_______ 。
(3)在“中和”步骤中加冰醋酸调节pH约等于7,中和后滤渣2的主要成分是_______ (填化学式)。
(4)“酸化”时加冰醋酸调节pH约等于5,写出酸化过程中发生反应的离子方程式:______ 。
(5)工序I经过滤、洗涤后获得粗产品,经工序Ⅱ得到661.5kg产品,则工序Ⅱ的操作方法是_______ ,生产过程的产率为______ 。
(6)测定产品中K2Cr2O7含量:称取样品2.50g配成250mL溶液,取25.00mL于锥形瓶中,加入足量稀硫酸和几滴指示剂,用0.1000mol•L-1(NH4)2Fe(SO4)2标准液进行滴定。三次实验消耗(NH4)2Fe(SO4)2标准液的平均体积为25.00mL。则样品中K2Cr2O7的纯度为_______ 。(滴定过程中发生的反应为Cr2O +Fe2++H+→Cr3++Fe3++H2O)
+Fe2++H+→Cr3++Fe3++H2O)
①焙烧时Fe(CrO2)2中的Fe元素转化为NaFeO2,Cr元素转化为Na2CrO4;铝的氧化物转化为NaAlO2。
②Fe(CrO2)2的摩尔质量为224g/mol,K2Cr2O7的摩尔质量为294g/mol。
③矿物中相关元素可溶性组分物质的量浓度c(mol•L-1)的对数值与pH的关系如图所示。
请回答下列问题:
(1)写出“焙烧”过程中发生的主要反应的化学方程式:
(2)“水浸”所得滤渣1的主要成分是Fe(OH)3,写出生成此滤渣的离子方程式:
(3)在“中和”步骤中加冰醋酸调节pH约等于7,中和后滤渣2的主要成分是
(4)“酸化”时加冰醋酸调节pH约等于5,写出酸化过程中发生反应的离子方程式:
(5)工序I经过滤、洗涤后获得粗产品,经工序Ⅱ得到661.5kg产品,则工序Ⅱ的操作方法是
(6)测定产品中K2Cr2O7含量:称取样品2.50g配成250mL溶液,取25.00mL于锥形瓶中,加入足量稀硫酸和几滴指示剂,用0.1000mol•L-1(NH4)2Fe(SO4)2标准液进行滴定。三次实验消耗(NH4)2Fe(SO4)2标准液的平均体积为25.00mL。则样品中K2Cr2O7的纯度为
 +Fe2++H+→Cr3++Fe3++H2O)
+Fe2++H+→Cr3++Fe3++H2O)
您最近半年使用:0次
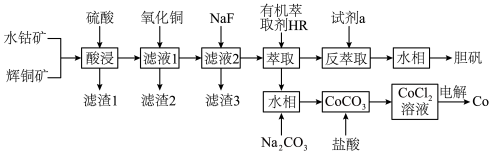
2 . 以水钴矿(Co2O3·H2O,含Fe2O3、MgO、CaO)和辉铜矿(Cu2S,含SiO2、Fe2O3)为原料制取胆矾和单质钴。
①常温下,Ksp(MgF2)=6.25×10-9,Ksp(CaSO4)=7.1×10-7,Ksp(CoCO3)=2.4×10-7;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
③萃取Cu2+的反应原理;Cu2++2HR CuR2+2H+;
CuR2+2H+;
④Mg、Ca、Fe、Co均能与强酸反应产生H2。
回答下列问题:
(1)“酸浸”过程硫元素价态变为+6价,写出“酸浸”过程中主要反应的化学方程式:___________ 。
(2)“滤渣1”的主要成分为___________ 。
(3)常温下,“滤液1”中(Fe元素都以Fe3+形式存在)加“氧化铜”调pH不小于___________ 。
(4)常温下,若“滤液2”中c(Mg2+)=0.015mol/L(忽略溶液中极少量的Ca2+),除去2L“滤液2”中的Mg2+,至少需加入NaF固体的质量为___________ g(忽略溶液体积的变化)。
(5)“反萃取”步骤中加入的“试剂a”为___________ 。
(6)采用惰性电极电解CoCl2溶液﹑在无离子交换膜的条件下,不能用CoSO4溶液代替CoCl2溶液的理由是___________ 。
(7)将制得的胆矾配成溶液,先加入足量氨水,得到深蓝色溶液,再通入SO2至弱酸性,生成白色沉淀。经仪器分析:白色沉淀含H、N,O、S、Cu五种元素,且Cu∶N∶S=1∶4∶l;所含Cu离子中无单电子;晶体的部分组成微粒的空间构型分别为三角锥形和正四面体形。则白色沉淀的化学式为___________ 。
①常温下,Ksp(MgF2)=6.25×10-9,Ksp(CaSO4)=7.1×10-7,Ksp(CoCO3)=2.4×10-7;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 金属离子 | Fe3+ | Fe2+ | Co2+ | Cu2+ |
| 开始沉淀时(c=0.01mol/L)的pH | 2.7 | 7.5 | 7.6 | 4.7 |
| 完全沉淀时(c=10-5mol/L)的pH | 3.7 | 9.0 | 9.1 | 6.2 |
 CuR2+2H+;
CuR2+2H+;④Mg、Ca、Fe、Co均能与强酸反应产生H2。
回答下列问题:
(1)“酸浸”过程硫元素价态变为+6价,写出“酸浸”过程中主要反应的化学方程式:
(2)“滤渣1”的主要成分为
(3)常温下,“滤液1”中(Fe元素都以Fe3+形式存在)加“氧化铜”调pH不小于
(4)常温下,若“滤液2”中c(Mg2+)=0.015mol/L(忽略溶液中极少量的Ca2+),除去2L“滤液2”中的Mg2+,至少需加入NaF固体的质量为
(5)“反萃取”步骤中加入的“试剂a”为
(6)采用惰性电极电解CoCl2溶液﹑在无离子交换膜的条件下,不能用CoSO4溶液代替CoCl2溶液的理由是
(7)将制得的胆矾配成溶液,先加入足量氨水,得到深蓝色溶液,再通入SO2至弱酸性,生成白色沉淀。经仪器分析:白色沉淀含H、N,O、S、Cu五种元素,且Cu∶N∶S=1∶4∶l;所含Cu离子中无单电子;晶体的部分组成微粒的空间构型分别为三角锥形和正四面体形。则白色沉淀的化学式为
您最近半年使用:0次
3 . 某科研小组通过以下方案制备连二亚硫酸钠( )并测定其纯度。
)并测定其纯度。
资料: 具有强还原性,空气中极易被氧化,易溶于水且随温度的升高溶解度增大,不溶于乙醇,在碱性介质中较稳定:低于52℃时
具有强还原性,空气中极易被氧化,易溶于水且随温度的升高溶解度增大,不溶于乙醇,在碱性介质中较稳定:低于52℃时 在水溶液中以
在水溶液中以 形态结晶,高于52℃时
形态结晶,高于52℃时 在碱性溶液中脱水成无水盐。
在碱性溶液中脱水成无水盐。
回答下列问题:
(1)无氧条件下,用锌粉还原 和
和 的混合液,即可制得连二亚硫酸钠;
的混合液,即可制得连二亚硫酸钠;

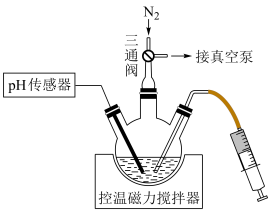
操作步骤:连接装置,关闭三通阀→___________ (填操作名称)→称取一定质量Zn置于三颈烧瓶中→___________ (填标号)pH传感→搅拌直至完全溶解。 和
和 的混合液→充入
的混合液→充入 →抽真空
→抽真空
B.抽真空→注入 和
和 的混合液→充入
的混合液→充入
C.抽真空→充入 →注入
→注入 和
和 的混合液
的混合液
(2)在上述所得溶液中滴加稍过量NaOH溶液控制pH在8.2~10.5之间,使 转化为
转化为 沉淀过滤除去:将所得溶液分批逐步加入一定量的NaCl固体搅拌,水蒸气加热略高于52℃左右结晶→
沉淀过滤除去:将所得溶液分批逐步加入一定量的NaCl固体搅拌,水蒸气加热略高于52℃左右结晶→___________ →用乙醇洗涤→干燥,可获得 。
。
(3)隔绝空气加热 固体完全分解得到固体产物
固体完全分解得到固体产物 、
、 和
和 ,但实验过程未能做到完全隔绝空气,设计实验证明该分解产物中含有
,但实验过程未能做到完全隔绝空气,设计实验证明该分解产物中含有 :
:___________ 。
(4)下图是硫的四种含氧酸根的结构推断具有强氧化性的是___________ (填标号); 转化为
转化为 的离子反应方程式为
的离子反应方程式为___________ 。
(5) 含量的测定
含量的测定
实验原理: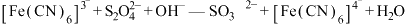 (未配平)。
(未配平)。
实验过程:称取0.25g产品加入三颈烧瓶中,维持氮气氛围,加入适量NaOH溶液,再滴加0.10
 标准溶液,达到滴定终点时消耗22.00mL标准溶液。则产品中
标准溶液,达到滴定终点时消耗22.00mL标准溶液。则产品中 的质量分数为
的质量分数为
___________ %(杂质不参与反应,保留四位有效数字)。
 )并测定其纯度。
)并测定其纯度。资料:
 具有强还原性,空气中极易被氧化,易溶于水且随温度的升高溶解度增大,不溶于乙醇,在碱性介质中较稳定:低于52℃时
具有强还原性,空气中极易被氧化,易溶于水且随温度的升高溶解度增大,不溶于乙醇,在碱性介质中较稳定:低于52℃时 在水溶液中以
在水溶液中以 形态结晶,高于52℃时
形态结晶,高于52℃时 在碱性溶液中脱水成无水盐。
在碱性溶液中脱水成无水盐。回答下列问题:
(1)无氧条件下,用锌粉还原
 和
和 的混合液,即可制得连二亚硫酸钠;
的混合液,即可制得连二亚硫酸钠;
操作步骤:连接装置,关闭三通阀→
 和
和 的混合液→充入
的混合液→充入 →抽真空
→抽真空B.抽真空→注入
 和
和 的混合液→充入
的混合液→充入
C.抽真空→充入
 →注入
→注入 和
和 的混合液
的混合液(2)在上述所得溶液中滴加稍过量NaOH溶液控制pH在8.2~10.5之间,使
 转化为
转化为 沉淀过滤除去:将所得溶液分批逐步加入一定量的NaCl固体搅拌,水蒸气加热略高于52℃左右结晶→
沉淀过滤除去:将所得溶液分批逐步加入一定量的NaCl固体搅拌,水蒸气加热略高于52℃左右结晶→ 。
。(3)隔绝空气加热
 固体完全分解得到固体产物
固体完全分解得到固体产物 、
、 和
和 ,但实验过程未能做到完全隔绝空气,设计实验证明该分解产物中含有
,但实验过程未能做到完全隔绝空气,设计实验证明该分解产物中含有 :
:(4)下图是硫的四种含氧酸根的结构推断具有强氧化性的是
A.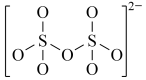 B.
B.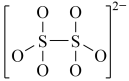 C.
C.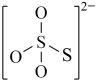 D.
D.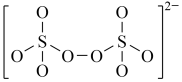
 转化为
转化为 的离子反应方程式为
的离子反应方程式为(5)
 含量的测定
含量的测定实验原理:
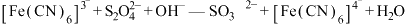 (未配平)。
(未配平)。实验过程:称取0.25g产品加入三颈烧瓶中,维持氮气氛围,加入适量NaOH溶液,再滴加0.10

 标准溶液,达到滴定终点时消耗22.00mL标准溶液。则产品中
标准溶液,达到滴定终点时消耗22.00mL标准溶液。则产品中 的质量分数为
的质量分数为
您最近半年使用:0次
解题方法
4 . 苯胺( ),沸点为184℃,有碱性,易被氧化,微溶于水,易溶于乙醚等有机物,广泛应用于医药和染料行业。实验室用硝基苯与H2反应制备苯胺的反应原理为:
),沸点为184℃,有碱性,易被氧化,微溶于水,易溶于乙醚等有机物,广泛应用于医药和染料行业。实验室用硝基苯与H2反应制备苯胺的反应原理为: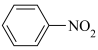 +3H2
+3H2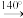
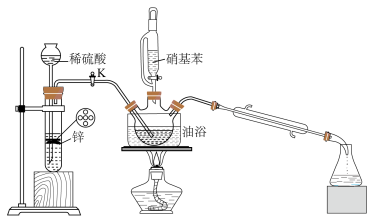
 +2H2O,实验装置如图所示(部分夹持装置省略)。
+2H2O,实验装置如图所示(部分夹持装置省略)。
已知: +HCl
+HCl
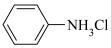 (苯胺盐酸盐,易溶于水)
(苯胺盐酸盐,易溶于水)
(1)试管中发生反应的离子方程式为
(2)实验时,须先打开K,通一段时间H2的原因是
(3)实验制得苯胺粗品中含有少量硝基苯,某同学设计如下流程提纯苯胺、回收硝基苯。
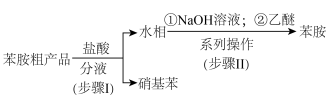
③“步骤Ⅱ”中,加入乙醚的作用是
A.浓硫酸 B.碱石灰 C.无水MgSO4 D.P2O5
您最近半年使用:0次
5 . 短周期主族元素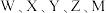 的原子序数依次增大,元素
的原子序数依次增大,元素 位于同一周期,且元素
位于同一周期,且元素 能组成红棕色的大气污染物,金属元素M的单质与冷水反应缓慢,但可与沸水迅速发生置换反应生成W的单质。下列有关说法错误的是
能组成红棕色的大气污染物,金属元素M的单质与冷水反应缓慢,但可与沸水迅速发生置换反应生成W的单质。下列有关说法错误的是
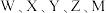 的原子序数依次增大,元素
的原子序数依次增大,元素 位于同一周期,且元素
位于同一周期,且元素 能组成红棕色的大气污染物,金属元素M的单质与冷水反应缓慢,但可与沸水迅速发生置换反应生成W的单质。下列有关说法错误的是
能组成红棕色的大气污染物,金属元素M的单质与冷水反应缓慢,但可与沸水迅速发生置换反应生成W的单质。下列有关说法错误的是A.简单离子半径: |
B.简单氢化物的还原性: |
C.由 三种元素组成的化合物的水溶液可能呈碱性 三种元素组成的化合物的水溶液可能呈碱性 |
D.M的氯化物的电子式为 |
您最近半年使用:0次
解题方法
6 . 某实验小组设计一体化实验,通过量气法测定阿伏加德罗常数,同时制得 并探究其性质.回答下列问题:
并探究其性质.回答下列问题:
I.测定阿伏加德罗常数同时制得 .实验装置如图所示:
.实验装置如图所示:___________ ,阴极发生的电极反应式是___________ ;
(2)烧杯中最终会看到___________ 色沉淀;
(3)在一定电流强度下电解一段时间,收集到的气体体积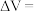
___________  (用含
(用含 的式子表示).将
的式子表示).将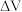 换算成标准状况下的体积记为
换算成标准状况下的体积记为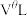 ,已知电路中通过的总电量为
,已知电路中通过的总电量为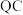 ,1个电子所带的电量为
,1个电子所带的电量为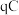 ,则阿伏伽德罗常数
,则阿伏伽德罗常数
___________ (用含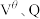 和q的表达式表示)。
和q的表达式表示)。
Ⅱ.探究 的性质.实验小组将上述电解得到的产物
的性质.实验小组将上述电解得到的产物 洗涤干净后,进行如下实验:
洗涤干净后,进行如下实验: 白色,
白色,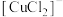 无色,
无色,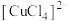 黄色.
黄色.
(4)检验电解产物 洗净需要用到的试剂是
洗净需要用到的试剂是___________ ;
(5)解释溶液颜色由无色变为黄色的原因___________ (用离子方程式表示);
Ⅲ.测量电解产物 的含量。
的含量。
(6)称取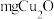 样品置于烧杯中(该样品杂质不与后续试剂反应),加入足量酸性
样品置于烧杯中(该样品杂质不与后续试剂反应),加入足量酸性 溶液,使
溶液,使 全部转化为
全部转化为 ,加入过量
,加入过量 溶液,然后用
溶液,然后用 溶液滴定至终点,消耗
溶液滴定至终点,消耗 .(己知:
.(己知: )
)
则测得电解产物中 的含量为
的含量为___________  。
。
 并探究其性质.回答下列问题:
并探究其性质.回答下列问题:I.测定阿伏加德罗常数同时制得
 .实验装置如图所示:
.实验装置如图所示:
(2)烧杯中最终会看到
(3)在一定电流强度下电解一段时间,收集到的气体体积
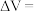
 (用含
(用含 的式子表示).将
的式子表示).将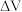 换算成标准状况下的体积记为
换算成标准状况下的体积记为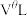 ,已知电路中通过的总电量为
,已知电路中通过的总电量为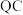 ,1个电子所带的电量为
,1个电子所带的电量为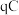 ,则阿伏伽德罗常数
,则阿伏伽德罗常数
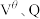 和q的表达式表示)。
和q的表达式表示)。Ⅱ.探究
 的性质.实验小组将上述电解得到的产物
的性质.实验小组将上述电解得到的产物 洗涤干净后,进行如下实验:
洗涤干净后,进行如下实验: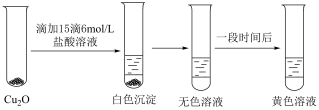
 白色,
白色,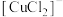 无色,
无色,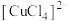 黄色.
黄色.(4)检验电解产物
 洗净需要用到的试剂是
洗净需要用到的试剂是(5)解释溶液颜色由无色变为黄色的原因
Ⅲ.测量电解产物
 的含量。
的含量。(6)称取
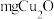 样品置于烧杯中(该样品杂质不与后续试剂反应),加入足量酸性
样品置于烧杯中(该样品杂质不与后续试剂反应),加入足量酸性 溶液,使
溶液,使 全部转化为
全部转化为 ,加入过量
,加入过量 溶液,然后用
溶液,然后用 溶液滴定至终点,消耗
溶液滴定至终点,消耗 .(己知:
.(己知: )
)则测得电解产物中
 的含量为
的含量为 。
。
您最近半年使用:0次
解题方法
7 . 高纯 具有强的抗反射、抗氧化、抗老化的特性,可用于光学镀膜等对纯度要求较高的领域.以氟硅酸制备高纯
具有强的抗反射、抗氧化、抗老化的特性,可用于光学镀膜等对纯度要求较高的领域.以氟硅酸制备高纯 的工艺流程如下:
的工艺流程如下:
回答下列问题:
(1)纯 不稳定,易分解为
不稳定,易分解为 和
和___________ ,但其水溶液可以较稳定存在,能完全电离成 和
和 中心原子的配位数为
中心原子的配位数为___________ .
(2) 在热水中会发生水解,得到两种弱酸和一种盐,写出其发生的化学方程式为
在热水中会发生水解,得到两种弱酸和一种盐,写出其发生的化学方程式为______________________ .
(3)若没有“干燥”工序,会导致“热分解”产生的 纯度降低,其原因是
纯度降低,其原因是______________________ .
(4)“热分解”工序若采用直接加热分解的方式,会观察到生成的副产品1熔融包裹着未分解的物质,且发现随着时间延长分解效率增加不明显,解释原因______________________ .
(5)“合成”时,为了提升产品纯度,反应温度应该控制在___________  .
.
a.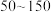 b.
b.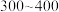 c.
c.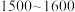
(6)在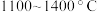 的条件下,将副产品2与
的条件下,将副产品2与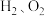 反应,可制得光导纤维的主要成分,反应的化学方程式为
反应,可制得光导纤维的主要成分,反应的化学方程式为______________________ .
 具有强的抗反射、抗氧化、抗老化的特性,可用于光学镀膜等对纯度要求较高的领域.以氟硅酸制备高纯
具有强的抗反射、抗氧化、抗老化的特性,可用于光学镀膜等对纯度要求较高的领域.以氟硅酸制备高纯 的工艺流程如下:
的工艺流程如下: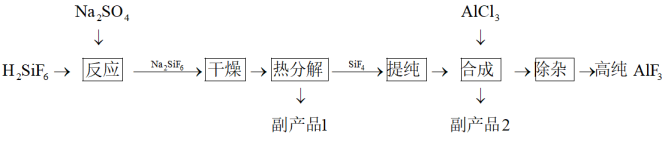
熔点 | 沸点 | 性质 | |
|
|
| 都易水解 |
|
| 57.6 | |
| 1040 | 1537 | |
| 194 | 178(升华) |
(1)纯
 不稳定,易分解为
不稳定,易分解为 和
和 和
和 中心原子的配位数为
中心原子的配位数为(2)
 在热水中会发生水解,得到两种弱酸和一种盐,写出其发生的化学方程式为
在热水中会发生水解,得到两种弱酸和一种盐,写出其发生的化学方程式为(3)若没有“干燥”工序,会导致“热分解”产生的
 纯度降低,其原因是
纯度降低,其原因是(4)“热分解”工序若采用直接加热分解的方式,会观察到生成的副产品1熔融包裹着未分解的物质,且发现随着时间延长分解效率增加不明显,解释原因
(5)“合成”时,为了提升产品纯度,反应温度应该控制在
 .
.a.
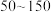 b.
b.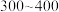 c.
c.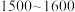
(6)在
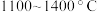 的条件下,将副产品2与
的条件下,将副产品2与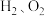 反应,可制得光导纤维的主要成分,反应的化学方程式为
反应,可制得光导纤维的主要成分,反应的化学方程式为
您最近半年使用:0次
解题方法
8 . 钛合金在航空航天领域有着广泛的应用.一种利用废脱硝催化剂(含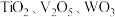 等成分)提取钛的工艺流程如图所示.下列说法错误的是
等成分)提取钛的工艺流程如图所示.下列说法错误的是
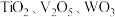 等成分)提取钛的工艺流程如图所示.下列说法错误的是
等成分)提取钛的工艺流程如图所示.下列说法错误的是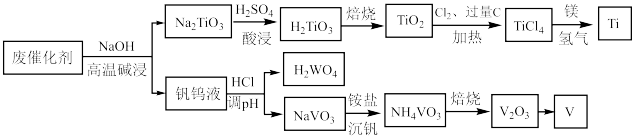
A.基态钛的价层电子排布式为 |
| B.上述流程中共涉及到3个氧化还原反应 |
C.高温碱浸生成 的离子方程式为: 的离子方程式为: |
| D.铝热反应制备钒与上述反应中镁冶炼钛的原理相似 |
您最近半年使用:0次
解题方法
9 . 下列反应的离子方程式错误的是
A. 去除废水中的 去除废水中的 |
B.铜与稀硝酸: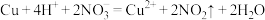 |
C. 加入水中: 加入水中: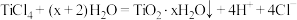 |
D. 溶液滴入 溶液滴入 溶液中: 溶液中: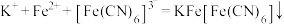 |
您最近半年使用:0次
解题方法
10 . 下列化学用语的表达错误的是
A | B |
| BeCl2的球棍模型 | 尿素的空间填充模型 |
|
|
C | D |
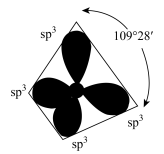
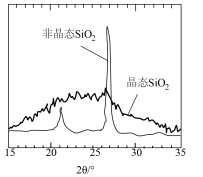
| CH4分子中碳原子杂化轨道的电子云轮廓图 | 非晶态和晶态SiO2粉末X射线衍射图谱对比 |
|
|
| A.A | B.B | C.C | D.D |
您最近半年使用:0次