1 . 某课外小组采用廉价原料NH4VO3、TiO2和Fe2O3,制出含VO2+、TiO2+和Fe3+的金属盐溶液,然后选择氨水作沉淀剂进行共沉淀反应,对共沉淀物[含VO(OH)2、Ti(OH)4、Fe(OH)3]进行煅烧还原制备合金样品,钒基固溶体合金是一类重要的贮氢材料。制备共沉淀物的装置如下图:_______ 、_______ 、_______ 。
(2)装置C中支管插入三颈烧瓶中的作用是_______ 。
(3)制备VO2+时,用草酸将 还原得VO2+。若把草酸改为盐酸,也能得到VO2+,但会产生一种有毒气体,该反应的离子方程式为
还原得VO2+。若把草酸改为盐酸,也能得到VO2+,但会产生一种有毒气体,该反应的离子方程式为_______ 。
(4)反应过程需控制温度为60℃,三颈烧瓶的加热方式是_______ 。
(5)往三颈烧瓶中滴加含金属离子的混合液,得悬浊液,取出充分沉降。
①检测上层清液是否含Fe3+的实验方案是_______ 。
②经过滤、无水乙醇洗涤、低温干燥,得共沉淀物。使用无水乙醇洗涤的优点是_______ 。
(6)将(5)所得共沉淀物煅烧并还原后得钒基固溶体合金。为测定产品中铁的质量分数,取50.60g产品溶于足量稀硫酸(其中V、Ti不溶),过滤,将滤液配成250.00mL,取25.00mL溶液,用0.1000mol/L酸性KMnO4溶液滴定,进行平行实验后,平均消耗KMnO4溶液的体积为20.00mL。则产品中铁的质量分数为_______ 。
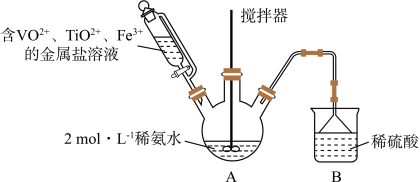
(2)装置C中支管插入三颈烧瓶中的作用是
(3)制备VO2+时,用草酸将
 还原得VO2+。若把草酸改为盐酸,也能得到VO2+,但会产生一种有毒气体,该反应的离子方程式为
还原得VO2+。若把草酸改为盐酸,也能得到VO2+,但会产生一种有毒气体,该反应的离子方程式为(4)反应过程需控制温度为60℃,三颈烧瓶的加热方式是
(5)往三颈烧瓶中滴加含金属离子的混合液,得悬浊液,取出充分沉降。
①检测上层清液是否含Fe3+的实验方案是
②经过滤、无水乙醇洗涤、低温干燥,得共沉淀物。使用无水乙醇洗涤的优点是
(6)将(5)所得共沉淀物煅烧并还原后得钒基固溶体合金。为测定产品中铁的质量分数,取50.60g产品溶于足量稀硫酸(其中V、Ti不溶),过滤,将滤液配成250.00mL,取25.00mL溶液,用0.1000mol/L酸性KMnO4溶液滴定,进行平行实验后,平均消耗KMnO4溶液的体积为20.00mL。则产品中铁的质量分数为
您最近一年使用:0次
2 . 过渡性金属元素在工业生产中有很重要的作用,如金属钼用于制火箭、卫星的合金构件,钼酸钠晶体(Na2MoO4·2H2O)是一种重要的金属缓蚀剂。某工厂利用钼精矿(主要成分MoS2,还含少量钙、镁等元素)为原料冶炼金属钼和钼酸钠晶体(Na2MoO4·2H2O)的主要流程图如下:_______ ,已知Rb(铷)质子数为37,在第五周期ⅠA,Mo的质子数为42,那么Mo在周期表中的位置为第五周期_______ 族。
(2)用浓氨水溶解粗产品的离子方程式是_______ ,由图中信息可以判断MoO3是_______ 氧化物。(填“酸性”、“碱性”或“两性”)
(3)操作Ⅰ是_______ ,操作Ⅱ所得的钼酸要水洗,检验钼酸是否洗涤干净的方法是_______ 。
(4)采用NaClO氧化钼矿的方法将矿石中的钼浸出,该过程放热。①请配平以下化学反应:_______ 。
_______NaClO+_______MoS2+_______NaOH→_______Na2MoO4+_______Na2SO4+_______NaCl+_______H2O
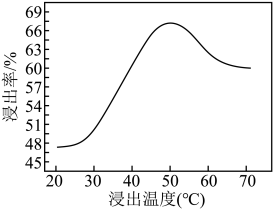
②钼的浸出率随着温度变化如图,当温度高于50℃后浸出率降低的可能原因是_______ (写一点)。 Lix(MoS2)n,则电池工作时正极上的电极反应式为
Lix(MoS2)n,则电池工作时正极上的电极反应式为_______ 。
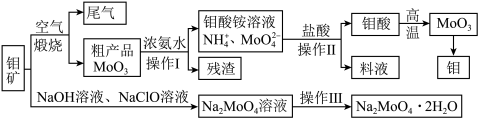
(2)用浓氨水溶解粗产品的离子方程式是
(3)操作Ⅰ是
(4)采用NaClO氧化钼矿的方法将矿石中的钼浸出,该过程放热。①请配平以下化学反应:
_______NaClO+_______MoS2+_______NaOH→_______Na2MoO4+_______Na2SO4+_______NaCl+_______H2O
②钼的浸出率随着温度变化如图,当温度高于50℃后浸出率降低的可能原因是
 Lix(MoS2)n,则电池工作时正极上的电极反应式为
Lix(MoS2)n,则电池工作时正极上的电极反应式为
您最近一年使用:0次
20-21高一上·全国·期末
3 . 已知反应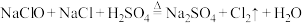 ,为探究氯气的性质,某同学设计了如图所示的实验装置。
,为探究氯气的性质,某同学设计了如图所示的实验装置。
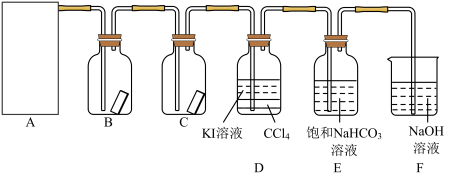
试回答下列问题:
(1)在该实验中,以下可用于制取氯气的装置是_______ (填字母)。
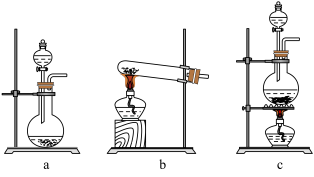
(2)装置B、C中依次放入的是干燥的红色布条和湿润的红色布条,实验过程中该同学发现装置B中的布条也褪色,其原因可能是_______ ,请提出合理的改进方法:_______ 。
(3)写出氯气与 溶液反应的离子方程式:
溶液反应的离子方程式:_______ ,该反应中氧化剂与还原剂的物质的量之比为_______ 。为验证尾气吸收后的溶液中存在 ,正确的操作是
,正确的操作是_______ 。
(4)氯气通入饱和 溶液中能产生无色气体,已知酸性:盐酸>碳酸>次氯酸,该实验可证明
溶液中能产生无色气体,已知酸性:盐酸>碳酸>次氯酸,该实验可证明 与
与 反应的产物中含有
反应的产物中含有_______ (填化学式)。
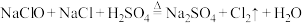 ,为探究氯气的性质,某同学设计了如图所示的实验装置。
,为探究氯气的性质,某同学设计了如图所示的实验装置。
试回答下列问题:
(1)在该实验中,以下可用于制取氯气的装置是

(2)装置B、C中依次放入的是干燥的红色布条和湿润的红色布条,实验过程中该同学发现装置B中的布条也褪色,其原因可能是
(3)写出氯气与
 溶液反应的离子方程式:
溶液反应的离子方程式: ,正确的操作是
,正确的操作是(4)氯气通入饱和
 溶液中能产生无色气体,已知酸性:盐酸>碳酸>次氯酸,该实验可证明
溶液中能产生无色气体,已知酸性:盐酸>碳酸>次氯酸,该实验可证明 与
与 反应的产物中含有
反应的产物中含有
您最近一年使用:0次
2024-03-04更新
|
46次组卷
|
7卷引用:期末模拟卷(一)-2020-2021学年高一化学必修第一册同步单元AB卷(新教材人教版)
(已下线)期末模拟卷(一)-2020-2021学年高一化学必修第一册同步单元AB卷(新教材人教版)(已下线)第二章单元检测 (测)--2020-2021学年上学期高一化学同步精品课堂(人教版必修第一册)重庆市巫山县官渡中学2020-2021学年高一下学期第一次月考化学试题四川省天府新区太平中学2022-2023学年高一上学期期末考试化学试题四川省宜宾市叙州区第二中学校2022-2023学年高一下学期开学考试化学试题安徽省宿州市泗县第一中学2023-2024学年高一下学期开学考试化学试题内蒙古自治区通辽市科尔沁左翼中旗实验高级中学2023-2024学年高一上学期1月期末化学试题
4 . 二氧化氯( )是国际公认的新一代高效、广谱、安全杀菌保鲜剂。
)是国际公认的新一代高效、广谱、安全杀菌保鲜剂。 沸点为11℃,性质不稳定,温度较高或浓度较大时易爆炸,通常用化学方法将其稳定在水溶液中,使用时再释放出来。实验室制备
沸点为11℃,性质不稳定,温度较高或浓度较大时易爆炸,通常用化学方法将其稳定在水溶液中,使用时再释放出来。实验室制备 并转化为“稳定态二氧化氯(
并转化为“稳定态二氧化氯( )”的装置如下(夹持装置省略):
)”的装置如下(夹持装置省略):
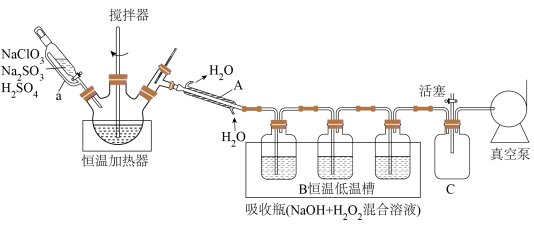
回答下列问题:
(1)仪器A的名称为___________ ,恒压分液漏斗导管a的作用是___________ ;恒温加热器内三颈瓶中发生反应生成 的化学方程式为
的化学方程式为___________ 。
(2)三个吸收瓶( 混合溶液)中发生反应的离子方程式为
混合溶液)中发生反应的离子方程式为___________ ,装置B“恒温低温槽”选择低温的原因是___________ 。
(3)装置C的作用是___________ 。
(4) 溶液中存在
溶液中存在 、
、 、
、 、
、 等四种含氧元素的微粒。经测定,25℃时
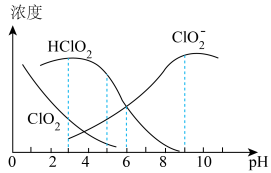
等四种含氧元素的微粒。经测定,25℃时 溶液中部分含氯元素微粒的浓度随pH变化情况如图所示(
溶液中部分含氯元素微粒的浓度随pH变化情况如图所示( 没有标出),则25℃时
没有标出),则25℃时 的电离平衡常数为
的电离平衡常数为
___________ ;pH=5时含氯元素的微粒浓度由大到小的关系为___________ 。
(5)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克 的氧化能力。
的氧化能力。 的有效氯含量为
的有效氯含量为___________ g。(计算结果保留两位小数)
 )是国际公认的新一代高效、广谱、安全杀菌保鲜剂。
)是国际公认的新一代高效、广谱、安全杀菌保鲜剂。 沸点为11℃,性质不稳定,温度较高或浓度较大时易爆炸,通常用化学方法将其稳定在水溶液中,使用时再释放出来。实验室制备
沸点为11℃,性质不稳定,温度较高或浓度较大时易爆炸,通常用化学方法将其稳定在水溶液中,使用时再释放出来。实验室制备 并转化为“稳定态二氧化氯(
并转化为“稳定态二氧化氯( )”的装置如下(夹持装置省略):
)”的装置如下(夹持装置省略):
回答下列问题:
(1)仪器A的名称为
 的化学方程式为
的化学方程式为(2)三个吸收瓶(
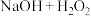 混合溶液)中发生反应的离子方程式为
混合溶液)中发生反应的离子方程式为(3)装置C的作用是
(4)
 溶液中存在
溶液中存在 、
、 、
、 、
、 等四种含氧元素的微粒。经测定,25℃时
等四种含氧元素的微粒。经测定,25℃时 溶液中部分含氯元素微粒的浓度随pH变化情况如图所示(
溶液中部分含氯元素微粒的浓度随pH变化情况如图所示( 没有标出),则25℃时
没有标出),则25℃时 的电离平衡常数为
的电离平衡常数为

(5)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克
 的氧化能力。
的氧化能力。 的有效氯含量为
的有效氯含量为
您最近一年使用:0次
5 . A、B、C、D四种可溶性物质,都是由下表中的离子形成的。
已知每种物质中阴阳离子互不重复。
①若把四种物质分别溶解于盛有蒸馏水的四支试管中,只有C溶液呈蓝色。
②若向①的四支试管中分别加盐酸,B溶液有沉淀产生,D溶液有无色无味的气体逸出。
(1)根据①②实验事实可推断它们的化学式为:
A___________ ,B___________ ,C___________ ,D___________ 。
(2)写出下列反应的离子方程式:
a.A溶液与C溶液混合:___________ 。
b.向A溶液中加入 溶液至
溶液至 恰好沉淀完全:
恰好沉淀完全:___________ 。
| 阳离子 |  、 、 、 、 、 、 |
| 阴离子 |  、 、 、 、 、 、 |
①若把四种物质分别溶解于盛有蒸馏水的四支试管中,只有C溶液呈蓝色。
②若向①的四支试管中分别加盐酸,B溶液有沉淀产生,D溶液有无色无味的气体逸出。
(1)根据①②实验事实可推断它们的化学式为:
A
(2)写出下列反应的离子方程式:
a.A溶液与C溶液混合:
b.向A溶液中加入
 溶液至
溶液至 恰好沉淀完全:
恰好沉淀完全:
您最近一年使用:0次
解题方法
6 . 中国载人潜水器“奋斗者”号,在西太平洋马里亚纳海沟成功下潜突破10000米,达到10909米,创造了中国载人深潜的新纪录。“奋斗者”号抗压关键——坚固、宽大的球形载人仓是由钛合金制成的。以钛铁矿[主要成分钛酸亚铁( )]为主要原料冶炼金属钛,同时还可得到副产物绿矾,其生产的工艺流程如图所示:
)]为主要原料冶炼金属钛,同时还可得到副产物绿矾,其生产的工艺流程如图所示:
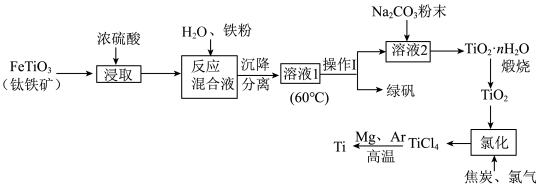
已知:钛铁矿与浓硫酸发生反应的化学方程式为 ;
; 易水解,只能存于强酸性溶液中。
易水解,只能存于强酸性溶液中。
回答下列问题:
(1) 中Ti的化合价为
中Ti的化合价为___________ ;反应混合液中加入铁粉的目的是___________ 。
(2)溶液1经“操作I”可得副产品绿矾,则操作I的名称为___________ ;在此操作过程中,需控制溶液的温度,若溶液1的温度过高,会使最终钛的产率___________ (填“升高”或“降低”),理由是___________ 。
(3)溶液2中含有的主要离子是 ,加入
,加入 粉末可得到固体
粉末可得到固体 ,请结合原理和化学用语解释其原因:
,请结合原理和化学用语解释其原因:___________ 。
(4)“氯化”是焦炭、氯气在高温下发生反应制取 ,并得到一种可燃性气体,其化学方程式为
,并得到一种可燃性气体,其化学方程式为___________ 。
(5)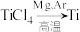 反应后得到Mg、
反应后得到Mg、 、Ti的混合物,可采用真空蒸馏的方法分离得到Ti,依据下表信息,蒸馏时需加热的温度应略高于
、Ti的混合物,可采用真空蒸馏的方法分离得到Ti,依据下表信息,蒸馏时需加热的温度应略高于___________ ℃即可。
(6)钛酸锂( )是一种理想型嵌入材料,插入与脱嵌对材料结构几乎没影响。某新型钛酸锂电池的总反应为
)是一种理想型嵌入材料,插入与脱嵌对材料结构几乎没影响。某新型钛酸锂电池的总反应为 ,则放电时其负极反应式为
,则放电时其负极反应式为___________ 。
 )]为主要原料冶炼金属钛,同时还可得到副产物绿矾,其生产的工艺流程如图所示:
)]为主要原料冶炼金属钛,同时还可得到副产物绿矾,其生产的工艺流程如图所示:
已知:钛铁矿与浓硫酸发生反应的化学方程式为
 ;
; 易水解,只能存于强酸性溶液中。
易水解,只能存于强酸性溶液中。回答下列问题:
(1)
 中Ti的化合价为
中Ti的化合价为(2)溶液1经“操作I”可得副产品绿矾,则操作I的名称为
(3)溶液2中含有的主要离子是
 ,加入
,加入 粉末可得到固体
粉末可得到固体 ,请结合原理和化学用语解释其原因:
,请结合原理和化学用语解释其原因:(4)“氯化”是焦炭、氯气在高温下发生反应制取
 ,并得到一种可燃性气体,其化学方程式为
,并得到一种可燃性气体,其化学方程式为(5)
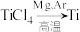 反应后得到Mg、
反应后得到Mg、 、Ti的混合物,可采用真空蒸馏的方法分离得到Ti,依据下表信息,蒸馏时需加热的温度应略高于
、Ti的混合物,可采用真空蒸馏的方法分离得到Ti,依据下表信息,蒸馏时需加热的温度应略高于| 物质 |  | Mg |  | Ti |
| 熔点/℃ | -25.0 | 648.8 | 714 | 1667 |
| 沸点/℃ | 136.4 | 1090 | 1412 | 3287 |
(6)钛酸锂(
 )是一种理想型嵌入材料,插入与脱嵌对材料结构几乎没影响。某新型钛酸锂电池的总反应为
)是一种理想型嵌入材料,插入与脱嵌对材料结构几乎没影响。某新型钛酸锂电池的总反应为 ,则放电时其负极反应式为
,则放电时其负极反应式为
您最近一年使用:0次
7 . 北京时间10月7日,2020年诺贝尔化学奖揭晓。法国科学家Emmanuelle Charpentier和美国科学家JenniferA.Doudna获奖,以表彰她们“开发出一种基因组编辑方法”。利用CRISPR/Cas9“基因剪刀”,现在可以在几周的时间内改变生命密码。研究表明,该“基因剪刀”中的Cas9蛋白质可以水解产生20种氨基酸,其中含量最多的一种氨基酸是赖氨酸(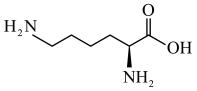 )。工业上制备赖氨酸有很多方法:
)。工业上制备赖氨酸有很多方法:
(1)由葡萄糖在一定的条件下进行耗氧发酵,生成赖氨酸的化学方程式为 。该反应的理论产率是
。该反应的理论产率是___________ (精确到0.1%,已知理论产率=目标产物的质量/反应物的质量,产物和反应物均只指有机物)。
(2)由尼龙-6生产过程中的废料(A)经过下列途径也可制备赖氨酸(E)。
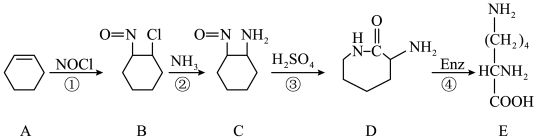
①物质A的名称是___________ ,赖氨酸中官能团的名称是___________ 。
②反应①的类型是___________ 。
③反应②的化学方程式为___________ 。
④C、D两种物质的关系是___________ 。
⑤E的同分异构体很多,同时满足下列条件的E的同分异构体有___________ 种(不含立体异构)。
A.能发生银镜反应和水解反应 B.分子中含两个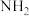 但不含
但不含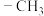
其中一氯取代物有三种的结构简式是___________ 。
(3)工业上也可用己内酰胺为原料,通过下述途径生产赖氨酸。

请补充完整该合成路线___________ 。
 )。工业上制备赖氨酸有很多方法:
)。工业上制备赖氨酸有很多方法:(1)由葡萄糖在一定的条件下进行耗氧发酵,生成赖氨酸的化学方程式为
 。该反应的理论产率是
。该反应的理论产率是(2)由尼龙-6生产过程中的废料(A)经过下列途径也可制备赖氨酸(E)。

①物质A的名称是
②反应①的类型是
③反应②的化学方程式为
④C、D两种物质的关系是
⑤E的同分异构体很多,同时满足下列条件的E的同分异构体有
A.能发生银镜反应和水解反应 B.分子中含两个
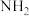 但不含
但不含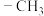
其中一氯取代物有三种的结构简式是
(3)工业上也可用己内酰胺为原料,通过下述途径生产赖氨酸。

请补充完整该合成路线
您最近一年使用:0次
8 . 如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
(1)该浓盐酸中HCl的物质的量浓度为________________ mol.L-1。
(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是_______________(填字母)。
(3)某学生欲用上述浓盐酸和蒸馏水配制500mL物质的量浓度为0.400mol.L-1的稀盐酸。
①该学生需要量取_______________ mL上述浓盐酸进行配制。
②在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(在括号内填A表示“偏大”、填B表示“偏小”、填C表示“无影响”)。
a.用量筒量取浓盐酸时俯视观察凹液面________
b定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水________
(4)①假设该同学成功配制了0.400mol.L-1的盐酸,他又用该盐酸中和含0.4gNaOH的NaOH溶液,则该同学需取_______________ mL盐酸。
②假设该同学用新配制的盐酸中和含0.4 g NaOH的NaOH溶液,发现比①中所求体积偏小,则可能的原因是_______________ 。(填字母)
A.浓盐酸挥发,浓度不足
B.配制溶液时,未洗涤烧杯
C.配制溶液时,俯视容量瓶刻度线
D.加水时超过刻度线,用胶头滴管吸出
| 盐酸 分子式:HCl 相对分子质量:36.5 密度:1.19g.cm-3 HCl的质量分数:36.5% |
(1)该浓盐酸中HCl的物质的量浓度为
(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是_______________(填字母)。
| A.溶液中HCl的物质的量 | B.溶液的物质的量浓度 |
| C.溶液中Cl-的数目 | D.溶液的密度 |
(3)某学生欲用上述浓盐酸和蒸馏水配制500mL物质的量浓度为0.400mol.L-1的稀盐酸。
①该学生需要量取
②在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(在括号内填A表示“偏大”、填B表示“偏小”、填C表示“无影响”)。
a.用量筒量取浓盐酸时俯视观察凹液面
b定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水
(4)①假设该同学成功配制了0.400mol.L-1的盐酸,他又用该盐酸中和含0.4gNaOH的NaOH溶液,则该同学需取
②假设该同学用新配制的盐酸中和含0.4 g NaOH的NaOH溶液,发现比①中所求体积偏小,则可能的原因是
A.浓盐酸挥发,浓度不足
B.配制溶液时,未洗涤烧杯
C.配制溶液时,俯视容量瓶刻度线
D.加水时超过刻度线,用胶头滴管吸出
您最近一年使用:0次
2024-01-07更新
|
20次组卷
|
2卷引用:云南省大理白族自治州实验中学2020-2021学年高一上学期12月月考化学试题
名校
解题方法
9 . 有A、B、C三种粉末,其焰色反应均为紫色,它们具有下列性质:
①均易溶于水,且A与B反应生成C;
②加热B的粉末时,生成无色无刺激性气味的气体D,D能使澄清的石灰水变浑浊,浑浊物为E;
③加热A、C时均不反应;
④向少量C溶液中通入D可以得到B;
⑤A溶液和D反应,A过量时生成C,A不足时生成B.
请回答下列问题:
(1)写出下列字母代表物质的化学式:A:_____ ;B:_____ 。
(2)用离子方程式表示下列反应:
A+B:_____ ;
D→E:_____ ;
A+D→B:_____ 。
①均易溶于水,且A与B反应生成C;
②加热B的粉末时,生成无色无刺激性气味的气体D,D能使澄清的石灰水变浑浊,浑浊物为E;
③加热A、C时均不反应;
④向少量C溶液中通入D可以得到B;
⑤A溶液和D反应,A过量时生成C,A不足时生成B.
请回答下列问题:
(1)写出下列字母代表物质的化学式:A:
(2)用离子方程式表示下列反应:
A+B:
D→E:
A+D→B:
您最近一年使用:0次
名校
10 . NiSO4主要用于电镀工业,作为电镀镍和化学镍的主要原料,也用于生产其他镍盐(如氧化镍、硫酸镍铵、碳酸镍等),从矿渣[含NiFe2O4(铁酸镍)、NiO、FeO、CaO、SiO2等]中回收NiSO4的工艺流程如图:
(1)“浸渣”的成分有Fe2O3、FeO(OH)、CaSO4外,还含有___________ (写化学式)。
(2)矿渣中部分FeO焙烧时与H2SO4反应生成Fe2(SO4)3的化学方程式为___________ 。
(3)向“浸取液”中加入NaF以除去溶液中Ca2+(浓度为1.0×10-3mol•L﹣1),当溶液中c(F﹣)=2.0×10-3.5mol•L-1时,除钙率为___________ [Ksp(CaF2)=4.0×10-11]。
(4)溶剂萃取可用于对溶液中的金属离子进行富集与分离:Fe2+(水相)+2RH(有机相) FeR(有机相)+2H+(水相)。萃取剂与溶液的体积比(V0/VA)对溶液中Ni2+、Fe2+的萃取率影响如图所示,V0/VA的最佳取值为
FeR(有机相)+2H+(水相)。萃取剂与溶液的体积比(V0/VA)对溶液中Ni2+、Fe2+的萃取率影响如图所示,V0/VA的最佳取值为 ___________ 。在 ___________ (填“强碱性”“强酸性”或“中性”)介质中“反萃取”能使有机相再生而循环利用。 。
。___________ ,离子交换膜(b)为 ___________ (填“阴”或“阳”)离子交换膜。
②向铁电极区出现的红褐色物质中加入少量的NaClO溶液,沉淀溶解。该反应的离子方程式为___________ 。
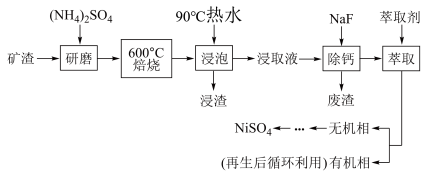
(1)“浸渣”的成分有Fe2O3、FeO(OH)、CaSO4外,还含有
(2)矿渣中部分FeO焙烧时与H2SO4反应生成Fe2(SO4)3的化学方程式为
(3)向“浸取液”中加入NaF以除去溶液中Ca2+(浓度为1.0×10-3mol•L﹣1),当溶液中c(F﹣)=2.0×10-3.5mol•L-1时,除钙率为
(4)溶剂萃取可用于对溶液中的金属离子进行富集与分离:Fe2+(水相)+2RH(有机相)
 FeR(有机相)+2H+(水相)。萃取剂与溶液的体积比(V0/VA)对溶液中Ni2+、Fe2+的萃取率影响如图所示,V0/VA的最佳取值为
FeR(有机相)+2H+(水相)。萃取剂与溶液的体积比(V0/VA)对溶液中Ni2+、Fe2+的萃取率影响如图所示,V0/VA的最佳取值为 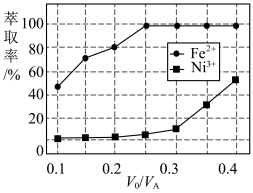
 。
。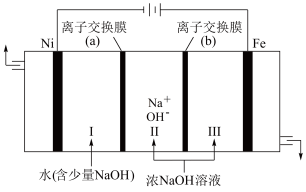
②向铁电极区出现的红褐色物质中加入少量的NaClO溶液,沉淀溶解。该反应的离子方程式为
您最近一年使用:0次
2023-10-03更新
|
553次组卷
|
7卷引用:【市级联考】山东省威海市2019届高三下学期5月高考模拟考试理科综合化学试题



