名校
解题方法
1 . 某稀溶液中含有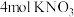 和
和 ,向其中加入
,向其中加入 ,充分反应(已知
,充分反应(已知 被还原为NO),最终溶液体积为
被还原为NO),最终溶液体积为 ,下列说法正确的是
,下列说法正确的是
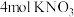 和
和 ,向其中加入
,向其中加入 ,充分反应(已知
,充分反应(已知 被还原为NO),最终溶液体积为
被还原为NO),最终溶液体积为 ,下列说法正确的是
,下列说法正确的是A.所得溶液中的溶质只有 、 、 |
B.所得溶液中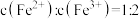 |
C.反应后生成NO的体积为 (标准状况下) (标准状况下) |
D.所得溶液中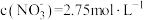 |
您最近一年使用:0次
名校
2 . 用 表示阿伏伽德罗常数的值,下列说法正确的是
表示阿伏伽德罗常数的值,下列说法正确的是
 表示阿伏伽德罗常数的值,下列说法正确的是
表示阿伏伽德罗常数的值,下列说法正确的是A.现有乙烯、丙烯的混合气体共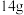 ,其原子数为 ,其原子数为 |
B.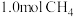 与 与 在光照下反应生成的 在光照下反应生成的 分子数为 分子数为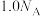 |
C.足量的铜与 浓硝酸充分反应,转移的电子数目为 浓硝酸充分反应,转移的电子数目为 |
D.常温常压下, 46%的乙醇溶液中,含H—O键的数目为 46%的乙醇溶液中,含H—O键的数目为 |
您最近一年使用:0次
名校
3 . 工业上制硫化钡普遍采用两种方法:一种为重晶石( )煤粉还原法(将重晶石和无烟煤混合后在1000-1200℃下还原焙烧1~2h);另一种为气体还原法(将重晶石在850-900℃通入氢气进行还原反应)。下列是实验室模拟高温下
)煤粉还原法(将重晶石和无烟煤混合后在1000-1200℃下还原焙烧1~2h);另一种为气体还原法(将重晶石在850-900℃通入氢气进行还原反应)。下列是实验室模拟高温下 还原重晶石法,装置如下。
还原重晶石法,装置如下。
(1)固体A的名称___________ 。
(2) 与
与 反应生成BaS,写出该反应的化学方程式
反应生成BaS,写出该反应的化学方程式___________ 。
(3)打开活塞K之后,管式炉升温之前,必须进行的操作为___________ 。
(4)测定BaS质量分数:
取生成物10.00 g,溶于蒸馏水后稀释至500 mL;取25.00 mL溶液于锥形瓶中,再加入10 mL2%醋酸溶液及10.00 mL 0.50 mol/L 标准溶液(过量),充分振荡、使BaS中的硫元素完全转化为硫单质;向锥形瓶中加入2滴淀粉溶液做指示剂,用0.50 mol/L
标准溶液(过量),充分振荡、使BaS中的硫元素完全转化为硫单质;向锥形瓶中加入2滴淀粉溶液做指示剂,用0.50 mol/L  标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 标准溶液体积10.00 mL(滴定反应为:
标准溶液体积10.00 mL(滴定反应为: )已知醋酸的酸性强于氢硫酸。
)已知醋酸的酸性强于氢硫酸。
①稀释至500 mL所需的玻璃仪器有烧杯、胶头滴管、___________ 和___________ 。
②写出 与BaS反应的化学方程式
与BaS反应的化学方程式___________ 。
③醋酸溶液加多了会导致测定结果偏小,原因可能是___________ 。
④计算样品中BaS( g/mol)质量分数:
g/mol)质量分数:___________ (保留3位有效数字)。
 )煤粉还原法(将重晶石和无烟煤混合后在1000-1200℃下还原焙烧1~2h);另一种为气体还原法(将重晶石在850-900℃通入氢气进行还原反应)。下列是实验室模拟高温下
)煤粉还原法(将重晶石和无烟煤混合后在1000-1200℃下还原焙烧1~2h);另一种为气体还原法(将重晶石在850-900℃通入氢气进行还原反应)。下列是实验室模拟高温下 还原重晶石法,装置如下。
还原重晶石法,装置如下。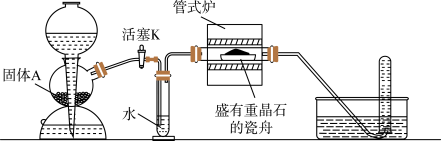
(1)固体A的名称
(2)
 与
与 反应生成BaS,写出该反应的化学方程式
反应生成BaS,写出该反应的化学方程式(3)打开活塞K之后,管式炉升温之前,必须进行的操作为
(4)测定BaS质量分数:
取生成物10.00 g,溶于蒸馏水后稀释至500 mL;取25.00 mL溶液于锥形瓶中,再加入10 mL2%醋酸溶液及10.00 mL 0.50 mol/L
 标准溶液(过量),充分振荡、使BaS中的硫元素完全转化为硫单质;向锥形瓶中加入2滴淀粉溶液做指示剂,用0.50 mol/L
标准溶液(过量),充分振荡、使BaS中的硫元素完全转化为硫单质;向锥形瓶中加入2滴淀粉溶液做指示剂,用0.50 mol/L  标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 标准溶液体积10.00 mL(滴定反应为:
标准溶液体积10.00 mL(滴定反应为: )已知醋酸的酸性强于氢硫酸。
)已知醋酸的酸性强于氢硫酸。①稀释至500 mL所需的玻璃仪器有烧杯、胶头滴管、
②写出
 与BaS反应的化学方程式
与BaS反应的化学方程式③醋酸溶液加多了会导致测定结果偏小,原因可能是
④计算样品中BaS(
 g/mol)质量分数:
g/mol)质量分数:
您最近一年使用:0次
名校
解题方法
4 . 氯化钡是重要的化工原料,是制备其他钡盐的主要中间原料,以毒重石(主要成分为 ,还含有
,还含有 及含Ca、Mg、Fe、Al的化合物)为原料制备
及含Ca、Mg、Fe、Al的化合物)为原料制备 的工艺流程如下:
的工艺流程如下: 、
、 、
、 、
、 形式存在于溶液中。
形式存在于溶液中。
回答下列问题:
(1)在“浸取”时,除温度、酸的浓度、液固比等因素影响钡的浸出率外,还有___________ 因素。
(2)下表列举了不同温度、盐酸的浓度、液固比下钡的浸出率实验数据,每个实验只改变一个条件:
分析表中数据,温度越高钡的浸出率越低的可能原因是___________ ;判断“浸取”的最佳液固比为___________ 。
(3)常温时,几种金属离子沉淀的pH如图所示,加 时发生反应的离子方程式为
时发生反应的离子方程式为___________ ;“调pH(Ⅰ)”时,调节溶液 ,则“滤渣Ⅱ”的主要成分为
,则“滤渣Ⅱ”的主要成分为___________ (填化学式)。___________ 。
 ,还含有
,还含有 及含Ca、Mg、Fe、Al的化合物)为原料制备
及含Ca、Mg、Fe、Al的化合物)为原料制备 的工艺流程如下:
的工艺流程如下: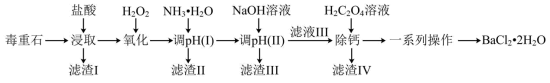
 、
、 、
、 、
、 形式存在于溶液中。
形式存在于溶液中。回答下列问题:
(1)在“浸取”时,除温度、酸的浓度、液固比等因素影响钡的浸出率外,还有
(2)下表列举了不同温度、盐酸的浓度、液固比下钡的浸出率实验数据,每个实验只改变一个条件:
| 改变的条件 | 温度(℃) | 盐酸的浓度(%) | 液固比 | ||||||||
| 30 | 55 | 75 | 10 | 15 | 20 | 25 | 3:1 | 4:1 | 5:1 | 6:1 | |
| 钡的浸出率(%) | 74.31 | 69.60 | 68.42 | 59.21 | 74.31 | 74.15 | 55.32 | 59.84 | 65.12 | 74.31 | 74.35 |
(3)常温时,几种金属离子沉淀的pH如图所示,加
 时发生反应的离子方程式为
时发生反应的离子方程式为 ,则“滤渣Ⅱ”的主要成分为
,则“滤渣Ⅱ”的主要成分为
您最近一年使用:0次
5 . 下列化学用语表达正确的是
A.HClO的结构式: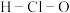 | B.中子数为20的氯原子: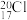 |
C. 的VSEPR模型: 的VSEPR模型: | D.羟基的电子式: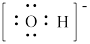 |
您最近一年使用:0次
名校
解题方法
6 . 下列图示或化学用语错误 的是
A.羟基的电子式: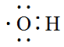 |
B.H2O的VSEPR模型: |
C.Mn2+的价电子的轨道表示式: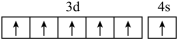 |
D.顺-2-丁烯的球棍模型为 |
您最近一年使用:0次
解题方法
7 . 下列方程式正确的是
A.在硫酸铜溶液中滴加少量氨水: |
B.锌锰碱性电池放电时正极反应式为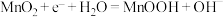 |
C.一定条件下,由乳酸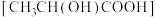 合成聚乳酸的化学方程式: 合成聚乳酸的化学方程式: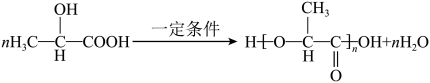 |
D.在新制 浊液中加入甲酸甲酯共热产生砖红色沉淀: 浊液中加入甲酸甲酯共热产生砖红色沉淀: |
您最近一年使用:0次
名校
解题方法
8 . 下列各组离子可能大量共存的是
| A.遇酚酞变红的溶液中:Na+、Cl-、Ba2+、CH3COO- |
B.常温下,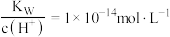 的溶液中: 的溶液中: 、Fe2+、 、Fe2+、 、 、 |
C.水电离出的 的溶液中:Na+、K+、Cl-、 的溶液中:Na+、K+、Cl-、 |
D.滴加KSCN溶液显红色的溶液中: 、K+、Cl-、I- 、K+、Cl-、I- |
您最近一年使用:0次
9 .  下,某反应体系只存在如下8种物质:
下,某反应体系只存在如下8种物质: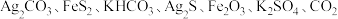 和
和 ,其中,甲既是氧化剂,又是还原剂,乙是还原产物,丙和丁是氧化产物,甲、乙、丙、丁四种物质的物质的量
,其中,甲既是氧化剂,又是还原剂,乙是还原产物,丙和丁是氧化产物,甲、乙、丙、丁四种物质的物质的量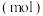 与时间关系如图所示。设
与时间关系如图所示。设 为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是
 下,某反应体系只存在如下8种物质:
下,某反应体系只存在如下8种物质: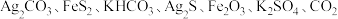 和
和 ,其中,甲既是氧化剂,又是还原剂,乙是还原产物,丙和丁是氧化产物,甲、乙、丙、丁四种物质的物质的量
,其中,甲既是氧化剂,又是还原剂,乙是还原产物,丙和丁是氧化产物,甲、乙、丙、丁四种物质的物质的量 与时间关系如图所示。设
与时间关系如图所示。设 为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是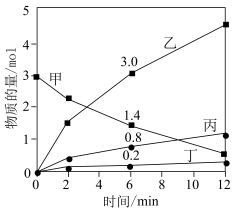
A.甲代表 ,丁为碱性氧化物 ,丁为碱性氧化物 |
B.还原产物、氧化产物的物质的量之比 |
C. 甲完全反应转移电子数为 甲完全反应转移电子数为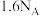 |
D.在该反应中,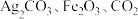 的化学计量数之比为 的化学计量数之比为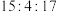 |
您最近一年使用:0次
10 . 金属钠及其化合物在人类生产生活中起着重要作用。回答下列问题:
(1)Na2O2的电子式为_______ 。Na2O2可作供氧剂,写出Na2O2与CO2反应的化学方程式_______ 。若有1molNa2O2参加反应则转移电子的物质的量为_______ mol。
(2)采用空气和Na为原料可直接制备Na2O2。空气与熔融金属Na反应前需依次通过_______ 、_______ (填序号)。
a.浓硫酸 b.饱和食盐水 c.NaOH溶液 d.KMnO4溶液
(3)天然碱的主要成分为Na2CO3·NaHCO3·2H2O,1molNa2CO3·NaHCO3·2H2O经充分加热得到Na2CO3的质量为_______ g。
(1)Na2O2的电子式为
(2)采用空气和Na为原料可直接制备Na2O2。空气与熔融金属Na反应前需依次通过
a.浓硫酸 b.饱和食盐水 c.NaOH溶液 d.KMnO4溶液
(3)天然碱的主要成分为Na2CO3·NaHCO3·2H2O,1molNa2CO3·NaHCO3·2H2O经充分加热得到Na2CO3的质量为
您最近一年使用:0次



