1 . 风绪小组探究 的相关性质。
的相关性质。
(1)对于 和水反应放出氧气的现象,他们推测,可能和
和水反应放出氧气的现象,他们推测,可能和 有关。通过实验发现,用冷水时,该反应放出气体的速率相对慢,而换用热水相对快。从而推测可能是
有关。通过实验发现,用冷水时,该反应放出气体的速率相对慢,而换用热水相对快。从而推测可能是 在水中反应生成了
在水中反应生成了 ,后
,后 分解。通过查阅资料得知:
分解。通过查阅资料得知: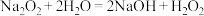 ,
,
①借助资料和实验,发现可以通过 溶于冷水制备少量的
溶于冷水制备少量的 。使用冷水的原因是
。使用冷水的原因是_______ 。
②为验证资料的真实性,他们向溶液中滴加适量的酸性 溶液,发现产生气泡,产生气泡的原因是(用方程式表示)
溶液,发现产生气泡,产生气泡的原因是(用方程式表示)_______ 。
(2)在有同学做实验时,还观察到了棕褐色沉淀,他们推测是 。猜测可能是
。猜测可能是 与
与 发生了反应。为验证猜想以及探究实验现象不一样的原因,他们做了如下实验。
发生了反应。为验证猜想以及探究实验现象不一样的原因,他们做了如下实验。
①先向沉淀中加入浓盐酸并加热,观察到有_______ 气体产生,发生反应_______ 。证明了猜想正确。
②后续得知,同学在制酸性 溶液时,加入的硫酸的量不一样。推测可能是
溶液时,加入的硫酸的量不一样。推测可能是 浓度不同造成的。于是,他们改用有
浓度不同造成的。于是,他们改用有 的
的 溶液滴入
溶液滴入 溶液中,仅观察到了
溶液中,仅观察到了_______ 沉淀,并证明是 ,反应方程式是
,反应方程式是_______ 。
(3) 在反应时,表现氧化性还是还原性,和
在反应时,表现氧化性还是还原性,和_______ 有关。
 的相关性质。
的相关性质。(1)对于
 和水反应放出氧气的现象,他们推测,可能和
和水反应放出氧气的现象,他们推测,可能和 有关。通过实验发现,用冷水时,该反应放出气体的速率相对慢,而换用热水相对快。从而推测可能是
有关。通过实验发现,用冷水时,该反应放出气体的速率相对慢,而换用热水相对快。从而推测可能是 在水中反应生成了
在水中反应生成了 ,后
,后 分解。通过查阅资料得知:
分解。通过查阅资料得知: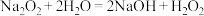 ,
,
①借助资料和实验,发现可以通过
 溶于冷水制备少量的
溶于冷水制备少量的 。使用冷水的原因是
。使用冷水的原因是②为验证资料的真实性,他们向溶液中滴加适量的酸性
 溶液,发现产生气泡,产生气泡的原因是(用方程式表示)
溶液,发现产生气泡,产生气泡的原因是(用方程式表示)(2)在有同学做实验时,还观察到了棕褐色沉淀,他们推测是
 。猜测可能是
。猜测可能是 与
与 发生了反应。为验证猜想以及探究实验现象不一样的原因,他们做了如下实验。
发生了反应。为验证猜想以及探究实验现象不一样的原因,他们做了如下实验。①先向沉淀中加入浓盐酸并加热,观察到有
②后续得知,同学在制酸性
 溶液时,加入的硫酸的量不一样。推测可能是
溶液时,加入的硫酸的量不一样。推测可能是 浓度不同造成的。于是,他们改用有
浓度不同造成的。于是,他们改用有 的
的 溶液滴入
溶液滴入 溶液中,仅观察到了
溶液中,仅观察到了 ,反应方程式是
,反应方程式是(3)
 在反应时,表现氧化性还是还原性,和
在反应时,表现氧化性还是还原性,和
您最近一年使用:0次
名校
解题方法
2 . 亚硝酸钠(NaNO2)的外观与NaCl相似,有毒。它在工业上可作染料、助染剂,医药上能用作器碱消毒剂、防腐剂等。
已知:①NaNO2有强氧化性又有还原性;
②NO能被酸性KMnO4氧化成硝酸根离子;
③亚硝酸是弱酸,很不稳定,易分解为NO2、NO和水。
某兴趣小组用下列装置(夹持仪器已省略)制取较纯净的NaNO2。
反应原理为:2NO+Na2O2=2NaNO2

回答下列问题:
(1)乙装置的仪器名称是____ ,装置乙的作用是____ 。
(2)甲中滴入稀硝酸前需先通入N2,原因是____ 。
(3)甲装置中发生反应的离子方程式为____ 。
(4)反应过程中观察到丙中的现象为___ 。
(5)丁中酸性KMnO4的作用是____ 。
(6)设计实验证明丙装置有NaNO2生成____ (写出操作、试剂和现象)。
已知:①NaNO2有强氧化性又有还原性;
②NO能被酸性KMnO4氧化成硝酸根离子;
③亚硝酸是弱酸,很不稳定,易分解为NO2、NO和水。
某兴趣小组用下列装置(夹持仪器已省略)制取较纯净的NaNO2。
反应原理为:2NO+Na2O2=2NaNO2

回答下列问题:
(1)乙装置的仪器名称是
(2)甲中滴入稀硝酸前需先通入N2,原因是
(3)甲装置中发生反应的离子方程式为
(4)反应过程中观察到丙中的现象为
(5)丁中酸性KMnO4的作用是
(6)设计实验证明丙装置有NaNO2生成
您最近一年使用:0次
2022-07-12更新
|
334次组卷
|
2卷引用:湖北省华中师范大学第一附属中学2022-2023学年高一上学期竞赛生10月测试化学试题
解题方法
3 . 为了研究不同浓度硝酸的性质,某小组设计了如下实验(固定装置和尾气处理装置略)。
(1)实验I中氧化剂和还原剂的物质的量之比是多少______ ?
(2)对实验I和实验II发生不同反应的原因提出如下解释:
①极稀的硝酸与金属锌反应时无气体产生,写出此时生成的硝酸盐的化学式______ 。
②浓硝酸具有较强的氧化性,可将NO转化为 ,请写出其反应的化学方程式
,请写出其反应的化学方程式______ 。
(3)对实验I所得溶液呈绿色,而实验II所得溶液呈蓝色的原因提出猜想:
查阅资料:i. 溶于浓硝酸后呈黄色;
溶于浓硝酸后呈黄色;
ii. 。
。 是弱酸,不稳定。
是弱酸,不稳定。
猜想一: 溶于浓硝酸,与蓝色溶液混合而呈现绿色。
溶于浓硝酸,与蓝色溶液混合而呈现绿色。
猜想二: 电离出的
电离出的 与
与 结合为绿色的
结合为绿色的 。
。
①向浓硝酸中先通入 ,再滴加少量蓝色
,再滴加少量蓝色 溶液,证实猜想一合理。上述两步操作所得溶液的颜色分别为
溶液,证实猜想一合理。上述两步操作所得溶液的颜色分别为_______ 、_______ 。
②向蒸馏水中通入 得到无色溶液,向其中滴加蓝色的
得到无色溶液,向其中滴加蓝色的 溶液,溶液变为绿色,再滴加少量硝酸,结果溶液由绿色又变为蓝色。由此推出,猜想二不是实验Ⅰ所得溶液呈绿色的主要原因,请说明理由
溶液,溶液变为绿色,再滴加少量硝酸,结果溶液由绿色又变为蓝色。由此推出,猜想二不是实验Ⅰ所得溶液呈绿色的主要原因,请说明理由______ 。
(4)金可溶于王水(浓盐酸和浓硝酸按体积比3:1混合而成)生成 ,同时产生无色气体(露置在空气中变为红棕色),请写出该反应的化学方程式
,同时产生无色气体(露置在空气中变为红棕色),请写出该反应的化学方程式______ ,并分析该反应不直接生成 的原因
的原因______ 。
| 装置 | 编号 | 试剂a | 现象 |
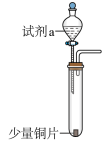 | I | 4mL浓硝酸(过量) | 铜片完全溶解,溶液变绿,出现大量红棕色气体 |
| II | 4mL稀硝酸(过量) | 铜片完全溶解,溶液变蓝,液面上方气体呈浅红棕色 |
(2)对实验I和实验II发生不同反应的原因提出如下解释:
①极稀的硝酸与金属锌反应时无气体产生,写出此时生成的硝酸盐的化学式
②浓硝酸具有较强的氧化性,可将NO转化为
 ,请写出其反应的化学方程式
,请写出其反应的化学方程式(3)对实验I所得溶液呈绿色,而实验II所得溶液呈蓝色的原因提出猜想:
查阅资料:i.
 溶于浓硝酸后呈黄色;
溶于浓硝酸后呈黄色;ii.
 。
。 是弱酸,不稳定。
是弱酸,不稳定。猜想一:
 溶于浓硝酸,与蓝色溶液混合而呈现绿色。
溶于浓硝酸,与蓝色溶液混合而呈现绿色。猜想二:
 电离出的
电离出的 与
与 结合为绿色的
结合为绿色的 。
。①向浓硝酸中先通入
 ,再滴加少量蓝色
,再滴加少量蓝色 溶液,证实猜想一合理。上述两步操作所得溶液的颜色分别为
溶液,证实猜想一合理。上述两步操作所得溶液的颜色分别为②向蒸馏水中通入
 得到无色溶液,向其中滴加蓝色的
得到无色溶液,向其中滴加蓝色的 溶液,溶液变为绿色,再滴加少量硝酸,结果溶液由绿色又变为蓝色。由此推出,猜想二不是实验Ⅰ所得溶液呈绿色的主要原因,请说明理由
溶液,溶液变为绿色,再滴加少量硝酸,结果溶液由绿色又变为蓝色。由此推出,猜想二不是实验Ⅰ所得溶液呈绿色的主要原因,请说明理由(4)金可溶于王水(浓盐酸和浓硝酸按体积比3:1混合而成)生成
 ,同时产生无色气体(露置在空气中变为红棕色),请写出该反应的化学方程式
,同时产生无色气体(露置在空气中变为红棕色),请写出该反应的化学方程式 的原因
的原因
您最近一年使用:0次
解题方法
4 . 下列有关物质的性质与应用相对应的是
| A.二氧化锰具有强氧化性,常用作双氧水分解的氧化剂 |
| B.碳酸钠溶液呈碱性,可用于洗去铁屑表面的油污 |
| C.碳具有还原性,一定条件下能将二氧化硅还原为硅 |
| D.甲醛能使蛋白质变性,可用福尔马林浸泡生物标本保存和水产品保鲜 |
您最近一年使用:0次
解题方法
5 . 劳动创造美好生活。下列劳动项目的原理解释正确的是
| 选项 | 劳动项目 | 原理解释 |
| A | 用石膏改良盐碱土壤 | 硫酸钙显酸性 |
| B | 用糯米酿制米酒 | 酵母菌可以使淀粉直接水解为酒精 |
| C | 用熟香蕉催熟猕猴桃生果 | 香蕉释放的酯可加速生果成熟 |
| D | 用“爆炸盐”(含2Na2CO3∙3H2O2)洗涤衣物 | 过碳酸钠水溶液显碱性、有强氧化性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-12-28更新
|
423次组卷
|
5卷引用:广东省普宁市勤建学校2022-2023学年高二下学期学科竞赛化学试题
广东省普宁市勤建学校2022-2023学年高二下学期学科竞赛化学试题广东省东莞市2022-2023学年高三上学期期末教学质量检查化学试题湖北省2022-2023学年高三上学期期末考试化学试题(已下线)广东省东莞市2022-2023学年高三上学期期末教学质量检查变式汇编(1-10)陕西省渭南市三贤中学2023-2024学年高三上学期11月月考化学试题
6 . 下列有关物质的性质和用途具有对应关系的是
| A.活性炭具有还原性,可用作制糖业的脱色剂 |
| B.晶体硅的熔点高、硬度大,可用作制造半导体材料 |
| C.二氧化氯具有强氧化性,可用作饮用水消毒 |
| D.氯化铁溶液具有酸性,可用作刻蚀铜电路板 |
您最近一年使用:0次
名校
解题方法
7 . 我国化学家侯德榜发明了联合制碱法,为世界制碱工业做出了巨大贡献。联合制碱法的主要过程如图所示(部分物质已略去)。
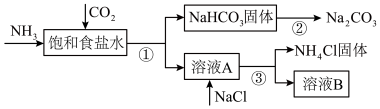
(1)饱和食盐水中通二氧化碳和氨气的化学方程式是_______
(2)下列说法中合理的是_______(填标号)。
(3)一场突如其来的新冠肺炎疫情,给人们的生活带来了巨大的冲击,在疫情期间外出需戴好口罩,返家后立即杀菌消毒。双氧水和84消毒液是日常生活常用的消毒剂,二氧化氯 气体是一种常用高效的自来水消毒剂。
气体是一种常用高效的自来水消毒剂。
①某同学设计如下实验研究 的性质,能证明
的性质,能证明 有还原性的实验是
有还原性的实验是_______ (填序号)
②某届奥运会期间,由于工作人员将84消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种原因可能是 与
与 反应产生
反应产生 促进藻类快速生长。该反应说明氧化性:
促进藻类快速生长。该反应说明氧化性:
_______  (填“>”或“<”);当有
(填“>”或“<”);当有 生成时,转移电子的物质的量为
生成时,转移电子的物质的量为_______ mol。
③ 和浓盐酸在一定温度下反应会生成
和浓盐酸在一定温度下反应会生成 和
和 ,该反应的离子方程式
,该反应的离子方程式_______ ,将 通入到硫化氢溶液中,然后加入少量的稀盐酸酸化的氯化钡溶液,发现有白色沉淀生成,写出二氧化氯与硫化氢溶液反应的化学方程式
通入到硫化氢溶液中,然后加入少量的稀盐酸酸化的氯化钡溶液,发现有白色沉淀生成,写出二氧化氯与硫化氢溶液反应的化学方程式_______ 。

(1)饱和食盐水中通二氧化碳和氨气的化学方程式是
(2)下列说法中合理的是_______(填标号)。
A.副产物 可用作氮肥 可用作氮肥 |
B.溶液B中的主要离子是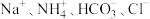 |
C.制碱流程中可回收并循环利用的物质只有碳酸氢钠分解产生的 |
| D.饱和食盐水中应该先通二氧化碳至饱和,再通入氨气至饱和 |
 气体是一种常用高效的自来水消毒剂。
气体是一种常用高效的自来水消毒剂。①某同学设计如下实验研究
 的性质,能证明
的性质,能证明 有还原性的实验是
有还原性的实验是| 序号 | 实验 | 实验现象 |
| 1 | 向 溶液中滴加酸性 溶液中滴加酸性 溶液 溶液 | a.溶液紫色裉去;b.有大量气泡产生 |
| 2 | 向 溶液中滴加淀粉碘化钾溶液 溶液中滴加淀粉碘化钾溶液 | c.溶液变蓝 |
 与
与 反应产生
反应产生 促进藻类快速生长。该反应说明氧化性:
促进藻类快速生长。该反应说明氧化性:
 (填“>”或“<”);当有
(填“>”或“<”);当有 生成时,转移电子的物质的量为
生成时,转移电子的物质的量为③
 和浓盐酸在一定温度下反应会生成
和浓盐酸在一定温度下反应会生成 和
和 ,该反应的离子方程式
,该反应的离子方程式 通入到硫化氢溶液中,然后加入少量的稀盐酸酸化的氯化钡溶液,发现有白色沉淀生成,写出二氧化氯与硫化氢溶液反应的化学方程式
通入到硫化氢溶液中,然后加入少量的稀盐酸酸化的氯化钡溶液,发现有白色沉淀生成,写出二氧化氯与硫化氢溶液反应的化学方程式
您最近一年使用:0次
2023-01-07更新
|
487次组卷
|
3卷引用:广东省广州市黄广中学2023-2024学年高一上学期化学竞赛选拔考试
名校
解题方法
8 . 根据实验操作及现象得出的结论正确的是
| 选项 | 实验操作及现象 | 结论 |
| A | 将充满氨气的试管倒置于滴有酚酞的水槽中,试管内迅速充满红色液体 | NH3极易溶于水且溶液显碱性 |
| B | 蔗糖中加入浓硫酸出现发黑现象 | 浓硫具有吸水性和强氧化性 |
| C | 向酸性KMnO4溶液中通入SO2,溶液褪色 | SO2有漂白性 |
| D | 向某盐溶液中加入NaOH溶液,加热,产生的气体能使湿润的红色石蕊试纸变蓝 | 该溶液中含有NH |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-01-28更新
|
493次组卷
|
3卷引用:山东省高密市第一中学2023-2024学年高一上学期1月冬学竞赛化学试题
名校
解题方法
9 . 如图,浓硫酸分别和三种钠盐反应,下列分析正确的是


| A.对比①和②可以说明还原性:Br->Cl- |
| B.①和③相比可说明氧化性:Br2>SO2 |
| C.②中试管口白雾是HCl遇水蒸气所致,说明非金属性:S>Cl |
| D.③中浓H2SO4与Na2SO3反应时,H2SO4被还原成SO2 |
您最近一年使用:0次
2023-04-05更新
|
188次组卷
|
2卷引用:湖南省绥宁县第一中学2022-2023学年高一下学期学科知识竞赛化学试题
名校
解题方法
10 . 某实验小组利用微型实验装置进行氯气的制备和性质探究,装置如图所示,下列有关说法错误的是
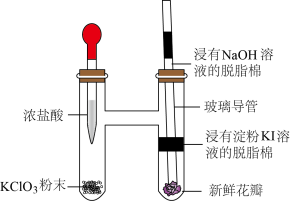
A. 与浓盐酸反应,HCl只体现还原性 与浓盐酸反应,HCl只体现还原性 |
B.浸有淀粉KI溶液的脱脂棉变蓝,说明氧化性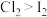 |
| C.新鲜花瓣褪色是因为氯气与水反应生成的HClO有漂白性 |
| D.浸有NaOH溶液的脱脂棉可吸收过量氯气 |
您最近一年使用:0次
2023-04-27更新
|
707次组卷
|
3卷引用:广东省揭阳市普宁市勤建学校2022-2023学年高一下学期学科竞赛化学试题



