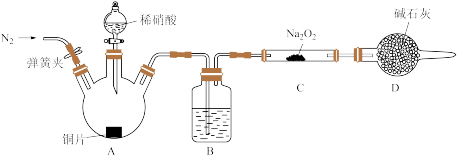
1 . 某化学活动小组想通过如图所示装置(夹持装置已略去)进行实验,探究Na2O2与NO反应的产物。
实验前,他们查阅有关资料得到如下信息:
①2NaNO3 2NaNO2+O2↑;
2NaNO2+O2↑;
②NaNO2为白色粉末状固体,既有氧化性又有还原性;
③NaNO2溶液显弱碱性。
请回答下列问题:
(1)实验开始时,打开弹簧夹,通入N2一段时间后,关闭弹簧夹,目的是___ 。装置B中的试剂是___ ,装置D的作用是___ 。
(2)如何检验反应中是否有氧气生成?___ 。
(3)假设Na2O2已反应完全,为确定装置C中固体产物的成分,甲、乙同学分别进行如下实验。
甲同学将固体溶于水后,经测定发现溶液显强碱性,再向溶液中加入酸性KMnO4溶液,紫色褪去。由此现象推断固体产物中可能含有的物质是___ (填化学式)。乙同学取适量固体于试管中密闭加热,发现白色固体部分变为淡黄色。此现象说明固体中还可能含有的成分是___ (填化学式)。根据以上推测,请写出Na2O2与NO反应的化学方程式:__ 。

实验前,他们查阅有关资料得到如下信息:
①2NaNO3
 2NaNO2+O2↑;
2NaNO2+O2↑;②NaNO2为白色粉末状固体,既有氧化性又有还原性;
③NaNO2溶液显弱碱性。
请回答下列问题:
(1)实验开始时,打开弹簧夹,通入N2一段时间后,关闭弹簧夹,目的是
(2)如何检验反应中是否有氧气生成?
(3)假设Na2O2已反应完全,为确定装置C中固体产物的成分,甲、乙同学分别进行如下实验。
甲同学将固体溶于水后,经测定发现溶液显强碱性,再向溶液中加入酸性KMnO4溶液,紫色褪去。由此现象推断固体产物中可能含有的物质是
您最近一年使用:0次
解题方法
2 . 利用下图,可以从不同角度研究含氯物质的性质及其转化关系,图中甲~辛均含氯元素。回答下列问题:
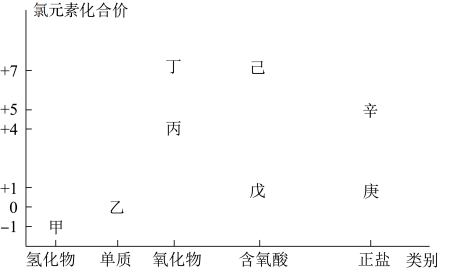
(1)丁属于___________ (“酸性”或“碱性”)氧化物;
(2)图中甲、乙、丙、戊中,属于电解质的是___________ (填化学式);根据氯元素的化合价判断,乙物质___________ ;
A. 只有氧化性 B. 只有还原性 C. 既有氧化性又有还原性
(3)电解甲溶液制备己的化学反应为: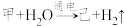 (未配平),则配平后参与反应的甲与H2O的物质的量之比是
(未配平),则配平后参与反应的甲与H2O的物质的量之比是___________ ;
(4)庚是漂白粉的有效成分,用乙制取庚的化学方程式为___________ ;
(5)已知己是最强的无机酸,写出己的电离方程式___________ 。

(1)丁属于
(2)图中甲、乙、丙、戊中,属于电解质的是
A. 只有氧化性 B. 只有还原性 C. 既有氧化性又有还原性
(3)电解甲溶液制备己的化学反应为:
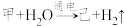 (未配平),则配平后参与反应的甲与H2O的物质的量之比是
(未配平),则配平后参与反应的甲与H2O的物质的量之比是(4)庚是漂白粉的有效成分,用乙制取庚的化学方程式为
(5)已知己是最强的无机酸,写出己的电离方程式
您最近一年使用:0次
2021-11-17更新
|
1152次组卷
|
4卷引用:第二章 海水中的重要元素——钠和氯
3 . 氮循环是海洋生态系统的基础和关键,其中无机氮循环过程如下图所示。
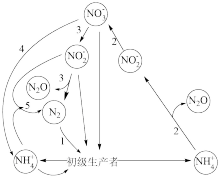
亚硝酸盐是氮循环中的重要物质。下列关于亚硝酸钠 性质的推测中,
性质的推测中,不合理 的是资料: 为弱酸,
为弱酸, 在碱性条件下能稳定存在。
在碱性条件下能稳定存在。

亚硝酸盐是氮循环中的重要物质。下列关于亚硝酸钠
 性质的推测中,
性质的推测中, 为弱酸,
为弱酸, 在碱性条件下能稳定存在。
在碱性条件下能稳定存在。A. 具有氧化性 具有氧化性 | B. 具有还原性 具有还原性 |
C. 能与 能与 反应 反应 | D. 能与 能与 反应 反应 |
您最近一年使用:0次
2023-01-05更新
|
815次组卷
|
6卷引用:章末检测卷(三) 物质的性质与转化
名校
4 . 硝酸是一种具有强氧化性、腐蚀性的强酸,其还原产物因硝酸浓度的不同而有变化,从总体上说,硝酸浓度越高,平均每分子硝酸得到的电子数越少,浓硝酸的还原产物主要为NO2、稀硝酸的还原产物为NO。实验室中,常用Cu与浓HNO3反应制取NO2,用Cu与稀HNO3反应制取NO。
(1)浓硝酸具有以下性质:
①强氧化性 ②酸性 ③还原性 ④不稳定性 ⑤挥发性
下列反应或者现象主要体现了硝酸的什么性质:
①久置浓硝酸显黄色___________ (填序号,下同)。
②用稀硝酸清洗试管壁上的银___________ 。
③稀硝酸清洗石灰水试剂瓶壁上的固体___________ 。
(2)请写出实验室中用Cu与稀HNO3反应制取NO的化学方程式并用双线桥标明电子的转移方向及数目___________ 。
(3)64gCu与适量的浓HNO3反应,铜全部作用后,共收集到22.4L气体(标准状况下),反应中消耗的HNO3的物质的量是___________ (填字母代号)。
A.0.5mol B.1.0mol C.2.0mol D.3.0mol
(4)硝酸的还原产物NO、NO2、N2O等对环境均有副作用,为了可持续发展,当今社会提出的一个新概念:“绿色化学”,它要求从经济、环保和技术上设计可行的化学反应,则下列由单质铜制取硝酸铜的方法可行且符合“绿色化学”的是___________ (填字母代号)。
A.Cu Cu(NO3)2
Cu(NO3)2
B.Cu CuO
CuO Cu(NO3)2
Cu(NO3)2
C.Cu CuO
CuO Cu(OH)2
Cu(OH)2 Cu(NO3)2
Cu(NO3)2
D.Cu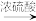 CuSO4
CuSO4  Cu(NO3)2
Cu(NO3)2
(5)实际上硝酸不仅可被还原为NO2或NO,浓度更稀时硝酸还可以被还原为N2O、N2、NH4NO3等,锌与很稀的硝酸反应生成硝酸锌、硝酸铵和水。写出该反应的化学方程式________ ,当生成a mol硝酸锌时,被还原的硝酸的物质的量为________ 。
(1)浓硝酸具有以下性质:
①强氧化性 ②酸性 ③还原性 ④不稳定性 ⑤挥发性
下列反应或者现象主要体现了硝酸的什么性质:
①久置浓硝酸显黄色
②用稀硝酸清洗试管壁上的银
③稀硝酸清洗石灰水试剂瓶壁上的固体
(2)请写出实验室中用Cu与稀HNO3反应制取NO的化学方程式并用双线桥标明电子的转移方向及数目
(3)64gCu与适量的浓HNO3反应,铜全部作用后,共收集到22.4L气体(标准状况下),反应中消耗的HNO3的物质的量是
A.0.5mol B.1.0mol C.2.0mol D.3.0mol
(4)硝酸的还原产物NO、NO2、N2O等对环境均有副作用,为了可持续发展,当今社会提出的一个新概念:“绿色化学”,它要求从经济、环保和技术上设计可行的化学反应,则下列由单质铜制取硝酸铜的方法可行且符合“绿色化学”的是
A.Cu
 Cu(NO3)2
Cu(NO3)2B.Cu
 CuO
CuO Cu(NO3)2
Cu(NO3)2C.Cu
 CuO
CuO Cu(OH)2
Cu(OH)2 Cu(NO3)2
Cu(NO3)2D.Cu
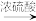 CuSO4
CuSO4  Cu(NO3)2
Cu(NO3)2 (5)实际上硝酸不仅可被还原为NO2或NO,浓度更稀时硝酸还可以被还原为N2O、N2、NH4NO3等,锌与很稀的硝酸反应生成硝酸锌、硝酸铵和水。写出该反应的化学方程式
您最近一年使用:0次
2010·全国·一模
名校
解题方法
5 . 人体血红蛋白中含有Fe2+,如果误食亚硝酸盐会使人中毒,因为亚硝酸盐会使Fe2+变Fe3+,生成高铁血红蛋白而丧失与O2结合的能力。服用维生素C可缓解亚硝酸盐中毒。说明维生素C具有
| A.氧化性 | B.还原性 | C.酸性 | D.碱性 |
您最近一年使用:0次
2020-11-09更新
|
1005次组卷
|
70卷引用:2018-2019学年鲁科版必修1第2章元素与物质世界本章测试题
2018-2019学年鲁科版必修1第2章元素与物质世界本章测试题(已下线)高考第一轮复习化学反应与能量变化单元测试(已下线)2010—2011学年云南省元阳一中高一上学期期末考试化学试卷(已下线)2011-2012学年上海理工大学附属中学高一上学期期末考试化学试卷(已下线)2011-2012学年广东省汕头金山中学高一第一学期期末考试化学(文)试卷(已下线)2011-2012学年浙江省余姚中学高一下学期期中考试文科化学试卷(已下线)2011-2012学年福建省泉州一中高一下学期期中考试化学试卷(已下线)2012-2013学年河北省邢台一中高一上学期第三次月考化学试卷(已下线)2012-2013学年浙江省杭州十四中高一上学期期末考试化学试卷(已下线)2012-2013学年上海市上海理工大学附属中学高一上期末考试化学试卷(已下线)2012-2013学年浙江省杭州地区七校高一下学期期中联考文科化学试卷(已下线)2013-2014学年山东省临沂市重点中学高一上学期期中考试化学试卷2014-2015山西省原平市一中高一上学期期末考试化学试卷2015-2016学年吉林省吉林五十五中高二上学期期中(文)化学试卷2015-2016学年广东广州执信中学高二上期中文化学试卷2015-2016学年宁夏吴忠中学高一上学期期末考试化学试卷2015-2016学年湖南省常德一中高一上学期期末化学试卷2015-2016学年福建省莆田二十五中高一下学期第一次月考化学试卷2015-2016学年山西晋城市高平市特立高级中学高二下期中理科化学卷2016-2017学年广东佛山一中高一上第一次段考化学卷2016-2017学年遵义市第四中学高二上学期期中考试化学(文)试卷2016-2017学年广东省广州执信中学高二上期中化学卷2016-2017学年广东省汕头市金山中学高二上学业水平测试化学卷甘肃省武威市河西成功学校2017-2018学年高一上学期期中考试化学试题山东省临沂市蒙阴县实验中学2017-2018学年高一上学期期中考试化学试题山东省桓台第二中学2017-2018学年高一12月月考化学试题陕西省西安市长安区第一中学2017-2018学年高二上学期期末考试化学(文)试题广东省惠州市2017-2018学年高一上学期期末教学质量检测化学试题湖南省师范大学附属中学2017-2018学年高二上学期期末考试化学(文)试题云南省昆明市黄冈实验学校2017-2018学年高二上学期期末考试化学(理)试题云南民族大学附属中学2017-2018学年高一下学期期中考试化学试题广东省普通高中2018-2019学年高二学业水平测试预测试题福建省晋江市季延中学2018-2019学年高二(文)上学期期中考试化学试题山西省祁县第二中学校2018-2019学年高二下学期5月考试化学试题江苏省苏州陆慕高级中学2018-2019学年高一下学期5月月考化学试题江苏省苏州市第五中学2018-2019学年高二上学期期中考试(必修)化学试题甘肃省嘉峪关市一中2017-2018学年高一上学期期中考试化学试题云南省云天化中学2019-2020学年高一9月月考化学试题黑龙江省哈尔滨市第三中学2019-2020学年高二上学期期中考试化学(文)试题黑龙江省哈尔滨市阿城区龙涤中学2019-2020学年高一上学期第一次段考化学试题上海市嘉定区封浜高中2019-2020学年高二上学期期中考试化学试题湖南省常德市2018-2019学年高二下学期第一次月考化学试题江西省抚州市南城县第二中学2019-2020学年高一上学期第二次月考化学试题江苏省海头高级中学2019-2020学年高一上学期第三次月考化学试题福建省晋江市养正中学2019-2020学年高二上学期第二次月考化学试题山西省运城市盐湖五中2019-2020学年高一上学期期中考试化学试题安徽省六安市第一中学2019-2020学年高一下学期疫情防控延期开学期间辅导测试(三)化学试题安徽省芜湖市2019-2020学年高二上学期期末考试化学(文)试题辽宁省东北育才学校科学高中部2020-2021学年高一上学期第一学段检测化学试题(已下线)【浙江新东方】7广东省佛山市第一中学2020-2021学年高一上学期第一次段考化学试题江苏省常州市2020-2021学年高一上学期期中考试化学试题江西省九江市浔阳区九江市第七中学2020-2021学年高一上学期期中考试化学试题吉林省大安市第六中学2019-2020学年高二下学期期末考试化学(理)试题上海市奉城高级中学2018-20219学年高二上学期期中考试化学试题河北省石家庄市第二中学西校区2020-2021学年高一上学期12月月考化学试卷河南省南阳市第四中学2020-2021学年高一上学期第二次月考化学试题河南省南阳市油田第一中学2020-2021学年高二上学期期中考试化学试题福建省莆田第一中学2021-2022学年高一上学期期中考试化学试题山西省大同市2021-2022学年高一上学期期末调研化学试题上海理工大学附属中学中2021-2022学年高一下学期期中考试化学试题江苏省常州市金坛区2021-2022学年高一上学期期中教学质量调研化学试题广东省华南师范大学附属中学2020-2021学年高一上学期期中考试化学试题辽宁省锦州市黑山县黑山中学2021-2022学年高一上学期12月月考化学试题北京清华大学附属中学2022-2023学年高一上学期期末考试化学试卷海南省临高县新盈中学2021-2022学年高二上学期(5-8班)期中考试化学试题湖南省株洲市炎陵县第一中学等2校2022-2023学年高一下学期3月月考化学试题甘肃省武威市天祝藏族自治县第一中学2022-2023学年高一下学期开学考试化学试题广东省汕头市潮阳第一中学2023-2024学年高一上学期12月月考化学试题北京市顺义区杨镇第一中学2023-2024学年高一上学期期中考试化学试题
6 .  溶液和84消毒液是生活中常用的两种消毒剂。请回答下列问题:
溶液和84消毒液是生活中常用的两种消毒剂。请回答下列问题:
(1)某同学设计如下实验研究 的性质:
的性质:
①理论上 既有氧化性又有还原性,具有还原性的原因是
既有氧化性又有还原性,具有还原性的原因是___________ 。
②能证明 具有还原性的是实验
具有还原性的是实验_________ (填序号)。
(2)84消毒液的有效成分为 。
。
①将 通入
通入 溶液中可制得84消毒液,化学方程式为
溶液中可制得84消毒液,化学方程式为_________ 。
②84消毒液不能用于钢制器具的消毒,原因是 具有
具有_______ 性。
③84消毒液吸收空气中的 ,其消毒杀菌能力增强,该过程中发生反应的化学方程式为
,其消毒杀菌能力增强,该过程中发生反应的化学方程式为______ 。
 溶液和84消毒液是生活中常用的两种消毒剂。请回答下列问题:
溶液和84消毒液是生活中常用的两种消毒剂。请回答下列问题:(1)某同学设计如下实验研究
 的性质:
的性质:| 实验 | 操作 | 现象 |
| i | 向5% 溶液中滴加酸性 溶液中滴加酸性 溶液 溶液 | a.溶液紫色褪去 b.有大量气泡产生 |
| ii | 向5% 溶液中滴加淀粉碘化钾溶液 溶液中滴加淀粉碘化钾溶液 | c.溶液变蓝 |
①理论上
 既有氧化性又有还原性,具有还原性的原因是
既有氧化性又有还原性,具有还原性的原因是②能证明
 具有还原性的是实验
具有还原性的是实验(2)84消毒液的有效成分为
 。
。①将
 通入
通入 溶液中可制得84消毒液,化学方程式为
溶液中可制得84消毒液,化学方程式为②84消毒液不能用于钢制器具的消毒,原因是
 具有
具有③84消毒液吸收空气中的
 ,其消毒杀菌能力增强,该过程中发生反应的化学方程式为
,其消毒杀菌能力增强,该过程中发生反应的化学方程式为
您最近一年使用:0次
解题方法
7 . 氮、硫、碳的氧化物都会引起环境问题,越来越引起人们的重视。如图是氮、硫元素的各种价态与物质类别的对应关系: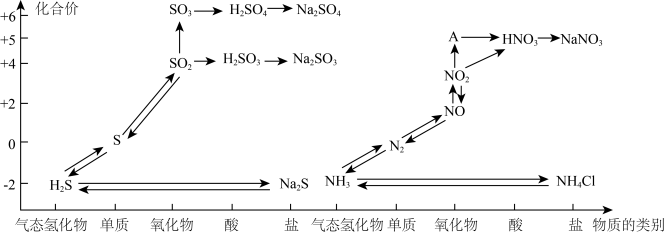
(1)根据A对应的化合价和物质类别,A为___________ (写分子式),从氮元素的化合价能否发生变化的角度判断,图中既有氧化性又有还原性的化合物有____________ 。
(2)浓、稀硝酸的性质既相似又有差别,若要除去铁制品表面的铜镀层应选择________ ,反应的离子方程式为______________ 。
(3)某同学设计了如图所示的套管实验装置(部分装置未画出)来制备SO2并利用实验现象来检验其还原性,制备SO2时选用的试剂为Cu和浓H2SO4。回答下列问题:

①写出制取SO2的化学方程式:_______________ 。
②该同学利用实验现象来检验SO2的还原性,则选用的试剂为_____ 。
A. 品红溶液 B. 酸性高锰酸钾溶液 C. 双氧水(H2O2)
(4)工厂里常采用NaOH溶液吸收NO、NO2的混合气体,使其转化为化工产品NaNO2,试写出其化学反应方程式_______ 。
(5)工业上把海水先进行氧化,再吸收溴,达到富集溴的目的。吸收工艺常用的方法是先用热空气吹出Br2,再用SO2吸收Br2。取吸收后的溶液,向其中加入氯化钡溶液有白色沉淀析出。写出SO2吸收Br2反应的化学方程式为____________ 。

(1)根据A对应的化合价和物质类别,A为
(2)浓、稀硝酸的性质既相似又有差别,若要除去铁制品表面的铜镀层应选择
(3)某同学设计了如图所示的套管实验装置(部分装置未画出)来制备SO2并利用实验现象来检验其还原性,制备SO2时选用的试剂为Cu和浓H2SO4。回答下列问题:

①写出制取SO2的化学方程式:
②该同学利用实验现象来检验SO2的还原性,则选用的试剂为
A. 品红溶液 B. 酸性高锰酸钾溶液 C. 双氧水(H2O2)
(4)工厂里常采用NaOH溶液吸收NO、NO2的混合气体,使其转化为化工产品NaNO2,试写出其化学反应方程式
(5)工业上把海水先进行氧化,再吸收溴,达到富集溴的目的。吸收工艺常用的方法是先用热空气吹出Br2,再用SO2吸收Br2。取吸收后的溶液,向其中加入氯化钡溶液有白色沉淀析出。写出SO2吸收Br2反应的化学方程式为
您最近一年使用:0次
2020-05-29更新
|
723次组卷
|
2卷引用:第五章 化工生产中的重要非金属元素 单元测试
20-21高一下·全国·单元测试
解题方法
8 . 某化学兴趣小组为了制取并探究氨气性质,按下列装置(部分夹持装置已略去)进行实验。(制取氨气的反应原理:2NH4Cl+Ca(OH)2 CaCl2+2NH3↑+2H2O)
CaCl2+2NH3↑+2H2O)

(实验探究)
(1)A装置N元素的化合价是__ 该反应是否是氧化还原反应:__ 。
(2)用5.35gNH4Cl固体与足量Ca(OH)2反应,最多可制得标准状况下氨气的体积为___ L。(NH4Cl的摩尔质量为53.5g•mol-1)
(3)气体通过C、D装置时,试纸颜色会发生变化的是D,原因是:___ 。
(4)当实验进行一段时间后,挤压E装置中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是___ 。
(5)检验氨气是否收集满的方法是___ 。
(6)某同学用如图所示装置进行氨气的性质实验,根据烧瓶内产生红色喷泉的现象,说明氨气具有__ 性质 填序号
填序号 。
。

a.还原性
b.极易溶于水
c.与水反应生成碱性物质
(7)氨气的用途很广。如可用氨气处理二氧化氮:8NH3+6NO2=7N2+12H2O该反应中氨气体现___ (填“氧化性”或“还原性”)。
 CaCl2+2NH3↑+2H2O)
CaCl2+2NH3↑+2H2O)
(实验探究)
(1)A装置N元素的化合价是
(2)用5.35gNH4Cl固体与足量Ca(OH)2反应,最多可制得标准状况下氨气的体积为
(3)气体通过C、D装置时,试纸颜色会发生变化的是D,原因是:
(4)当实验进行一段时间后,挤压E装置中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是
(5)检验氨气是否收集满的方法是
(6)某同学用如图所示装置进行氨气的性质实验,根据烧瓶内产生红色喷泉的现象,说明氨气具有
 填序号
填序号 。
。
a.还原性
b.极易溶于水
c.与水反应生成碱性物质
(7)氨气的用途很广。如可用氨气处理二氧化氮:8NH3+6NO2=7N2+12H2O该反应中氨气体现
您最近一年使用:0次
9 . 为了探究铁及其化合物的氧化性或还原性,某同学设计如下实验操作,对应的实验现象、实验结论及离子方程式均正确的是
| 选项 | 实验操作 | 实验现象 | 实验结论 | 离子方程式 |
| A | 向 溶液中加入 溶液中加入 片 片 | 浅绿色溶液变为无色,溶液中有黑色固体生成 |  具有还原性 具有还原性 |  |
| B | 向 溶液中滴加新制氯水 溶液中滴加新制氯水 | 浅绿色溶液变为棕黄色 |  具有还原性 具有还原性 | 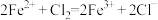 |
| C | 向 溶液中加入铁粉 溶液中加入铁粉 | 棕黄色溶液变为浅绿色 |  具有还原性 具有还原性 | 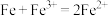 |
| D | 向 溶液中加入铜粉 溶液中加入铜粉 | 蓝色溶液变为棕黄色 |  具有氧化性 具有氧化性 | 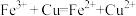 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-06-05更新
|
1079次组卷
|
8卷引用:第三章 铁 金属材料(B卷·能力提升练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第一册)
(已下线)第三章 铁 金属材料(B卷·能力提升练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第一册)(苏教版2019)必修第二册专题9 金属与人类文明 第二单元 探究铁及其化合物的转化(已下线)微专题13 亚铁离子、三价铁离子的性质及检验-备战2022年高考化学考点微专题(已下线)3.1.2 铁盐和亚铁盐-2021-2022学年高一化学课后培优练(人教版2019必修第一册)重庆市万州第二高级中学2022-2023学年高一上学期12月线上考试化学试题内蒙古巴彦淖尔市第一中学2022-2023学年高一上学期1月期末考试化学试题湖南省泸溪县第一中学等多校联考2023-2024学年高二上学期8月月考化学试题云南省保山市腾冲市第八中学2023--2024学年高一上学期期末化学强化训练
解题方法
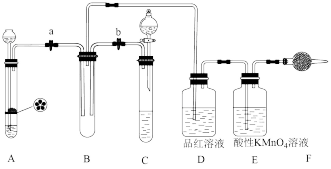
10 . 某课外学习小组的同学设计了如图所示的实验装置(夹持装置略),以验证 的氧化性、还原性和漂白性。
的氧化性、还原性和漂白性。
请回答下列问题:
(1)用Na2SO3固体和70%的浓硫酸反应制取SO2气体,应选用____________ (填“A”或“C”)装置作气体发生装置,不选用另一装置的理由是_______________________________ 。
(2)该课外学习小组的同学用FeS固体和稀硫酸反应制取H2S气体,反应的化学方程式为___________________________ 。
(3)SO2气体通过D装置时的现象是___________________________ ,通过E装置时的现象是__________________________ ;SO2与H2S在B装置中反应,现象是__________________________ 。
(4)F装置中盛有碱石灰,其作用是_______________________________ 。
 的氧化性、还原性和漂白性。
的氧化性、还原性和漂白性。请回答下列问题:
(1)用Na2SO3固体和70%的浓硫酸反应制取SO2气体,应选用
(2)该课外学习小组的同学用FeS固体和稀硫酸反应制取H2S气体,反应的化学方程式为
(3)SO2气体通过D装置时的现象是
(4)F装置中盛有碱石灰,其作用是

您最近一年使用:0次



