名校
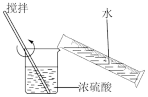
1 . 实验装置不能达到实验目的的是
| A | B | C | D |
|
|
|
|
| 稀释浓硫酸 | 制备并检验 气体 气体 | 用该装置制备少量白色的 沉淀 沉淀 | 吸收NO中的 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-12-30更新
|
866次组卷
|
11卷引用:湖南省绥宁县第一中学2022-2023学年高一下学期学科知识竞赛化学试题
湖南省绥宁县第一中学2022-2023学年高一下学期学科知识竞赛化学试题福建省厦门第一中学2021-2022学年高一上学期12月月考化学试题(已下线)解密11 化学实验(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)湖北省襄阳市第一中学2021-2022学年高一下学期3月月考化学试题山西省榆次第一中学校2021-2022学年高一下学期期中线上测试化学试题辽宁省东北师范大学连山实验高中2021-2022学年高一下学期第一次线上考试化学试题(已下线)仿真卷02-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)化学(人教版2019B卷)-学易金卷:2022-2023学年高一下学期期中考前必刷卷河南省驻马店市2022-2023学年高一下学期4月期中考试化学试题新疆塔城地区第一高级中学2022-2023学年高一下学期5月期中考试化学试题安徽省安庆市第九中学2022-2023学年高一下学期期中考试化学试题
2 . 下列实验室制备氨气装置中检查气密性、制备氨气、配制银氨溶液并进行尾气处理的装置和原理,不能达到实验目的的是
| A | B | C | D |
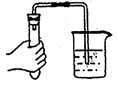 | 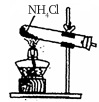 | 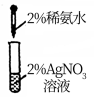 | 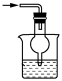 |
| 检查气密性 | 制备氨气 | 配制银氨溶液 | 尾气处理 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2010高三·湖北·竞赛
解题方法
3 . 化学实验兴趣小组在实验室进行氢气在氯气中的燃烧实验。
(1)设计如下图所示装置I制备和收集干燥纯净的氯气以备后续实验;

烧瓶中发生反应的离子方程式为_______ ;
请根据实验目的将装置I中虚线框内装置补充完整并在括号内注明所需试剂;_________
(2)在右图所示装置Ⅱ中,在试管中先加入过量铁粉,再滴入少量CuSO4溶液,最后加入一定量稀盐酸,塞上胶塞,观察到有大量气泡产生。

①检查制取氢气装置气密性的操作方法是____________
②当点燃氢后,将导管伸入盛有氯气的集气瓶中,观察到的现象是____________
(3)当氢气停止燃烧后,取出导管,同学们进行了分组探究实验。A组同学发现制氢气后的试管中还有较多固体剩余,同学们将足量氯气通入试管中,发现固体全部消失,但未观察到有气泡产生,请解释可能原因(用离子方程式表示);_______ 、________ 、_______ 、____ ;B组同学向集气瓶中注入适量水,用力振荡后,向其中加入少量Na2S2O3溶液,发现溶液中没有出现黄色沉淀,但再向溶液中滴入稀盐酸酸化的氯化钡溶液后,生成了白色沉淀。[已知Na2S2O3+H2SO4=Na2SO4+S↓+SO2↑+H2O],同学们分析是由于集气瓶中还有少量氯气残留的缘故。可以解释该实验现象的两个离子方程式是:①_____________ ②____________
(1)设计如下图所示装置I制备和收集干燥纯净的氯气以备后续实验;

烧瓶中发生反应的离子方程式为
请根据实验目的将装置I中虚线框内装置补充完整并在括号内注明所需试剂;
(2)在右图所示装置Ⅱ中,在试管中先加入过量铁粉,再滴入少量CuSO4溶液,最后加入一定量稀盐酸,塞上胶塞,观察到有大量气泡产生。

①检查制取氢气装置气密性的操作方法是
②当点燃氢后,将导管伸入盛有氯气的集气瓶中,观察到的现象是
(3)当氢气停止燃烧后,取出导管,同学们进行了分组探究实验。A组同学发现制氢气后的试管中还有较多固体剩余,同学们将足量氯气通入试管中,发现固体全部消失,但未观察到有气泡产生,请解释可能原因(用离子方程式表示);
您最近一年使用:0次
4 . 研究性学习小组设计了如下图所示实验装置(部分夹持装置已省略)制备NO,并进行NO的检验和性质探究实验。

已知:NO在 溶液中发生反应
溶液中发生反应 (棕色),该反应可以用于检验NO。
(棕色),该反应可以用于检验NO。
(1)仪器a的名称是_______ 。装置A内发生主要反应的离子方程式为_______ 。
(2)实验开始前,向装置中通入一段时间 的目的是
的目的是_______ 。
(3)装置B、C中蒸馏水和无水 的作用分别是
的作用分别是_______ 、_______ 。
(4)装置D中Fe粉与NO以物质的量之比 发生反应,生成
发生反应,生成 和另一种固体产物。该固体产物的化学式为
和另一种固体产物。该固体产物的化学式为_______ 。
(5)进行实验时,装置E中的实验现象为_______ 。

已知:NO在
 溶液中发生反应
溶液中发生反应 (棕色),该反应可以用于检验NO。
(棕色),该反应可以用于检验NO。(1)仪器a的名称是
(2)实验开始前,向装置中通入一段时间
 的目的是
的目的是(3)装置B、C中蒸馏水和无水
 的作用分别是
的作用分别是(4)装置D中Fe粉与NO以物质的量之比
 发生反应,生成
发生反应,生成 和另一种固体产物。该固体产物的化学式为
和另一种固体产物。该固体产物的化学式为(5)进行实验时,装置E中的实验现象为
您最近一年使用:0次
名校
5 . 某化学兴趣小组模拟“侯氏制碱法”制纯碱并进行后续实验。
I.制备纯碱:先以NaCl、NH3、CO2和水等为原料,用下图所示装置制取NaHCO3,然后再将NaHCO3制备成Na2CO3。
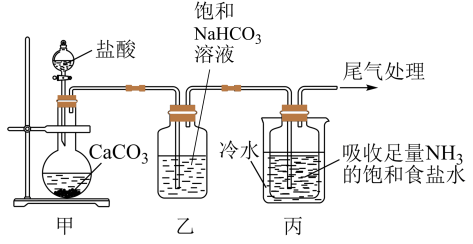
(1)装置乙的作用是_______ ,反应的化学方程式为_______ 。
(2)反应进行一段时间后,观察到装置丙中试剂瓶内溶液中有白色固体析出,经检验该白色固体是NaHCO3。装置丙中可得两种产物,分别是NaHCO3和另一种盐,装置丙中反应的化学方程式为____ 。
(3)用装置丙中产生的NaHCO3制取Na2CO3时,需要进行的实验操作有过滤、洗涤、_______ ,最后一步发生反应的化学方程式为_______ 。
II.测定所得产品的组成和纯度
(4)检验纯碱样品中是否混有NaHCO3,请选择下列装置设计实验,并完成下表:
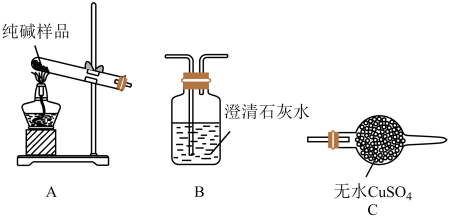
(5)测定该纯碱样品的纯度:称取m1g样品,置于小烧杯中,加水溶解,滴加足量CaCl2溶液。将反应混合物过滤、洗涤、干燥、称量,得到固体的质量为m2g。则该纯碱样品的纯度为_______ 。请另设计一个实验方案,测定纯碱样品的纯度(样品中只含有NaHCO3杂质)_______ 。
I.制备纯碱:先以NaCl、NH3、CO2和水等为原料,用下图所示装置制取NaHCO3,然后再将NaHCO3制备成Na2CO3。

(1)装置乙的作用是
(2)反应进行一段时间后,观察到装置丙中试剂瓶内溶液中有白色固体析出,经检验该白色固体是NaHCO3。装置丙中可得两种产物,分别是NaHCO3和另一种盐,装置丙中反应的化学方程式为
(3)用装置丙中产生的NaHCO3制取Na2CO3时,需要进行的实验操作有过滤、洗涤、
II.测定所得产品的组成和纯度
(4)检验纯碱样品中是否混有NaHCO3,请选择下列装置设计实验,并完成下表:

| 选择的装置(填编号) | 实验现象 | 实验结论 |
| 样品中含NaHCO3 |
您最近一年使用:0次
2022-08-21更新
|
474次组卷
|
2卷引用:甘肃省天水市2023-2024学年高一上学期10月份化学竞赛试卷
解题方法
6 . 某合作学习小组在实验室进行了由食盐制备纯碱的实验探究。请回答下列实验方案中的有关问题:
(1)制备原理:饱和氯化钠与碳酸氢铵反应得碳酸氢钠晶体,碳酸氢钠分解得到纯碱。反应为___ (写化学方程式)。
制备碳酸氢钠有以下三种方案,其中最好的方案是___ (填方案代号)。
方案A:分别将二氧化碳和氨气通入饱和食盐水中;
方案B:将二氧化碳通入含大量氨的饱和食盐水中;
方案C:将氨气通入含二氧化碳的饱和食盐水中。
(2)制备流程:
配制含氨的饱和食盐水→配制二氧化碳→制备碳酸氢钠→制备碳酸钠
实验中使用的部分简易装置如图所示:

其中装置乙的作用为___ ,装置丙的作用为___ ;实验中在装置乙丙之间还应连接制备碳酸氢钠的装置,且反应温度控制在30-35℃,请在答题卡上方框内画出该装置的简易图示___ 。实验的最后一步是将碳酸氢钠晶体转移到___ 中,加热至无水蒸气逸出既得碳酸钠。
(3)实验探究:制备碳酸氢钠的温度要控制在30-35℃,其理由是____ 。
本方法制得的纯碱中可能含有氯化钠,请设计检验实验方案,完成表中内容。
(1)制备原理:饱和氯化钠与碳酸氢铵反应得碳酸氢钠晶体,碳酸氢钠分解得到纯碱。反应为
制备碳酸氢钠有以下三种方案,其中最好的方案是
方案A:分别将二氧化碳和氨气通入饱和食盐水中;
方案B:将二氧化碳通入含大量氨的饱和食盐水中;
方案C:将氨气通入含二氧化碳的饱和食盐水中。
(2)制备流程:
配制含氨的饱和食盐水→配制二氧化碳→制备碳酸氢钠→制备碳酸钠
实验中使用的部分简易装置如图所示:

其中装置乙的作用为
(3)实验探究:制备碳酸氢钠的温度要控制在30-35℃,其理由是
本方法制得的纯碱中可能含有氯化钠,请设计检验实验方案,完成表中内容。
| 实验步骤 | 实验现象与结论 |
您最近一年使用:0次
解题方法
7 . 下图是中学化学实验中出现频率较高的装置,它是由物质制备、生成物性质检验和尾气处理三部分组成。请你用中学化学常见试剂设计一个实验,通过乙中的反应和丙中的实验现象,得出三种物质性质递变的结论。试将试剂名称、丙中的实验现象及由此得出的实验结论填入下列空白处。

(1)所用试剂的名称:甲_______ ,乙_______ ,丙_______ 。
(2)丙中现象:_______ 。丙中反应的化学方程式:_______ 。
(3)实验结论:_______ 。

(1)所用试剂的名称:甲
(2)丙中现象:
(3)实验结论:
您最近一年使用:0次
解题方法
8 . 根据下列操作及现象,能达到目的是
| 选项 | 操作及现象 | 实验目的 |
| A | 向20mLNa2CO3和NaOH混合溶液中,滴入几滴酚酞试液,用0.1000mol/L盐酸标准溶液滴定至粉红色 | 测定NaOH的浓度 |
| B | 向溶有SO2的BaCl2溶液中加入Fe(NO3)3溶液,有白色沉淀生成 | 说明 具有强氧化性 具有强氧化性 |
| C | 向5mL0.1mol/LKI溶液中滴加1mL0.1mol/LFeCl3溶液,充分反应后再滴加少量KSCN溶液,溶液变红 | 证明KI与FeCl3的反应属于可逆反应 |
| D | 分别向2mL乙醇和乙二醇中加入一粒绿豆大小的金属钠,乙二醇产生气泡的速度更快 | 证明乙二醇中羟基数目多 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
9 . 下列实验目的、实验操作及现象、结论都正确的是
| 选项 | 实验目的 | 实验及现象 | 结论 |
| A | 验证肉桂醛中含碳碳双键 | 向肉桂醛(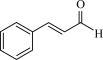 )中加入酸性KMnO4溶液 )中加入酸性KMnO4溶液 | 肉桂醛中含有碳碳双键 |
| B | 比较CuSO4和KMnO4的催化效果 | 向等体积等浓度的H2O2溶液中分别加入5滴等浓度的CuSO4溶液和KMnO4溶液,CuSO4溶液产生气泡速率快 | CuSO4催化H2O2溶液分解效果更好 |
| C | 验证菠菜中含有铁元素 | 将新鲜菠菜剪碎、研磨、溶解、过滤,向滤液中加入几滴KSCN溶液,溶液不变红 | 说明菠菜中不含铁元素 |
| D | 判断强酸和弱酸 | NaHCO3溶液显碱性,NaHSO3溶液显酸性 | 可以确定H2CO3是弱酸,无法判断H2SO3是否为弱酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-06-19更新
|
785次组卷
|
2卷引用:江西省赣州地区2023-2024学年十大教学能手选拔赛高中化学试题
解题方法
10 . 下列实验操作及现象均正确的是
| 选项 | 实验目的 | 实验操作 | 实验现象 |
| A | 探究硼酸和碳酸的酸性强弱 | 将足量硼酸滴入Na2CO3溶液中 | 有气泡产生 |
| B | 验证铜和浓硫酸反应的产物中有硫酸铜生成 | 直接向反应后的试管中加入蒸馏水 | 溶液变蓝 |
| C | 探究维生素C可以还原Fe3+ | 向盛有FeCl3溶液的试管中滴加适量浓维生素C溶液 | 溶液由黄色变为浅绿色 |
| D | 探究Fe3+和I-之间的反应为可逆反应 | 向氯化铁溶液中滴入少量 KI溶液,将反应后的溶液两等分,向其中一份滴入KSCN溶液,另一份滴淀粉溶液 | 一份溶液显血红色,另一份溶液显蓝色 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次