解题方法
1 . Ⅰ.研究铁的腐蚀,实验步骤如下:
步骤1:将铁粉放置于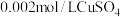 溶液中浸泡,过滤后用水洗涤。
溶液中浸泡,过滤后用水洗涤。
步骤2:向 溶液(用盐酸调至
溶液(用盐酸调至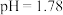 )中加入浸泡过的Fe粉。
)中加入浸泡过的Fe粉。
步骤3:采集溶液pH随时间变化的数据。_______ 。
(2)第二、三阶段主要发生吸氧腐蚀。
①析氧腐蚀时Cu上发生的电极反应为_______ 。
②第一阶段和第二阶段发生不同种类腐蚀的主要影响因素是_______ 。
Ⅱ.研究铁的防护
(3)在铁表面镀锌可有效防止铁被腐蚀
已知: 放电的速率缓慢且平稳时有利于得到致密、细腻的镀层。
放电的速率缓慢且平稳时有利于得到致密、细腻的镀层。
①镀件Fe应与电源的_______ 相连。
②向 电解液中加入NaCN溶液,将
电解液中加入NaCN溶液,将 转化为
转化为 ,电解得到的镀层更加致密、细腻,原因是
,电解得到的镀层更加致密、细腻,原因是_______ 。
(4)电镀后的废水中含有 ,一种测定其含量的方法是取废水50mL,再加KI溶液1mL,用
,一种测定其含量的方法是取废水50mL,再加KI溶液1mL,用 溶液滴定,达到滴定终点时,消耗
溶液滴定,达到滴定终点时,消耗 溶液
溶液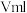 。
。
已知 (无色)
(无色) 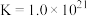
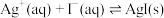 (黄色)
(黄色) 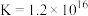
①滴定终点的现象是______________ 。
②废水中 的含量是
的含量是_______ g/L(用含C、V的代数式表示)。
步骤1:将铁粉放置于
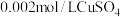 溶液中浸泡,过滤后用水洗涤。
溶液中浸泡,过滤后用水洗涤。步骤2:向
 溶液(用盐酸调至
溶液(用盐酸调至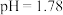 )中加入浸泡过的Fe粉。
)中加入浸泡过的Fe粉。步骤3:采集溶液pH随时间变化的数据。
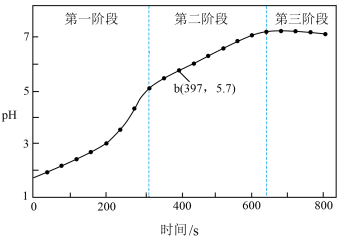
(2)第二、三阶段主要发生吸氧腐蚀。
①析氧腐蚀时Cu上发生的电极反应为
②第一阶段和第二阶段发生不同种类腐蚀的主要影响因素是
Ⅱ.研究铁的防护
(3)在铁表面镀锌可有效防止铁被腐蚀
已知:
 放电的速率缓慢且平稳时有利于得到致密、细腻的镀层。
放电的速率缓慢且平稳时有利于得到致密、细腻的镀层。①镀件Fe应与电源的
②向
 电解液中加入NaCN溶液,将
电解液中加入NaCN溶液,将 转化为
转化为 ,电解得到的镀层更加致密、细腻,原因是
,电解得到的镀层更加致密、细腻,原因是(4)电镀后的废水中含有
 ,一种测定其含量的方法是取废水50mL,再加KI溶液1mL,用
,一种测定其含量的方法是取废水50mL,再加KI溶液1mL,用 溶液滴定,达到滴定终点时,消耗
溶液滴定,达到滴定终点时,消耗 溶液
溶液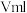 。
。已知
 (无色)
(无色) 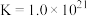
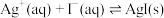 (黄色)
(黄色) 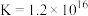
①滴定终点的现象是
②废水中
 的含量是
的含量是
您最近一年使用:0次
2 . 下列物质的检验中,其结论一定正确的是
A.加入 溶液,生成白色沉淀,加稀盐酸沉淀不溶解时,可确定有 溶液,生成白色沉淀,加稀盐酸沉淀不溶解时,可确定有 存在 存在 |
B.检验铵盐中含有 的操作是取少量某盐放入试管中,加入稀氢氧化钠溶液,用湿润的红色石蕊试纸放在试管口 的操作是取少量某盐放入试管中,加入稀氢氧化钠溶液,用湿润的红色石蕊试纸放在试管口 |
C.加入稀盐酸,生成的气体能使澄清石灰水变浑浊,可确定有 存在 存在 |
D.取少量久置的 样品于试管中加水溶解,若加足量盐酸时有气体产生,再加 样品于试管中加水溶解,若加足量盐酸时有气体产生,再加 溶液时有白色沉淀产生,则说明 溶液时有白色沉淀产生,则说明 样品已部分被氧化 样品已部分被氧化 |
您最近一年使用:0次
3 . 明矾是生活中常见的净水剂,用铝土矿 含30%SiO2、40.8%Al2O3和和少量
含30%SiO2、40.8%Al2O3和和少量 等
等 制取明矾的工艺如下:
制取明矾的工艺如下: (少部分发生类似反应),气体
(少部分发生类似反应),气体 的化学式为
的化学式为_____ 。
(2)操作①的名称是_____ ,操作①后,需洗涤固体 表面吸附的离子,判断固体
表面吸附的离子,判断固体 是否洗涤干净的实验方法是:取最后一次洗涤后的浸出液于试管中,滴加
是否洗涤干净的实验方法是:取最后一次洗涤后的浸出液于试管中,滴加 溶液,观察到
溶液,观察到_____ ,说明已洗涤干净。
(3)固体 加稀硫酸反应的离子方程式为
加稀硫酸反应的离子方程式为_____ 。
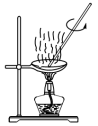
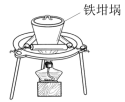
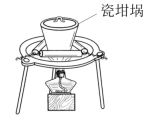
(4)固体 与
与 固体焙烧可制备防火材料,下列装置适合的是
固体焙烧可制备防火材料,下列装置适合的是_____  填字母编号
填字母编号 。
。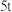 铝土矿,理论上可制得明矾
铝土矿,理论上可制得明矾_____ 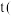 明矾的相对分子质量为474)。
明矾的相对分子质量为474)。
 含30%SiO2、40.8%Al2O3和和少量
含30%SiO2、40.8%Al2O3和和少量 等
等 制取明矾的工艺如下:
制取明矾的工艺如下: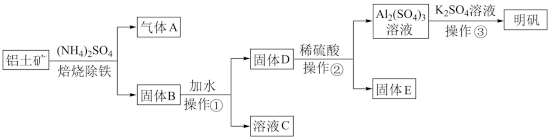
 (少部分发生类似反应),气体
(少部分发生类似反应),气体 的化学式为
的化学式为(2)操作①的名称是
 表面吸附的离子,判断固体
表面吸附的离子,判断固体 是否洗涤干净的实验方法是:取最后一次洗涤后的浸出液于试管中,滴加
是否洗涤干净的实验方法是:取最后一次洗涤后的浸出液于试管中,滴加 溶液,观察到
溶液,观察到(3)固体
 加稀硫酸反应的离子方程式为
加稀硫酸反应的离子方程式为(4)固体
 与
与 固体焙烧可制备防火材料,下列装置适合的是
固体焙烧可制备防火材料,下列装置适合的是 填字母编号
填字母编号 。
。



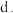
 铝土矿,理论上可制得明矾
铝土矿,理论上可制得明矾 明矾的相对分子质量为474)。
明矾的相对分子质量为474)。
您最近一年使用:0次
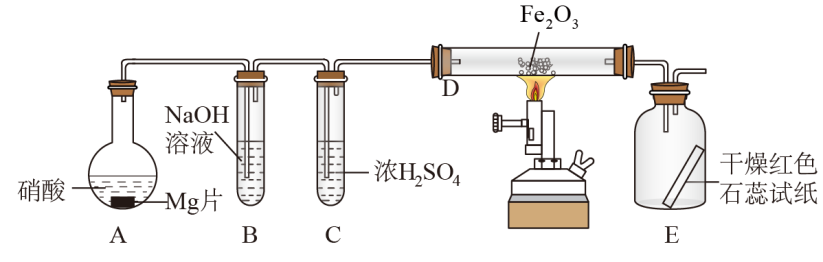
4 . 硝酸与金属反应时,浓度不同生成的还原产物也可能不同,某兴趣小组进行了如下图所示的实验探究,实验现象及相关数据如下:
②从C进入D中的气体有两种,且体积比为1∶1;
③将D加热一段时间后,E中干燥的红色石蕊试纸逐渐变蓝。(设实验前,装置中的空气已排尽;气体的体积均在同温同压下测定)
已知:2NO2+2NaOH=NaNO3+NaNO2+H2O,NO2+NO+2NaOH=2NaNO2+H2O,且水蒸气的体积忽略不计,实验中的液体药品均过量。请回答:
(1)装置中仪器A的名称___________ ;硝酸与Mg片反应生成的气体成分是___________ (用化学式表示)。
(2)硝酸在装置A的反应中所表现的性质有___________ 。
(3)利用所提供的试剂(NaNO2溶液、KMnO4溶液、KI溶液、稀硫酸、淀粉溶液)设计实验,证明B中生成的这种盐在酸性条件下具有氧化性___________ 。
(4)写出D中发生反应的化学方程式___________ 。
(5)若向反应后的A中加入足量的NaOH固体,使产生的气体全部逸出,其体积为硝酸与Mg片反应生成的气体体积的 (同温同压),写出符合上述实验事实的硝酸与Mg片反应的离子方程式
(同温同压),写出符合上述实验事实的硝酸与Mg片反应的离子方程式___________ 。
②从C进入D中的气体有两种,且体积比为1∶1;
③将D加热一段时间后,E中干燥的红色石蕊试纸逐渐变蓝。(设实验前,装置中的空气已排尽;气体的体积均在同温同压下测定)
已知:2NO2+2NaOH=NaNO3+NaNO2+H2O,NO2+NO+2NaOH=2NaNO2+H2O,且水蒸气的体积忽略不计,实验中的液体药品均过量。请回答:
(1)装置中仪器A的名称
(2)硝酸在装置A的反应中所表现的性质有
(3)利用所提供的试剂(NaNO2溶液、KMnO4溶液、KI溶液、稀硫酸、淀粉溶液)设计实验,证明B中生成的这种盐在酸性条件下具有氧化性
(4)写出D中发生反应的化学方程式
(5)若向反应后的A中加入足量的NaOH固体,使产生的气体全部逸出,其体积为硝酸与Mg片反应生成的气体体积的
 (同温同压),写出符合上述实验事实的硝酸与Mg片反应的离子方程式
(同温同压),写出符合上述实验事实的硝酸与Mg片反应的离子方程式
您最近一年使用:0次
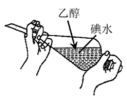
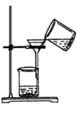
5 . 下列实验操作及其装置(加热装置已略去)合理的是
|
|
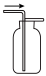
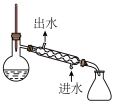
| A.用该装置收集CO2 | B.分离乙醇和水的混合物 |
|
|
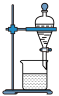
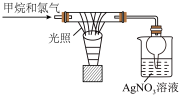
| C.分离甘油和乙酸乙酯 | D.验证甲烷和氯气发生了取代反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
6 . 钠、铝和铁是中学化学常见的三种重要金属。请回答下列问题:
(1)常温下,金属钠露置在空气中会发生变化,实验室通常把钠保存在_______ 中。
(2)除去碳酸钠固体中碳酸氢钠的方法是______________ 。
(3)实验室在保存含有Fe2+的溶液时,为了防止Fe2+变质,经常向其中加入_______ (填“铁粉”或“铜粉”)。
(4)Fe(OH)3不溶于水,但能溶于酸,请写出Fe(OH)3与盐酸反应的离子方程式:_______________ 。
(5)铝制餐具不宜用来蒸煮或长时间存放酸性或碱性食物,是因为Al和Al2O3均能与酸、碱反应。则Al2O3属于__________ (填“碱性”或“两性”)氧化物。
(1)常温下,金属钠露置在空气中会发生变化,实验室通常把钠保存在
(2)除去碳酸钠固体中碳酸氢钠的方法是
(3)实验室在保存含有Fe2+的溶液时,为了防止Fe2+变质,经常向其中加入
(4)Fe(OH)3不溶于水,但能溶于酸,请写出Fe(OH)3与盐酸反应的离子方程式:
(5)铝制餐具不宜用来蒸煮或长时间存放酸性或碱性食物,是因为Al和Al2O3均能与酸、碱反应。则Al2O3属于
您最近一年使用:0次
7 . 下列实验方法或操作正确的是
|
|
|
|
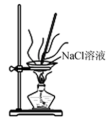
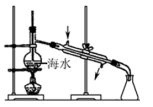
| A.萃取碘水中的碘 | B.过滤 | C.获取NaCl | D.制取淡水 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
8 . 实验室需要0.1 mol⋅L NaOH溶液450 mL和0.5 mol⋅L
NaOH溶液450 mL和0.5 mol⋅L 硫酸溶液450 mL。根据这两种溶液的配制情况回答下列问题:
硫酸溶液450 mL。根据这两种溶液的配制情况回答下列问题:
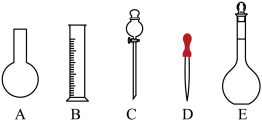
(1)如图所示的仪器中配制溶液肯定不需要的是___________ (填字母)。仪器C的名称是___________ ,本实验所需玻璃仪器E的规格和名称是___________ 。___________ (填“大于”“等于”或“小于”,下同)0.1 mol⋅L 。若NaOH溶液未冷却即转移至容量瓶定容,则所配制溶液浓度
。若NaOH溶液未冷却即转移至容量瓶定容,则所配制溶液浓度___________ 0.1 mol⋅L 。
。
(3)根据计算得知,所需质量分数为98%、密度为1.84 g⋅cm 的浓硫酸的体积为
的浓硫酸的体积为___________ mL(计算结果保留一位小数)。如果实验室有10 mL、25 mL、50 mL量筒,应选用___________ mL规格的量筒最好。
(4)如果定容时不小心超过刻度线,应如何操作:___________ 。
 NaOH溶液450 mL和0.5 mol⋅L
NaOH溶液450 mL和0.5 mol⋅L 硫酸溶液450 mL。根据这两种溶液的配制情况回答下列问题:
硫酸溶液450 mL。根据这两种溶液的配制情况回答下列问题:(1)如图所示的仪器中配制溶液肯定不需要的是
 。若NaOH溶液未冷却即转移至容量瓶定容,则所配制溶液浓度
。若NaOH溶液未冷却即转移至容量瓶定容,则所配制溶液浓度 。
。(3)根据计算得知,所需质量分数为98%、密度为1.84 g⋅cm
 的浓硫酸的体积为
的浓硫酸的体积为(4)如果定容时不小心超过刻度线,应如何操作:
您最近一年使用:0次
9 . 下列有关实验操作或说法正确的是
A.配制125 mL 1.0 mol⋅L 的氯化钠溶液需要用到130 mL的容量瓶 的氯化钠溶液需要用到130 mL的容量瓶 |
| B.探究碳酸钠和碳酸氢钠热稳定性实验应分别加入碳酸钠与碳酸氢钠 |
| C.制备氢氧化铁胶体的实验中应将氯化铁溶液加入到温水中,继续煮沸至红褐色即可 |
| D.干燥的氯气使湿润的鲜花变色,干燥的氯气具有漂白性 |
您最近一年使用:0次
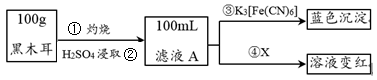
10 . 黑木耳富含蛋白质、铁、具有还原性的维生素C等,每100 g黑木耳含铁量高达185 mg。
I.为了确定黑木耳中含有铁元素,甲同学设计实验方案如下。____________ 。
(2)步骤④检验Fe3+所用试剂是_____________ (填化学式)溶液。
(3)已知:3Fe2++2[Fe(CN)6]3-=Fe3[Fe(CN)6]2↓,则滤液A中大量含有的阳离子 的离子符号为____________ 。
II.紫色的KMnO4溶液在酸性条件下具有强氧化性,其还原产物是无色的Mn2+。本实验用KMnO4酸性溶液来测定黑木耳中铁元素的含量,乙同学设计实验方案如下。_______ (填序号)。
a.Na b.Cu c.Fe
(5)步骤⑥的离子方程式为_______________ 。
(6)若乙同学实验操作规范,但测得含铁量远远偏高,其可能的原因是_______________ 。
I.为了确定黑木耳中含有铁元素,甲同学设计实验方案如下。
(2)步骤④检验Fe3+所用试剂是
(3)已知:3Fe2++2[Fe(CN)6]3-=Fe3[Fe(CN)6]2↓,则滤液A中大量含有的
II.紫色的KMnO4溶液在酸性条件下具有强氧化性,其还原产物是无色的Mn2+。本实验用KMnO4酸性溶液来测定黑木耳中铁元素的含量,乙同学设计实验方案如下。
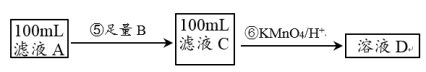
a.Na b.Cu c.Fe
(5)步骤⑥的离子方程式为
(6)若乙同学实验操作规范,但测得含铁量远远偏高,其可能的原因是
您最近一年使用:0次