真题
名校
1 . Na2SO3·7H2O是食品工业中常用的漂白剂、抗氧化剂和防腐剂。Na2SO3在30℃时的溶解度为35.5g/100gH2O。
1)计算30℃时Na2SO3饱和溶液中Na2SO3的质量分数
________ 。(保留2位小数)
2)计算30℃时271g Na2SO3饱和溶液中水的质量___________ 。
3)将30℃的Na2SO3饱和溶液271g冷却到10℃,析出Na2SO3·7H2O晶体79.5g。计算10℃时Na2SO3在水中的溶解度__________ 。
1)计算30℃时Na2SO3饱和溶液中Na2SO3的质量分数

2)计算30℃时271g Na2SO3饱和溶液中水的质量
3)将30℃的Na2SO3饱和溶液271g冷却到10℃,析出Na2SO3·7H2O晶体79.5g。计算10℃时Na2SO3在水中的溶解度
您最近一年使用:0次
2020-08-21更新
|
139次组卷
|
4卷引用:2010年全国普通高等学校招生统一考试上海卷化学试题
真题
2 . 碳酸氢铵是一种重要的铵盐。实验室中,将二氧化碳通入氨水可制得碳酸氢铵,用碳酸氢铵和氯化钠可制得纯碱。完成下列填空:
(1)二氧化碳通入氨水的过程中,先有__ 晶体(填写化学式)析出,然后晶体溶解,最后析出NH4HCO3晶体。
(2)含0.800 mol NH3的水溶液质量为54.0 g,向该溶液通入二氧化碳至反应完全,过滤,得到滤液31.2g,则NH4HCO3的产率为____ %。
(3)粗盐(含Ca2+、Mg2+)经提纯后,加入碳酸氢铵可制得碳酸钠。实验步骤依次为:①粗盐溶解;②加入试剂至沉淀完全,煮沸;③__ ;④加入盐酸调pH;⑤加入__ ;⑥过滤;⑦灼烧,冷却,称重。
(4)上述步骤②中所加入的试剂为__ 、__ 。
(5)上述步骤④中加盐酸调pH的目的是__ 。
(6)为探究NH4HCO3和NaOH的反应,设计实验方案如下:含0.1 mol NH4HCO3的溶液中加入0.1 mol NaOH,反应完全后,滴加氯化钙稀溶液。若有沉淀,则NH4HCO3与NaOH的反应可能为_____ (写离子方程式);若无沉淀,则NH4HCO3与NaOH的反应可能为______ (写离子方程式)。该实验方案有无不妥之处?若有,提出修正意见_____ 。
(1)二氧化碳通入氨水的过程中,先有
(2)含0.800 mol NH3的水溶液质量为54.0 g,向该溶液通入二氧化碳至反应完全,过滤,得到滤液31.2g,则NH4HCO3的产率为
(3)粗盐(含Ca2+、Mg2+)经提纯后,加入碳酸氢铵可制得碳酸钠。实验步骤依次为:①粗盐溶解;②加入试剂至沉淀完全,煮沸;③
(4)上述步骤②中所加入的试剂为
(5)上述步骤④中加盐酸调pH的目的是
(6)为探究NH4HCO3和NaOH的反应,设计实验方案如下:含0.1 mol NH4HCO3的溶液中加入0.1 mol NaOH,反应完全后,滴加氯化钙稀溶液。若有沉淀,则NH4HCO3与NaOH的反应可能为
您最近一年使用:0次
3 . 钠是活泼的碱金属元素,钠及其化合物在生产和生活中有广泛的应用。完成下列计算:
(1)叠氮化钠(NaN3)受撞击完全分解产生钠和氮气,故可应用于汽车安全气囊。若产生40.32 L(标准状况下)氮气,至少需要叠氮化钠___ g。
(2)钠-钾合金可在核反应堆中用作热交换液。5.05 g钠-钾合金溶于200 mL水生成0.075 mol氢气。
①计算溶液中氢氧根离子的物质的量浓度________ (忽略溶液体积变化)。
②计算并确定该钠-钾合金的化学式________ 。
(3)氢氧化钠溶液处理铝土矿井过滤,得到含铝酸钠的溶液。向该溶液中通入二氧化碳,有下列反应:2NaAl(OH)4+CO2→2Al(OH)3↓ +Na2CO3+H2O。已知通入二氧化碳336 L(标准状况下),生成24 mol Al(OH)3和15 mol Na2CO3,若通入溶液的二氧化碳为112L(标准状况下),计算生成的Al(OH)3和Na2CO3的物质的量之比________ 。
(4)常温下,称取不同氢氧化钠样品溶于水,加盐酸中和至pH=7,然后将溶液蒸干得氯化钠晶体,蒸干过程中产品无损失。
上述实验①②③所用氢氧化钠均不含杂质,且实验数据可靠。通过计算,分析和比较上表3组数据,给出结论________ 。
(1)叠氮化钠(NaN3)受撞击完全分解产生钠和氮气,故可应用于汽车安全气囊。若产生40.32 L(标准状况下)氮气,至少需要叠氮化钠
(2)钠-钾合金可在核反应堆中用作热交换液。5.05 g钠-钾合金溶于200 mL水生成0.075 mol氢气。
①计算溶液中氢氧根离子的物质的量浓度
②计算并确定该钠-钾合金的化学式
(3)氢氧化钠溶液处理铝土矿井过滤,得到含铝酸钠的溶液。向该溶液中通入二氧化碳,有下列反应:2NaAl(OH)4+CO2→2Al(OH)3↓ +Na2CO3+H2O。已知通入二氧化碳336 L(标准状况下),生成24 mol Al(OH)3和15 mol Na2CO3,若通入溶液的二氧化碳为112L(标准状况下),计算生成的Al(OH)3和Na2CO3的物质的量之比
(4)常温下,称取不同氢氧化钠样品溶于水,加盐酸中和至pH=7,然后将溶液蒸干得氯化钠晶体,蒸干过程中产品无损失。
| 氢氧化钠质量(g) | 氯化钠质量(g) | |
| ① | 2.40 | 3.51 |
| ② | 2.32 | 2.34 |
| ③ | 3.48 | 3.51 |
上述实验①②③所用氢氧化钠均不含杂质,且实验数据可靠。通过计算,分析和比较上表3组数据,给出结论
您最近一年使用:0次
真题
解题方法
4 . 碱式碳酸铜【Cu2(OH)2CO3】是一种用途广泛的化工原料,实验室以废铜屑为原料制取碱式碳酸铜的步骤如下:
步骤一:废铜屑制硝酸铜。如图,用胶头滴管吸取浓HNO3缓慢加到锥形瓶内的废铜屑中(废铜屑过量),充分反应后过滤,得到硝酸铜溶液。

步骤二:碱式碳酸铜的制备。向大试管中加入碳酸钠溶液和硝酸铜溶液,水浴加热至70℃左右,用0.4 mol/L的NaOH溶液调节pH至8.5,振荡,静置,过滤,用热水洗涤,烘干,得到碱式碳酸铜产品。完成下列填空:
(1)写出浓硝酸与铜反应的离子方程式____ 。
(2)上图装置中NaOH溶液的作用是__ 。反应结束后,广口瓶内的溶液中,除了含有NaOH外,还有____ (填写化学式)。
(3)步骤二中,水浴加热所需仪器有____ 、__ (加热、夹持仪器、石棉网除外);洗涤的目的是____ 。
(4)步骤二的滤液中可能含有CO32-,写出检验CO32-的方法_____ 。
(5)影响产品产量的主要因素有____ 。
(6)若实验得到2.42 g样品(只含CuO杂质),取此样品加热至分解完全后,得到1.80 g固体,此样品中碱式碳酸铜的质量分数是____ 。
步骤一:废铜屑制硝酸铜。如图,用胶头滴管吸取浓HNO3缓慢加到锥形瓶内的废铜屑中(废铜屑过量),充分反应后过滤,得到硝酸铜溶液。

步骤二:碱式碳酸铜的制备。向大试管中加入碳酸钠溶液和硝酸铜溶液,水浴加热至70℃左右,用0.4 mol/L的NaOH溶液调节pH至8.5,振荡,静置,过滤,用热水洗涤,烘干,得到碱式碳酸铜产品。完成下列填空:
(1)写出浓硝酸与铜反应的离子方程式
(2)上图装置中NaOH溶液的作用是
(3)步骤二中,水浴加热所需仪器有
(4)步骤二的滤液中可能含有CO32-,写出检验CO32-的方法
(5)影响产品产量的主要因素有
(6)若实验得到2.42 g样品(只含CuO杂质),取此样品加热至分解完全后,得到1.80 g固体,此样品中碱式碳酸铜的质量分数是
您最近一年使用:0次
5 . 实验室制取少量干燥的氨气涉及下列装置,其中正确的是
A. 是氨气发生装置 是氨气发生装置 |
B.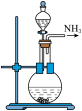 是氨气发生装置 是氨气发生装置 |
C.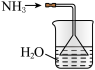 是氨气吸收装置 是氨气吸收装置 |
D.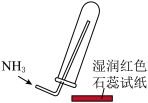 是氨气收集、检验装置 是氨气收集、检验装置 |
您最近一年使用:0次
2020-03-20更新
|
4930次组卷
|
84卷引用:2012年上海市高考化学试题
2012年上海市高考化学试题上海市北虹高级中学2018-2019学年高一下学期期中考试化学试题上海市交通大学附属中学2018-2019学年高一下学期期中考试化学试题(已下线)上海交大附中2018-2019学年高一下学期期中化学试题上海市七宝中学2017届高三上学期期中考试化学试题上海市金山中学2019-2020学年高一下学期期中考试化学试题上海市实验学校2022-2023学年高一上学期期末考试化学试题上海市松江一中2022-2023学年高一下学期期中考试化学试题上海市进才中学2022-2023学年高一下学期5月月考化学试题(已下线)2012-2013学年江苏省南通市海安县高一上学期期末考试化学试卷(已下线)2012-2013学年天津市天津一中高一上学期期末考试化学试卷(已下线)2014陕西西安市长安一中高一上学期期末化学(实验班)试卷2016届江苏省海门中学高三上学期9月学情调研化学试卷2015-2016学年湖北省黄石市高一上学期期末考试化学试卷2015-2016学年山东省寿光现代中学高一下开学测化学试卷2015-2016学年浙江省宁波市北仑中学高二下学期期中考试化学试卷(已下线)同步君 必修1 第4章 第4节 氨2017届江西师大附中高三上学期期中化学试卷2016-2017学年甘肃省武威市第十八中学高一下学期第一次月考化学试卷2016-2017学年山东省淄博市淄川中学高二下学期学分认定(期中)考试化学试卷(已下线)4.4.1 氨高中化学人教版 必修1 第四章 非金属及其化合物 4.氨 硫酸 硝酸 氨河南省南阳市第一中学2017-2018学年高一上学期第五次月考化学试题湖北省沙市中学2017-2018学年高一上学期期末考试化学试题山东省寿光现代中学2017-2018学年高一下学期开学考试化学试题云南省腾冲市第八中学2017-2018学年高一下学期第一次月考化学试题【全国百强校】黑龙江省鹤岗市第一中学2019届高三上学期第一次月考化学试题(已下线)2018年12月10日 《每日一题》人教必修1-氨的实验室制法安徽省滁州市定远县民族中学2018-2019学年高一上学期12月月考化学试题【市级联考】北京市2018 -2019学年高一上学期期末质量检测模拟化学试题【全国百强校】黑龙江省双鸭山市第一中学2018-2019学年高一下学期4月月考化学试题福建省泉州市泉港区第一中学2018-2019学年高一下学期期中考试化学试题【全国百强校】黑龙江省大庆市实验中学2018-2019学年高一(理)下学期期中考试化学试题新疆疏勒县八一中学2018-2019学年高一上学期期末考试化学试题江苏省南京市金陵中学2019-2020学年高二上学期学情调研化学试题福建省泉州第十六中学2020届高三上学期期中考试化学试题(已下线)2019年12月9日 《每日一题》化学人教版(必修1)——氨的实验室制法步步为赢高一化学寒假作业:作业十五 氨 硝酸 硫酸(已下线)2020年1月5日 《每日一题》人教版(必修1)——每周一测安徽省合肥市六校2019-2020学年高一上学期期末考试化学试题福建省厦门市思明区厦门外国语学校2019-2020学年高三上学期周末练习12——化学试题人教版(2019)必修第二册第五章第二节 课时2 氨和铵盐广东省2020年普通高中学业水平考试化学合格性考试模拟试题(六)湖北省荆州市荆州中学2019-2020学年高一下学期3月月考化学试题吉林省白山市第七中学2019-2020学年高一下学期第一次月考化学试题四川省眉山市2018-2019学年高一下学期期末教学质量检测化学试题湖北省宜昌市第二中学2019-2020高一下学期4 月线上检测化学试题吉林省辽源市辽县第一高级中学2019-2020高一下学期期中考试化学试题云南省曲靖市宣威市民族中学2019-2020学年高一下学期第一次月考化学试题陕西省西安中学2018-2019学年高一下学期期末考试化学题必修第二册RJ第5章第二节 氮及其化合物 课时2 氨和铵盐甘肃省武威市民勤县第一中学2019-2020学年高一下学期期中考试化学(文) 试题安徽省蚌埠第三中学2019-2020学年高一下学期开学考试化学试题辽宁省抚顺县高级中学2019-2020学年高一下学期期中网课学习质量检测化学试题甘肃省平凉市泾川县第一中学2020-2021学年高一上学期期末考试化学试题人教版2019必修第二册 第五章 本章达标检测(已下线)7.3.1 铵盐的性质 练习 -2020-2021学年下学期高一化学同步精品课堂(苏教版2019必修第二册)(已下线)7.2.1 氨气 练习 -2020-2021学年下学期高一化学同步精品课堂(苏教版2019必修第二册)江苏省苏州市工业园区星海实验中学高一下学期3月月考化学试题吉林省延边朝鲜族自治州汪清县第六中学2020-2021学年高一下学期3月月考化学试题安徽省黄山市屯溪第一中学、中科大附中2020-2021学年高一下学期期中联考化学试题(苏教版2019)必修第二册专题7 氮与社会可持续发展 第三单元 含氮化合物的合理使用 课时1 按盐的性质 常见氮肥及其使用(已下线)第29讲 常见气体的制备与性质实验(练) — 2022年高考化学一轮复习讲练测(新教材新高考)广东省广州市第八十九中学2021-2022学年高一上学期期中考试化学试题(已下线)第06讲 铵盐(word讲义)-【帮课堂】2021-2022学年高一化学同步精品讲义(人教版2019必修第二册)课后-5.2.2 氨和铵盐-人教2019必修第二册河北省武安市第一中学2020-2021学年高一下学期第二次月考化学试卷题江苏省南京市中华中学2020-2021学年高一下学期期中考试化学试题(已下线)第17讲 氨的转化与生成-【暑假自学课】2022年新高一化学暑假精品课(鲁科版2019必修第一册)广东省江门市江门一中2020-2021学年高一下学期第二次月考化学试题广东省华南师范大学附属中学2021-2022学年高一下学期期末考试化学试题黑龙江省大庆市大庆中学2021-2022学年高一下学期期末考试化学试题内蒙古自治区2019-2020学年普通高中学业水平考试(高二会考)化学真题山东省菏泽市单县第二中学2021-2022学年高一上学期(实验班)12月段考化学试题(已下线)广东省东莞市2022-2023学年高三上学期期末教学质量检查变式汇编(1-10)(已下线)5.2.2 氨和铵盐——同步学习必备知识福建省三明市永安第九中学2022-2023学年高一下学期返校考化学试题天津市第二十中学2022-2023学年高一下学期3月月考化学试题广东省佛山市顺德区容山中学2022-2023学年高一下学期3月月考化学试题山西省太原市2022-2023学年高一下学期期中考试化学试题甘肃省天水市第一中学2022-2023学年高一下学期5月期中考试化学试题河北省衡水市河北武强中学2023-2024学年高二上学期开学考试化学试题广东省深圳市光明中学2023-2024学年高一下学期3月第一次统测化学试题广东省茂名市高州中学2023-2024学年高一下学期期中考试化学(合格考)试题
6 . 下列有机化合物中均含有酸性杂质,除去这些杂质的方法中正确的是
| A.苯中含苯酚杂质:加入溴水,过滤 |
| B.乙醇中含乙酸杂质:加入碳酸钠溶液洗涤,分液 |
| C.乙醛中含乙酸杂质:加入氢氧化钠溶液洗涤,分液 |
| D.乙酸丁酯中含乙酸杂质:加入碳酸钠溶液洗涤,分液 |
您最近一年使用:0次
2020-03-20更新
|
1186次组卷
|
33卷引用:2012年上海市高考化学试题
2012年上海市高考化学试题上海市同济中学2016届高三上学期期中考试化学试题2019届上海奉贤区高考第一次模拟化学试题2020届上海市奉贤区高考化学一模试卷(已下线)2013-2014陕西省岐山县第二学期高二期末化学试卷(已下线)2013-2014山西省广灵县第一中学第二学期期末考试高二化学试卷2015-2016学年吉林省松原市油田高中高二下期中化学试卷2015-2016学年河南省南阳一中高二下期末模拟化学试卷2015-2016学年云南省玉溪一中高二下期末化学试卷2014-2015学年辽宁省锦州市高二下学期期末化学试卷2016-2017学年云南省云天化中学高二上期中化学卷云南省玉溪市第一中学2016-2017学年高二下学期期中考试化学试题江西省景德镇市第一中学2016-2017学年高一(17班)下学期期末考试化学试题河南省驻马店市2016-2017学年高二下学期期末考试化学试题湖北省荆门市2016-2017学年高二下学期期末质量检测化学试题内蒙古杭锦后旗奋斗中学2017-2018学年高二上学期第一次月考化学试题内蒙古太仆寺旗宝昌一中2017-2018学年高二上学期期中考试化学试题河南省南阳市第一中学2017-2018学年高二下学期第二次月考化学试题【全国百强校】河南省林州市第一中学2017-2018学年高二上学期期中考试(火箭班)化学试题【全国市级联考】河北省石家庄市2017-2018学年高二下学期期末考试化学试题【全国百强校】内蒙古自治区巴彦淖尔一中2018-2019学年高二上学期10月月考化学试题【校级联考】湖南省醴陵二中、醴陵四中2018-2019学年高二下学期期中联考化学试题湖南省株洲市2019-2020学年高二上学期期中考试化学试题安徽省肥东县第二中学2019-2020学年高二下学期期中考试(共建班)化学试题河北省沧州市盐山县盐山中学2019-2020学年高二下学期开学考试化学试题辽宁省葫芦岛市建昌县高级中学2019-2020学年高二下学期期初考试化学试题江苏省盐城市一中、射阳中学等五校2020-2021学年高二上学期期中联考化学(选修)试题(已下线)小题11 简单代表物的组成、结构与性质 ——备战2021年高考化学经典小题考前必刷(全国通用)广东省广州市广雅中学2020-2021学年高二下学3月阶段考试化学试题河北省沧州市肃宁一中2020-2021学年高二下学期4月月考化学试题黑龙江省大庆铁人中学2021-2022学年高二下学期期中考试化学试题四川省自贡市富顺县城关中学2021-2022学年高二下学期期中考试化学试题黑龙江省牡丹江市第二高级中学2022-2023学年高二下学期6月月考化学试题
真题
7 . CuSO4·5H2O是铜的重要化合物,有着广泛的应用。以下是CuSO4·5H2O的实验室制备流程图。
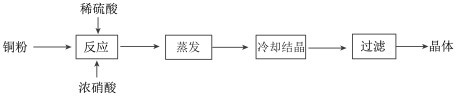
根据题意完成下列填空:
(1)向含铜粉的稀硫酸中滴加浓硝酸,在铜粉溶解时可以观察到的实验现象:______ 、______ 。
(2)如果铜粉、硫酸及硝酸都比较纯净,则制得的CuSO4·5H2O中可能存在的杂质是________ ,除去这种杂质的实验操作称为_________ 。
(3)已知:CuSO4+2NaOH=Cu(OH)2↓+ Na2SO4。称取0.1000 g提纯后的CuSO4·5H2O试样于锥形瓶中,加入0.1000 mol/L氢氧化钠溶液28.00 mL,反应完全后,过量的氢氧化钠用0.1000 mol/L盐酸滴定至终点,耗用盐酸20.16 mL,则0.1000 g该试样中含CuSO4·5H2O________ g。
(4)上述滴定中,滴定管在注入盐酸之前,先用蒸馏水洗净,再用_________ 。在滴定中,准确读数应该是滴定管上蓝线_________ 所对应的刻度。
(5)如果采用重量法测定CuSO4·5H2O的含量,完成下列步骤:①__________ ②加水溶解③加氯化钡溶液,沉淀④过滤(其余步骤省略)在过滤前,需要检验是否沉淀完全,其操作是_________
(6)如果1.040 g提纯后的试样中含CuSO4·5H2O的准确值为1.015 g,而实验测定结果是l.000 g 测定的相对误差为______________ 。

根据题意完成下列填空:
(1)向含铜粉的稀硫酸中滴加浓硝酸,在铜粉溶解时可以观察到的实验现象:
(2)如果铜粉、硫酸及硝酸都比较纯净,则制得的CuSO4·5H2O中可能存在的杂质是
(3)已知:CuSO4+2NaOH=Cu(OH)2↓+ Na2SO4。称取0.1000 g提纯后的CuSO4·5H2O试样于锥形瓶中,加入0.1000 mol/L氢氧化钠溶液28.00 mL,反应完全后,过量的氢氧化钠用0.1000 mol/L盐酸滴定至终点,耗用盐酸20.16 mL,则0.1000 g该试样中含CuSO4·5H2O
(4)上述滴定中,滴定管在注入盐酸之前,先用蒸馏水洗净,再用
(5)如果采用重量法测定CuSO4·5H2O的含量,完成下列步骤:①
(6)如果1.040 g提纯后的试样中含CuSO4·5H2O的准确值为1.015 g,而实验测定结果是l.000 g 测定的相对误差为
您最近一年使用:0次
真题
8 . 氨和联氨(N2H4)是氮的两种常见化合物,在科学技术和生产中有重要的应用。
根据题意完成下列计算:
(1)联氨用亚硝酸氧化生成氮的另一种氢化物,该氢化物的相对分子质量为43.0,其中氮原子的质量分数为0.977,计算确定该氢化物的分子式___________ 。该氢化物受撞击则完全分解为氮气和氢气。4.30 g该氢化物受撞击后产生的气体在标准状况下的体积为___________ L。
(2)联氨和四氧化二氮可用作火箭推进剂,联氨是燃料,四氧化二氮作氧化剂,反应产物是氮气和水。
由联氨和四氧化二氮组成的火箭推进剂完全反应生成72.0 kg水,计算推进剂中联氨的质量___________ 。
(3)氨的水溶液可用于吸收NO与NO2混合气体,反应方程式为6NO+ 4NH3=5N2+6H2O,6NO2+ 8NH3=7N2+12H2O;NO与NO2混合气体180 mol被8.90×103g氨水(质量分数0.300)完全吸收,产生156 mol氮气。吸收后氨水密度为0.980 g/cm3。计算:①该混合气体中NO与NO2的体积比____________ 。②吸收后氨水的物质的量浓度_______________ (答案保留1位小数)。
(4)氨和二氧化碳反应可生成尿素CO(NH2)2。尿素在一定条件下会失去氨而缩合,如两分子尿素失去一分子氨形成二聚物:
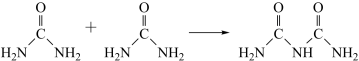 +NH3
+NH3
已知常压下120 mol CO(NH2)2在熔融状态发生缩合反应,失去80 mol NH3,生成二聚物(C2H5N3O2)和三聚物。测得缩合产物中二聚物的物质的量分数为0.60,推算缩合产物中各缩合物的物质的量之比__________ 。
根据题意完成下列计算:
(1)联氨用亚硝酸氧化生成氮的另一种氢化物,该氢化物的相对分子质量为43.0,其中氮原子的质量分数为0.977,计算确定该氢化物的分子式
(2)联氨和四氧化二氮可用作火箭推进剂,联氨是燃料,四氧化二氮作氧化剂,反应产物是氮气和水。
由联氨和四氧化二氮组成的火箭推进剂完全反应生成72.0 kg水,计算推进剂中联氨的质量
(3)氨的水溶液可用于吸收NO与NO2混合气体,反应方程式为6NO+ 4NH3=5N2+6H2O,6NO2+ 8NH3=7N2+12H2O;NO与NO2混合气体180 mol被8.90×103g氨水(质量分数0.300)完全吸收,产生156 mol氮气。吸收后氨水密度为0.980 g/cm3。计算:①该混合气体中NO与NO2的体积比
(4)氨和二氧化碳反应可生成尿素CO(NH2)2。尿素在一定条件下会失去氨而缩合,如两分子尿素失去一分子氨形成二聚物:
 +NH3
+NH3已知常压下120 mol CO(NH2)2在熔融状态发生缩合反应,失去80 mol NH3,生成二聚物(C2H5N3O2)和三聚物。测得缩合产物中二聚物的物质的量分数为0.60,推算缩合产物中各缩合物的物质的量之比
您最近一年使用:0次
真题
名校
9 . 草酸晶体(H2C2O4·2H2O)100 ℃开始失水,101.5 ℃熔化,150 ℃左右分解产生H2O、CO和CO2。用加热草酸晶体的方法使其分解获取某些气体,应该选择的气体发生装置是( )
A.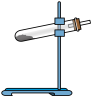 | B.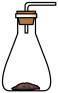 | C.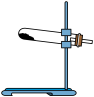 | D.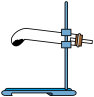 |
您最近一年使用:0次
2019-10-11更新
|
1078次组卷
|
26卷引用:2011年上海市高考化学试题
2011年上海市高考化学试题(已下线)2011-2012学年上海市吴淞中学高二上学期期中考试化学试卷(已下线)第10讲 过滤 结晶 蒸馏-【暑假自学课】2022年新高一化学暑假精品课(沪科版2020必修第一册)(已下线)1.3.2 过滤、结晶、蒸馏-【帮课堂】2022-2023学年高一化学同步精品讲义(沪科版2020必修第一册)上海市奉贤中学2021-2022学年高一上学期期中考试化学试题(已下线)2011-2012学年辽宁省五校协作体高一上学期期中考试化学试卷(已下线)2011-2012学年山东省微山一中高二上学期期中考试化学试卷(已下线)2012届甘肃省天水市一中高三第四阶段考试化学试卷(已下线)2012届陕西省兴平市秦岭中学高三上学期期末练习化学试卷(已下线)2011-2012学年浙江省嵊泗中学高二上学期第一次月考化学试试卷二2016-2017学年安徽省合肥一中高一上第一次月考化学卷甘肃省张掖市民乐县第一中学2019届高三上学期10月月考化学试题【全国百强校】安徽省合肥市第六中学2018-2019学年高一上学期第一次段考化学试题安徽省合肥市第六中学2018-2019学年高二上学期第一次段考化学试题陕西省蓝田县焦岱中学2019届高三上学期第一次月考化学试题吉林省靖宇县一中2019-2020学年高一上学期第一次月考化学试题江西省南昌市第二中学2019-2020学年高一上学期第一次月考化学试题(已下线)考点20 化学基础实验——《备战2020年高考精选考点专项突破题集》(已下线)【南昌新东方】2019 南昌二中 高一上第一次月考江西省南昌江西师范大学附属中学2020-2021学年高一上学期第一次月考化学试题(已下线)【南昌新东方】12. 南大附中 项金辉 袁斌.(已下线)【南昌新东方】1. 师大附中 蔡辉(已下线)微专题44 以气体制备为主体的实验-备战2023年高考化学一轮复习考点微专题安徽省徽师联盟2023-2024学年高三10月联考化学试题(已下线)第1讲 常用的仪器及基本操作(已下线)微专题 仪器的组合与创新使用
10 . (A)如图所示,将甲、乙两个装有不同物质的针筒用导管连接起来,将乙针筒内的物质压到甲针筒内,进行下表所列的不同实验(气体在同温同压下测定)。试回答下列问题:

(1)实验1中,沉淀最终变为________ 色,写出沉淀变色的化学方程式_______________________________ 。
(2)实验2甲针筒内的现象是:有___________ 生成,活塞________ 移动(填向外、向内、不)。反应后甲针筒内有少量的残留气体,正确的处理方法是将其通入___________ 溶液中。
(3)实验3中,甲中的3mL气体是NO2和N2O4的混合气体,那么甲中最后剩余的无色气体是_______ ,写出NO2与H2O反应的化学方程式为_______________________________ 。
(4)实验4中,已知:3Cl2+2NH3→N2+6HCl。甲针筒内活塞有移动,针筒内有白烟产生外,气体的颜色变为____________ 。最后针筒内剩余气体的体积约为________ mL。

| 实验序号 | 甲针筒内物质 | 乙针筒内物质 | 甲针简的现象 |
| 1 | 10mLFeSO4溶液 | 10mLNH3 | 生成白色沉淀,后变色 |
| 2 | 20mLH2S | 10mLSO2 | |
| 3 | 30mLNO2(主要) | 10mLH2O(l) | 剩有无色气体,活塞自动向内压缩 |
| 4 | 15mLCl2 | 40mLNH3 |
(1)实验1中,沉淀最终变为
(2)实验2甲针筒内的现象是:有
(3)实验3中,甲中的3mL气体是NO2和N2O4的混合气体,那么甲中最后剩余的无色气体是
(4)实验4中,已知:3Cl2+2NH3→N2+6HCl。甲针筒内活塞有移动,针筒内有白烟产生外,气体的颜色变为
您最近一年使用:0次



