解题方法
1 . 某工业食盐样品中混有NaBr杂质,现对其进行提纯,并获取液态溴,可设计实验流程如图所示:

下列说法错误的是

下列说法错误的是
A.依据实验流程可知,操作Ⅰ为萃取、分液,可选取 作为萃取剂 作为萃取剂 |
| B.由液体D中获取液溴时采用蒸馏操作,所用温度计的水银球应插入液面以下 |
| C.在进行操作Ⅱ时,需要的主要仪器有铁架台(带铁圈)、酒精灯、蒸发皿、玻璃棒、坩埚钳 |
| D.若样品为44.0g,最终获得42.1g氯化钠固体,则原固体混合物中氯化钠的质量分数约为90% |
您最近一年使用:0次
2022高一·上海·专题练习
解题方法
2 . 某浓盐酸的质量分数是36.5%,密度约1.18g·mL-1。求:
(1)该盐酸的物质的量浓度为____ 。
(2)取该盐酸10mL加水稀释到100mL,则稀释后溶液中c(HCl)=___ ,其中含有HCl的质量为____ (保留2位小数)。
(3)取稀释后的该100mL盐酸与足量的锌粒反应,生成标准状况下气体的体积是_____ (保留2位小数),质量为____ (保留2位小数)。
(1)该盐酸的物质的量浓度为
(2)取该盐酸10mL加水稀释到100mL,则稀释后溶液中c(HCl)=
(3)取稀释后的该100mL盐酸与足量的锌粒反应,生成标准状况下气体的体积是
您最近一年使用:0次
名校
3 . 设阿伏加德罗常数的值为NA,下列说法不正确的是
| A.常温下,100g质量分数46%的乙醇(C2H5OH)水溶液中,含有的氧原子数为4NA |
| B.1mol钠与氧气完全反应生成Na2O或Na2O2时,失电子数目均为NA |
| C.Na2O2与水反应时,生成0.1molO2转移的电子数为0.2NA |
| D.17g14N1H3所含中子数目为10NA |
您最近一年使用:0次
2022-02-24更新
|
513次组卷
|
3卷引用:卷03 阿伏伽德罗常数有关计算-【小题小卷】冲刺2022年高考化学小题限时集训(全国卷专用)
(已下线)卷03 阿伏伽德罗常数有关计算-【小题小卷】冲刺2022年高考化学小题限时集训(全国卷专用)广东省东莞市东华高级中学2021-2022学年高一上学期期末考试化学试题广东省江门市广雅中学2023-2024学年高一上学期12月月考化学试题B卷
名校
4 . 用NA代表阿伏加德罗常数的值。下列说法正确的是
A.1L pH=4的0.1mol/L K2Cr2O7溶液中Cr2O 离子数为0.1NA 离子数为0.1NA |
| B.1mol HClO中含有H—Cl键数为NA |
| C.反应生成22.4LO2,转移电子数为4NA |
| D.100g质量分数为46%的乙醇溶液,含有的O—H键数目为7NA |
您最近一年使用:0次
2022-02-22更新
|
554次组卷
|
3卷引用:专题02 阿伏伽德罗常数的判断-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)
(已下线)专题02 阿伏伽德罗常数的判断-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)湖南省衡阳市第八中学2021-2022学年高三下学期开学考试(第六次月考)化学试题安徽省滁州市定远县育才学校2021-2022学年高三下学期第二次月考理科综合化学试题
2024高三·全国·专题练习
解题方法
5 . 热重分析法测定结晶的含量:氮气气氛中以升温速率10℃/min测定某化合物(K2[Cu(C2O4)2]·nH2O)的热失重曲线,如图所示晶体在107℃失重10.2%,失去全部结晶水。
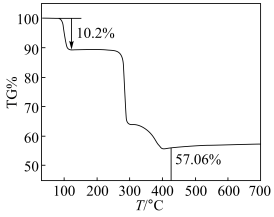
(1)通过热失重分析,蓝色晶体的化学式中n=___________ ,经过实验测定后,蓝色晶体的化学式为___________ 。
(2)加热400℃之后,剩余物质的质量不再发生变化。为探究剩余固体的成分,冷却后取少量固体于试管中,加水溶解有红色不溶物,过滤后向滤液中加入稀盐酸产生无色无味气体。则剩余固体的成分为___________ 。

(1)通过热失重分析,蓝色晶体的化学式中n=
(2)加热400℃之后,剩余物质的质量不再发生变化。为探究剩余固体的成分,冷却后取少量固体于试管中,加水溶解有红色不溶物,过滤后向滤液中加入稀盐酸产生无色无味气体。则剩余固体的成分为
您最近一年使用:0次
2023高三上·全国·专题练习
解题方法
6 . 请完成下列填空:
(1)一定条件下Fe(OH)3与KClO在KOH溶液中反应可制得K2FeO4。生成0.1 mol K2FeO4转移的电子的物质的量_______ mol。
(2)二氧化铈(CeO2)是一种重要的稀土氧化物,在平板电视显示屏中有着重要的应用CeO2在稀硫酸和H2O2的作用下可生成Ce3+,H2O2在该反应中作_______ (填“氧化”“还原”)剂,每有1 mol H2O2参加反应,转移电子的物质的量为_______ 。
(3)反应2LiBH4=2LiH+2B+3H2↑,生成22.4 L的H2(标准状况)时,转移电子的物质的量为_______ mol。
(4)用酸性高锰酸钾溶液滴定法可测定双氧水中H2O2的含量:H2O2+KMnO4+H2SO4→MnSO4+K2SO4+O2↑+H2O(未配平),若滴定中消耗0.50 mol/L的高锰酸钾溶液40.00 mL,则此双氧水溶液中溶质的质量为_______ g。
(5)取300 mL0.2 mol/L的KI溶液与一定量的酸性KMnO4溶液恰好反应,生成等物质的量的I2和KIO3,则消耗KMnO4的物质的量的是_______ mol。
(1)一定条件下Fe(OH)3与KClO在KOH溶液中反应可制得K2FeO4。生成0.1 mol K2FeO4转移的电子的物质的量
(2)二氧化铈(CeO2)是一种重要的稀土氧化物,在平板电视显示屏中有着重要的应用CeO2在稀硫酸和H2O2的作用下可生成Ce3+,H2O2在该反应中作
(3)反应2LiBH4=2LiH+2B+3H2↑,生成22.4 L的H2(标准状况)时,转移电子的物质的量为
(4)用酸性高锰酸钾溶液滴定法可测定双氧水中H2O2的含量:H2O2+KMnO4+H2SO4→MnSO4+K2SO4+O2↑+H2O(未配平),若滴定中消耗0.50 mol/L的高锰酸钾溶液40.00 mL,则此双氧水溶液中溶质的质量为
(5)取300 mL0.2 mol/L的KI溶液与一定量的酸性KMnO4溶液恰好反应,生成等物质的量的I2和KIO3,则消耗KMnO4的物质的量的是
您最近一年使用:0次
解题方法
7 . 现有一瓶常见一元酸形成的铵盐固体,为测定其中的含氮量可以采用“甲醛法”,即: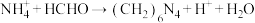 (未配平)。现称取4g该铵盐溶于水,加入足量的甲醛溶液后,再加入水配成100mL溶液。取出5mL,滴入酚酞后再逐滴滴入
(未配平)。现称取4g该铵盐溶于水,加入足量的甲醛溶液后,再加入水配成100mL溶液。取出5mL,滴入酚酞后再逐滴滴入 的NaOH溶液,当滴到25mL时溶液呈粉红色,且在半分钟内不褪色。计算:
的NaOH溶液,当滴到25mL时溶液呈粉红色,且在半分钟内不褪色。计算:
(1)过程中消耗的甲醛物质的量为_______ mol。
(2)该铵盐中氮的质量分数是_______ %。(写出计算过程)
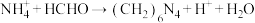 (未配平)。现称取4g该铵盐溶于水,加入足量的甲醛溶液后,再加入水配成100mL溶液。取出5mL,滴入酚酞后再逐滴滴入
(未配平)。现称取4g该铵盐溶于水,加入足量的甲醛溶液后,再加入水配成100mL溶液。取出5mL,滴入酚酞后再逐滴滴入 的NaOH溶液,当滴到25mL时溶液呈粉红色,且在半分钟内不褪色。计算:
的NaOH溶液,当滴到25mL时溶液呈粉红色,且在半分钟内不褪色。计算:(1)过程中消耗的甲醛物质的量为
(2)该铵盐中氮的质量分数是
您最近一年使用:0次
2022-05-19更新
|
896次组卷
|
3卷引用:专题讲座(一) 化学计算的常用方法(练)-2023年高考化学一轮复习讲练测(全国通用)
(已下线)专题讲座(一) 化学计算的常用方法(练)-2023年高考化学一轮复习讲练测(全国通用)浙江省Z20名校联盟(名校新高考研究联盟)2022届高三第三次联考化学试题浙江省Z20名校联盟2022届高三第三次联考化学试题
名校
解题方法
8 . 将a g CuO和铜粉的混合物样品加入到体积为1L的H2SO4和Fe2(SO4)3的混合溶液中,样品完全溶解,溶液中只有Fe2+、Cu2+、H+三种阳离子,且三种阳离子物质的量之比为5︰3︰1(不考虑盐的水解及溶液体积的变化)。若测得反应后溶液的c(H+)=0.1 mol/L,下列说法正确的是
| A.原溶液中c(H2SO4)为0.05 mol/L |
| B.向反应前的溶液中加入足量铁粉,产生的气体体积为4.48L |
| C.混合物中铜的质量分数为60% |
| D.将足量的H2通入灼热的混合物,反应结束后,混合物的质量减少了0.8g |
您最近一年使用:0次
2021-08-06更新
|
1252次组卷
|
10卷引用:专题六 铁及其化合物(B卷)-2021-2022学年高一化学优选好题单元专题双测卷(人教版2019必修第一册)
(已下线)专题六 铁及其化合物(B卷)-2021-2022学年高一化学优选好题单元专题双测卷(人教版2019必修第一册)(已下线)专题3.1.3 铁盐与亚铁盐(备作业)-【上好课】2021-2022学年高一化学同步备课系列(人教版2019必修第一册)重庆市南开中学2020-2021学年高一上学期期末考试化学试题江苏省泰州中学2021-2022学年高一上学期第二次月度检测化学试题湖北省荆州中学2021-2022学年高一上学期期末考试化学试题重庆市第七中学校2021-2022高一上学期第四次月检测化学试题湖北省襄阳市第四中学2021-2022学年高一下学期2月考试化学试题内蒙古鄂尔多斯市第一中学2022-2023 学年高一上学期期末考试化学试题2023年广西高中学生竞赛(高一、高二同卷)化学试题2023年第37届中国化学奥林匹克广西预选赛化学试题
2021高三·全国·专题练习
解题方法
9 . 2.76 g CaO2·8H2O样品受热脱水过程的热重曲线(样品质量随温度变化的曲线,140 ℃时完全脱水,杂质受热不分解)如图所示。

①试确定60 ℃时CaO2·xH2O中x=___________ 。
②该样品中CaO2的质量分数为___________ 。

①试确定60 ℃时CaO2·xH2O中x=
②该样品中CaO2的质量分数为
您最近一年使用:0次
10 . 设NA为阿伏加德罗常数的值。下列说法正确的是
| A.标准状况下,1.12LSO3含有的质子数为2NA |
| B.100g质量分数17%H2O2溶液中含有H-O键数目为NA |
| C.将0.1 mol Cl2通入到足量的水中,溶液中Cl−、HClO、ClO−微粒总数为0.2 NA |
| D.已知CrO5中Cr元素的化合价为+6,则13.2g CrO5中存在过氧键的数目为0.2 NA |
您最近一年使用:0次



