名校
1 . 实验室中利用硫化亚铁和硫化锌混合物进行如图实验(忽略 在水中的溶解)。下列说法错误的是。
在水中的溶解)。下列说法错误的是。

 在水中的溶解)。下列说法错误的是。
在水中的溶解)。下列说法错误的是。
| A.“4.5g固体”一定是铁锌混合物 | B.“溶液2”中的溶质只有 |
| C.混合物中硫元素的质量分数约为38% | D.反应②能生成标准状况下 |
您最近一年使用:0次
2022-10-28更新
|
885次组卷
|
4卷引用:专题五 化学常用计量与化学计算-实战高考·二轮复习核心突破
(已下线)专题五 化学常用计量与化学计算-实战高考·二轮复习核心突破河南省安阳市2022-2023学年高三上学期第一次联考(二)全国卷化学试题广东省2023届高三一轮复习联考(二)广东卷化学试题广东省部分学校2022-2023学年高三上学期一轮复习联考(二)化学试题
2 . 阿伏加德罗常数的值用NA表示。下列说法中正确的是( )
| A.常温常压下,11.2LSO2含有的氧原子数大于NA |
| B.一定条件下,Ca与O2反应生成7.2gCaO2,转移电子的个数为0.4 NA |
| C.10g质量分数为98%的浓硫酸含有的氢原子数为0.2 NA |
| D.0.1mool Na2O2和Na2O的混合物中含有的离子总数等于0.3 NA |
您最近一年使用:0次
3 . 工业上,常采用生物堆浸法处理低品位黄铜矿[二硫化亚铁铜( )含量较低]。生物堆浸过程发生的反应有
)含量较低]。生物堆浸过程发生的反应有 。设
。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 )含量较低]。生物堆浸过程发生的反应有
)含量较低]。生物堆浸过程发生的反应有 。设
。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.1LpH=1的稀硫酸中含有的 数目为2 数目为2 |
B.22.4L 转移电子数目为4 转移电子数目为4 |
C.等浓度的 和 和 溶液中含阴离子数目相等 溶液中含阴离子数目相等 |
D.2.0g 中含有的质子数目为 中含有的质子数目为 |
您最近一年使用:0次
2022高一·上海·专题练习
解题方法
4 . 溶质的质量分数为14%的KOH溶液,经加热蒸发去100 g水后,质量分数变成28%,体积为80 mL,则此时溶液的物质的量浓度为
| A.5 mol·L-1 | B.6 mol·L-1 | C.6.75 mol·L-1 | D.6.25 mol·L-1 |
您最近一年使用:0次
5 . NA为阿伏加德罗常数的值。下列说法正确的是
| A.标况下,34gH2O2中含有的非极性键数目为3NA |
B.标况下,22.4LCO2与足量NaOH溶液完全反应,所得溶液中:N( )+N( )+N( )+N(H2CO3)=NA )+N(H2CO3)=NA |
| C.100g质量分数为63%的HNO3溶液中氧原子的数目为3NA |
| D.6.9gNa与1L0.2mol/L盐酸反应生成的H2分子数为0.1NA |
您最近一年使用:0次
解题方法
6 . 设 为阿伏加德罗常数的值。下列有关叙述正确的是
为阿伏加德罗常数的值。下列有关叙述正确的是
 为阿伏加德罗常数的值。下列有关叙述正确的是
为阿伏加德罗常数的值。下列有关叙述正确的是A.1mol Cu与S完全反应,转移的电子数为 |
B.1mol Fe与稀硝酸完全反应,转移电子数一定为 |
C.标准状况下,22.4L的 通入水中生成 通入水中生成 分子数为 分子数为 |
D.50g质量分数为46%的乙醇水溶液中含H—O键数目为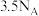 |
您最近一年使用:0次
2022高三·全国·专题练习
7 . 10g质量分数为34%的H2O2溶液含有的氢原子数为0.2NA。(_____)
您最近一年使用:0次
8 . 设 为阿伏加德罗常数的值。反应
为阿伏加德罗常数的值。反应 常用于监测
常用于监测 含量是否达到排放标准。下列说法正确的是
含量是否达到排放标准。下列说法正确的是
 为阿伏加德罗常数的值。反应
为阿伏加德罗常数的值。反应 常用于监测
常用于监测 含量是否达到排放标准。下列说法正确的是
含量是否达到排放标准。下列说法正确的是A.生成2.33g 沉淀时,转移电子数目为0.04 沉淀时,转移电子数目为0.04 |
B.标准状况下,22.4L 中硫原子的孤电子对数为2 中硫原子的孤电子对数为2 |
C.25℃时, 的HCl溶液中含有 的HCl溶液中含有 的数目为0.1 的数目为0.1 |
D. 晶体和 晶体和 晶体混合物共1 mol,则极性键数目为2 晶体混合物共1 mol,则极性键数目为2 |
您最近一年使用:0次
2024-03-15更新
|
888次组卷
|
4卷引用:题型3 有关NA的综合考查(25题)-2024年高考化学常考点必杀300题(新高考通用)
(已下线)题型3 有关NA的综合考查(25题)-2024年高考化学常考点必杀300题(新高考通用)(已下线)选择题1-5广东省江门市2023-2024学年高三一模考试化学卷河南省南阳市华龙高中2023-2024学年高二下学期3月月考化学试题
9 .  2在生活、生产中有重要用途,使用不当会造成环境污染。回答下列问题:
2在生活、生产中有重要用途,使用不当会造成环境污染。回答下列问题:
(1)硫酸亚铁加热至高温会分解,生成三种氧化物。为探究硫酸亚铁的分解产物,将无水硫酸亚铁装入反应管A并连接如图所示的装置,打开 1和
1和 2,缓缓通入
2,缓缓通入 2,加热。实验后反应管A中残留的固体为红色粉末
2,加热。实验后反应管A中残留的固体为红色粉末
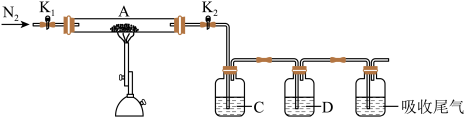
①装置C的溶液为_______ (填标号)。装置D可观察到的实验现象为_______ 。
a.品红 b.NaOH c.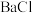 2 d.
2 d. e.浓硫酸
e.浓硫酸
②写出硫酸亚铁高温分解的化学方程式_______ 。
(2)某兴趣小组用如图所示装置模拟测定空气中的二氧化硫的含量。当注入标准状况下VmL空气时,酸性 4溶液恰好褪色,停止实验。
4溶液恰好褪色,停止实验。
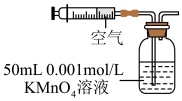
①二氧化硫和酸性 4溶液反应的离子方程式为
4溶液反应的离子方程式为_______ 。
②该空气中二氧化硫的体积分数为_______ (用含Ⅴ的代数式表示)。
(3)某化工厂用如图所示工艺流程除去燃煤产生的 2。
2。

①过程I发生的反应中,氧化剂与还原剂的物质的量之比为_______ 。
②过程Ⅱ发生反应的化学方程式为_______ 。
 2在生活、生产中有重要用途,使用不当会造成环境污染。回答下列问题:
2在生活、生产中有重要用途,使用不当会造成环境污染。回答下列问题:(1)硫酸亚铁加热至高温会分解,生成三种氧化物。为探究硫酸亚铁的分解产物,将无水硫酸亚铁装入反应管A并连接如图所示的装置,打开
 1和
1和 2,缓缓通入
2,缓缓通入 2,加热。实验后反应管A中残留的固体为红色粉末
2,加热。实验后反应管A中残留的固体为红色粉末
①装置C的溶液为
a.品红 b.NaOH c.
 2 d.
2 d. e.浓硫酸
e.浓硫酸②写出硫酸亚铁高温分解的化学方程式
(2)某兴趣小组用如图所示装置模拟测定空气中的二氧化硫的含量。当注入标准状况下VmL空气时,酸性
 4溶液恰好褪色,停止实验。
4溶液恰好褪色,停止实验。
①二氧化硫和酸性
 4溶液反应的离子方程式为
4溶液反应的离子方程式为②该空气中二氧化硫的体积分数为
(3)某化工厂用如图所示工艺流程除去燃煤产生的
 2。
2。
①过程I发生的反应中,氧化剂与还原剂的物质的量之比为
②过程Ⅱ发生反应的化学方程式为
您最近一年使用:0次
10 . 过氧化银(Ag2O2)广泛应用于抗菌消毒和化学能源等领域,NaClO-NaOH溶液与AgNO3溶液反应,能制得纳米级Ag2O2,用该方法制得的Ag2O2会含有少量的Ag2O。可用热重分析法测定Ag2O2的纯度,其步骤如下:取27.12 g样品在N2气氛下加热,测得剩余固体的质量与温度的关系曲线如图所示,下列说法错误的是
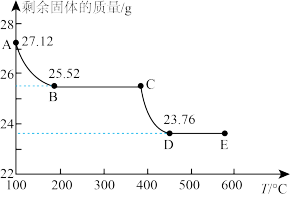

| A.制备Ag2O2反应的离子方程式为2Ag++2OH-+ClO-=Ag2O2↓+Cl-+H2O |
B.CD段发生反应的化学方程式为 |
| C.AB段反应转移的电子的物质的量为0.2 mol |
| D.样品中Ag2O2的质量分数约为91.45% |
您最近一年使用:0次
2022-09-06更新
|
203次组卷
|
3卷引用:2022年福建省高考真题变式题(选择题6-10)



