名校
1 . 2021年,我国科学家首次在实验室实现 到淀粉的全合成,其合成路线如下。设
到淀粉的全合成,其合成路线如下。设 表示阿伏加德罗常数的值,下列有关说法错误的是
表示阿伏加德罗常数的值,下列有关说法错误的是
 到淀粉的全合成,其合成路线如下。设
到淀粉的全合成,其合成路线如下。设 表示阿伏加德罗常数的值,下列有关说法错误的是
表示阿伏加德罗常数的值,下列有关说法错误的是
| A.反应②、③无法在高温下进行 |
B.标准状况下,11.2L 中含有共用电子对数目为 中含有共用电子对数目为 |
C.将1mol 与足量乙酸混合,在一定条件下发生取代反应,可消耗乙酸分子数目为 与足量乙酸混合,在一定条件下发生取代反应,可消耗乙酸分子数目为 |
D.反应②中,3.2g 生成 生成 时转移电子数目为 时转移电子数目为 |
您最近一年使用:0次
2022-04-24更新
|
245次组卷
|
4卷引用:易混易错2 阿伏加德罗常数应用中的易错点
2022·广东汕头·一模
名校
2 . 2021年,我国科学家首次在实验室实现 到淀粉的全合成,其合成路线如下:设
到淀粉的全合成,其合成路线如下:设 为阿伏加德罗常数,下列有关说法不正确的是
为阿伏加德罗常数,下列有关说法不正确的是
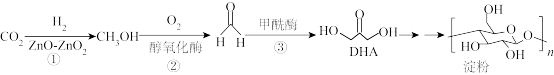
 到淀粉的全合成,其合成路线如下:设
到淀粉的全合成,其合成路线如下:设 为阿伏加德罗常数,下列有关说法不正确的是
为阿伏加德罗常数,下列有关说法不正确的是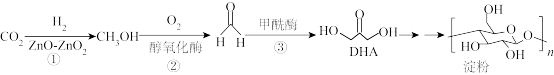
A.标况下,11.2L  中含有共用电子对数目为2 中含有共用电子对数目为2 |
| B.反应②、③无法在高温下进行 |
C.反应②中,3.2g  生成HCHO时转移电子数目为0.2 生成HCHO时转移电子数目为0.2 |
D.1mol DHA与乙酸发生取代反应,可消耗乙酸分子数目为 |
您最近一年使用:0次
2022-03-01更新
|
1422次组卷
|
9卷引用:押广东卷化学第11题 阿伏加德罗常数-备战2022年高考化学临考题号押题(广东卷)
(已下线)押广东卷化学第11题 阿伏加德罗常数-备战2022年高考化学临考题号押题(广东卷)(已下线)第一章 化学计量在实验中的应用(测)-2023年高考化学一轮复习讲练测(全国通用)(已下线)专题09 物质的量-备战2023年高考化学母题题源解密(广东卷)广东省汕头市2022届高三下学期第一次模拟考试化学试题北京市通州区2022届高三查缺补漏化学试题北京市顺义牛栏山第一中学2022届高三下学期保温练习化学试题广西南宁市第二中学2021-2022学年高三下学期5月诊断理科综合化学试题北京市第十七中学2021-2022学年高三下学期5月模拟考试化学试题北京市顺义区第一中学2022届高三下学期三模化学试题
2022·天津和平·一模
名校
3 . 2021年,我国科学家首次在实验室实现CO2到淀粉的全合成,其合成路线如图,设NA为阿伏加德罗常数的值,下列有关说法不正确的是
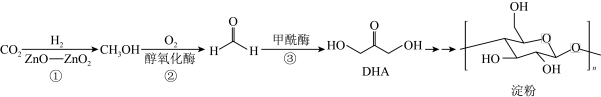

| A.标况下,11.2LCO2中含有共用电子对数目为2NA |
| B.反应②、③无法在高温下进行 |
| C.反应②中,3.2gCH3OH生成HCHO时转移电子数目为0.2NA |
| D.量取1mol DHA与乙酸发生取代反应,消耗乙酸分子数目为2NA |
您最近一年使用:0次
21-22高二下·安徽安庆·期中
名校
4 . 2021 年,我国科学家首次在实验室实现CO2到淀粉的全合成,其合成路线如下,设NA为阿伏加德罗常数,下列有关说法不正确的是
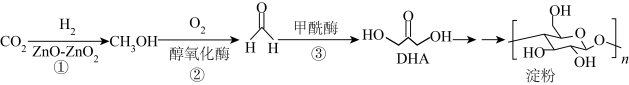

| A.标况下,11.2L CO2中含有共用电子对数目为2 NA |
| B.反应②、③无法在高温下进行 |
| C.反应②中,3.2g CH3OH 生成HCHO时转移电子数目为0.2NA |
| D.DHA与乙酸发生取代反应,可消耗乙酸分子数目为2 NA |
您最近一年使用:0次
2022-04-21更新
|
408次组卷
|
4卷引用:押全国卷理综第13题 反应机理图分析、能垒图分析等创新题型及阿伏加德罗常数-备战2022年高考化学临考题号押题(全国卷)
(已下线)押全国卷理综第13题 反应机理图分析、能垒图分析等创新题型及阿伏加德罗常数-备战2022年高考化学临考题号押题(全国卷)安徽省怀宁中学2021-2022学年高二下学期期中考试化学试题(已下线)化学-2022年高考押题预测卷02(天津卷)天津市耀华中学2022届高三下学期一模化学试题
5 . 二氧化铈( )可用作玻璃工业添加剂和有机反应催化剂。以氟碳铈矿(主要含有
)可用作玻璃工业添加剂和有机反应催化剂。以氟碳铈矿(主要含有 )为原料制备二氧化铈的一种工艺流程如图所示。
)为原料制备二氧化铈的一种工艺流程如图所示。
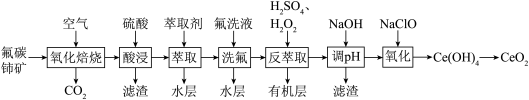
已知:① 能与
能与 结合成
结合成 ,
, 也能与
也能与 结合成
结合成 ;②
;② 能被萃取剂
能被萃取剂 萃取,而
萃取,而 不能。
不能。
回答下列问题:
(1)“氧化焙烧”时,为了增大反应速率,提高原料利用率,可采取的措施有_______ (写出一种)。
(2)“氧化焙烧”后的固体产物中含有 和
和 ,二者物质的量之比为3:1,“酸浸”时发生反应的离子方程式为
,二者物质的量之比为3:1,“酸浸”时发生反应的离子方程式为_______ 。
(3) 是一种有机萃取剂,“萃取”时发生反应:
是一种有机萃取剂,“萃取”时发生反应: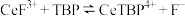 ,氟洗液中添加
,氟洗液中添加 的作用是
的作用是_______ 。
(4)“反萃取”时加入 和
和 的混合液,
的混合液, 的作用为
的作用为_______ 。
(5)“反萃取”后的水层溶液中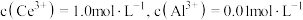 。室温下,“调
。室温下,“调 ”时,先除去
”时,先除去 ,若忽略过程中溶液的体积变化,则需加入
,若忽略过程中溶液的体积变化,则需加入 调节溶液
调节溶液 的范围为
的范围为_______ ,过滤后,再向滤液中加入 使
使 沉淀完全(已知:室温下,当溶液中的离子浓度
沉淀完全(已知:室温下,当溶液中的离子浓度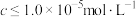 时,可认为该离子沉淀完全。
时,可认为该离子沉淀完全。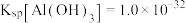 ,
,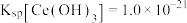 )。
)。
(6)“氧化”时发生反应的化学方程式为_______
(7)用10吨含70%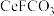 的矿石,按上述工艺生产,制得4.48吨
的矿石,按上述工艺生产,制得4.48吨 ,则
,则 的产率为
的产率为_______ (保留3位有效数字)。
 )可用作玻璃工业添加剂和有机反应催化剂。以氟碳铈矿(主要含有
)可用作玻璃工业添加剂和有机反应催化剂。以氟碳铈矿(主要含有 )为原料制备二氧化铈的一种工艺流程如图所示。
)为原料制备二氧化铈的一种工艺流程如图所示。
已知:①
 能与
能与 结合成
结合成 ,
, 也能与
也能与 结合成
结合成 ;②
;② 能被萃取剂
能被萃取剂 萃取,而
萃取,而 不能。
不能。回答下列问题:
(1)“氧化焙烧”时,为了增大反应速率,提高原料利用率,可采取的措施有
(2)“氧化焙烧”后的固体产物中含有
 和
和 ,二者物质的量之比为3:1,“酸浸”时发生反应的离子方程式为
,二者物质的量之比为3:1,“酸浸”时发生反应的离子方程式为(3)
 是一种有机萃取剂,“萃取”时发生反应:
是一种有机萃取剂,“萃取”时发生反应: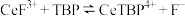 ,氟洗液中添加
,氟洗液中添加 的作用是
的作用是(4)“反萃取”时加入
 和
和 的混合液,
的混合液, 的作用为
的作用为(5)“反萃取”后的水层溶液中
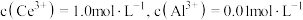 。室温下,“调
。室温下,“调 ”时,先除去
”时,先除去 ,若忽略过程中溶液的体积变化,则需加入
,若忽略过程中溶液的体积变化,则需加入 调节溶液
调节溶液 的范围为
的范围为 使
使 沉淀完全(已知:室温下,当溶液中的离子浓度
沉淀完全(已知:室温下,当溶液中的离子浓度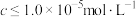 时,可认为该离子沉淀完全。
时,可认为该离子沉淀完全。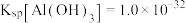 ,
,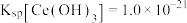 )。
)。(6)“氧化”时发生反应的化学方程式为
(7)用10吨含70%
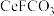 的矿石,按上述工艺生产,制得4.48吨
的矿石,按上述工艺生产,制得4.48吨 ,则
,则 的产率为
的产率为
您最近一年使用:0次
6 . 超导材料为具有零电阻及反磁性物质,以Y2O3、BaCO3和CuO为原料.经研磨烧结可合成一种高温超导物质YBa2Cu3Ox现欲合成0.5mol此高温超导物,依化学计量比例,需取Y2O3 、 BaCO3和CuO的物质的量(单位为mol)以及x的值分别为( )
| A.0.50、0.50、0.50、5.5 | B.1.0、0.25、0.17、3.5 |
| C.0.50、1.0、1.5、4.5 | D.0.25、1.0、1.5、6.5 |
您最近一年使用:0次
2016·上海·高考真题
真题
解题方法
7 . CO2是重要的化工原料,也是应用广发的化工产品。CO2与过氧化钠或超氧化钾反应可产生氧气。
完成下列计算:
(1)CO2通入氨水生成NH4HCO3,NH4HCO3很容易分解。2.00 mol NH4HCO3完全分解,分解产物经干燥后的体积为_______ L(标准状况)。
(2)某H2中含有2.40 molCO2,该混合气体通入2.00 L NaOH溶液中,CO2被完全吸收。如果NaOH完全反应,该NaOH溶液的浓度为_______ 。
(3)CO2和KO2有下列反应:4KO2+2CO2→2K2CO3+3O2,4KO2+4CO2+2H2O→4KHCO3+3O2,若9 mol CO2在密封舱内和KO2反应后生成9 mol O2,则反应前密封舱内H2O的量应该是多少_______ ?列式计算。
(4)甲烷和水蒸气反应的产物是合成甲醇的原料:CH4+H2O CO+3H2,已知:CO+2H2
CO+3H2,已知:CO+2H2 CH3OH,CO2+3H2
CH3OH,CO2+3H2 CH3OH+H2O。300 mol CH4完全反应后的产物中,加入100 mol CO2后合成甲醇。若获得甲醇350 mol,残留氢气120 mol,计算CO2的转化率
CH3OH+H2O。300 mol CH4完全反应后的产物中,加入100 mol CO2后合成甲醇。若获得甲醇350 mol,残留氢气120 mol,计算CO2的转化率_______ 。
完成下列计算:
(1)CO2通入氨水生成NH4HCO3,NH4HCO3很容易分解。2.00 mol NH4HCO3完全分解,分解产物经干燥后的体积为
(2)某H2中含有2.40 molCO2,该混合气体通入2.00 L NaOH溶液中,CO2被完全吸收。如果NaOH完全反应,该NaOH溶液的浓度为
(3)CO2和KO2有下列反应:4KO2+2CO2→2K2CO3+3O2,4KO2+4CO2+2H2O→4KHCO3+3O2,若9 mol CO2在密封舱内和KO2反应后生成9 mol O2,则反应前密封舱内H2O的量应该是多少
(4)甲烷和水蒸气反应的产物是合成甲醇的原料:CH4+H2O
 CO+3H2,已知:CO+2H2
CO+3H2,已知:CO+2H2 CH3OH,CO2+3H2
CH3OH,CO2+3H2 CH3OH+H2O。300 mol CH4完全反应后的产物中,加入100 mol CO2后合成甲醇。若获得甲醇350 mol,残留氢气120 mol,计算CO2的转化率
CH3OH+H2O。300 mol CH4完全反应后的产物中,加入100 mol CO2后合成甲醇。若获得甲醇350 mol,残留氢气120 mol,计算CO2的转化率
您最近一年使用:0次
2016-12-09更新
|
293次组卷
|
6卷引用:2019年高考化学一轮复习讲练测1.2 物质的量浓度 练
(已下线)2019年高考化学一轮复习讲练测1.2 物质的量浓度 练(已下线)2019高考备考一轮复习精品资料 第二章 化学物质及其变化第4讲 守恒思想在化学中的应用——守恒法解题技巧【教学案】(已下线)2019高考备考二轮复习精品资料-专题2 化学常用计量(教学案)2016年全国普通高等学校招生统一考试化学(上海卷精编版)人教版2017届高三单元精练检测一化学试题2016年全国普通高等学校招生统一考试化学(上海卷参考版)



