名校
解题方法
1 . 氧钒(IV)碱式碳酸铵化学式为(NH4)5[(VO)6(CO3)4(OH)9]•10H2O,它是制备热敏材料VO2的原料,已知VO2+在酸性条件下易被氧化,氧钒(IV)碱式碳酸铵的制备流程如图:
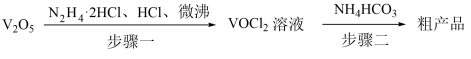
回答下列问题:
(1)步骤一盐酸不宜过量,原因可能_______ ;生成VOCl2的同时,还生成一种无色无污染的气体,该反应的化学方程式为_______ 。
(2)步骤二可在如图装置中进行。

①接口的连接顺序为a→_______ 。
②实验开始时,先关闭K2,打开K1,当_______ 时(写实验现象),再关闭K1,打开K2,充分反应,静置,得到固体。
(3)测定产品纯度
称取mg样品用稀硫酸溶解后,加入50.0mL0.02mol•L-1KMnO4溶液,VO2+转化成VO ,向反应后溶液中滴加0.025mol•L-1Na2SO3标准液,至剩余的KMnO4溶液恰好反应完全,消耗Na2SO3标准液40.00mL。
,向反应后溶液中滴加0.025mol•L-1Na2SO3标准液,至剩余的KMnO4溶液恰好反应完全,消耗Na2SO3标准液40.00mL。
①滴定至反应终点的现象为_______ ;
②样品中氧钒(IV)碱式碳酸铵(摩尔质量为Mg•mol-1)的质量分数为_______ %;
③下列情况会导致产品纯度偏大的是_______ (填标号)。
A.Na2SO3溶液部分变质
B.滴定达终点时,俯视刻度线读数
C.用标准液润洗滴定管后,液体从上口倒出
D.滴定达终点时,发现滴定管尖嘴内有气泡生成
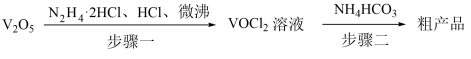
回答下列问题:
(1)步骤一盐酸不宜过量,原因可能
(2)步骤二可在如图装置中进行。

①接口的连接顺序为a→
②实验开始时,先关闭K2,打开K1,当
(3)测定产品纯度
称取mg样品用稀硫酸溶解后,加入50.0mL0.02mol•L-1KMnO4溶液,VO2+转化成VO
 ,向反应后溶液中滴加0.025mol•L-1Na2SO3标准液,至剩余的KMnO4溶液恰好反应完全,消耗Na2SO3标准液40.00mL。
,向反应后溶液中滴加0.025mol•L-1Na2SO3标准液,至剩余的KMnO4溶液恰好反应完全,消耗Na2SO3标准液40.00mL。①滴定至反应终点的现象为
②样品中氧钒(IV)碱式碳酸铵(摩尔质量为Mg•mol-1)的质量分数为
③下列情况会导致产品纯度偏大的是
A.Na2SO3溶液部分变质
B.滴定达终点时,俯视刻度线读数
C.用标准液润洗滴定管后,液体从上口倒出
D.滴定达终点时,发现滴定管尖嘴内有气泡生成
您最近一年使用:0次
2023-06-18更新
|
375次组卷
|
3卷引用:T15-实验探究题
2 . 铅在氧化物中的价态有+2价和+4价,含+4价铅的氧化物是一种很强的氧化剂,常温时在酸性条件下可将 氧化成
氧化成 ,自身还原为+2价。
,自身还原为+2价。 在加热过程发生分解的失重曲线如下图所示。
在加热过程发生分解的失重曲线如下图所示。

已知: 。
。
请计算:
(1)若用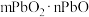 表示A点的化学组成,则
表示A点的化学组成,则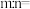
_______ 。
(2)取71.7g ,加热一段时间后冷却,在剩余的固体中加足量浓盐酸充分反应,生成7.1g
,加热一段时间后冷却,在剩余的固体中加足量浓盐酸充分反应,生成7.1g 。求剩余固体中氧元素的质量
。求剩余固体中氧元素的质量_______ 。(写出计算过程)
 氧化成
氧化成 ,自身还原为+2价。
,自身还原为+2价。 在加热过程发生分解的失重曲线如下图所示。
在加热过程发生分解的失重曲线如下图所示。
已知:
 。
。请计算:
(1)若用
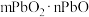 表示A点的化学组成,则
表示A点的化学组成,则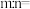
(2)取71.7g
 ,加热一段时间后冷却,在剩余的固体中加足量浓盐酸充分反应,生成7.1g
,加热一段时间后冷却,在剩余的固体中加足量浓盐酸充分反应,生成7.1g 。求剩余固体中氧元素的质量
。求剩余固体中氧元素的质量
您最近一年使用:0次
2021高三·全国·专题练习
3 . 国际计量大会第26次会议新修订阿伏加德罗常数(NA=6.02214076×1023mol-1)并于2019年5月20日正式生效。下列说法正确的是
| A.常温常压下,46g14CO2中含有的氧原子数为2NA |
| B.标准状况下,11.2L丙烯和环丙烷的混合气体中含有C-H键的数目为4NA |
C.1mol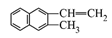 中共平面的碳原子数最多为12NA 中共平面的碳原子数最多为12NA |
| D.0.1mol∙L-1(NH4)2Fe(SO4)2溶液与足量酸性K2Cr2O7溶液反应,转移电子的数目为0.1NA |
您最近一年使用:0次
4 . NA代表阿伏伽德罗常数的值。下列有关叙述正确的是
| A.常温常压下,1.8g甲基(—CD3)中含有的中子数为NA |
| B.2.3g钠被O2完全氧化时,钠得到的电子数目为0.1NA |
| C.9.2 g甲苯被酸性KMnO4氧化生成苯甲酸时,反应中转移电子数为0.6NA |
| D.常温下,1L pH=9的CH3COONa溶液中,发生电离的水分子数为1×10−9NA |
您最近一年使用:0次
2018-06-06更新
|
658次组卷
|
3卷引用:2020届人教版高三化学二轮复习选择题专攻练——阿伏加德罗常数
名校
5 . 实验室测定氧化物X(FexO)的组成实验如下:
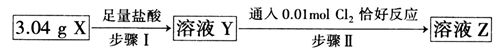
下列有关说法正确的是

下列有关说法正确的是
| A.样品X中氧元素的质量分数约为26.3% |
| B.溶液Y中c(Fe2+):c(Fe3+)=2:1 |
| C.用酸性高锰酸钾溶液检验溶液Z中是否含有Fe2+ |
| D.根据步骤I、Ⅱ可以判断X的组成为Fe0.75O |
您最近一年使用:0次
2017-11-24更新
|
326次组卷
|
3卷引用:黄金30题系列 高三化学 小题好拿分【提升版】



