2019高三·全国·专题练习
1 . Ⅰ.卫生部严令禁止在面粉生产中添加过氧化钙(CaO2)等食品添加剂。过氧化钙(CaO2)是一种安全无毒物质,带有结晶水,通常还含有CaO。
(1)称取5.42 g过氧化钙样品,灼热时发生如下反应:2[CaO2·xH2O]→2CaO+O2↑+2xH2O,得到O2在标准状况下的体积为672 mL,该样品中CaO2的物质的量为________ 。
(2)另取同一样品5.42 g,溶于适量稀盐酸中,然后加入足量的Na2CO3溶液,将溶液中Ca2+全部转化为CaCO3沉淀,得到干燥的CaCO3 7.0 g。
①样品中CaO的质量为_________________ 。
②样品中CaO2·xH2O的x值为__________ 。
Ⅱ.臭氧层是地球生命的保护神,臭氧比氧气具有更强的氧化性。实验室可将氧气通过高压放电来制取臭氧:3O2=2O3。
(1)若在上述反应中有30%的氧气转化为臭氧,所得混合气的平均摩尔质量为_____ g·mol-1(保留一位小数)。
(2)将8 L氧气通过放电管后,恢复到原状况,得到气体6.5 L,其中臭氧为________ L。
(3)实验室将氧气和臭氧的混合气体0.896 L(标准状况)通入盛有20.0 g铜粉的反应容器中,充分加热后,粉末的质量变为21.6 g。则原混合气中臭氧的体积分数为_____________ 。
(1)称取5.42 g过氧化钙样品,灼热时发生如下反应:2[CaO2·xH2O]→2CaO+O2↑+2xH2O,得到O2在标准状况下的体积为672 mL,该样品中CaO2的物质的量为
(2)另取同一样品5.42 g,溶于适量稀盐酸中,然后加入足量的Na2CO3溶液,将溶液中Ca2+全部转化为CaCO3沉淀,得到干燥的CaCO3 7.0 g。
①样品中CaO的质量为
②样品中CaO2·xH2O的x值为
Ⅱ.臭氧层是地球生命的保护神,臭氧比氧气具有更强的氧化性。实验室可将氧气通过高压放电来制取臭氧:3O2=2O3。
(1)若在上述反应中有30%的氧气转化为臭氧,所得混合气的平均摩尔质量为
(2)将8 L氧气通过放电管后,恢复到原状况,得到气体6.5 L,其中臭氧为
(3)实验室将氧气和臭氧的混合气体0.896 L(标准状况)通入盛有20.0 g铜粉的反应容器中,充分加热后,粉末的质量变为21.6 g。则原混合气中臭氧的体积分数为
您最近一年使用:0次
真题
名校
2 . 臭氧层是地球生命的保护神,臭氧比氧气具有更强的氧化性。实验室可将氧气通过高压放电管来制取臭氧: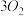


(1)若在上述反应中有30%的氧气转化为臭氧,所得混合气的平均摩尔质量为______ g/mol(保留一位小数)。
(2)将8L氧气通过放电管后,恢复到原状况,得到气体6.5L,其中臭氧为_____________ L。
(3)实验室将氧气和臭氧的混合气体0.896L(标准状况)通入盛有20.0g铜粉的反应器中,充分加热后,粉末的质量变为21.6g。则原混合气中臭氧的体积分数为__________________ 。
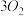


(1)若在上述反应中有30%的氧气转化为臭氧,所得混合气的平均摩尔质量为
(2)将8L氧气通过放电管后,恢复到原状况,得到气体6.5L,其中臭氧为
(3)实验室将氧气和臭氧的混合气体0.896L(标准状况)通入盛有20.0g铜粉的反应器中,充分加热后,粉末的质量变为21.6g。则原混合气中臭氧的体积分数为
您最近一年使用:0次
2019-01-30更新
|
1437次组卷
|
16卷引用:2014年高考化学一轮复习课后规范训练1-2练习卷
(已下线)2014年高考化学一轮复习课后规范训练1-2练习卷2018版化学(苏教版)高考总复习专题一课时跟踪训练:物质的量 气体摩尔体积(已下线)2019高考备考一轮复习精品资料 第一章 从实验学化学 第1讲 物质的量、气体摩尔体积【押题专练】(已下线)【备战2019年浙江新高考-考点】——考点02 物质的量(已下线)2019高考热点题型和提分秘籍 第一章 物质的量 第1讲 物质的量 气体摩尔体积( 题型专练)2009年普通高等学校招生统一考试化学试题(上海卷)2009高考真题汇编—氧族元素,环境保护2009高考真题汇编-化学计算(已下线)2011-2012学年武汉二中高一上学期期中考试化学试卷(已下线)2011-2012学年甘肃省天水一中高二第二学段测试化学试卷(已下线)2013-2014学年湖北省武汉二中高一上学期期中考试化学试卷(已下线)2013-2014学年河南省内黄一中高一上学期第一次月考化学试卷2015-2016学年天津市蓟县高一上学期期中化学试卷吉林省白城市第一中学2018-2019学年高二6月月考化学试题内蒙古赤峰二中人教版高中化学必修1练习:化学计量及其应用(3)(已下线)上海虹口区2011届高三一模化学试题
真题
3 . 铜是人类发现最早并广泛使用的一种金属。回答下列问题:
(1)实验室使用稀硫酸和H2O2溶解铜片,该反应的化学方程式为__________________ 。
(2)电子工业使用FeCl3溶液刻蚀印刷电路板铜箔,写出该过程的离子方程式____________ 。配制的FeCl3溶液应保持_______ (填“酸性”“碱性”或“中性”),原因是_____________ 。
(3)溶液中Cu2+的浓度可采用碘量法测得:
①2Cu2++5I-=2CuI↓+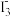 ②I3- +2
②I3- +2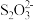 =3I-+2
=3I-+2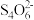
反应①中的氧化剂为_____________ 。现取20.00 mL含Cu2+的溶液,加入足量KI充分反应后,用0.1000 mol·L¯1 Na2S2O3标准溶液滴定至终点,消耗Na2S2O3溶液25.00 mL,此溶液中Cu2+的浓度为_______ mol·L¯1。
(1)实验室使用稀硫酸和H2O2溶解铜片,该反应的化学方程式为
(2)电子工业使用FeCl3溶液刻蚀印刷电路板铜箔,写出该过程的离子方程式
(3)溶液中Cu2+的浓度可采用碘量法测得:
①2Cu2++5I-=2CuI↓+
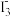 ②I3- +2
②I3- +2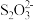 =3I-+2
=3I-+2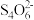
反应①中的氧化剂为
您最近一年使用:0次
2018-11-28更新
|
3133次组卷
|
5卷引用:第10讲 金属材料及金属矿物的开发利用(精练)-2022年高考化学一轮复习讲练测
(已下线)第10讲 金属材料及金属矿物的开发利用(精练)-2022年高考化学一轮复习讲练测(已下线)第5讲 金属材料与金属的冶炼2018年普通高等学校招生全国统一考试化学(海南卷)吉林松原市油田第十一中学2021届高三第二次阶段考试化学试题福建省泉州科技中学2021-2022学年高三上学期第一次月考化学试题
4 . 向100mL FeI2溶液中逐渐通入Cl2,其中n(I2)、n(Fe3+)随通入n(Cl2)的变化如图所示,下列说法不正确的是
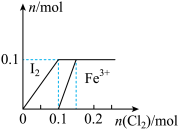

| A.氧化性强弱:I2<Fe3+ |
| B.n(Cl2)=0.12mol时,溶液中的离子主要有Fe2+、Fe3+、Clˉ |
| C.由图可知,该FeI2溶液的浓度为1mol· L-l |
| D.n(Cl2):n(FeI2)=1:2时,反应的离子方程式为:2Fe2++Cl2=2Fe3++2Cl- |
您最近一年使用:0次
2018-03-04更新
|
823次组卷
|
11卷引用:专题07 氧化还原反应分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)
(已下线)专题07 氧化还原反应分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)浙江省金华十校2017~2018学年第一学期期末调研考试高一化学试题浙江省慈溪中学2018-2019学年高一下学期期中复习模拟化学试题云南省迪庆州维西县第二中学2019-2020学年高一上学期期末考试化学试题云南省红河县第一中学2019-2020学年高一上学期期末考试化学试题(已下线)【新东方】2020-46河北省石家庄市第二中学2018-2019学年高一上学期期末考试化学试题云南省玉溪市民族中学2021-2022学年高一上学期期末考试化学试题浙江省宁波市镇海中学2023-2024学年高一上学期化学期末复习提分卷 浙江省湖州市第二中学2023-2024学年高一上学期12月月考化学试题 2023新东方高一上期末考化学05
5 . 为测定某补血剂样品[主要成分是硫酸亚铁晶体(FeSO4·7HO,M=278gmol-1)]中铁元素的含量,某化学兴趣小组设计了如下实验方案。取10片补血剂,加入一定量稀硫酸溶解后,配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.00500mol·L-1酸性KMnO4溶液滴定,重复实验平均消耗酸性KMnO4溶液10.00mL。已知滴定过程反应的离子方程式为:MnO +5Fe2++8H+=Mn2++5Fe3++4H2O
+5Fe2++8H+=Mn2++5Fe3++4H2O
(1)若实验无损耗,则每片补血剂含FeSO4·7H2O含量为____ mg(列式计算)。
(2)正常人每天应补充14mg左右的铁,如果全部通过服用含FeSO4·7H2O的片剂来补充铁,则正常人每天最少需服用含FeSO4·7H2O的片剂____ 片。
 +5Fe2++8H+=Mn2++5Fe3++4H2O
+5Fe2++8H+=Mn2++5Fe3++4H2O(1)若实验无损耗,则每片补血剂含FeSO4·7H2O含量为
(2)正常人每天应补充14mg左右的铁,如果全部通过服用含FeSO4·7H2O的片剂来补充铁,则正常人每天最少需服用含FeSO4·7H2O的片剂
您最近一年使用:0次
2020-11-30更新
|
445次组卷
|
6卷引用:解密02 物质的量(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练
(已下线)解密02 物质的量(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密02 物质的量(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密02 物质的量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)解密02 物质的量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)浙江省十校联盟2021届高三10月联考化学试题浙江省瑞安中学十校联盟2020-2021学年高三10月联考化学试题
2014高三·全国·专题练习
解题方法
6 . 铜单质及其化合物是应用极其广泛的物质。
(1)铜是氢后金属,不能与盐酸发生置换反应,但将单质铜置于浓氢碘酸中,会有可燃性气体及白色沉淀生成,又知氧化性:Cu2+>I2,则铜与氢碘酸反应的化学方程式为__________________________________
(2)已知Cu2O能溶于醋酸溶液或盐酸中,同时得到蓝色溶液和红色固体,则Cu2O与稀硫酸反应的离子方程式为____________________________________ ;
Cu2O与稀硝酸反应的离子方程式为_____________________________ ;
只用稀硫酸来确定某红色固体是 Cu2O与Cu组成的混合物的方法:称取m g该红色固体置于足量稀硫酸中,充分反应后过滤,然后___________________ 。
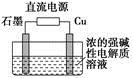
(3)Cu2O是一种半导体材料,基于绿色化学理念设计的制取Cu2O的电解装置如图所示,电解总反应:2Cu+H2O Cu2O+H2↑,则石墨应与电源的
Cu2O+H2↑,则石墨应与电源的________ 极相连,铜电极上的电极反应式为________ ;电解过程中,阴极区周围溶液pH________ (填“变大”、“变小”或“不变”)。
(4)现向Cu、Cu2O、CuO组成的混合物中加入1 L 0.6 mol/L HNO3恰好使混合物溶解,同时收集到2 240 mL NO(标准状况)。若将上述混合物用足量的氢气还原,所得固体的质量为________ ;若混合物中含有0.1 mol Cu,将该混合物与稀硫酸充分反应,至少消耗硫酸的物质的量为________ 。
(1)铜是氢后金属,不能与盐酸发生置换反应,但将单质铜置于浓氢碘酸中,会有可燃性气体及白色沉淀生成,又知氧化性:Cu2+>I2,则铜与氢碘酸反应的化学方程式为
(2)已知Cu2O能溶于醋酸溶液或盐酸中,同时得到蓝色溶液和红色固体,则Cu2O与稀硫酸反应的离子方程式为
Cu2O与稀硝酸反应的离子方程式为
只用稀硫酸来确定某红色固体是 Cu2O与Cu组成的混合物的方法:称取m g该红色固体置于足量稀硫酸中,充分反应后过滤,然后

(3)Cu2O是一种半导体材料,基于绿色化学理念设计的制取Cu2O的电解装置如图所示,电解总反应:2Cu+H2O
 Cu2O+H2↑,则石墨应与电源的
Cu2O+H2↑,则石墨应与电源的(4)现向Cu、Cu2O、CuO组成的混合物中加入1 L 0.6 mol/L HNO3恰好使混合物溶解,同时收集到2 240 mL NO(标准状况)。若将上述混合物用足量的氢气还原,所得固体的质量为
您最近一年使用:0次
7 . 影响化学反应速率的因素很多,某课外兴趣小组用实验的方法进行探究。
实验一:取等物质的量浓度等体积H2O2溶液分别进行下列实验,实验报告如下表所示。
(1)实验1、2的目的是研究__________ 因素对H2O2分解速率的影响。
(2)实验1对应的化学方程式为___________________________ 。
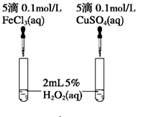
实验二:经研究知Cu2+对H2O2分解也具有催化作用,为比较Fe3+和Cu2+对H2O2分解的催化效果,该小组的同学分别设计了如图所示的实验。可通过观察_________ 得出结论。 有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是____________________ 。
实验三:已知在高锰酸钾(KMnO4)酸性溶液和草酸(H2C2O4)溶液反应时,发现开始一段时间,反应速率较慢,溶液褪色不明显,但不久突然褪色,反应速率明显加快。
(1)写出硫酸酸化的高锰酸钾溶液和草酸溶液反应的化学方程式____________
(2)针对上述实验现象,某同学认为KMnO4与H2C2O4反应是放热反应,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你的猜想还可能是______ 。
(3)若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液试剂外,还需要选择的试剂最合理的是__________ 。
A、硫酸钾 B、硫酸锰 C、水 D、氯化锰
(4)若实验过程中将2.0mL0.10mol/LH2C2O4溶液与4.0mL0.010mol/L酸性KMnO4溶液混合(忽略溶液混合后体积的变化),测得溶液的褪色时间为40s,这段时间内平均反应速率v(KMnO4)=__________ mol·L-1·min-1。
实验一:取等物质的量浓度等体积H2O2溶液分别进行下列实验,实验报告如下表所示。

序号 | 条件 | 现象 | 结论 | |
| 温度/℃ | 催化剂 | |||
| 1 | 40 | FeCl3溶液 | ||
| 2 | 20 | FeCl3溶液 | ||
| 3 | 20 | MnO2 | ||
| 4 | 20 | 无 | ||
(1)实验1、2的目的是研究
(2)实验1对应的化学方程式为
实验二:经研究知Cu2+对H2O2分解也具有催化作用,为比较Fe3+和Cu2+对H2O2分解的催化效果,该小组的同学分别设计了如图所示的实验。可通过观察
实验三:已知在高锰酸钾(KMnO4)酸性溶液和草酸(H2C2O4)溶液反应时,发现开始一段时间,反应速率较慢,溶液褪色不明显,但不久突然褪色,反应速率明显加快。
(1)写出硫酸酸化的高锰酸钾溶液和草酸溶液反应的化学方程式
(2)针对上述实验现象,某同学认为KMnO4与H2C2O4反应是放热反应,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你的猜想还可能是
(3)若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液试剂外,还需要选择的试剂最合理的是
A、硫酸钾 B、硫酸锰 C、水 D、氯化锰
(4)若实验过程中将2.0mL0.10mol/LH2C2O4溶液与4.0mL0.010mol/L酸性KMnO4溶液混合(忽略溶液混合后体积的变化),测得溶液的褪色时间为40s,这段时间内平均反应速率v(KMnO4)=
您最近一年使用:0次
9-10高一·全国·单元测试
8 . 标准状况下有22.4L氯气和氢气的混合气体,在一密闭容器中使其充分反应,冷却后将此气体与1L1mol·L-1的NaOH溶液充分反应,最后此溶液( )
| A.一定显酸性 |
| B.一定显碱性 |
| C.可能显酸性,可能显碱性,也可能显中性 |
| D.以上都不正确 |
您最近一年使用:0次
名校
解题方法
9 . 氧钒(IV)碱式碳酸铵化学式为(NH4)5[(VO)6(CO3)4(OH)9]•10H2O,它是制备热敏材料VO2的原料,已知VO2+在酸性条件下易被氧化,氧钒(IV)碱式碳酸铵的制备流程如图:
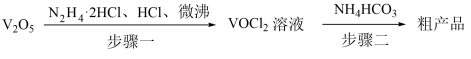
回答下列问题:
(1)步骤一盐酸不宜过量,原因可能_______ ;生成VOCl2的同时,还生成一种无色无污染的气体,该反应的化学方程式为_______ 。
(2)步骤二可在如图装置中进行。

①接口的连接顺序为a→_______ 。
②实验开始时,先关闭K2,打开K1,当_______ 时(写实验现象),再关闭K1,打开K2,充分反应,静置,得到固体。
(3)测定产品纯度
称取mg样品用稀硫酸溶解后,加入50.0mL0.02mol•L-1KMnO4溶液,VO2+转化成VO ,向反应后溶液中滴加0.025mol•L-1Na2SO3标准液,至剩余的KMnO4溶液恰好反应完全,消耗Na2SO3标准液40.00mL。
,向反应后溶液中滴加0.025mol•L-1Na2SO3标准液,至剩余的KMnO4溶液恰好反应完全,消耗Na2SO3标准液40.00mL。
①滴定至反应终点的现象为_______ ;
②样品中氧钒(IV)碱式碳酸铵(摩尔质量为Mg•mol-1)的质量分数为_______ %;
③下列情况会导致产品纯度偏大的是_______ (填标号)。
A.Na2SO3溶液部分变质
B.滴定达终点时,俯视刻度线读数
C.用标准液润洗滴定管后,液体从上口倒出
D.滴定达终点时,发现滴定管尖嘴内有气泡生成
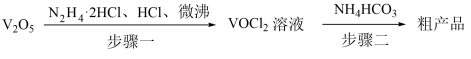
回答下列问题:
(1)步骤一盐酸不宜过量,原因可能
(2)步骤二可在如图装置中进行。

①接口的连接顺序为a→
②实验开始时,先关闭K2,打开K1,当
(3)测定产品纯度
称取mg样品用稀硫酸溶解后,加入50.0mL0.02mol•L-1KMnO4溶液,VO2+转化成VO
 ,向反应后溶液中滴加0.025mol•L-1Na2SO3标准液,至剩余的KMnO4溶液恰好反应完全,消耗Na2SO3标准液40.00mL。
,向反应后溶液中滴加0.025mol•L-1Na2SO3标准液,至剩余的KMnO4溶液恰好反应完全,消耗Na2SO3标准液40.00mL。①滴定至反应终点的现象为
②样品中氧钒(IV)碱式碳酸铵(摩尔质量为Mg•mol-1)的质量分数为
③下列情况会导致产品纯度偏大的是
A.Na2SO3溶液部分变质
B.滴定达终点时,俯视刻度线读数
C.用标准液润洗滴定管后,液体从上口倒出
D.滴定达终点时,发现滴定管尖嘴内有气泡生成
您最近一年使用:0次
2023-06-18更新
|
375次组卷
|
3卷引用:T15-实验探究题
2023高三·全国·专题练习
10 . 工业上利用硫酸亚铁与草酸反应制备草酸亚铁晶体,其离子方程式为Fe2++H2C2O4+xH2O=FeC2O4·xH2O↓+2H+,测定草酸亚铁晶体(FeC2O4·xH2O)的x值,实验如下:称取0.540 0 g草酸亚铁晶体溶于一定浓度的硫酸中,用酸性KMnO4溶液滴定。到达滴定终点时,消耗0.100 0 mol·L-1的酸性KMnO4溶液18.00 mL。已知:滴定过程中铁、碳元素被氧化为Fe3+、CO2,锰元素被还原为Mn2+,则FeC2O4·xH2O中x=________ (FeC2O4的摩尔质量是144 g·mol-1)
您最近一年使用:0次



