名校
1 .  为阿伏加德罗常数,下列说法正确的是
为阿伏加德罗常数,下列说法正确的是
 为阿伏加德罗常数,下列说法正确的是
为阿伏加德罗常数,下列说法正确的是A.pH=4的醋酸溶液中,含有的 数目为 数目为 |
B.60g二氧化硅晶体中含有Si-O键数为 |
C.给铁片上电镀铜,阴极增重32g时,外电路转移电子数为 |
D.2mL0.5mol/L硅酸钠溶液中滴入盐酸制硅酸胶体,所得胶粒数目为 |
您最近一年使用:0次
解题方法
2 . 如图是某学校实验室从化学试剂商店买回来的氢氧化钠试剂标签上的部分内容。某同学从该试剂瓶中取出24.0 g固体,配成1 L溶液,请计算:
(1)所得氢氧化钠溶液的物质的量浓度为___________ 。
(2)从所得氢氧化钠溶液中取出200 mL于一烧杯中,投入2.7 g的金属铝,产生的气体在标准状况下的体积为___________ 。(写出解答步骤)
| 氢氧化钠 化学纯(CP) 500 g 品名:氢氧化钠 化学式:NaOH 相对分子质量:40 |
(2)从所得氢氧化钠溶液中取出200 mL于一烧杯中,投入2.7 g的金属铝,产生的气体在标准状况下的体积为
您最近一年使用:0次
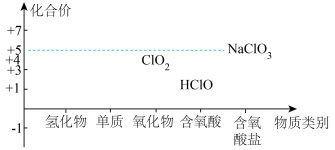
3 . 氯及其化合物的价类二维图如图,回答下列问题: 。写出反应①离子方程式
。写出反应①离子方程式___________ ;反应②中HCl体现的性质是___________ 。
(2)溶质质量分数为36.5%、密度为1.2g/cm3的浓盐酸中,盐酸的物质的量浓度为___________ mol/L,取用任意体积的该盐酸时,下列物理量中不随所取体积的多少而变化的是___________ 。
A.溶液中HCl的物质的量 B.溶液的浓度 C.溶液中Cl-的数目 D.溶液的密度
(3)若用(2)中浓盐酸配制500 mL0.3mol/L稀盐酸。该学生需要用量筒量取___________ mL上述浓盐酸进行配制。完成此实验需用到的玻璃仪器除了量筒、烧杯、玻璃棒、胶头滴管外,还需要___________ 。
(4)现将200 mL0.3 mol/L盐酸与300 mL0.4 mol/LCuCl2溶液混合,溶液体积变化忽略不计,所得溶液中Cl-的物质的量浓度是___________ mol/L。
 。写出反应①离子方程式
。写出反应①离子方程式(2)溶质质量分数为36.5%、密度为1.2g/cm3的浓盐酸中,盐酸的物质的量浓度为
A.溶液中HCl的物质的量 B.溶液的浓度 C.溶液中Cl-的数目 D.溶液的密度
(3)若用(2)中浓盐酸配制500 mL0.3mol/L稀盐酸。该学生需要用量筒量取
(4)现将200 mL0.3 mol/L盐酸与300 mL0.4 mol/LCuCl2溶液混合,溶液体积变化忽略不计,所得溶液中Cl-的物质的量浓度是
您最近一年使用:0次
4 . 根据所学知识,回答下列问题:
(1)常温常压下,HCl气体溶于水形成的盐酸溶液,其溶质质量分数为
 ,密度为
,密度为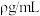 ,该溶液浓度为
,该溶液浓度为 。
。(2)“可燃冰”是由水和甲烷在一定条件下形成的类冰结晶化合物.
 “可燃冰”(
“可燃冰”( )的物质的量与
)的物质的量与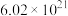 个水分子的物质的量相等,则该“可燃冰”的摩尔质量为
个水分子的物质的量相等,则该“可燃冰”的摩尔质量为(3)过氧化钠可用作呼吸面罩供氧剂,其原理可用方程式
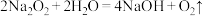 ,
,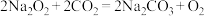 表示。若生成标况下
表示。若生成标况下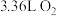 ,转移电子的数目为
,转移电子的数目为(4)现有
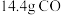 和
和 的混合气体,在标准状况下所占的体积约为
的混合气体,在标准状况下所占的体积约为 。将混合气体依次通过如图装置,最后收集在气球中,气球中收集到的气体在标况下的体积为
。将混合气体依次通过如图装置,最后收集在气球中,气球中收集到的气体在标况下的体积为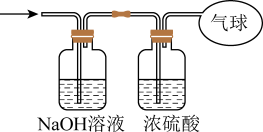
您最近一年使用:0次
5 . 物质的量是高中化学常用的物理量,请完成以下有关计算(设阿伏加德罗常数的值为NA):
(1)在标准状况下,0.5molO2的体积为_______ L。
(2)将0.2moLMgCl2固体溶于水配成400mL溶液,MgCl2溶液的物质的量浓度为_______ 。
(3)0.2molCH4含有_______ NA个氢原子。
(4)49g 的物质的量是
的物质的量是_______ mol。
(5)标准状况下,2gH2的体积是_______ L。
(6)等物质的量的 和
和 的质量之比为
的质量之比为_______ 。
(7)标准状况下6.72L某气体质量13.2g,该物质的摩尔质量为_______ 。
(1)在标准状况下,0.5molO2的体积为
(2)将0.2moLMgCl2固体溶于水配成400mL溶液,MgCl2溶液的物质的量浓度为
(3)0.2molCH4含有
(4)49g
 的物质的量是
的物质的量是(5)标准状况下,2gH2的体积是
(6)等物质的量的
 和
和 的质量之比为
的质量之比为(7)标准状况下6.72L某气体质量13.2g,该物质的摩尔质量为
您最近一年使用:0次
名校
6 . 下列溶液中 的浓度最小的是
的浓度最小的是
 的浓度最小的是
的浓度最小的是A. 的 的 溶液 溶液 | B.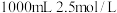 的 的 溶液 溶液 |
C.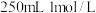 的 的 溶液 溶液 | D.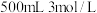 的 的 溶液 溶液 |
您最近一年使用:0次
名校
7 . 某食品经检测含 浓度为
浓度为 ,则
,则 的物质的量浓度为
的物质的量浓度为
 浓度为
浓度为 ,则
,则 的物质的量浓度为
的物质的量浓度为A.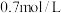 | B.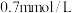 | C. | D.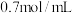 |
您最近一年使用:0次
名校
8 . 下列关于物质的量浓度表述正确的是
A.将7.8g  溶于水,配成100g溶液,所得溶液质量分数为7.8% 溶于水,配成100g溶液,所得溶液质量分数为7.8% |
B.质量分数为3.65%的200g盐酸溶液中,含 分子的数目为 分子的数目为 |
C.将25g胆矾( )溶于75克水中,可得到质量分数为16% )溶于75克水中,可得到质量分数为16% 的溶液 的溶液 |
D.将7.1g  通入水中,完全溶于水得到100g溶液,理论上可获得3.65%的盐酸溶液 通入水中,完全溶于水得到100g溶液,理论上可获得3.65%的盐酸溶液 |
您最近一年使用:0次
9 . 完成下列计算
(1)标况下,将4.48 L的氯化氢气体溶于水中配制成2 L溶液,所得溶液浓度为______ 。
(2)2 L硫酸铝溶液中含2.7 g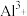 ,则该溶液中
,则该溶液中 的物质的量浓度是
的物质的量浓度是______ 。
(3)将10 mL 1.0 mol/L 溶液加水稀释至100 mL,所得的溶液中Na+物质的量浓度为
溶液加水稀释至100 mL,所得的溶液中Na+物质的量浓度为______ 。
(4)100 mL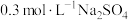 溶液和50 mL
溶液和50 mL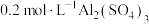 溶液混合后,溶液中
溶液混合后,溶液中 的物质的量浓度为
的物质的量浓度为______ 。
(5)某同学配制的植物营养液中有4种离子,其中所含的 、
、 、
、 的物质的量浓度分别为
的物质的量浓度分别为 、
、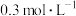 、
、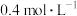 ,则
,则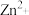 的物质的量浓度是
的物质的量浓度是______ 。
(1)标况下,将4.48 L的氯化氢气体溶于水中配制成2 L溶液,所得溶液浓度为
(2)2 L硫酸铝溶液中含2.7 g
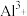 ,则该溶液中
,则该溶液中 的物质的量浓度是
的物质的量浓度是(3)将10 mL 1.0 mol/L
 溶液加水稀释至100 mL,所得的溶液中Na+物质的量浓度为
溶液加水稀释至100 mL,所得的溶液中Na+物质的量浓度为(4)100 mL
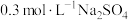 溶液和50 mL
溶液和50 mL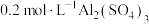 溶液混合后,溶液中
溶液混合后,溶液中 的物质的量浓度为
的物质的量浓度为(5)某同学配制的植物营养液中有4种离子,其中所含的
 、
、 、
、 的物质的量浓度分别为
的物质的量浓度分别为 、
、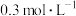 、
、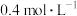 ,则
,则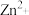 的物质的量浓度是
的物质的量浓度是
您最近一年使用:0次
名校
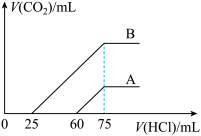
10 . 取A、B两份物质的量浓度相等的NaOH溶液,体积均为50mL,分别向其中通入一定量的 后,再分别稀释到100mL,在稀释后的溶液中分别滴加0.1mol/L的盐酸,产生的
后,再分别稀释到100mL,在稀释后的溶液中分别滴加0.1mol/L的盐酸,产生的 体积(标准状况)与所加盐酸的体积关系如图,下列说法正确的是
体积(标准状况)与所加盐酸的体积关系如图,下列说法正确的是
 后,再分别稀释到100mL,在稀释后的溶液中分别滴加0.1mol/L的盐酸,产生的
后,再分别稀释到100mL,在稀释后的溶液中分别滴加0.1mol/L的盐酸,产生的 体积(标准状况)与所加盐酸的体积关系如图,下列说法正确的是
体积(标准状况)与所加盐酸的体积关系如图,下列说法正确的是
A.原NaOH溶液的物质的量浓度 |
B.A曲线表明原溶液通入 后,所得溶质为 后,所得溶质为 和 和 且物质的量之比为1∶3 且物质的量之比为1∶3 |
C.B曲线表明原溶液通入 后,所得溶质为 后,所得溶质为 和 和 且物质的量之比为1∶l 且物质的量之比为1∶l |
D.B曲线表明原溶液通入 后,所得溶质与盐酸反应产生气体的最大体积为33.6mL标准状况) 后,所得溶质与盐酸反应产生气体的最大体积为33.6mL标准状况) |
您最近一年使用:0次



