1 . 物质的量是学习中重要的物理量,下列说法正确的是
A.1个 分子的质量是 分子的质量是 |
B. 的质量大于 的质量大于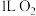 的质量 的质量 |
C.若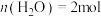 , , 中含有的电子的物质的量是 中含有的电子的物质的量是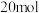 |
D.标准状况下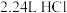 溶于 溶于 水中,溶液的物质的量浓度是 水中,溶液的物质的量浓度是 |
您最近一年使用:0次
名校
2 . NA表示阿伏加德罗常数的值。下列说法错误的是
| A.标况下,3.36L氮气所含共用电子对的数目为0.45NA |
B.0.2mol 与水恰好完全反应转移0.4mol电子 与水恰好完全反应转移0.4mol电子 |
C.1.8g的NH 中含有的电子数为1NA 中含有的电子数为1NA |
D.1 L 0.1 mol/L的 溶液中, 溶液中, 的物质的量为 的物质的量为 |
您最近一年使用:0次
3 . 实验室通常利用质量分数36.5%盐酸(密度为1.14g/mL)与二氧化锰通过反应制取Cl2。通过计算回答下列问题:
(1)质量分数36.5%(密度为1.14g/mL)盐酸的物质的量浓度为_______ 。
(2)若要制取2.24L Cl2(标准状况),理论上需要消耗MnO2质量为_______ 克。
(3)此时,被氧化HCl的物质的量为_______ 。
(1)质量分数36.5%(密度为1.14g/mL)盐酸的物质的量浓度为
(2)若要制取2.24L Cl2(标准状况),理论上需要消耗MnO2质量为
(3)此时,被氧化HCl的物质的量为
您最近一年使用:0次
4 . 抗击新冠病毒期间,各地大规模进行环境消毒,其中“84”消毒液试用比较广泛。如图是某“84”消毒液的标签,该“84”消毒液的物质的量浓度为_____  ?某同学取100mL该“84”消毒液,稀释成1L用于消毒,稀释后的溶液中NaClO的物质的量浓度为
?某同学取100mL该“84”消毒液,稀释成1L用于消毒,稀释后的溶液中NaClO的物质的量浓度为_____  ?
?
 ?某同学取100mL该“84”消毒液,稀释成1L用于消毒,稀释后的溶液中NaClO的物质的量浓度为
?某同学取100mL该“84”消毒液,稀释成1L用于消毒,稀释后的溶液中NaClO的物质的量浓度为 ?
?| “84”消毒液 [有效成分]NaClO [规格]1000mL [质量分数]37.25% [密度] 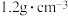 |
您最近一年使用:0次
5 . 试回答下列问题:
(1)0.5mol的 气体中:
气体中:
①质量为________ g,②约含________ 个氢原子,③标准状况下的体积为________ L;
(2)含 的
的 溶液100mL,取出10mL,
溶液100mL,取出10mL, 的物质的量浓度为
的物质的量浓度为________ mol/L。
(1)0.5mol的
 气体中:
气体中: ①质量为
(2)含
 的
的 溶液100mL,取出10mL,
溶液100mL,取出10mL, 的物质的量浓度为
的物质的量浓度为
您最近一年使用:0次
解题方法
6 . 铅(Pb)元素的主要化合价有+2价和+4价,溶液中铅为+2价(Pb2+或 ,铅单质及其化合物在日常生活和工业生产中具有非常广泛的用途。
,铅单质及其化合物在日常生活和工业生产中具有非常广泛的用途。
(1)Pb3O4 俗名红丹,在涂料工业中用作防锈颜料,Pb3O4中+2价铅和+4价铅的原子个数之比为
(2)Pb、PbO2可用于制造铅蓄电池,铅蓄电池工作时的反应方程式为:Pb+PbO2+2H2SO4=2PbSO4+2H2O,该反应中还原产物为
(3)工业上利用铅渣(主要成分是PbO、Pb,以及少量不溶于硝酸的杂质)生产PbSO4的流程如图:
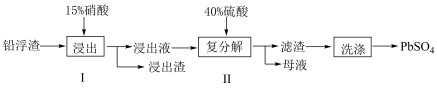
已知步骤1有NO产生,试写出Pb与硝酸反应的化学方程式
(4)血铅是指血液中铅元素的含量。血铅超标会引起机体的神经系统、血液系统、消化系统的一系列异常表现。某人血液中铅的浓度为0.4μg/mL,若转化为物质的量浓度为
您最近一年使用:0次
7 . 以物质的量为中心的计算在高中化学学习中很重要。请完成下列题目。
(1)1gH2中含有_______ 个H。
(2)6.02×1023个CO2分子与16gO2,二者在标况下的体积之比_______ 。
(3)从2L0.5mol·L-1NaOH溶液中取出1L,则所取出的溶液中含NaOH的质量是_______ g。
(1)1gH2中含有
(2)6.02×1023个CO2分子与16gO2,二者在标况下的体积之比
(3)从2L0.5mol·L-1NaOH溶液中取出1L,则所取出的溶液中含NaOH的质量是
您最近一年使用:0次
8 . 下列说法正确的是
| A.1 mol O2的质量是32g/mol |
| B.常温常压下,22.4 L CH4的物质的量为1 mol |
| C.1 L 1 mol · L-1 Na2SO4 溶液中含有2 mol Na+ |
| D.17克 NH3中含有的原子数约为6.02×1023 |
您最近一年使用:0次
9 . NA为阿伏加德罗常数的值。下列说法正确的是
| A.1.7 g NH3中含有的质子数约为6.02×1023 |
| B.1 mol N2与3 mol H2反应生成的NH3分子数为2NA |
| C.标准状况下,2.24 L CCl4含有的共价键数为0.4NA |
D.0.1 mol/L NH4Cl溶液中的NH 数约为0.1NA 数约为0.1NA |
您最近一年使用:0次
2024-03-17更新
|
233次组卷
|
2卷引用:湖南省邵阳市绥宁县第一中2022-2023学年高一下学期期末考试化学试题
10 . 按要求完成下列问题。
(1)现需配制0.1mol/LNaOH溶液450mL。
①该实验要用的玻璃仪器有:烧杯、玻璃棒、胶头滴管、_______ 。
②根据计算得知,所需NaOH的质量为_______ 。
③下列操作对溶液浓度的影响(填写“偏高”、“偏低”或“无影响”)
i.定容时,俯视容量瓶的刻度线,所配制的溶液浓度_______ ;
ii.溶液未冷却至室温就移液和定容,所配制的溶液浓度_______ 。
(2)①10.6g的Na2CO3含有_______ mol氧原子。
②标准状况下6.72LNH3分子中所含原子总数与_______ gH2O所含原子总数相等。
③14.2gNa2SO4溶于水,配制成500mL的溶液,该溶液中钠离子的物质的量浓度c=_______ mol/L。
(1)现需配制0.1mol/LNaOH溶液450mL。
①该实验要用的玻璃仪器有:烧杯、玻璃棒、胶头滴管、
②根据计算得知,所需NaOH的质量为
③下列操作对溶液浓度的影响(填写“偏高”、“偏低”或“无影响”)
i.定容时,俯视容量瓶的刻度线,所配制的溶液浓度
ii.溶液未冷却至室温就移液和定容,所配制的溶液浓度
(2)①10.6g的Na2CO3含有
②标准状况下6.72LNH3分子中所含原子总数与
③14.2gNa2SO4溶于水,配制成500mL的溶液,该溶液中钠离子的物质的量浓度c=
您最近一年使用:0次



