1 . 抗击新冠病毒期间,各地大规模进行环境消毒,其中“84”消毒液试用比较广泛。如图是某“84”消毒液的标签,该“84”消毒液的物质的量浓度为_____  ?某同学取100mL该“84”消毒液,稀释成1L用于消毒,稀释后的溶液中NaClO的物质的量浓度为
?某同学取100mL该“84”消毒液,稀释成1L用于消毒,稀释后的溶液中NaClO的物质的量浓度为_____  ?
?
 ?某同学取100mL该“84”消毒液,稀释成1L用于消毒,稀释后的溶液中NaClO的物质的量浓度为
?某同学取100mL该“84”消毒液,稀释成1L用于消毒,稀释后的溶液中NaClO的物质的量浓度为 ?
?| “84”消毒液 [有效成分]NaClO [规格]1000mL [质量分数]37.25% [密度] 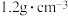 |
您最近一年使用:0次
名校
2 . 100g 12mol/L(密度为1.19g/mL)的盐酸用100g水稀释后,其物质的量浓度_______ (填“大于”、“等于”或“小于”)6mol/L。
您最近一年使用:0次
名校
3 . 化学学科的发展经历了从定性到定量的过程。在生产和科学实验中,我们经常用到一定浓度的溶液。
I.某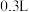 无土栽培用的营养液中含有
无土栽培用的营养液中含有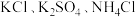 三种溶质,测得该营养液中部分离子的浓度柱状图如图所示:
三种溶质,测得该营养液中部分离子的浓度柱状图如图所示:
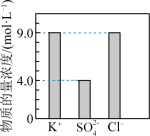
(1)该营养液中 的物质的量浓度为
的物质的量浓度为___________ ;
(2)已知 ,若要使该份溶液中的
,若要使该份溶液中的 完全反应,需加入
完全反应,需加入 的
的 溶液
溶液______ mL。
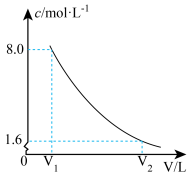
(3)将该营养液加水稀释,稀释过程中 的浓度(c)随溶液体积(V)变化的曲线如图所示,则
的浓度(c)随溶液体积(V)变化的曲线如图所示,则
___________ 。
II.在标准状况下,一定体积的氯化氢溶解在 的水(设此温度下水的密度为
的水(设此温度下水的密度为 )中,形成密度为
)中,形成密度为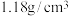 的溶液,经测定该盐酸的质量分数为
的溶液,经测定该盐酸的质量分数为 。
。
(4)此溶液的物质的量浓度为___________ 。
(5)该条件下,此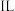 水中溶解的氯化氢的体积为
水中溶解的氯化氢的体积为___________ L(保留一位小数)。
III.某学生现需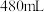 物质的量浓度为
物质的量浓度为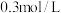 稀盐酸。
稀盐酸。
(6)配制时所用的玻璃仪器除量筒、烧杯、玻璃棒外,还有___________ 。
(7)在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(在横线填“偏大”、“偏小”或“无影响”)。
①洗涤量筒并将洗涤液转移至容量瓶中___________ 。
②转移前,容量瓶中含有少量蒸馏水___________ 。
③定容时,俯视读数___________ 。
I.某
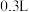 无土栽培用的营养液中含有
无土栽培用的营养液中含有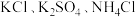 三种溶质,测得该营养液中部分离子的浓度柱状图如图所示:
三种溶质,测得该营养液中部分离子的浓度柱状图如图所示:
(1)该营养液中
 的物质的量浓度为
的物质的量浓度为(2)已知
 ,若要使该份溶液中的
,若要使该份溶液中的 完全反应,需加入
完全反应,需加入 的
的 溶液
溶液(3)将该营养液加水稀释,稀释过程中
 的浓度(c)随溶液体积(V)变化的曲线如图所示,则
的浓度(c)随溶液体积(V)变化的曲线如图所示,则

II.在标准状况下,一定体积的氯化氢溶解在
 的水(设此温度下水的密度为
的水(设此温度下水的密度为 )中,形成密度为
)中,形成密度为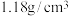 的溶液,经测定该盐酸的质量分数为
的溶液,经测定该盐酸的质量分数为 。
。(4)此溶液的物质的量浓度为
(5)该条件下,此
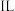 水中溶解的氯化氢的体积为
水中溶解的氯化氢的体积为III.某学生现需
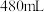 物质的量浓度为
物质的量浓度为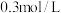 稀盐酸。
稀盐酸。(6)配制时所用的玻璃仪器除量筒、烧杯、玻璃棒外,还有
(7)在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(在横线填“偏大”、“偏小”或“无影响”)。
①洗涤量筒并将洗涤液转移至容量瓶中
②转移前,容量瓶中含有少量蒸馏水
③定容时,俯视读数
您最近一年使用:0次
名校
4 . 化学计量在化学知识体系中占有重要地位,请回答下列问题。
(1)标准状况下,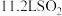 的物质的量是
的物质的量是___________ ,质量是___________ g。
(2)同温同压下,质量相等的 、
、 、
、 、
、 四种气体中,含有分子数目最多的是
四种气体中,含有分子数目最多的是___________ ,密度最大的是___________ 。
(3) 中含有的
中含有的 为
为 ,则X的摩尔质量为
,则X的摩尔质量为___________ 。
(4) 的盐酸与
的盐酸与 铁屑反应,参与反应的
铁屑反应,参与反应的 物质的量为
物质的量为___________ ,生成的 在标准状况下的体积为
在标准状况下的体积为___________ L。
(5)现有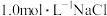 溶液
溶液 ,若取
,若取 该溶液用水稀释到
该溶液用水稀释到 ,所得溶液的
,所得溶液的 的物质的量浓度为
的物质的量浓度为___________ 。
(1)标准状况下,
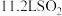 的物质的量是
的物质的量是(2)同温同压下,质量相等的
 、
、 、
、 、
、 四种气体中,含有分子数目最多的是
四种气体中,含有分子数目最多的是(3)
 中含有的
中含有的 为
为 ,则X的摩尔质量为
,则X的摩尔质量为(4)
 的盐酸与
的盐酸与 铁屑反应,参与反应的
铁屑反应,参与反应的 物质的量为
物质的量为 在标准状况下的体积为
在标准状况下的体积为(5)现有
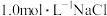 溶液
溶液 ,若取
,若取 该溶液用水稀释到
该溶液用水稀释到 ,所得溶液的
,所得溶液的 的物质的量浓度为
的物质的量浓度为
您最近一年使用:0次
名校
解题方法
5 . 《黄帝九鼎神丹经诀》卷九中记载着“炼石胆取精华法”,即干馏石胆(胆矾)而获得硫酸。硫酸是一种重要的工业原料,可用于制造肥料、药物、炸药、颜料、洗涤剂、蓄电池等,也广泛应用于净化石油、金属冶炼等工业中。请根据要求回答下列问题:
(1)纯净的液态硫酸______ (填“能”或“几乎不能”)导电,在硫酸不断稀释的过程中,溶液导电能力的变化情况为______ 。
(2)硫酸是强酸,具有酸的通性,如稀硫酸与氧化铁反应的化学方程式为______ ,但浓硫酸与氧化亚铁反应的化学方程式为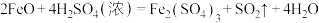 ,该反应属于
,该反应属于______ (填“氧化还原反应”或“非氧化还原反应”)。
(3)某浓硫酸的说明如图所示。该浓硫酸的物质的量浓度为______  ,从中取出100mL,则该100mL浓硫酸的物质的量浓度为
,从中取出100mL,则该100mL浓硫酸的物质的量浓度为______  ,含
,含 的物质的量为
的物质的量为______ mol。
(4)如果取5mL该浓硫酸,加水稀释至10mL,那么稀释后的硫酸的质量分数______ (填“大于”、“小于”或“等于”,下同)49%;如果取5mL该浓硫酸,加等质量的水稀释,那么稀释后的硫酸的物质的量浓度______ 原浓硫酸的物质的量浓度的一半。
(1)纯净的液态硫酸
(2)硫酸是强酸,具有酸的通性,如稀硫酸与氧化铁反应的化学方程式为
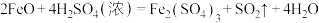 ,该反应属于
,该反应属于(3)某浓硫酸的说明如图所示。该浓硫酸的物质的量浓度为
 ,从中取出100mL,则该100mL浓硫酸的物质的量浓度为
,从中取出100mL,则该100mL浓硫酸的物质的量浓度为 ,含
,含 的物质的量为
的物质的量为| 硫酸 化学纯 CP 500mL 品名:硫酸 化学式:  相对分子质量:98 密度:1.84  质量分数:98% |
您最近一年使用:0次
名校
解题方法
6 . 84消毒液、ClO2是常见的含氯消毒剂。
资料:84消毒液中含氟微粒主要有ClO-、Cl-、HClO;相同浓度时,HClO的氧化性强于ClO-;ORP是反映物质的氧化一还原性,ORP值越大,氧化性越强。通常情况下,应将84消毒液原液稀释后使用;一般不用于衣服等纺织品的洗涤消毒。
(1)制备ClO2的一种反应为:2NaClO3+2NaCl+2H2SO4=2ClO2↑+Cl2↑+2Na2SO4+2H2O,用单线桥法标出其电子转移的方向和数目_______ 。
(2)取含次氯酸钠0.2mol·L-1的消毒液1mL,加水稀释至200mL,则稀释后次氯酸钠的物质的量浓度为_______ mol·L-1。
(3)为研究84消毒液的性质与使用条件,进行下列实验:
【实验1】向两支试管中分别加入2mL84消毒液,在试管l中加入2mL水,试管2中加入2mL白醋,再分别放入相同的红色纸片。观察到试管2中纸片褪色更快。
①实验中在试管l中加入2mL水的目的是_______ 。
②试管2中纸片褪色更快的原因是_______ 。
③如果实验中加浓盐酸,会有黄绿色气体产生,反应的离子方程式是_______ 。
【实验2】测定84消毒液在不同温度时ORP随时间的变化情况,结果如图所示。
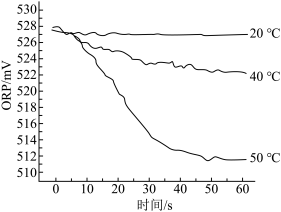
④实验表明,随温度升高,ORP值下降。50℃时ORP值下降较快的原因是_______ 。
资料:84消毒液中含氟微粒主要有ClO-、Cl-、HClO;相同浓度时,HClO的氧化性强于ClO-;ORP是反映物质的氧化一还原性,ORP值越大,氧化性越强。通常情况下,应将84消毒液原液稀释后使用;一般不用于衣服等纺织品的洗涤消毒。
(1)制备ClO2的一种反应为:2NaClO3+2NaCl+2H2SO4=2ClO2↑+Cl2↑+2Na2SO4+2H2O,用单线桥法标出其电子转移的方向和数目
(2)取含次氯酸钠0.2mol·L-1的消毒液1mL,加水稀释至200mL,则稀释后次氯酸钠的物质的量浓度为
(3)为研究84消毒液的性质与使用条件,进行下列实验:
【实验1】向两支试管中分别加入2mL84消毒液,在试管l中加入2mL水,试管2中加入2mL白醋,再分别放入相同的红色纸片。观察到试管2中纸片褪色更快。
①实验中在试管l中加入2mL水的目的是
②试管2中纸片褪色更快的原因是
③如果实验中加浓盐酸,会有黄绿色气体产生,反应的离子方程式是
【实验2】测定84消毒液在不同温度时ORP随时间的变化情况,结果如图所示。

④实验表明,随温度升高,ORP值下降。50℃时ORP值下降较快的原因是
您最近一年使用:0次
7 . 实验时需用约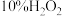 溶液
溶液 ,现用市售
,现用市售 (密度近似为
(密度近似为 )的
)的 来配制,简述其具体配制方法
来配制,简述其具体配制方法_______ 。
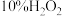 溶液
溶液 ,现用市售
,现用市售 (密度近似为
(密度近似为 )的
)的 来配制,简述其具体配制方法
来配制,简述其具体配制方法
您最近一年使用:0次
2023高三·全国·专题练习
8 . 现有浓H3PO4质量分数为85%,密度为1.7g/mL。若实验需100mL1.7mol/L的H3PO4溶液,则需浓H3PO4_______ mL(保留一位小数)。
您最近一年使用:0次
名校
9 . 硫酸的工业制取原理为① ,②
,②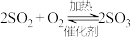 ,③
,③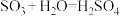 。请回答下列问题:
。请回答下列问题:
(1)请配平反应①的化学方程式:_______
 。
。
(2)标准状况下,
 的摩尔质量为
的摩尔质量为_______ ,质量为_______ g。
(3) 、120℃下,等质量的
、120℃下,等质量的 和
和 的物质的量之比为
的物质的量之比为_______ ,密度之比为_______ 。
(4)质量分数为98%的浓硫酸(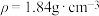 )的物质的量浓度为
)的物质的量浓度为_______  ;实验室需要配制
;实验室需要配制
 硫酸溶液,需要用量筒量取该浓硫酸的体积为
硫酸溶液,需要用量筒量取该浓硫酸的体积为_______ mL;若从配制好的硫酸溶液中取出 ,其浓度为
,其浓度为_______  ,将这
,将这 硫酸溶液稀释至
硫酸溶液稀释至 ,溶液中
,溶液中 浓度为
浓度为_______  。
。
 ,②
,②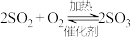 ,③
,③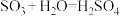 。请回答下列问题:
。请回答下列问题:(1)请配平反应①的化学方程式:
 。
。(2)标准状况下,

 的摩尔质量为
的摩尔质量为(3)
 、120℃下,等质量的
、120℃下,等质量的 和
和 的物质的量之比为
的物质的量之比为(4)质量分数为98%的浓硫酸(
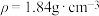 )的物质的量浓度为
)的物质的量浓度为 ;实验室需要配制
;实验室需要配制
 硫酸溶液,需要用量筒量取该浓硫酸的体积为
硫酸溶液,需要用量筒量取该浓硫酸的体积为 ,其浓度为
,其浓度为 ,将这
,将这 硫酸溶液稀释至
硫酸溶液稀释至 ,溶液中
,溶液中 浓度为
浓度为 。
。
您最近一年使用:0次
2022-12-07更新
|
204次组卷
|
3卷引用:四川省成都市四校2022-2023学年高一上学期12月联考化学试题
名校
10 . 下图是化学实验室浓盐酸试剂标签上的部分内容。

(1)写出工业上制HCl的化学方程式_______ ,在实验室中进行该反应,现象是_______
(2)该盐酸的物质的量浓度为_______ ,
(3)同学计划用该浓盐酸配制 的稀盐酸,现实验需要稀盐酸470 mL,可供选用的仪器有:
的稀盐酸,现实验需要稀盐酸470 mL,可供选用的仪器有:
A.胶头滴管;B.烧瓶;C.烧杯;D.药匙;E玻璃棒。
①配制稀盐酸时,选择的仪器有:_______ (填序号),还缺少的仪器有_______ 。
②经计算,配制 的稀盐酸需要用量筒量取上述浓盐酸的体积为
的稀盐酸需要用量筒量取上述浓盐酸的体积为_______ mL。
③测定所配制的稀盐酸,发现其浓度大于 ,引起误差的原因可能是
,引起误差的原因可能是_______ 。
A.量取浓盐酸时俯视刻度线
B.将量取的浓盐酸倒入烧杯后,洗涤量筒,洗涤液也注入容量瓶
C.转移溶液后,未洗涤烧杯和玻璃棒
D.定容时俯视容量瓶刻度线
E.定容摇匀后发现液面低于容量瓶的刻度线,再加水至刻度线
(4)现有该浓盐酸100g,需要加入一定量的水将其物质的量浓度稀释为原来的1/2,则加入水的体积是_______ 。
A.大于100 mL B.小于100 mL C.等于100 mL

(1)写出工业上制HCl的化学方程式
(2)该盐酸的物质的量浓度为
(3)同学计划用该浓盐酸配制
 的稀盐酸,现实验需要稀盐酸470 mL,可供选用的仪器有:
的稀盐酸,现实验需要稀盐酸470 mL,可供选用的仪器有:A.胶头滴管;B.烧瓶;C.烧杯;D.药匙;E玻璃棒。
①配制稀盐酸时,选择的仪器有:
②经计算,配制
 的稀盐酸需要用量筒量取上述浓盐酸的体积为
的稀盐酸需要用量筒量取上述浓盐酸的体积为③测定所配制的稀盐酸,发现其浓度大于
 ,引起误差的原因可能是
,引起误差的原因可能是A.量取浓盐酸时俯视刻度线
B.将量取的浓盐酸倒入烧杯后,洗涤量筒,洗涤液也注入容量瓶
C.转移溶液后,未洗涤烧杯和玻璃棒
D.定容时俯视容量瓶刻度线
E.定容摇匀后发现液面低于容量瓶的刻度线,再加水至刻度线
(4)现有该浓盐酸100g,需要加入一定量的水将其物质的量浓度稀释为原来的1/2,则加入水的体积是
A.大于100 mL B.小于100 mL C.等于100 mL
您最近一年使用:0次
2022-12-07更新
|
464次组卷
|
5卷引用:四川省成都市第七中学2022-2023学年高一上学期12月月考化学试题



