1 . Ⅰ.按要求回答下列问题。
(1)①稀硫酸 ②液氨 ③氯气 ④铝条 ⑤碳酸钙 ⑥石墨 ⑦氢氧化钡溶液 ⑧二氧化硫 ⑨水 ⑩熔融氯化钠 ⑪蔗糖溶液 ⑫乙醇
上述物质是电解质且能导电的有_______ ,是非电解质的有_______ (以上各空均填序号)。
Ⅱ.利用相关知识填空。
(2)标准状况下11.2LNH3中含______ mol氢原子。
(3)等质量的SO2和SO3所含的氧原子个数之比是_________ 。
(4)12.4gNa2R含Na+0.4mol,则Na2R的摩尔质量为_________ 。
(5)在标准状况下,测得1.32g某气体的体积为0.672L。则此气体的摩尔质量为___________ 。
Ⅲ.定量实验是研究化学的重要手段,工业上硫酸钠在印染、玻璃制造等有重要的应用,实验室要配制90mL0.5mol/LNa2SO4溶液。
(6)需用托盘天平称取Na2SO4固体的质量为_______ g。
(7)实验过程中需要用到的玻璃仪器有烧杯、量筒、______ 、_____ 和_____ 。
(8)取出配制准确的该溶液50mL,将其稀释到500mL,此时溶液中Na+的物质的量浓度为__________ 。
(9)下列操作会造成所配溶液浓度偏高的是_______ 。
A.使用有少量蒸馏水的容量瓶配制溶液
B.转移溶液后的烧杯未用蒸馏水洗涤
C.若定容时不小心加水超过了刻度线
D.定容时俯视液面
E.定容摇匀后,发现液面低于刻度线,再加蒸馏水至刻度线
(1)①稀硫酸 ②液氨 ③氯气 ④铝条 ⑤碳酸钙 ⑥石墨 ⑦氢氧化钡溶液 ⑧二氧化硫 ⑨水 ⑩熔融氯化钠 ⑪蔗糖溶液 ⑫乙醇
上述物质是电解质且能导电的有
Ⅱ.利用相关知识填空。
(2)标准状况下11.2LNH3中含
(3)等质量的SO2和SO3所含的氧原子个数之比是
(4)12.4gNa2R含Na+0.4mol,则Na2R的摩尔质量为
(5)在标准状况下,测得1.32g某气体的体积为0.672L。则此气体的摩尔质量为
Ⅲ.定量实验是研究化学的重要手段,工业上硫酸钠在印染、玻璃制造等有重要的应用,实验室要配制90mL0.5mol/LNa2SO4溶液。
(6)需用托盘天平称取Na2SO4固体的质量为
(7)实验过程中需要用到的玻璃仪器有烧杯、量筒、
(8)取出配制准确的该溶液50mL,将其稀释到500mL,此时溶液中Na+的物质的量浓度为
(9)下列操作会造成所配溶液浓度偏高的是
A.使用有少量蒸馏水的容量瓶配制溶液
B.转移溶液后的烧杯未用蒸馏水洗涤
C.若定容时不小心加水超过了刻度线
D.定容时俯视液面
E.定容摇匀后,发现液面低于刻度线,再加蒸馏水至刻度线
您最近一年使用:0次
2 . Ⅰ.对锂原子结构及其性质的研究
(1)基态 原子的核外电子排布式为
原子的核外电子排布式为_______ ,其处于元素周期表中的_______ (填“s”、“d”、"ds”或“p”)区。
(2)基态 原子的电子发生跃迁形成激发态
原子的电子发生跃迁形成激发态 原子时,
原子时,_______ (填“吸收”或“释放”)能量。
(3)已知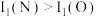 ,从原子结构的角度解释第一电离能
,从原子结构的角度解释第一电离能 大于
大于 的原因:
的原因:_______ 。
(4)请按电负性由大到小的顺序排列 三种元素:
三种元素:_______ 。
Ⅱ.常温下,某小组同学用图1装置探究 的沉淀溶解平衡。
的沉淀溶解平衡。

实验操作:向蒸馏水中加入足量 粉末,一段时间后再加入少量蒸馏水。(图1中传感器为电导率传感器,实验测得电导率随时间变化的曲线如图2所示。)
粉末,一段时间后再加入少量蒸馏水。(图1中传感器为电导率传感器,实验测得电导率随时间变化的曲线如图2所示。)
已知:ⅰ.在稀溶液中,溶液中离子浓度越大,电导率越大。
(5) 点电导率不等于0的原因是水能发生
点电导率不等于0的原因是水能发生_______ 。
(6)由图2可知,在 悬浊液中加入少量水的时刻为
悬浊液中加入少量水的时刻为_______ (填“b”、“c”或“d”)点。
(7)分析电导率在de段逐渐上升的原因: 时刻,
时刻,
_______ (填“>”、“<”或“=”) ,导致
,导致_______ (结合沉淀溶解平衡解释原因)。
已知:ⅱ.
(8) 常被用于水质改良剂,能够使水体
常被用于水质改良剂,能够使水体 约为9,进而抑制细莑的生长。
约为9,进而抑制细莑的生长。 时,水体中
时,水体中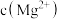 约为
约为_______  。
。
(1)基态
 原子的核外电子排布式为
原子的核外电子排布式为(2)基态
 原子的电子发生跃迁形成激发态
原子的电子发生跃迁形成激发态 原子时,
原子时,(3)已知
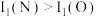 ,从原子结构的角度解释第一电离能
,从原子结构的角度解释第一电离能 大于
大于 的原因:
的原因:(4)请按电负性由大到小的顺序排列
 三种元素:
三种元素:Ⅱ.常温下,某小组同学用图1装置探究
 的沉淀溶解平衡。
的沉淀溶解平衡。
实验操作:向蒸馏水中加入足量
 粉末,一段时间后再加入少量蒸馏水。(图1中传感器为电导率传感器,实验测得电导率随时间变化的曲线如图2所示。)
粉末,一段时间后再加入少量蒸馏水。(图1中传感器为电导率传感器,实验测得电导率随时间变化的曲线如图2所示。)已知:ⅰ.在稀溶液中,溶液中离子浓度越大,电导率越大。
(5)
 点电导率不等于0的原因是水能发生
点电导率不等于0的原因是水能发生(6)由图2可知,在
 悬浊液中加入少量水的时刻为
悬浊液中加入少量水的时刻为(7)分析电导率在de段逐渐上升的原因:
 时刻,
时刻,
 ,导致
,导致已知:ⅱ.

(8)
 常被用于水质改良剂,能够使水体
常被用于水质改良剂,能够使水体 约为9,进而抑制细莑的生长。
约为9,进而抑制细莑的生长。 时,水体中
时,水体中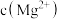 约为
约为 。
。
您最近一年使用:0次
名校
解题方法
3 . 分类是学习化学的重要方法,下列归纳正确的是
| A.胆矾、水银、烧碱、硫酸均为电解质 |
| B.熔融氧化铝、氨水既是电解质又能导电 |
| C.碘酒、淀粉溶液、水雾、纳米材料均为胶体 |
D. 小苏打均为化合物 小苏打均为化合物 |
您最近一年使用:0次
名校
解题方法
4 . 回答下列问题
(1)下列物质中① ②液态
②液态 ③纯醋酸④硫酸钡⑤液氨⑥酒精(C2H5OH)⑦
③纯醋酸④硫酸钡⑤液氨⑥酒精(C2H5OH)⑦ ⑧铝 请用以上物质回答下列问题。(填序号)
⑧铝 请用以上物质回答下列问题。(填序号)
①属于强电解质的是___________ 。
②属于弱电解质的是___________ 。
③属于非电解质,但其水溶液能导电的是___________ 。
(2)某温度下纯水中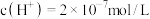 ,则此时溶液中的
,则此时溶液中的
___________  。若温度不变,滴入稀盐酸使
。若温度不变,滴入稀盐酸使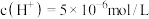 ,则此时溶液中的
,则此时溶液中的
___________  。
。
(3)将 的
的 的
的 溶液与常温下的
溶液与常温下的 的稀盐酸混合,并保持
的稀盐酸混合,并保持 的恒温,欲使混合溶液的
的恒温,欲使混合溶液的 ,则
,则 溶液与盐酸的体积比为
溶液与盐酸的体积比为___________ (忽略水和氯化氢的挥发,忽略混合后溶液体积的变化)。
(4)向氨水中滴加稀硫酸,使其恰好完全中和,则所得溶液中离子浓度由大到小的关系:___________ 。
(5)常温下, 的两种一元酸
的两种一元酸 和
和 ,体积均为
,体积均为 ,稀释过程中
,稀释过程中 与溶液体积的关系如图所示。分别中和
与溶液体积的关系如图所示。分别中和 溶液并使其恰好反应,消耗
溶液并使其恰好反应,消耗 溶液的体积为
溶液的体积为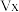 、
、 。请比较
。请比较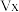
___________  (填“>”或“<”)
(填“>”或“<”)

(6) 的水溶液呈
的水溶液呈___________ (填“酸”、“中”、“碱”)性,常温时的
___________ 7(填“>”或“=”或“<”),实验室在配制 的溶液时,常将
的溶液时,常将 固体先溶于硫酸中,然后再用蒸馏水稀释到所需的浓度,以
固体先溶于硫酸中,然后再用蒸馏水稀释到所需的浓度,以___________ (填“促进”、“抑制”)其水解。
(7)泡沫灭火器中的主要成分是 和
和 溶液,反应的离子方程式为
溶液,反应的离子方程式为___________ 。
(1)下列物质中①
 ②液态
②液态 ③纯醋酸④硫酸钡⑤液氨⑥酒精(C2H5OH)⑦
③纯醋酸④硫酸钡⑤液氨⑥酒精(C2H5OH)⑦ ⑧铝 请用以上物质回答下列问题。(填序号)
⑧铝 请用以上物质回答下列问题。(填序号)①属于强电解质的是
②属于弱电解质的是
③属于非电解质,但其水溶液能导电的是
(2)某温度下纯水中
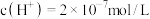 ,则此时溶液中的
,则此时溶液中的
 。若温度不变,滴入稀盐酸使
。若温度不变,滴入稀盐酸使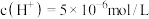 ,则此时溶液中的
,则此时溶液中的
 。
。(3)将
 的
的 的
的 溶液与常温下的
溶液与常温下的 的稀盐酸混合,并保持
的稀盐酸混合,并保持 的恒温,欲使混合溶液的
的恒温,欲使混合溶液的 ,则
,则 溶液与盐酸的体积比为
溶液与盐酸的体积比为(4)向氨水中滴加稀硫酸,使其恰好完全中和,则所得溶液中离子浓度由大到小的关系:
(5)常温下,
 的两种一元酸
的两种一元酸 和
和 ,体积均为
,体积均为 ,稀释过程中
,稀释过程中 与溶液体积的关系如图所示。分别中和
与溶液体积的关系如图所示。分别中和 溶液并使其恰好反应,消耗
溶液并使其恰好反应,消耗 溶液的体积为
溶液的体积为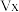 、
、 。请比较
。请比较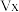
 (填“>”或“<”)
(填“>”或“<”)
(6)
 的水溶液呈
的水溶液呈
 的溶液时,常将
的溶液时,常将 固体先溶于硫酸中,然后再用蒸馏水稀释到所需的浓度,以
固体先溶于硫酸中,然后再用蒸馏水稀释到所需的浓度,以(7)泡沫灭火器中的主要成分是
 和
和 溶液,反应的离子方程式为
溶液,反应的离子方程式为
您最近一年使用:0次
名校
5 . 完成下列问题。
(1)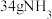 与标况下
与标况下___________ L 气体含相同数目H原子。
气体含相同数目H原子。
(2)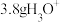 含电子数目为
含电子数目为___________ 。
(3)三种盐混合溶液中含 和
和 ,则
,则 的物质的量为
的物质的量为___________ 。
(4)取某浓度氢氧化钠溶液 ,通入一定量
,通入一定量 ,随后取
,随后取 溶液,向其中逐滴滴入
溶液,向其中逐滴滴入 的盐酸,在标准状况下产生
的盐酸,在标准状况下产生 的体积(y轴)与所加入盐酸的体积(x轴)的关系如图:
的体积(y轴)与所加入盐酸的体积(x轴)的关系如图:
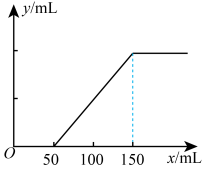
①通入 后所得溶液溶质是
后所得溶液溶质是___________ (填化学式),其物质的量之比为___________ 。
②氢氧化钠溶液的物质的量浓度为___________ 。
(5)下列几种导电性变化图象,把符合要求的图象序号填在相应的题目后面横线上:
A. B.
B.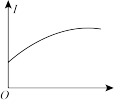 C.
C.
向 溶液中通入
溶液中通入 直至过量
直至过量______ (提示 );向
);向 溶液通入少量
溶液通入少量
____ ;)向氨水中通入 直至过量
直至过量______ ;向饱和石灰水中不断通入
______ 。
(1)
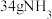 与标况下
与标况下 气体含相同数目H原子。
气体含相同数目H原子。(2)
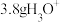 含电子数目为
含电子数目为(3)三种盐混合溶液中含
 和
和 ,则
,则 的物质的量为
的物质的量为(4)取某浓度氢氧化钠溶液
 ,通入一定量
,通入一定量 ,随后取
,随后取 溶液,向其中逐滴滴入
溶液,向其中逐滴滴入 的盐酸,在标准状况下产生
的盐酸,在标准状况下产生 的体积(y轴)与所加入盐酸的体积(x轴)的关系如图:
的体积(y轴)与所加入盐酸的体积(x轴)的关系如图:
①通入
 后所得溶液溶质是
后所得溶液溶质是②氢氧化钠溶液的物质的量浓度为
(5)下列几种导电性变化图象,把符合要求的图象序号填在相应的题目后面横线上:
A.
 B.
B. C.
C.
向
 溶液中通入
溶液中通入 直至过量
直至过量 );向
);向 溶液通入少量
溶液通入少量
 直至过量
直至过量
您最近一年使用:0次
名校
6 . 回答下列问题:
(1)今有11种物质:①盐酸;②石墨;③氯气;④ 晶体;⑤纯硫酸;⑥金刚石;⑦碱石灰;⑧乙醇;⑨熔融的
晶体;⑤纯硫酸;⑥金刚石;⑦碱石灰;⑧乙醇;⑨熔融的 ;⑩
;⑩ ;其中:
;其中:
①能导电的是(填序号,下同)_____________ ;
②属于电解质的是_____________ ;
(2)①19g某二价金属氯化物( )中含有
)中含有 ,则
,则 的摩尔质量是
的摩尔质量是______ ;
②现有标准状况下CO和 混合气体6.72L,其质量为11.6g,则此混合气体中,CO和
混合气体6.72L,其质量为11.6g,则此混合气体中,CO和 的物质的量之比是
的物质的量之比是______ ;
③质量相同的①HCl、② 、③
、③ 、④
、④ 四种气体中,在同温同压条件下,所占体积最小的是(填序号)
四种气体中,在同温同压条件下,所占体积最小的是(填序号)______ 。
(1)今有11种物质:①盐酸;②石墨;③氯气;④
 晶体;⑤纯硫酸;⑥金刚石;⑦碱石灰;⑧乙醇;⑨熔融的
晶体;⑤纯硫酸;⑥金刚石;⑦碱石灰;⑧乙醇;⑨熔融的 ;⑩
;⑩ ;其中:
;其中:①能导电的是(填序号,下同)
②属于电解质的是
(2)①19g某二价金属氯化物(
 )中含有
)中含有 ,则
,则 的摩尔质量是
的摩尔质量是②现有标准状况下CO和
 混合气体6.72L,其质量为11.6g,则此混合气体中,CO和
混合气体6.72L,其质量为11.6g,则此混合气体中,CO和 的物质的量之比是
的物质的量之比是③质量相同的①HCl、②
 、③
、③ 、④
、④ 四种气体中,在同温同压条件下,所占体积最小的是(填序号)
四种气体中,在同温同压条件下,所占体积最小的是(填序号)
您最近一年使用:0次
2023-12-11更新
|
78次组卷
|
2卷引用:天津市第四十七中学2023-2024学年高一上学期11月期中考试化学试题
名校
解题方法
7 . “化学——我们的生活,我们的未来”,学习化学应该明白“从生活中来,到生活中去”的道理。请填空:
(1)通过学习,我们掌握了胶体的知识,请完成下列问题:
①鉴别胶体和溶液的方法(只需写出方法名称,不用展开写)___________ ;
②请写出实验室制备氢氧化铁胶体的化学方程式为___________ 。
(2)写出下列物质在溶液中的电离方程式:Al2(SO4)3________ ,NaHCO3________ 。
(3)无色气体A在一种黄绿色气体B中可安静地燃烧,发出苍白色火焰,反应生成气体C,推断出各种物质后,回答下列问题:
①写出反应的化学方程式___________ 。
②1g物质A中含有的分子数约为___________ 。
(1)通过学习,我们掌握了胶体的知识,请完成下列问题:
①鉴别胶体和溶液的方法(只需写出方法名称,不用展开写)
②请写出实验室制备氢氧化铁胶体的化学方程式为
(2)写出下列物质在溶液中的电离方程式:Al2(SO4)3
(3)无色气体A在一种黄绿色气体B中可安静地燃烧,发出苍白色火焰,反应生成气体C,推断出各种物质后,回答下列问题:
①写出反应的化学方程式
②1g物质A中含有的分子数约为
您最近一年使用:0次
8 . 某小组以盐酸、醋酸为例探究其酸性的强弱。按要求回答下列问题。
(1)取相同体积、相同浓度的盐酸和醋酸,分别测其pH和导电能力,对比分析,在下表填写空白。已知: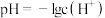
③此温度下,CH3COOH的电离平衡常数Ka=___________ (填计算式,不化简)。
(2)在上述醋酸溶液中加入如下表所示物质,分析其中粒子的变化等,填写空白。
(3)向两个锥形瓶中各加入0.06g镁条,塞紧橡胶塞,然后用注射器分别注入2mL 2mol/L盐酸、2mol/L醋酸。
①反应前n(Mg)=___________ mol;充分反应后,剩余的n(Mg)=___________ mol。
②两锥形瓶内气体n随时间变化,对比分析后,在如下坐标中将示意曲线补充完整。___________

(1)取相同体积、相同浓度的盐酸和醋酸,分别测其pH和导电能力,对比分析,在下表填写空白。已知:
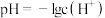
| 酸 | 0.1mol/L盐酸 | 0.1mol/L醋酸 | |
| pH(25℃) | 1 | 3 | |
| 导电能力 | 强 | 弱 | |
| 分析与结论 | ①微观解释(写出溶质在溶液中的存在形式,填粒子的化学式) | ||
| ②电离方程式 | |||
(2)在上述醋酸溶液中加入如下表所示物质,分析其中粒子的变化等,填写空白。
| 加入少量的物质 | 醋酸电离平衡移动方向 填“→”“←”或“不移动” | c(H⁺)/c(CH3COOH)比值变化 填“变大”“变小”或“不变” |
| ①CH3COONa(s) | ||
| ②水 |
(3)向两个锥形瓶中各加入0.06g镁条,塞紧橡胶塞,然后用注射器分别注入2mL 2mol/L盐酸、2mol/L醋酸。
①反应前n(Mg)=
②两锥形瓶内气体n随时间变化,对比分析后,在如下坐标中将示意曲线补充完整。

您最近一年使用:0次
名校
解题方法
9 . 将2mL1mol/L的醋酸滴入到饱和Na2CO3溶液中,观察到有气泡产生。下列有关说法不正确的是
A.电离方程式: |
| B.酸性:CH3COOH>H2CO3 |
| C.电离常数:K(CH3COOH)>Ka1(H2CO3) |
| D.H2CO3的电离常数:Ka1>>Ka2 |
您最近一年使用:0次
2023-11-08更新
|
325次组卷
|
4卷引用:天津市河西区2023-2024学年高二上学期11月期中化学试题
名校
解题方法
10 . 下列说法中正确的是个数为
①漂白粉、水玻璃、福尔马林都是混合物
②CO2、SiO2、P2O5 均为酸性氧化物
③用玻璃棒蘸取少量某溶液进行焰色试验,火焰呈黄色,该溶液中一定含Na+
④纳米铁粉可以除被污染水体中的重金属离子
⑤氯化铝溶液与氢氧化铝胶体具有的共同性质是:能透过滤纸
⑥苛性钾、次氯酸、氯气按顺序分类依次为强电解质、弱电解质和非电解质
⑦强电解质都是离子化合物,因此NaCl是离子化合物
⑧醋酸溶液的导电能力可能比稀硫酸强
⑨CaO水溶液能导电,所以CaO是电解质
①漂白粉、水玻璃、福尔马林都是混合物
②CO2、SiO2、P2O5 均为酸性氧化物
③用玻璃棒蘸取少量某溶液进行焰色试验,火焰呈黄色,该溶液中一定含Na+
④纳米铁粉可以除被污染水体中的重金属离子
⑤氯化铝溶液与氢氧化铝胶体具有的共同性质是:能透过滤纸
⑥苛性钾、次氯酸、氯气按顺序分类依次为强电解质、弱电解质和非电解质
⑦强电解质都是离子化合物,因此NaCl是离子化合物
⑧醋酸溶液的导电能力可能比稀硫酸强
⑨CaO水溶液能导电,所以CaO是电解质
| A.5个 | B.6个 | C.7个 | D.8个 |
您最近一年使用:0次



