1 . 向一定量的 溶液中缓慢滴加盐酸,并不断搅拌。随着盐酸的加入,溶液中离子数目也发生相应变化。如图所示,四条曲线与溶液中离子的对应关系完全正确的是( )
溶液中缓慢滴加盐酸,并不断搅拌。随着盐酸的加入,溶液中离子数目也发生相应变化。如图所示,四条曲线与溶液中离子的对应关系完全正确的是( )

 溶液中缓慢滴加盐酸,并不断搅拌。随着盐酸的加入,溶液中离子数目也发生相应变化。如图所示,四条曲线与溶液中离子的对应关系完全正确的是( )
溶液中缓慢滴加盐酸,并不断搅拌。随着盐酸的加入,溶液中离子数目也发生相应变化。如图所示,四条曲线与溶液中离子的对应关系完全正确的是( )
| a | b | c | d | |
| A |  |  |  |  |
| B |  |  |  |  |
| C |  |  |  |  |
| D |  |  |  |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2020-10-01更新
|
504次组卷
|
2卷引用:人教版(2019)高一必修第一册 第二章 海水中的重要元素 第一节 钠及其化合物 教材帮
2 . 利用元素的化合价推测物质的性质是化学研究的重要手段.如图是硫元素的常见化合价与部分物质类别的对应关系(图中X是H2S):
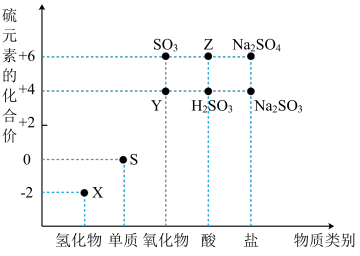
(1)从硫元素化合价变化的角度分析,图中既有氧化性又有还原性的化合物有________ (填化学式);
(2)将X与Y混合,可生成S单质(淡黄色沉淀)。该反应的化学方程式为_______________ ,其中氧化产物与还原产物的物质的量之比为________ ;
(3)写出Z的稀溶液与Ba(OH)2溶液发生化学反应的离子方程式___________________________ ;
(4)Na2S2O3是重要的化工原料.从氧化还原反应的角度分析,下列制备Na2S2O3的方案理论上可行的是________ (填代号);
a.Na2S+S b.Na2SO3+S c.SO2+Na2SO4 d.Na2SO3+Na2SO4
(5)已知Na2SO3能被K2Cr2O7氧化为Na2SO4则24mL 0.05mol•L﹣1的Na2SO3溶液与 20mL 0.02mol•L﹣1的K2Cr2O7溶液恰好反应时,Cr元素在还原产物中的化合价为_______ 。

(1)从硫元素化合价变化的角度分析,图中既有氧化性又有还原性的化合物有
(2)将X与Y混合,可生成S单质(淡黄色沉淀)。该反应的化学方程式为
(3)写出Z的稀溶液与Ba(OH)2溶液发生化学反应的离子方程式
(4)Na2S2O3是重要的化工原料.从氧化还原反应的角度分析,下列制备Na2S2O3的方案理论上可行的是
a.Na2S+S b.Na2SO3+S c.SO2+Na2SO4 d.Na2SO3+Na2SO4
(5)已知Na2SO3能被K2Cr2O7氧化为Na2SO4则24mL 0.05mol•L﹣1的Na2SO3溶液与 20mL 0.02mol•L﹣1的K2Cr2O7溶液恰好反应时,Cr元素在还原产物中的化合价为
您最近一年使用:0次
17-18高三上·北京·期中
名校
解题方法
3 . 下列事实、离子方程式及其对应关系均正确的是
| A.铁溶于稀硝酸,溶液变为浅绿色:Fe+4H++NO3-=Fe3++NO↑+2H2O |
| B.向淀粉碘化钾溶液中滴加稀硫酸,在空气中放置一段时间后溶液变蓝:4H++4I-+O2=2I2+2H2O |
C.向 溶液中滴加少量浓 溶液中滴加少量浓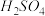 ,溶液变为黄色:Cr2O72-(橙色)+H2O ,溶液变为黄色:Cr2O72-(橙色)+H2O 2CrO42-(黄色)+2H+ 2CrO42-(黄色)+2H+ |
D.向水杨酸(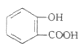 )中滴加 )中滴加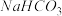 溶液,放出无色气体: 溶液,放出无色气体: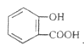 +2HCO3-→ +2HCO3-→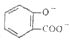 +2CO2↑+2H2O +2CO2↑+2H2O |
您最近一年使用:0次
10-11高三上·河北唐山·期中
4 . (1)某学生在实验室做了5个实验
①在铝盐溶液中逐滴加入稀氨水直至过量,
②在明矾溶液中加入NaOH溶液直至过量,
③在强碱性溶液中逐滴加入铝盐溶液直至过量,
④在偏铝酸钠溶液中通入CO2直至过量,
⑤在强酸溶液中逐滴加入偏铝酸钠溶液直至过量。
并根据以上实验画出下列5种图象(纵坐标为沉淀的物质的量,横坐标为溶液中加入物质的量)实验与图象对应关系正确的是:___________ 。
A.①和(a) B.②和(b) C.③和(e) D.④和(c)

(2)已知:氧化性:KMnO4>HNO3;Bi位于周期表中VA,+3价较稳定,NaBiO3溶液为无色。取一定量的Mn(NO3)2溶液依次进行下列实验,现象记录如下。
①滴加适量的NaBiO3溶液,溶液变为紫红色。
②继续滴加适量H2O2,紫红色褪去,并有气泡产生。
③再加入适量的PbO2固体,固体溶解,溶液又变为紫红色。
④最后通入足量的SO2气体,
请回答下列问题:
(a)KMnO4、H2O2、PbO2氧化性由强到弱的顺序为___________________ ;
(b)实验④中的现象为:___________________ ;
(c)实验②③反应的离子方程式分别是:__________ 、____________ 。
①在铝盐溶液中逐滴加入稀氨水直至过量,
②在明矾溶液中加入NaOH溶液直至过量,
③在强碱性溶液中逐滴加入铝盐溶液直至过量,
④在偏铝酸钠溶液中通入CO2直至过量,
⑤在强酸溶液中逐滴加入偏铝酸钠溶液直至过量。
并根据以上实验画出下列5种图象(纵坐标为沉淀的物质的量,横坐标为溶液中加入物质的量)实验与图象对应关系正确的是:
A.①和(a) B.②和(b) C.③和(e) D.④和(c)

(2)已知:氧化性:KMnO4>HNO3;Bi位于周期表中VA,+3价较稳定,NaBiO3溶液为无色。取一定量的Mn(NO3)2溶液依次进行下列实验,现象记录如下。
①滴加适量的NaBiO3溶液,溶液变为紫红色。
②继续滴加适量H2O2,紫红色褪去,并有气泡产生。
③再加入适量的PbO2固体,固体溶解,溶液又变为紫红色。
④最后通入足量的SO2气体,
请回答下列问题:
(a)KMnO4、H2O2、PbO2氧化性由强到弱的顺序为
(b)实验④中的现象为:
(c)实验②③反应的离子方程式分别是:
您最近一年使用:0次
14-15高三上·北京朝阳·期末
名校
5 . 下列事实、离子方程式及其对应关系均正确的是( )
| A.铁溶于稀硝酸,溶液变为浅绿色:Fe+4H++NO3-=== Fe3++NO↑+2H2O |
B.向K2Cr2O7溶液中滴加少量浓H2SO4,溶液变为黄色:Cr2O72-+H2O 2CrO42-+2H+ 2CrO42-+2H+ |
| C.向淀粉碘化钾溶液中滴加稀硫酸,在空气中放置一段时间后溶液变蓝:4H++4I+O2 === 2I2+2H2O |
D.向水杨酸( )中滴加NaHCO3溶液,放出无色气体: )中滴加NaHCO3溶液,放出无色气体: +2HCO3- +2HCO3- 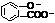 +2CO2↑+2H2O +2CO2↑+2H2O |
您最近一年使用:0次
2016-12-09更新
|
662次组卷
|
4卷引用:2014届北京市朝阳区高三上学期期末考试化学试卷
(已下线)2014届北京市朝阳区高三上学期期末考试化学试卷(已下线)2014届山西省山大附中高三下学期第一次月考化学试卷【全国百强校】北京市北京师范大学附属中学2017-2018学年高二下学期期末考试化学试题江西省南康中学2018-2019学年高二下学期期中考试化学试题
6 . 下列实验“操作和现象”与“结论”对应关系正确的是
| 选项 | 操作和现象 | 结论 |
| A | CH4和Cl2混合于试管中光照,颜色逐渐褪去 | 二者发生了化合反应 |
| B | 微热滴有2滴酚酞的饱和NaHCO3溶液,溶液颜色加深 | NaHCO3受热分解生成了Na2CO3 |
| C | 向淀粉溶液中加入20%的硫酸,加热几分钟,冷却后再加入银氨溶液,水浴,没有银镜生成 | 淀粉没发生水解 |
| D | 向装有Fe(NO3)2溶液的试管中加入稀硫酸,观察到试管口有红棕色气体产生 | 酸性环境下,NO3-被Fe2+还原为NO,NO遇氧气生成NO2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7 . 用四种溶液进行实验,下表中“操作及现象”与“溶液”对应关系错误的是
| 选项 | 操作及现象 | 溶液 |
| A | 通入CO2,溶液变浑浊 | 饱和Na2CO3溶液 |
| B | 通入CO2,溶液变浑浊,继续通CO2至过量,浑浊消失 | Na2SiO3溶液 |
| C | 通入CO2,溶液变浑浊,继续通CO2至过量,浑浊消失,再加入足量NaOH溶液,又变浑浊 | 澄清石灰水 |
| D | 通入CO2,溶液变浑浊,再加入品红溶液,红色褪去 | Ca(ClO)2溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
8 . 下表中对应关系错误的是
| A | NaCl=Na++Cl- NH3•H2O⇌NH4++OH- | 均属于电离方程式 |
| B | Ba2++SO42-=BaSO4 HCO3-+OH-=CO32-+H2O | 均可表示一类反应 |
| C | SO2使酸性高锰酸钾溶液褪色; SO2使碱性酚酞溶液褪色 | 均属于SO2的同一性质 |
| D | Cl2+2NaOH=NaClO+NaCl+ H2O;3S+6NaOH=2Na2S+Na2SO3+3H2O | Cl2和S在反应中即作氧化剂又作还原剂 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2015-01-15更新
|
145次组卷
|
4卷引用:2015届山东省高密市高三12月检测理综化学试卷
解题方法
9 . 化合物 含有三种元素,其中两种为非金属元素,且原子个数比为
含有三种元素,其中两种为非金属元素,且原子个数比为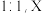 不溶于水,能溶于强酸。某研究小组为探究其组成和性质,设计并完成了如下实验。
不溶于水,能溶于强酸。某研究小组为探究其组成和性质,设计并完成了如下实验。
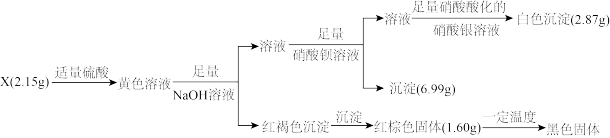
(1)写出红棕色固体的一种用途___________ 。
(2) 的化学式是
的化学式是___________ 。
(3)写出检验黄色溶液中金属阳离子的实验操作:___________ 。
(4)黄色溶液中加入铜片,铜片表面被腐蚀,对应的离子方程式是___________ 。
 含有三种元素,其中两种为非金属元素,且原子个数比为
含有三种元素,其中两种为非金属元素,且原子个数比为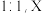 不溶于水,能溶于强酸。某研究小组为探究其组成和性质,设计并完成了如下实验。
不溶于水,能溶于强酸。某研究小组为探究其组成和性质,设计并完成了如下实验。
(1)写出红棕色固体的一种用途
(2)
 的化学式是
的化学式是(3)写出检验黄色溶液中金属阳离子的实验操作:
(4)黄色溶液中加入铜片,铜片表面被腐蚀,对应的离子方程式是
您最近一年使用:0次
名校
10 . 已知A为淡黄色固体,T、R为两种常见的用途很广的金属单质,D是具有磁性的黑色晶体。他们之间有如图转化关系:
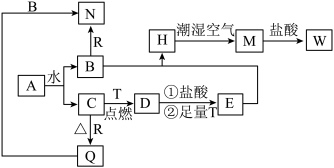
(1)写出下列反应离子方程式:
①B+R:_______ ,
②灵敏检验W中阳离子的原理:________ ,
③D→E:________ ,
④H→M:________ 。
(2)实验室保存E溶液时需向其中加入铁粉,原因为:________ (结合离子方程式说明)。
(3)将B溶液加入铵明矾[NH4Al(SO4)2]溶液至生成的沉淀全部溶解的离子方程式为:_______ 。
(4)现有一定量的RCl3和TCl3混合溶液,已知其中R3+、T3+的物质的量之和为0.10mol,若向此溶液中加入170mL2mol/L的NaOH溶液,设R3+物质的量与总物质的量(0.10mol)的比值为x,则当x=0.4时,沉淀的物质的量为________ mol。请在图中画出沉淀总量(y)随x(0→1.0)的变化曲线________ 。
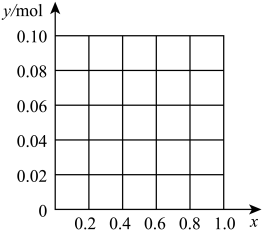

(1)写出下列反应离子方程式:
①B+R:
②灵敏检验W中阳离子的原理:
③D→E:
④H→M:
(2)实验室保存E溶液时需向其中加入铁粉,原因为:
(3)将B溶液加入铵明矾[NH4Al(SO4)2]溶液至生成的沉淀全部溶解的离子方程式为:
(4)现有一定量的RCl3和TCl3混合溶液,已知其中R3+、T3+的物质的量之和为0.10mol,若向此溶液中加入170mL2mol/L的NaOH溶液,设R3+物质的量与总物质的量(0.10mol)的比值为x,则当x=0.4时,沉淀的物质的量为

您最近一年使用:0次



