名校
解题方法
1 . 下列各组离子中,在给定的环境中一定能大量共存的是
A.能使甲基橙变红的溶液:S2-、 、 、 、Na+ 、Na+ |
B.常温下,由水电离的c(H+)=10-12的溶液中:Be2+、 、K+、Cl- 、K+、Cl- |
C.在水溶液中: 、 、 、Ba2+、F- 、Ba2+、F- |
D.在漂白液中:OH-、Rb+、 、 、 |
您最近一年使用:0次
名校
解题方法
2 . 室温下,经过指定操作后,可得到无色澄清溶液的是
A.含 、 、 、 、 、 、 的溶液中,加入足量 的溶液中,加入足量 溶液 溶液 |
B.含 、 、 、 、 、 、 的溶液中,加入足量浓氨水 的溶液中,加入足量浓氨水 |
C.含 、 、 、 、 、 、 的溶液中,加入少量 的溶液中,加入少量 溶液 溶液 |
D.含 、 、 、 、 、 、 的溶液中,通入足量 的溶液中,通入足量 气体 气体 |
您最近一年使用:0次
解题方法
3 . 常温下,下列说法正确的是
A. 的溶液中: 的溶液中: 、 、 、 、 、 、 可以大量共存 可以大量共存 |
B.将均为 的盐酸和醋酸溶液等体积混合, 的盐酸和醋酸溶液等体积混合, 电离程度增大 电离程度增大 |
C.浓度均为0.1mol/L的 和NaF两溶液中阴离子: 和NaF两溶液中阴离子: |
D.分别向等体积AgCl和AgI的饱和溶液中加入足量 固体,生成沉淀质量AgCl大 固体,生成沉淀质量AgCl大 |
您最近一年使用:0次
名校
4 . Ⅰ.完成下列问题
(1)医院里医生给“病人”做心电图时,在仪器与皮肤接触部位擦的一种电解质溶液是_______
(2)把0.05molBa(OH)2固体加入100mL下列液体中,溶液的导电能力明显减弱的是_______
(3)有关溶液中所含离子的检验,下列判断正确的是_______
(4)下列关于强电解质与弱电解质的说法正确的是_______
(5)能用离子方程式2H++CO =CO2↑+H2O表示的是
=CO2↑+H2O表示的是
(6)下列离子方程式中正确的是_______
(7)在酸性溶液中能大量共存且溶液为无色透明的离子组是_______
Ⅱ.有9种物质:①液态氯化氢②乙醇③熔融的KNO3④Cu⑤Na2O固体⑥氨水⑦NaHCO3溶液⑧无水醋酸⑨NaOH溶液。
(8)属于电解质的是___________ ;属于非电解质的有___________ 。
(9)写出⑧在水溶液中的电离方程式___________ 。
(10)写出⑨在水溶液中的电离方程式___________ 。
(11)已知亚磷酸H3PO3是二元弱酸,其与足量⑨反应后的产物为水和___________ 。
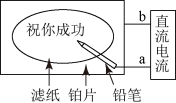
(12)以氯化钠为原料设计了“黑笔写红字”的趣味实验。滤纸先用氯化钠、无色酚酞的混合液浸湿,然后平铺在一块铂片上,b端与铂片连接,a端与铅笔笔芯连接。接通电源后,用铅笔在滤纸上写字,会出现红色字迹。下列叙述正确的是________
(1)医院里医生给“病人”做心电图时,在仪器与皮肤接触部位擦的一种电解质溶液是_______
| A.氯化钠 | B.医用酒精 | C.葡萄糖 | D.碘酒 |
(2)把0.05molBa(OH)2固体加入100mL下列液体中,溶液的导电能力明显减弱的是_______
| A.水 | B.1mol·L-1MgCl2溶液 |
| C.1mol·L-1醋酸溶液 | D.0.5mol·L-1 H2SO4溶液 |
(3)有关溶液中所含离子的检验,下列判断正确的是_______
A.滴加BaCl2溶液,有白色沉淀生成,则原溶液中一定含有SO |
B.滴加盐酸,生成能使澄清石灰水变浑浊的气体,则原溶液中一定含有CO |
| C.滴加碳酸钠溶液产生白色沉淀,再加盐酸沉淀消失,则原溶液中一定含有Ba2+ |
| D.用某溶液做焰色反应时火焰为黄色,则该溶液中一定有钠元素,可能还有钾元素 |
(4)下列关于强电解质与弱电解质的说法正确的是_______
| A.强电解质溶液中不存在溶质分子,弱电解质溶液中只存在溶质分子 |
| B.强电解质在水中的溶解度大于弱电解质在水中的溶解度 |
| C.强电解质溶液的导电能力比弱电解质溶液强 |
| D.强电解质在水中全部电离,弱电解质在水中部分电离 |
(5)能用离子方程式2H++CO
 =CO2↑+H2O表示的是
=CO2↑+H2O表示的是| A.H2SO4和Na2CO3 | B.HCl和BaCO3 |
| C.CH3COOH和Na2CO3 | D.HI和NaHCO3 |
(6)下列离子方程式中正确的是_______
| A.Fe与稀硫酸的反应:2Fe+6H+=Fe3++3H2↑ |
B.硫酸钠与氯化钡浴液混合:SO +Ba2+=BaSO4↓ +Ba2+=BaSO4↓ |
| C.硝酸滴在石灰石上:CaCO3+2H+=Ca2++H2CO3 |
D.氧化铜与硫酸混合:Cu2++SO =CuSO4 =CuSO4 |
(7)在酸性溶液中能大量共存且溶液为无色透明的离子组是_______
A.K+、MnO 、Na+、Cl- 、Na+、Cl- | B.K+、Na+、NO 、SO 、SO |
C.Ba2+、Na+、NO 、SO 、SO | D.Mg2+、Na+、Cl-、SO |
Ⅱ.有9种物质:①液态氯化氢②乙醇③熔融的KNO3④Cu⑤Na2O固体⑥氨水⑦NaHCO3溶液⑧无水醋酸⑨NaOH溶液。
(8)属于电解质的是
(9)写出⑧在水溶液中的电离方程式
(10)写出⑨在水溶液中的电离方程式
(11)已知亚磷酸H3PO3是二元弱酸,其与足量⑨反应后的产物为水和
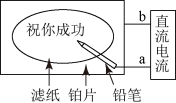
(12)以氯化钠为原料设计了“黑笔写红字”的趣味实验。滤纸先用氯化钠、无色酚酞的混合液浸湿,然后平铺在一块铂片上,b端与铂片连接,a端与铅笔笔芯连接。接通电源后,用铅笔在滤纸上写字,会出现红色字迹。下列叙述正确的是________
| A.b极发生还原反应 |
| B.铂片端作阴极 |
| C.铅笔端有少量的氯气产生 |
| D.a处是负极 |
您最近一年使用:0次
5 . 化学是一门实验的科学,滴定法是一种常用的化学定量分析的方法。室温下,用 溶液分别滴定体积均为20.00mL、浓度均为
溶液分别滴定体积均为20.00mL、浓度均为 的盐酸和醋酸溶液,得到滴定过程中溶液的pH随加入NaOH溶液体积而变化的两条滴定曲线。
的盐酸和醋酸溶液,得到滴定过程中溶液的pH随加入NaOH溶液体积而变化的两条滴定曲线。
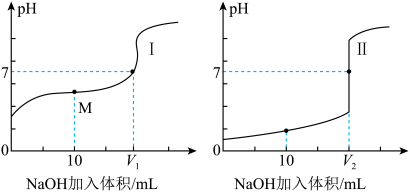
(1)滴定醋酸溶液的曲线是___________ 。(填“Ⅰ”或“Ⅱ”)。
(2)若采用氨水滴定醋酸,写出氨水与醋酸反应的离子反应方程式___________ 。
(3)滴定开始前,三种溶液中由水电离出的 最大的是
最大的是______ 。
A. 溶液 B.
溶液 B. 盐酸 C.
盐酸 C. 醋酸
醋酸
(4)该 溶液的pH为
溶液的pH为______ ;给该溶液加热,pH______ (填“变大”“变小”或“不变”)。
(5)在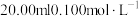 的盐酸中,滴加
的盐酸中,滴加 溶液后,此时溶液的pH=
溶液后,此时溶液的pH=___________ 。
(6)取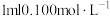 的盐酸稀释1000倍后,溶液pH=
的盐酸稀释1000倍后,溶液pH=___________ ,此时水电离出的 浓度为
浓度为___________ 。
(7)下列离子一定能大量共存的是___________。
(8)下列叙述正确的是___________。
(9)下列有关实验的说法,正确的是___________。
 溶液分别滴定体积均为20.00mL、浓度均为
溶液分别滴定体积均为20.00mL、浓度均为 的盐酸和醋酸溶液,得到滴定过程中溶液的pH随加入NaOH溶液体积而变化的两条滴定曲线。
的盐酸和醋酸溶液,得到滴定过程中溶液的pH随加入NaOH溶液体积而变化的两条滴定曲线。
(1)滴定醋酸溶液的曲线是
(2)若采用氨水滴定醋酸,写出氨水与醋酸反应的离子反应方程式
(3)滴定开始前,三种溶液中由水电离出的
 最大的是
最大的是A.
 溶液 B.
溶液 B. 盐酸 C.
盐酸 C. 醋酸
醋酸(4)该
 溶液的pH为
溶液的pH为(5)在
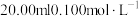 的盐酸中,滴加
的盐酸中,滴加 溶液后,此时溶液的pH=
溶液后,此时溶液的pH=(6)取
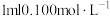 的盐酸稀释1000倍后,溶液pH=
的盐酸稀释1000倍后,溶液pH= 浓度为
浓度为(7)下列离子一定能大量共存的是___________。
A.甲基橙呈黄色的溶液中: 、 、 、 、 、 、 |
B.加入铝粉后产生大量氢气的溶液中: 、 、 、 、 、 、 |
C.石蕊呈蓝色的溶液中: 、 、 、 、 、 、 |
D.pH=1的溶液中: 、 、 、 、 、 、 |
(8)下列叙述正确的是___________。
A.无论是纯水,还是酸性、碱性或中性稀溶液,在常温下其 |
B.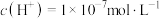 的溶液一定是中性溶液 的溶液一定是中性溶液 |
C.向水中加入少量固体 ,水的电离平衡逆向移动, ,水的电离平衡逆向移动, 减小 减小 |
D.将水加热, 增大,pH不变 增大,pH不变 |
(9)下列有关实验的说法,正确的是___________。
| A.测定HClO溶液pH时,用玻璃棒蘸取溶液,点在干燥pH试纸上 |
| B.等体积、等pH的硫酸与醋酸溶液分别与足量锌反应,醋酸产生的氢气多 |
| C.等体积、等浓度的盐酸和醋酸分别与相同大小的锌粒反应,醋酸初始反应速率快 |
| D.使用pH试纸测定溶液的pH时,若先润湿,则测得溶液的pH一定有误差 |
您最近一年使用:0次
名校
解题方法
6 . 无色溶液A中各离子浓度均相同,且溶液A中只可能含有表中的若干种离子:
分别取溶液A进行如下实验:
实验i.向50.0mL溶液A中加入足量稀盐酸,共收集到0.56L气体a。
实验ⅱ.向另一份50.0mL溶液A中加入足量碳酸钠溶液,产生白色沉淀b,过滤,洗涤、干燥,测得白色沉淀的质量为2.5g。
实验ⅲ.用洁净的铂丝蘸取溶液A在酒精灯上灼烧,观察到火焰呈黄色。
注:①产生的气体全部逸出且所测的体积均已换算成标准状况;
②水自身电离出的微量的离子忽略不计。
试回答下列问题:
(1)根据溶液颜色可知溶液A中不含有_______ (填离子符号);实验i中生成的气体a为_______ (填化学式),收集到的气体a的总质量为_______ g。
(2)实验ⅱ中生成沉淀的离子方程式为_______ ;过滤时需要用到的玻璃仪器有烧杯、_______ 。
(3)由实验Ⅲ中的现象可知溶液A中含有_______ (填离子符号,下同);通过实验可知该溶液中含有的离子有_______ ,每种离子的浓度均为_______ mol∙L-1。
| 阳离子 | K+、Ca2+、Na+、Cu2+ |
| 阴离子 |  、 、 、 、 、Cl- 、Cl- |
实验i.向50.0mL溶液A中加入足量稀盐酸,共收集到0.56L气体a。
实验ⅱ.向另一份50.0mL溶液A中加入足量碳酸钠溶液,产生白色沉淀b,过滤,洗涤、干燥,测得白色沉淀的质量为2.5g。
实验ⅲ.用洁净的铂丝蘸取溶液A在酒精灯上灼烧,观察到火焰呈黄色。
注:①产生的气体全部逸出且所测的体积均已换算成标准状况;
②水自身电离出的微量的离子忽略不计。
试回答下列问题:
(1)根据溶液颜色可知溶液A中不含有
(2)实验ⅱ中生成沉淀的离子方程式为
(3)由实验Ⅲ中的现象可知溶液A中含有
您最近一年使用:0次
名校
解题方法
7 . 某工业废水仅含下表中的某些离子(不考虑水电离产生的 和
和 )。
)。
甲同学欲探究废水的组成,进行如下实验:
Ⅰ.取 溶液,滴加一滴氨水有沉淀生成,且离子种类不变。
溶液,滴加一滴氨水有沉淀生成,且离子种类不变。
Ⅱ.取 溶液加入过量盐酸,无气体和沉淀生成。
溶液加入过量盐酸,无气体和沉淀生成。
Ⅲ.取 溶液,滴加过量
溶液,滴加过量 后,过滤、洗涤、干燥得到
后,过滤、洗涤、干燥得到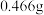 沉淀,滴加足量
沉淀,滴加足量 ,得
,得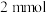 沉淀。
沉淀。
Ⅳ.取 溶液,加入过量
溶液,加入过量 溶液并加热,得到标准状况下
溶液并加热,得到标准状况下 气体。
气体。
请回答下列问题:
(1)以下物质属于电解质的是___________(填字母)。
(2)根据上述信息推断一定存在的阳离子有___________ ,阴离子有___________ 。
(3)实验Ⅰ的现象为___________ 。
(4)实验Ⅲ中发生反应的离子方程式有___________ 、___________ 。
(5)原溶液中浓度最大和最小的离子的物质的量浓度是_______  ,
,_________  。
。
(6)取 溶液,通入
溶液,通入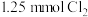 ,对应离子方程式为
,对应离子方程式为___________ 。
 和
和 )。
)。| 阳离子 |  |  |  |  |
| 阴离子 |  |  |  |  |
Ⅰ.取
 溶液,滴加一滴氨水有沉淀生成,且离子种类不变。
溶液,滴加一滴氨水有沉淀生成,且离子种类不变。Ⅱ.取
 溶液加入过量盐酸,无气体和沉淀生成。
溶液加入过量盐酸,无气体和沉淀生成。Ⅲ.取
 溶液,滴加过量
溶液,滴加过量 后,过滤、洗涤、干燥得到
后,过滤、洗涤、干燥得到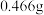 沉淀,滴加足量
沉淀,滴加足量 ,得
,得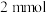 沉淀。
沉淀。Ⅳ.取
 溶液,加入过量
溶液,加入过量 溶液并加热,得到标准状况下
溶液并加热,得到标准状况下 气体。
气体。请回答下列问题:
(1)以下物质属于电解质的是___________(填字母)。
| A.氨气 | B.氨水 | C.液氨 | D.一水合氨 |
(3)实验Ⅰ的现象为
(4)实验Ⅲ中发生反应的离子方程式有
(5)原溶液中浓度最大和最小的离子的物质的量浓度是
 ,
, 。
。(6)取
 溶液,通入
溶液,通入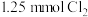 ,对应离子方程式为
,对应离子方程式为
您最近一年使用:0次
名校
解题方法
8 . 水的电离平衡曲线如图所示,下列说法正确的是
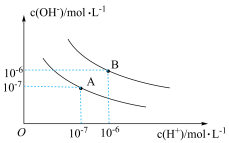

| A.A点温度大于25℃,B点温度25℃ |
B.B点 ,溶液为酸性 ,溶液为酸性 |
| C.A点温度下,在水中加入少量的盐可能抑制水的电离 |
D.A点温度下,由水电离产生的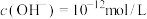 的溶液中: 的溶液中: 、 、 、 、 、 、 可能共存 可能共存 |
您最近一年使用:0次
2023-12-25更新
|
190次组卷
|
2卷引用:湖北省武汉市东华中师范大学第一附属中学2023-2024学年高二上学期11月期中化学试题
9 . 下列说法正确的是
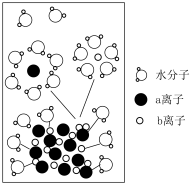

A.上图为 固体溶解并形成水合离子的示意图:a离子为 固体溶解并形成水合离子的示意图:a离子为 ,b离子为 ,b离子为 |
B. 在熔融状态下的电离方程式为: 在熔融状态下的电离方程式为: |
C.透明溶液中一定能大量共存的离子: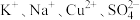 |
D.与铝反应放出 的溶液中可能大量共存的离子: 的溶液中可能大量共存的离子: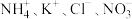 |
您最近一年使用:0次
名校
10 . 某溶液中存在 、
、 、
、 、
、 ,向其中通入以下物质:
,向其中通入以下物质:
①足量 ②少量
②少量 ③足量
③足量 ④足量
④足量 ⑤少量
⑤少量 ⑥足量
⑥足量 后,溶液依旧澄清透明的是
后,溶液依旧澄清透明的是
 、
、 、
、 、
、 ,向其中通入以下物质:
,向其中通入以下物质:①足量
 ②少量
②少量 ③足量
③足量 ④足量
④足量 ⑤少量
⑤少量 ⑥足量
⑥足量 后,溶液依旧澄清透明的是
后,溶液依旧澄清透明的是| A.①②④ | B.①③⑥ | C.②④⑤ | D.③⑤⑥ |
您最近一年使用:0次
2023-12-05更新
|
180次组卷
|
2卷引用:安徽省A10联盟2023-2024学年高三上学期11月期中考试化学试题



