1 . 水合肼 常用于生产火箭燃料,其沸点是
常用于生产火箭燃料,其沸点是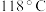 ,受热易分解。尿素法合成水合肼的基本流程如图所示。
,受热易分解。尿素法合成水合肼的基本流程如图所示。

回答下列问题:
(1) 是二元弱碱,在水中的电离方式与氨相似,写出
是二元弱碱,在水中的电离方式与氨相似,写出 第二步电离的方程式:
第二步电离的方程式:___________ 。
(2)已知次氯酸钠与盐酸混合能够生成 ,说明氧化性
,说明氧化性
___________  (填“>”或“<”)。实验发现,
(填“>”或“<”)。实验发现, 与烧碱溶液反应可以生成
与烧碱溶液反应可以生成 ,说明
,说明 与
与 的氧化性强弱关系与
的氧化性强弱关系与___________ 有关。
(3) 强碱性溶液与尿素
强碱性溶液与尿素 水溶液加热制备水合肼的离子方程式为
水溶液加热制备水合肼的离子方程式为___________ 。
(4)常通过减压蒸馏从反应后的混合溶液中获得水合肼,采用该操作的原因是___________ 。
(5)水合肼与硫酸反应生成的盐是农业上重要的杀虫剂、灭菌剂,写出水合肼与硫酸反应生成的碱式盐的化学式:___________ 。
(6)电化学方法制备 的装置如图所示。其中双极膜是阴、阳复合膜,层间的
的装置如图所示。其中双极膜是阴、阳复合膜,层间的 解离成
解离成 和
和 并可分别通过阴、阳膜定向移动。
并可分别通过阴、阳膜定向移动。

①双极膜中产生的___________ (填“ ”或“
”或“ ”)移向多孔铂电极。
”)移向多孔铂电极。
②若电路中转移2mol电子,理论上负极区溶液增重___________ g。
 常用于生产火箭燃料,其沸点是
常用于生产火箭燃料,其沸点是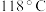 ,受热易分解。尿素法合成水合肼的基本流程如图所示。
,受热易分解。尿素法合成水合肼的基本流程如图所示。
回答下列问题:
(1)
 是二元弱碱,在水中的电离方式与氨相似,写出
是二元弱碱,在水中的电离方式与氨相似,写出 第二步电离的方程式:
第二步电离的方程式:(2)已知次氯酸钠与盐酸混合能够生成
 ,说明氧化性
,说明氧化性
 (填“>”或“<”)。实验发现,
(填“>”或“<”)。实验发现, 与烧碱溶液反应可以生成
与烧碱溶液反应可以生成 ,说明
,说明 与
与 的氧化性强弱关系与
的氧化性强弱关系与(3)
 强碱性溶液与尿素
强碱性溶液与尿素 水溶液加热制备水合肼的离子方程式为
水溶液加热制备水合肼的离子方程式为(4)常通过减压蒸馏从反应后的混合溶液中获得水合肼,采用该操作的原因是
(5)水合肼与硫酸反应生成的盐是农业上重要的杀虫剂、灭菌剂,写出水合肼与硫酸反应生成的碱式盐的化学式:
(6)电化学方法制备
 的装置如图所示。其中双极膜是阴、阳复合膜,层间的
的装置如图所示。其中双极膜是阴、阳复合膜,层间的 解离成
解离成 和
和 并可分别通过阴、阳膜定向移动。
并可分别通过阴、阳膜定向移动。
①双极膜中产生的
 ”或“
”或“ ”)移向多孔铂电极。
”)移向多孔铂电极。②若电路中转移2mol电子,理论上负极区溶液增重
您最近一年使用:0次
名校
解题方法
2 . 某小组通过实验探究氧化还原反应的规律。
已知:氧化还原反应电位传感器可以测量不同溶液的电位值,根据电位值大小可比较物质的氧化性/还原性强弱;数值越大,氧化性越强;数值越小,还原性越强。测得几种物质的电位值如表所示。(注:实验中进行酸化时均用稀硫酸)
根据表中数据,回答下列问题:
(1)浓度相同的下列三种溶液,氧化性由强到弱的顺序为_________ (填序号)。
甲. 乙.酸性
乙.酸性 丙.酸性
丙.酸性
(2)结合上述信息思考:对于 、
、 混合溶液,若控制性氧化
混合溶液,若控制性氧化 而不氧化
而不氧化 ,请提出两种合理的氧化方案:①加入
,请提出两种合理的氧化方案:①加入_________ ;②加入_________ 。
(3)向等浓度的 和
和 混合溶液滴加少量酸性
混合溶液滴加少量酸性 溶液(对应还原产物为
溶液(对应还原产物为 ),发生反应的离子方程式为
),发生反应的离子方程式为_________ 。
(4)已知下列四种氧化剂(均可氧化 )对应的还原产物情况如下:
)对应的还原产物情况如下:
请判断,等物质的量的四种氧化剂分别与足量 作用,得到
作用,得到 最多的是
最多的是___________ 。
(5)造纸、印刷等工业废水中含有大量的硫化物(主要成分为 ),可用如图转化方式除去。
),可用如图转化方式除去。
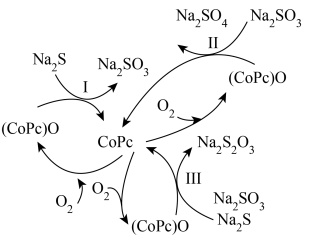
①反应Ⅰ和Ⅱ的转移电子数相等时,还原剂物质的量之比为___________ 。
②在废水处理整个过程中,催化剂为___________ ,氧化剂为___________ 。
③反应Ⅲ中 与
与 等物质的量反应,写出反应的化学方程式
等物质的量反应,写出反应的化学方程式_________________ 。
已知:氧化还原反应电位传感器可以测量不同溶液的电位值,根据电位值大小可比较物质的氧化性/还原性强弱;数值越大,氧化性越强;数值越小,还原性越强。测得几种物质的电位值如表所示。(注:实验中进行酸化时均用稀硫酸)
| 物质 |  |  (酸化) (酸化) |  (酸化) (酸化) |  |  |  |
| 浓度 | 0.10M(M为物质的量浓度的单位) | |||||
电位值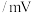 | 171 | 1130 | 603 | 662 | 116 | -361 |
(1)浓度相同的下列三种溶液,氧化性由强到弱的顺序为
甲.
 乙.酸性
乙.酸性 丙.酸性
丙.酸性
(2)结合上述信息思考:对于
 、
、 混合溶液,若控制性氧化
混合溶液,若控制性氧化 而不氧化
而不氧化 ,请提出两种合理的氧化方案:①加入
,请提出两种合理的氧化方案:①加入(3)向等浓度的
 和
和 混合溶液滴加少量酸性
混合溶液滴加少量酸性 溶液(对应还原产物为
溶液(对应还原产物为 ),发生反应的离子方程式为
),发生反应的离子方程式为(4)已知下列四种氧化剂(均可氧化
 )对应的还原产物情况如下:
)对应的还原产物情况如下:| 氧化剂 |  |  |  |  |
| 还原产物 |  |  |  |  |
 作用,得到
作用,得到 最多的是
最多的是(5)造纸、印刷等工业废水中含有大量的硫化物(主要成分为
 ),可用如图转化方式除去。
),可用如图转化方式除去。
①反应Ⅰ和Ⅱ的转移电子数相等时,还原剂物质的量之比为
②在废水处理整个过程中,催化剂为
③反应Ⅲ中
 与
与 等物质的量反应,写出反应的化学方程式
等物质的量反应,写出反应的化学方程式
您最近一年使用:0次
2023-12-04更新
|
380次组卷
|
2卷引用:山东省青岛市莱西市2023-2024学年高一上学期11月期中考试化学试题
名校
解题方法
3 . 虽然化学反应分类的方法不同,但四种基本反应类型和离子反应、氧化还原反应之间也存在着一定的关系,回答下列问题:
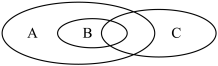
(1)如图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是______ (填字母)。
(2)配平化学方程式,并用单线桥法标出电子转移方向和数目________ 。
______H2O+_____Fe(NO3)3+_____SO2=___FeSO4+_____N2O+_____H2SO4
(3)向FeCl3和BaCl2的酸性混合溶液中通入SO2气体,有白色沉淀生成,此沉淀是_______ (填写化学式)。
(4)配平化学方程式(化学计量数可含x)________ 。
_____Na2Sx+______NaClO+______NaOH=____Na2SO4+_____NaCl+_____H2O
(1)如图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是

(2)配平化学方程式,并用单线桥法标出电子转移方向和数目
______H2O+_____Fe(NO3)3+_____SO2=___FeSO4+_____N2O+_____H2SO4
(3)向FeCl3和BaCl2的酸性混合溶液中通入SO2气体,有白色沉淀生成,此沉淀是
(4)配平化学方程式(化学计量数可含x)
_____Na2Sx+______NaClO+______NaOH=____Na2SO4+_____NaCl+_____H2O
您最近一年使用:0次
4 . 电镀废水中含有的络合态镍(Ⅱ)和甘氨酸铬(Ⅲ)等重金属污染已成为世界性环境问题。常用的处理方法是臭氧法和纳米零价铁法。
I.臭氧法
(1)在废水中通入 ,在紫外光(UV)照射下产生羟基自由基(·OH),氧化分解络合态Ni(Ⅱ)使镍离子游离到废水中,部分机理如下:
,在紫外光(UV)照射下产生羟基自由基(·OH),氧化分解络合态Ni(Ⅱ)使镍离子游离到废水中,部分机理如下:
ⅰ.
ⅱ.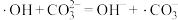
ⅲ.
①写出产生·OH的化学方程式:__________ 。
②加入一定量的 有利于提高氧化效果,原因是
有利于提高氧化效果,原因是____________ 。
Ⅱ.纳米零价铁法
(2)制备纳米零价铁。
将 和
和 溶液在乙醇和水的混合溶液中混合搅拌(
溶液在乙醇和水的混合溶液中混合搅拌( 氛围),充分反应得到纳米零价铁、
氛围),充分反应得到纳米零价铁、 、HCl、NaCl和
、HCl、NaCl和 。写出反应的化学方程式
。写出反应的化学方程式_______________ 。
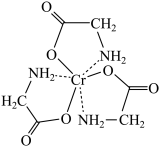
(3)纳米零价铁处理甘氨酸铬。
①甘氨酸铬(结构简式如图)分子中与铬配位的原子为_________ 。
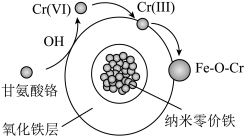
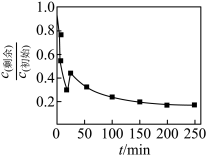
②研究表明:纳米零价铁对有机物的降解通常是产生液相·OH对有机物官能团进行断键,使有机络合态Cr(Ⅲ)被释放到溶液中,同时氧化成无机Cr(Ⅵ)。纳米零价铁对甘氨酸铬的去除机理如图所示:
对初始铬浓度为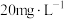 的甘氨酸铬去除率进行研究,总铬去除率随时间的变化如图所示,其可能的原因是
的甘氨酸铬去除率进行研究,总铬去除率随时间的变化如图所示,其可能的原因是____________ 。
I.臭氧法
(1)在废水中通入
 ,在紫外光(UV)照射下产生羟基自由基(·OH),氧化分解络合态Ni(Ⅱ)使镍离子游离到废水中,部分机理如下:
,在紫外光(UV)照射下产生羟基自由基(·OH),氧化分解络合态Ni(Ⅱ)使镍离子游离到废水中,部分机理如下:ⅰ.

ⅱ.
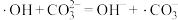
ⅲ.

①写出产生·OH的化学方程式:
②加入一定量的
 有利于提高氧化效果,原因是
有利于提高氧化效果,原因是Ⅱ.纳米零价铁法
(2)制备纳米零价铁。
将
 和
和 溶液在乙醇和水的混合溶液中混合搅拌(
溶液在乙醇和水的混合溶液中混合搅拌( 氛围),充分反应得到纳米零价铁、
氛围),充分反应得到纳米零价铁、 、HCl、NaCl和
、HCl、NaCl和 。写出反应的化学方程式
。写出反应的化学方程式(3)纳米零价铁处理甘氨酸铬。
①甘氨酸铬(结构简式如图)分子中与铬配位的原子为

②研究表明:纳米零价铁对有机物的降解通常是产生液相·OH对有机物官能团进行断键,使有机络合态Cr(Ⅲ)被释放到溶液中,同时氧化成无机Cr(Ⅵ)。纳米零价铁对甘氨酸铬的去除机理如图所示:

对初始铬浓度为
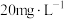 的甘氨酸铬去除率进行研究,总铬去除率随时间的变化如图所示,其可能的原因是
的甘氨酸铬去除率进行研究,总铬去除率随时间的变化如图所示,其可能的原因是
您最近一年使用:0次
名校
解题方法
5 . 化学让生活更美好,各类水处理剂能让水质得到提升达到饮用水的标准。生活中较常见的水处理剂有:氯气、次氯酸钠、漂白粉(主要成分为次氯酸钙)、二氧化氯、明矾、硫酸铁、高铁酸钠等等。
(1)氯气常用于自来水的消毒,请写出舍勒研究软锰矿时发现氯气的化学方程式:___________ 。
(2)氯气能用于制备易于保存、使用方便的漂白液,但若温度过高会发生副反应生成NaCl、NaClO3。请写出在加热时,当NaOH与Cl2反应生成的n(NaClO):n(NaClO3)=5:1时,NaOH与Cl2反应的化学方程式:___________ 。
(3)下列有关水资源及水质净化的说法,不正确的是___________(填序号)。
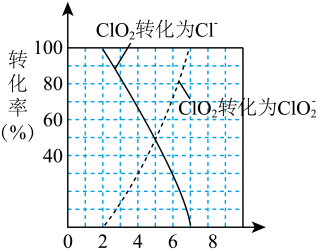
(4)近年来有科学家提出,氯气消毒时,会与水中的有机物发生反应,生成的有机氯化物可能对人体有害。因此,人们已开始研究并试用新的自来水消毒剂,如二氧化氯(ClO2)、臭氧等。ClO2被世界卫生组织(WHO)列为A级高效、安全灭菌消毒剂,将逐渐取代Cl2成为自来水的消毒剂。ClO2气体具有强氧化性,其还原产物ClO 、Cl﹣的转化率与pH关系如图所示。ClO2对污水中S2﹣、CN﹣等也有明显的去除效果,请写出pH≤2时,ClO2与S2﹣反应的离子方程式:
、Cl﹣的转化率与pH关系如图所示。ClO2对污水中S2﹣、CN﹣等也有明显的去除效果,请写出pH≤2时,ClO2与S2﹣反应的离子方程式:___________ 。某工厂污水中含CN﹣amg/L,现用ClO2将CN﹣氧化,生成了两种无毒无害的气体,处理50m3这种污水,至少需要ClO2___________ mol。
(5)高铁酸钠(Na2FeO4)在水中既能消毒杀菌,其产物Fe(OH)3胶体又能净水除去悬浮杂质,是一种理想的水处理剂。如果以单位质量的氧化剂所得到的电子数来表示消毒效率,那么,Cl2、ClO2(pH≤2时)、Na2FeO4三种消毒杀菌剂的消毒效率由大到小的顺序是___________ 。
(1)氯气常用于自来水的消毒,请写出舍勒研究软锰矿时发现氯气的化学方程式:
(2)氯气能用于制备易于保存、使用方便的漂白液,但若温度过高会发生副反应生成NaCl、NaClO3。请写出在加热时,当NaOH与Cl2反应生成的n(NaClO):n(NaClO3)=5:1时,NaOH与Cl2反应的化学方程式:
(3)下列有关水资源及水质净化的说法,不正确的是___________(填序号)。
| A.将自来水煮沸烧开后再饮用更健康、因为能除去残留的Cl2及溶于其中的Cl﹣ |
| B.自来水用于洗涤后得到的含磷污水是很好的肥料,可灌溉庄稼,能直接排放到自然界水体中 |
| C.煤、石油的燃烧和汽车排放的尾气都会引起大气污染,且会出现酸雨等环境问题 |
| D.纳米铁粉可以高效地去除被污染水体中的Pb2+、Cu2+、Cd2+、Hg2+等重金属离子,其本质是纳米铁粉对重金属离子有较强的物理吸附 |
 、Cl﹣的转化率与pH关系如图所示。ClO2对污水中S2﹣、CN﹣等也有明显的去除效果,请写出pH≤2时,ClO2与S2﹣反应的离子方程式:
、Cl﹣的转化率与pH关系如图所示。ClO2对污水中S2﹣、CN﹣等也有明显的去除效果,请写出pH≤2时,ClO2与S2﹣反应的离子方程式:(5)高铁酸钠(Na2FeO4)在水中既能消毒杀菌,其产物Fe(OH)3胶体又能净水除去悬浮杂质,是一种理想的水处理剂。如果以单位质量的氧化剂所得到的电子数来表示消毒效率,那么,Cl2、ClO2(pH≤2时)、Na2FeO4三种消毒杀菌剂的消毒效率由大到小的顺序是

您最近一年使用:0次
解题方法
6 . 配平下列方程式
(1) ;
;________ 。
(2) ;
;________ 。
(1)
 ;
;(2)
 ;
;
您最近一年使用:0次
2022高二上·安徽阜阳·竞赛
解题方法
7 . 化学一直都在发展……
①利用非水体系中的化学反应,可以用来制备无水盐,工业上原来制备无水硝酸铜的过程如下(步骤I得到的是硝酸铜溶液),据此回答:
CuO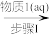 Cu(NO3)2
Cu(NO3)2 Cu(NO3)2·n H2O
Cu(NO3)2·n H2O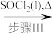 Cu(NO3)2(无水)
Cu(NO3)2(无水)
已知:步骤III的气体产物仅有两种,均呈酸性,其中一种分子量为64
(1)步骤I中加入的物质1(aq)为_______ (填写化学式),步骤III中加入SOCl2的作用是_______ ,写出步骤III发生的化学反应的化学方程式_______ 。
(2)已知若步骤III中不加入SOCl2,直接加热含结晶水的硝酸铜,会生成碱式硝酸铜[Cu(NO3)2·3Cu(OH)2],其原因是硝酸铜发生了_______ (填反应类型),其反应的化学方程式为_______ 。
②现如今化学家们发明了另一种制备方法:
Cu(s) Cu(NO3)2·n N2O4
Cu(NO3)2·n N2O4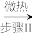 Cu(NO3)2
Cu(NO3)2
已知:在液态N2O4中存在一下自耦电离平衡:N2O4 NO++
NO++ ,步骤I,II均放出有毒气体,两者均为汽车尾气的主要成分
,步骤I,II均放出有毒气体,两者均为汽车尾气的主要成分
(3)试写出步骤I与步骤II的方程式:步骤I_______ ;步骤II_______ 。
(4)该反应的优点(写出一条即可):_______ 。
①利用非水体系中的化学反应,可以用来制备无水盐,工业上原来制备无水硝酸铜的过程如下(步骤I得到的是硝酸铜溶液),据此回答:
CuO
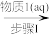 Cu(NO3)2
Cu(NO3)2 Cu(NO3)2·n H2O
Cu(NO3)2·n H2O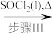 Cu(NO3)2(无水)
Cu(NO3)2(无水)已知:步骤III的气体产物仅有两种,均呈酸性,其中一种分子量为64
(1)步骤I中加入的物质1(aq)为
(2)已知若步骤III中不加入SOCl2,直接加热含结晶水的硝酸铜,会生成碱式硝酸铜[Cu(NO3)2·3Cu(OH)2],其原因是硝酸铜发生了
②现如今化学家们发明了另一种制备方法:
Cu(s)
 Cu(NO3)2·n N2O4
Cu(NO3)2·n N2O4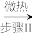 Cu(NO3)2
Cu(NO3)2已知:在液态N2O4中存在一下自耦电离平衡:N2O4
 NO++
NO++ ,步骤I,II均放出有毒气体,两者均为汽车尾气的主要成分
,步骤I,II均放出有毒气体,两者均为汽车尾气的主要成分(3)试写出步骤I与步骤II的方程式:步骤I
(4)该反应的优点(写出一条即可):
您最近一年使用:0次
8 . 书写方程式
(1)硫酸铝和硅酸钠溶液反应的离子方程式_______ 。
(2)酚醛树脂的合成_______ 。
(3)用重铬酸钾和浓盐酸制氯气_______ 。
(4) 和
和 固体混合物在高温下发生反应,放出的气体均为黄绿色(
固体混合物在高温下发生反应,放出的气体均为黄绿色( 为黄绿色)
为黄绿色)_______ 。
(5) 将雌黄铁矿(
将雌黄铁矿(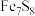 )中的S氧化成
)中的S氧化成
_______ 。
(1)硫酸铝和硅酸钠溶液反应的离子方程式
(2)酚醛树脂的合成
(3)用重铬酸钾和浓盐酸制氯气
(4)
 和
和 固体混合物在高温下发生反应,放出的气体均为黄绿色(
固体混合物在高温下发生反应,放出的气体均为黄绿色( 为黄绿色)
为黄绿色)(5)
 将雌黄铁矿(
将雌黄铁矿(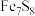 )中的S氧化成
)中的S氧化成
您最近一年使用:0次
解题方法
9 . 卡尔-费休(Karl-Fischer) 法是测定有机溶剂中的微量水含量的经典方法。所用试剂由碘、二氧化硫、吡啶(C5H5N,有机碱,与H+反应生成C5H5NH+)和无水甲醇按一定比例配制而成。该试剂与待测溶剂中的水反应后,产物的含量用库仑滴定法来测定。
(1)该方法的基本原理是利用碘与二氧化硫反应,反应方程式为___________ 。
(2)上述反应在测量条件下,是可逆反应,加入吡啶的作用是___________ 。
(3)加入甲醇可以进一步稳定产物,生成C5H5NHSO4CH3,请写出总反应。的化学方程式:___________ 。。
(4)测定20.0 mL有机溶剂含水量____ 。库仑滴定时,以24.8 mA恒定电流通电302s时达到反应终点(电极反应: 2I-- 2e = I2)。求该有机溶剂的含水量(mg·L-1) ____ 。已知: 1 mol电子的电量为9.65× 104C,电量计算公式Q=It
(1)该方法的基本原理是利用碘与二氧化硫反应,反应方程式为
(2)上述反应在测量条件下,是可逆反应,加入吡啶的作用是
(3)加入甲醇可以进一步稳定产物,生成C5H5NHSO4CH3,请写出总反应。的化学方程式:
(4)测定20.0 mL有机溶剂含水量
您最近一年使用:0次
解题方法
10 . 写出下列反应的方程式
(1)硫代硫酸钠与稀盐酸混合,生成有刺激性气味的气体_______
(2)氯酸钾、硫酸锰与氢氧化钾共熔,生成绿色物质_______
(3)在重铬酸钾溶液中加入少量银离子,生成砖红色沉淀_______
(4)金溶解在王水中_______
(1)硫代硫酸钠与稀盐酸混合,生成有刺激性气味的气体
(2)氯酸钾、硫酸锰与氢氧化钾共熔,生成绿色物质
(3)在重铬酸钾溶液中加入少量银离子,生成砖红色沉淀
(4)金溶解在王水中
您最近一年使用:0次



