1 . 一种二氧化硫催化氧化反应的机理如图所示。下列说法正确的是


| A.过程①中SO2被还原 |
| B.过程②中发生反应的化学方程式为2SO3+V2O4=2VOSO4 |
| C.过程③中氧化剂与还原剂的物质的量之比为1∶2 |
| D.过程①②③均为氧化还原反应 |
您最近一年使用:0次
解题方法
2 . 如图是中学化学中常见物质的转化关系。E为红棕色气体,单质G可被磁铁吸引, 和
和 的浓溶液靠近会出现白烟。
的浓溶液靠近会出现白烟。
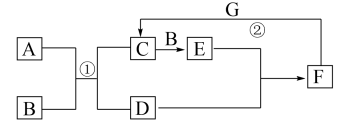
回答下列问题:
(1)D的电子式为_____ ,C的化学式是_____ 。
(2)实验室中常将F的浓溶液保存在_____ 色细口瓶中并置于阴凉处。用化学方程式解释原因______ 。
(3)过量G发生反应②后,向溶液中加入足量氢氧化钠溶液,现象为_____ 。
(4)为防止E污染环境,可用CH4与其反应生成无污染气体和水,写出该反应的化学方程式______ 。
 和
和 的浓溶液靠近会出现白烟。
的浓溶液靠近会出现白烟。
回答下列问题:
(1)D的电子式为
(2)实验室中常将F的浓溶液保存在
(3)过量G发生反应②后,向溶液中加入足量氢氧化钠溶液,现象为
(4)为防止E污染环境,可用CH4与其反应生成无污染气体和水,写出该反应的化学方程式
您最近一年使用:0次
解题方法
3 . Na、K属于碱金属元素,其形成的物质在生活生产中有广泛应用。NaCl不仅可以作调味剂,在工业生产中也占据着重要地位。
(1)写出Na+电子式____ ,比较Na+和Cl-的半径大小____ ,NaCl属于___ 晶体。
(2)NaCl是氯碱工业的原料,此工业可以制取的产品有____ (至少写出2种)。
(3)KIO3常用作食盐中的补碘剂,可用“氯酸钾氧化法”制备,该方法的第一步反应为:______I2+______KClO3+______→______KH(IO3)2+5KCl+3Cl2↑。配平该反应的化学方程式____ 。反应中生成的Cl2可用____ 吸收制备漂粉精。
NaHCO3俗称小苏打,可用于治疗胃酸过多。
(4)有实验小组利用pH传感器探究Na2CO3和NaHCO3的性质,实验过程如表所示。
写出Na2CO3与澄清石灰水反应的离子方程式___ ,OH-未参与该反应的实验证据是____ 。
(5)结合离子方程式说明NaHCO3可用于治疗胃酸过多的原因____ 。胃酸过多易引起胃溃疡,小苏打可用于治疗胃溃疡,如果处于胃溃疡的活动期,医生不建议服用小苏打,请猜测医生不建议的原因____ 。
(1)写出Na+电子式
(2)NaCl是氯碱工业的原料,此工业可以制取的产品有
(3)KIO3常用作食盐中的补碘剂,可用“氯酸钾氧化法”制备,该方法的第一步反应为:______I2+______KClO3+______→______KH(IO3)2+5KCl+3Cl2↑。配平该反应的化学方程式
NaHCO3俗称小苏打,可用于治疗胃酸过多。
(4)有实验小组利用pH传感器探究Na2CO3和NaHCO3的性质,实验过程如表所示。
| 实验操作 | 实验数据 |
 |  |
写出Na2CO3与澄清石灰水反应的离子方程式
(5)结合离子方程式说明NaHCO3可用于治疗胃酸过多的原因
您最近一年使用:0次
名校
解题方法
4 . 下列由实验现象所得结论正确的是
A.向 溶液中滴入稀硫酸酸化的 溶液中滴入稀硫酸酸化的 溶液,溶液由浅绿色变为黄色,证明 溶液,溶液由浅绿色变为黄色,证明 氧化性大于 氧化性大于 |
B.向某无色溶液中滴加1—2滴酚酞试液,一段时间后溶液仍呈无色,证明该溶液的 |
C.常温下将带火星的木条放入浓 加热分解生成的气体中,木条复燃,证明 加热分解生成的气体中,木条复燃,证明 支持燃烧 支持燃烧 |
D.将某气体通入淀粉和 的混合溶液,蓝色褪去,证明该气体具有漂白性 的混合溶液,蓝色褪去,证明该气体具有漂白性 |
您最近一年使用:0次
2024-02-11更新
|
367次组卷
|
2卷引用:山东省济宁市2023-2024学年高三上学期1月期末化学试题
5 . 用废旧硬质刀具(含碳化钨、钴、铁)回收金属钻,工艺流程如图。下列说法错误的是
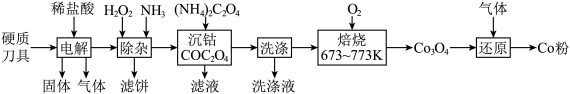

A.“电解”时硬质刀具做阳极,气体为 |
| B.洗涤不充分不影响最终产品的纯度,但会污染环境 |
C.“焙烧”时发生的主要反应为 |
D.还原性: |
您最近一年使用:0次
名校
6 . 羟基氧化铁 为淡黄色固体,简称铁黄,可作颜料。制备铁黄的关键是先制备铁黄晶种,否则只能得到稀薄的、颜色暗淡的色浆,不具备颜料性能。实验室以硫酸亚铁铵为主要原料制备铁黄的实验步骤如下:
为淡黄色固体,简称铁黄,可作颜料。制备铁黄的关键是先制备铁黄晶种,否则只能得到稀薄的、颜色暗淡的色浆,不具备颜料性能。实验室以硫酸亚铁铵为主要原料制备铁黄的实验步骤如下:
 .产品制备及产率计算
.产品制备及产率计算
①制备晶种:称取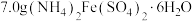 放入三颈烧瓶中,加入
放入三颈烧瓶中,加入 去离子水,恒温水浴加热至
去离子水,恒温水浴加热至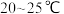 ,搅拌溶解,慢慢滴加
,搅拌溶解,慢慢滴加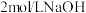 溶液,用
溶液,用 试纸检验至溶液
试纸检验至溶液 为
为 ,停止加碱,观察到出现沉淀并伴随沉淀颜色变化。
,停止加碱,观察到出现沉淀并伴随沉淀颜色变化。
②氧化过程:称取足量 ,加入上述溶液,于
,加入上述溶液,于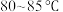 恒温水浴中进行氧化。氧化过程中,边搅拌边不断滴加
恒温水浴中进行氧化。氧化过程中,边搅拌边不断滴加 溶液至
溶液至 为
为 时,停止加热。
时,停止加热。
③洗涤、干燥:用去离子水洗涤生成的固体,抽滤,弃去母液,得到淡黄色固体。将其转入蒸发皿中,在水浴加热条件下烘干,称量,计算产率。
回答下列问题:
(1)用 试纸检验溶液
试纸检验溶液 的操作为
的操作为___________ 。
(2)①中观察到沉淀的颜色变为___________ 色时,证明已经成功制备晶种。
(3)②氧化过程中,发生反应的离子方程式为___________ 。
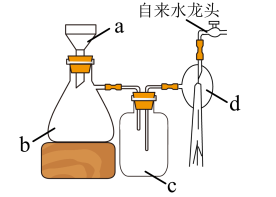
(4)抽滤装置如图,仪器c的作用为___________ ,和普通过滤相比,抽滤的优点有过滤速度更快和___________ 。 .产品纯度测定
.产品纯度测定
铁黄纯度可以通过产品的耗酸量确定。 ,
,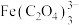 不与稀
不与稀 溶液反应。
溶液反应。
(5)铁黄溶于 标准液的离子方程式为
标准液的离子方程式为___________ 。
(6) 标准液和
标准液和 标准液浓度均为
标准液浓度均为 ,消耗两溶液的体积依次为
,消耗两溶液的体积依次为 ,计算铁黄的纯度为
,计算铁黄的纯度为___________ (列出计算式,不需化简)。
(7)若 溶液过量,会使测定结果
溶液过量,会使测定结果___________ (填“偏大”、“偏小”或“无影响”)。(已知草酸的电离平衡常数: )
)
 为淡黄色固体,简称铁黄,可作颜料。制备铁黄的关键是先制备铁黄晶种,否则只能得到稀薄的、颜色暗淡的色浆,不具备颜料性能。实验室以硫酸亚铁铵为主要原料制备铁黄的实验步骤如下:
为淡黄色固体,简称铁黄,可作颜料。制备铁黄的关键是先制备铁黄晶种,否则只能得到稀薄的、颜色暗淡的色浆,不具备颜料性能。实验室以硫酸亚铁铵为主要原料制备铁黄的实验步骤如下: .产品制备及产率计算
.产品制备及产率计算①制备晶种:称取
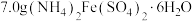 放入三颈烧瓶中,加入
放入三颈烧瓶中,加入 去离子水,恒温水浴加热至
去离子水,恒温水浴加热至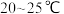 ,搅拌溶解,慢慢滴加
,搅拌溶解,慢慢滴加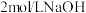 溶液,用
溶液,用 试纸检验至溶液
试纸检验至溶液 为
为 ,停止加碱,观察到出现沉淀并伴随沉淀颜色变化。
,停止加碱,观察到出现沉淀并伴随沉淀颜色变化。②氧化过程:称取足量
 ,加入上述溶液,于
,加入上述溶液,于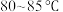 恒温水浴中进行氧化。氧化过程中,边搅拌边不断滴加
恒温水浴中进行氧化。氧化过程中,边搅拌边不断滴加 溶液至
溶液至 为
为 时,停止加热。
时,停止加热。③洗涤、干燥:用去离子水洗涤生成的固体,抽滤,弃去母液,得到淡黄色固体。将其转入蒸发皿中,在水浴加热条件下烘干,称量,计算产率。
回答下列问题:
(1)用
 试纸检验溶液
试纸检验溶液 的操作为
的操作为(2)①中观察到沉淀的颜色变为
(3)②氧化过程中,发生反应的离子方程式为
(4)抽滤装置如图,仪器c的作用为
 .产品纯度测定
.产品纯度测定铁黄纯度可以通过产品的耗酸量确定。

 ,
,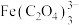 不与稀
不与稀 溶液反应。
溶液反应。(5)铁黄溶于
 标准液的离子方程式为
标准液的离子方程式为(6)
 标准液和
标准液和 标准液浓度均为
标准液浓度均为 ,消耗两溶液的体积依次为
,消耗两溶液的体积依次为 ,计算铁黄的纯度为
,计算铁黄的纯度为(7)若
 溶液过量,会使测定结果
溶液过量,会使测定结果 )
)
您最近一年使用:0次
2024-05-26更新
|
393次组卷
|
3卷引用:2024届黑龙江省哈尔滨师范大学附属中学高三下学期三模化学试题
解题方法
7 . 某化学兴趣小组采用次氯酸钙与稀盐酸反应制取氯气,并探究了氯气的性质。实验装置如图所示,下列说法正确的是
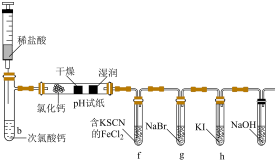
A.b试管中的离子方程式为: |
B.湿润的 试纸先变红后褪色,说明 试纸先变红后褪色,说明 有酸性,同时又有漂白性 有酸性,同时又有漂白性 |
C.f处变红,是因为 被氧化为 被氧化为 , , 遇 遇 溶液变红 溶液变红 |
D.g处变为橙色,h处变为黄色,说明氧化性: |
您最近一年使用:0次
2024-03-26更新
|
412次组卷
|
2卷引用:2024届广东省大亚湾区普通高中毕业年级高三1月份联合模拟考试(一)化学试卷
8 . 通常利用反应: 定性检验
定性检验 ,关于该反应的下列说法中,
,关于该反应的下列说法中,不正确 的是
 定性检验
定性检验 ,关于该反应的下列说法中,
,关于该反应的下列说法中,A. 被氧化 被氧化 | B.每消耗1mol ,转移2mol ,转移2mol |
C. 和 和 的物质的量之比为5∶2 的物质的量之比为5∶2 | D.在该反应的条件下,氧化性: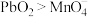 |
您最近一年使用:0次
2023-01-05更新
|
370次组卷
|
4卷引用:北京市东城区2022-2023学年高一上学期期末统一检测化学试卷
解题方法
9 . 金属钌在电子制造、化学工业及催化剂生产等行业中有关键作用,六氯钌酸铵[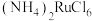 ]是生产金属钌的重要中间产物。一种利用精炼镍阳极泥(主要含金属Ru、Os及Pb等)制备六氯钌酸铵的工业流程如图所示:
]是生产金属钌的重要中间产物。一种利用精炼镍阳极泥(主要含金属Ru、Os及Pb等)制备六氯钌酸铵的工业流程如图所示:
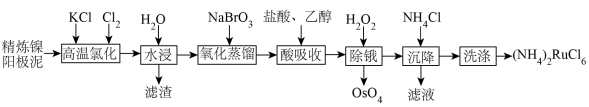
已知:六氯钌酸铵在冷水、乙醇中的溶解度较小。
回答下列问题:
(1)“高温氯化”后得到 、
、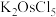 ,
,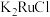 。
。 中Ru元素的化合价为
中Ru元素的化合价为___________ ,生成 的化学方程式为
的化学方程式为___________ 。
(2)“氧化蒸馏”过程中蒸出 、
、 ,生成
,生成 的离子方程式为
的离子方程式为___________ 。
(3)“酸吸收”过程中加入乙醇的作用是___________ 。
(4)“除锇”过程中元素钌化合价不变,溶液的主要成分为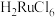 ,溶液中存在
,溶液中存在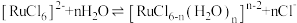
 ,六氯钌酸铵中水含量低,有利于六氯钌酸铵结晶物的粉碎焙烧。为降低六氯钌酸铵中水的含量,可以采用的措施有
,六氯钌酸铵中水含量低,有利于六氯钌酸铵结晶物的粉碎焙烧。为降低六氯钌酸铵中水的含量,可以采用的措施有___________ 。
(5)检验滤液中主要阴离子的实验方法是___________ ,“洗涤”时最合适的试剂为___________ 。
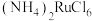 ]是生产金属钌的重要中间产物。一种利用精炼镍阳极泥(主要含金属Ru、Os及Pb等)制备六氯钌酸铵的工业流程如图所示:
]是生产金属钌的重要中间产物。一种利用精炼镍阳极泥(主要含金属Ru、Os及Pb等)制备六氯钌酸铵的工业流程如图所示:
已知:六氯钌酸铵在冷水、乙醇中的溶解度较小。
回答下列问题:
(1)“高温氯化”后得到
 、
、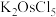 ,
,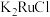 。
。 中Ru元素的化合价为
中Ru元素的化合价为 的化学方程式为
的化学方程式为(2)“氧化蒸馏”过程中蒸出
 、
、 ,生成
,生成 的离子方程式为
的离子方程式为(3)“酸吸收”过程中加入乙醇的作用是
(4)“除锇”过程中元素钌化合价不变,溶液的主要成分为
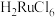 ,溶液中存在
,溶液中存在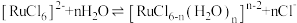
 ,六氯钌酸铵中水含量低,有利于六氯钌酸铵结晶物的粉碎焙烧。为降低六氯钌酸铵中水的含量,可以采用的措施有
,六氯钌酸铵中水含量低,有利于六氯钌酸铵结晶物的粉碎焙烧。为降低六氯钌酸铵中水的含量,可以采用的措施有(5)检验滤液中主要阴离子的实验方法是
您最近一年使用:0次
解题方法
10 . 绿水青山就是金山银山。每一个人都应该自觉地保护自然环境。某次化学实验后,回收的废液中存在Ag+、Ba2+、Cu2+。某同学欲从废液中除去这些离子并分别回收铜、银两种金属,设计如下处理方案:

下列说法正确的是

下列说法正确的是
| A.欲对废液中的三种离子逐一沉淀分离,可以依次加入HCl、H2SO4、NaOH |
| B.检验废液中含有Ba2+可以用Na2SO4溶液 |
| C.由处理方案可知离子的氧化性:Fe3+>Ag+>Cu2+>Fe2+ |
| D.向滤液丙和丁中通入氯气,可重新获得FeCl3溶液,用于循环利用 |
您最近一年使用:0次
2023-08-04更新
|
380次组卷
|
3卷引用:山东省东营市2022-2023学年高一上学期1月期末考试化学试题
山东省东营市2022-2023学年高一上学期1月期末考试化学试题(已下线)专项02 离子反应和氧化还原反应的应用-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(人教版2019必修第一册)山东省临沂第十八中学2023-2024学年高一上学期12月份阶段性测试化学试题



