1 . 化学实验中,如使某步中的有害产物作为另一步的反应物,形成一个循环,就可以减少该有害物质向环境排放。例如:

(1)Na2Cr2O7中Cr元素的化合价是___________ ,该物质属于___________ (填序号)。
①酸 ②碱 ③盐 ④氧化物
(2)在上述转化中,Cr元素化合价不变的步骤是___________ (填序号)。
(3)反应①为:Na2Cr2O7+HCl=NaCl+CrCl3+Cl2↑+H2O(未配平)。其中还原剂为___________ ,若生成2molCl2转移的电子为___________ mol。Na2Cr2O7与Cl2的反应系数比为___________ 。
(4)完成反应④的配平,并用单线桥 标出电子转移的方向和数目。___________

(1)Na2Cr2O7中Cr元素的化合价是
①酸 ②碱 ③盐 ④氧化物
(2)在上述转化中,Cr元素化合价不变的步骤是
(3)反应①为:Na2Cr2O7+HCl=NaCl+CrCl3+Cl2↑+H2O(未配平)。其中还原剂为
(4)完成反应④的配平,并用
您最近一年使用:0次
2 . 科学家舍勒和戴维对氯气的制取和研究做出了重大贡献。某兴趣小组利用所给仪器在实验室制备纯净干燥的氯气。请回答下列问题:
I.实验室制备和收集氯气的常用装置如下图。

(1)利用该装置制备氯气的化学方程式为__________ 。
(2)在实验过程中饱和食盐水的作用是__________ 。
(3)实验装置接口的连接顺序为e→__________ → → → →i→h→g→f。
(4)实验室除了可用二氧化锰和浓盐酸反应制取氯气外,还可以用其他很多方法制取氯气,其中用高锰酸钾和浓盐酸反应制备氯气的化学方程式可表示为:
2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,该反应中HCl的作用是还原性和__________ ,若反应产生5个Cl2,则反应转移的电子数是__________ 。
I.实验室制备和收集氯气的常用装置如下图。

(1)利用该装置制备氯气的化学方程式为
(2)在实验过程中饱和食盐水的作用是
(3)实验装置接口的连接顺序为e→
(4)实验室除了可用二氧化锰和浓盐酸反应制取氯气外,还可以用其他很多方法制取氯气,其中用高锰酸钾和浓盐酸反应制备氯气的化学方程式可表示为:
2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,该反应中HCl的作用是还原性和
您最近一年使用:0次
解题方法
3 . 火箭推进剂中常使用N2H4(肼,结构式为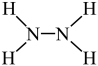 )作为燃烧剂,N2O4作为氧化剂。反应的化学方程式为:2N2H4+N2O4=3N2+4H2O。下列说法
)作为燃烧剂,N2O4作为氧化剂。反应的化学方程式为:2N2H4+N2O4=3N2+4H2O。下列说法不正确 的是
 )作为燃烧剂,N2O4作为氧化剂。反应的化学方程式为:2N2H4+N2O4=3N2+4H2O。下列说法
)作为燃烧剂,N2O4作为氧化剂。反应的化学方程式为:2N2H4+N2O4=3N2+4H2O。下列说法| A.电负性:H<N<O |
| B.肼具有碱性 |
| C.H2O是一种极性分子 |
| D.每生成3molN2时,转移4mol电子 |
您最近一年使用:0次
名校
4 . 高铁酸钾  是一种环保、高效、多功能饮用水处理剂,在水处理过程中,高铁酸钾转化为
是一种环保、高效、多功能饮用水处理剂,在水处理过程中,高铁酸钾转化为  胶体,制备高铁酸钾流程如图所示。
胶体,制备高铁酸钾流程如图所示。

下列叙述
A.反应 的化学方程式是 的化学方程式是 |
B.用  溶液吸收反应 溶液吸收反应  中尾气所得产物可再利用 中尾气所得产物可再利用 |
C.反应  中氧化剂与还原剂的个数比为 中氧化剂与还原剂的个数比为  |
D.用  对饮用水杀菌消毒的同时,生成的 对饮用水杀菌消毒的同时,生成的  胶体吸附杂质净化水 胶体吸附杂质净化水 |
您最近一年使用:0次
2024-03-18更新
|
187次组卷
|
2卷引用:北京师范大学附属中学2023-2024学年高一上学期期末考试化学试卷
5 . 反应3Cl2+6KOH=5KCl+KClO3+3H2O中,还原剂与氧化剂的分子个数之比是
| A.1:1 | B.1:5 | C.5:1 | D.3:2 |
您最近一年使用:0次
解题方法
6 . Mg在CO2中燃烧的反应可用于火星电站发电、人员取暖等,反应的化学方程式为2Mg+CO2 2MgO+C。
2MgO+C。
(1)做氧化剂的物质是___________ ,Mg被___________ (填“氧化”或“还原”),碳元素的化合价___________ (填“升高”或“降低”)。
(2)反应中每生成1 mol MgO,消耗Mg的物质的量是___________ mol,转移电子的物质的量是___________ mol。
 2MgO+C。
2MgO+C。(1)做氧化剂的物质是
(2)反应中每生成1 mol MgO,消耗Mg的物质的量是
您最近一年使用:0次
7 . 已知KClO3+6HCl=KCl+3Cl2↑+3H2O,下列说法不正确 的是
| A.KClO3是氧化剂 | B.Cl2既是氧化产物,也是还原产物 |
| C.该反应中,HCl体现还原性和酸性 | D.氧化剂、还原剂物质的量之比为1:6 |
您最近一年使用:0次
解题方法
8 . 煤的气化是煤炭综合利用的重要途径之一,主要反应为C+H2O(g)  CO+H2。
CO+H2。
(1)该反应中,化合价升高的元素是___________ (填元素符号),氧化剂是___________ (填化学式),氧化产物是___________ (填化学式)。
(2)若消耗了1 mol C,则生成CO的体积约是___________ L(标准状况),转移电子的物质的量为___________ mol。
 CO+H2。
CO+H2。(1)该反应中,化合价升高的元素是
(2)若消耗了1 mol C,则生成CO的体积约是
您最近一年使用:0次
解题方法
9 . 实验室中可用该反应吸收氯气:3Cl2+6KOH=5KCl+ KClO3+3H2O,此反应中氧化剂与还原剂的物质的量之比为
| A.1 :1 | B.3 :2 | C.1 :5 | D.5 :1 |
您最近一年使用:0次
10 . 氨是一种重要的化工原料。氨催化氧化制硝酸过程中涉及如下反应。

(1)作为氧化剂的物质是___________ 。
(2)氮元素的化合价___________ (填“升高”或“降低”)。
(3) 发生
发生___________ (填“氧化”或“还原”)反应。
(4)若反应中消耗了 ,则生成NO的物质的量为
,则生成NO的物质的量为___________ mol,转移电子的物质的量为___________ mol。

(1)作为氧化剂的物质是
(2)氮元素的化合价
(3)
 发生
发生(4)若反应中消耗了
 ,则生成NO的物质的量为
,则生成NO的物质的量为
您最近一年使用:0次



