名校
解题方法
1 . 碳酸锌在工业上用途广泛。利用某种浸锌渣(主要含有 )制备
)制备 的一种流程如下:
的一种流程如下: ;
;
②室温下,部分离子浓度的对数 与
与 的关系如下图所示(其中
的关系如下图所示(其中 和
和 分别代表含铝、含硅和含锌微粒):
分别代表含铝、含硅和含锌微粒):
(1)“焙烧”时,金属硫化物均转化为氧化物,生成的气体 中主要成分是
中主要成分是______ (填化学式)。
(2)“碱浸”后,浸出液中含有金属元素的离子主要是 和
和______ (填离子符号);欲使浸出液中的含锌微粒完全沉淀,应调节 的范围是
的范围是______ 。
(3)浸渣回收银的过程中有配合物 生成,在碱性条件下用
生成,在碱性条件下用 还原该配合物,还原产物为银单质,同时放出N2,该反应中氧化剂与还原剂的物质的量之比为
还原该配合物,还原产物为银单质,同时放出N2,该反应中氧化剂与还原剂的物质的量之比为______ 。
(4)“除杂”时滤渣的主要成分是______ (填化学式)。
(5)“沉锌”时发生反应的离子方程式为______ ;此过程不宜用碳酸钠代替碳酸氢铵,原因是______ 。
 )制备
)制备 的一种流程如下:
的一种流程如下: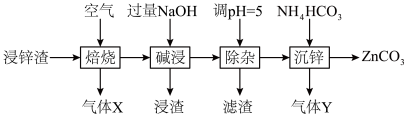
 ;
;②室温下,部分离子浓度的对数
 与
与 的关系如下图所示(其中
的关系如下图所示(其中 和
和 分别代表含铝、含硅和含锌微粒):
分别代表含铝、含硅和含锌微粒):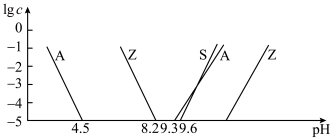
(1)“焙烧”时,金属硫化物均转化为氧化物,生成的气体
 中主要成分是
中主要成分是(2)“碱浸”后,浸出液中含有金属元素的离子主要是
 和
和 的范围是
的范围是(3)浸渣回收银的过程中有配合物
 生成,在碱性条件下用
生成,在碱性条件下用 还原该配合物,还原产物为银单质,同时放出N2,该反应中氧化剂与还原剂的物质的量之比为
还原该配合物,还原产物为银单质,同时放出N2,该反应中氧化剂与还原剂的物质的量之比为(4)“除杂”时滤渣的主要成分是
(5)“沉锌”时发生反应的离子方程式为
您最近一年使用:0次
2024-05-17更新
|
212次组卷
|
2卷引用:云南省罗平第一中学2024年高三二模考试化学试题
2 . 有效去除大气中的 是环境保护的重要课题。
是环境保护的重要课题。
(1)用水吸收 的相关热化学方程式如下:
的相关热化学方程式如下:
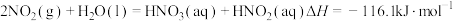
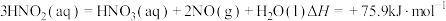
反应 的
的
___________  。
。
(2)用稀硝酸吸收 ,得到
,得到 和
和 的混合溶液,电解该混合溶液可获得较浓的硝酸,写出电解时阳极的电极反应式:
的混合溶液,电解该混合溶液可获得较浓的硝酸,写出电解时阳极的电极反应式:___________ 。( 是弱酸)
是弱酸)
(3)用酸性 水溶液吸收
水溶液吸收 ,吸收过程中存在
,吸收过程中存在 与
与 生成
生成 和
和 的反应,写出该反应的化学方程式:
的反应,写出该反应的化学方程式:___________ 。
(4)在有氧条件下,新型催化剂 能催化
能催化 与
与 反应生成
反应生成 。
。
① 与
与 生成
生成 的反应中,当生成
的反应中,当生成 时,转移的电子数为
时,转移的电子数为___________  。
。
②将一定比例的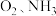 和
和 的混合气体,匀速通入装有催化剂
的混合气体,匀速通入装有催化剂 的反应器中反应(装置见图):
的反应器中反应(装置见图): 的去除率随反应温度的变化曲线如图所示,在
的去除率随反应温度的变化曲线如图所示,在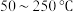 范围内随着温度的升高,
范围内随着温度的升高, 的去除率先迅速上升后缓慢上升的主要原因是
的去除率先迅速上升后缓慢上升的主要原因是___________ 。 (氯的化合价为
(氯的化合价为 价),其原理是
价),其原理是
 接电源的
接电源的___________ (填“正”或“负”)极。
②阳极反应式是___________ 。
 是环境保护的重要课题。
是环境保护的重要课题。(1)用水吸收
 的相关热化学方程式如下:
的相关热化学方程式如下: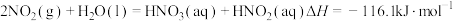
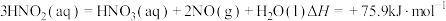
反应
 的
的
 。
。(2)用稀硝酸吸收
 ,得到
,得到 和
和 的混合溶液,电解该混合溶液可获得较浓的硝酸,写出电解时阳极的电极反应式:
的混合溶液,电解该混合溶液可获得较浓的硝酸,写出电解时阳极的电极反应式: 是弱酸)
是弱酸)(3)用酸性
 水溶液吸收
水溶液吸收 ,吸收过程中存在
,吸收过程中存在 与
与 生成
生成 和
和 的反应,写出该反应的化学方程式:
的反应,写出该反应的化学方程式:(4)在有氧条件下,新型催化剂
 能催化
能催化 与
与 反应生成
反应生成 。
。①
 与
与 生成
生成 的反应中,当生成
的反应中,当生成 时,转移的电子数为
时,转移的电子数为 。
。②将一定比例的
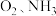 和
和 的混合气体,匀速通入装有催化剂
的混合气体,匀速通入装有催化剂 的反应器中反应(装置见图):
的反应器中反应(装置见图):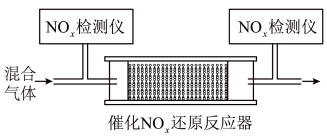
 的去除率随反应温度的变化曲线如图所示,在
的去除率随反应温度的变化曲线如图所示,在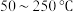 范围内随着温度的升高,
范围内随着温度的升高, 的去除率先迅速上升后缓慢上升的主要原因是
的去除率先迅速上升后缓慢上升的主要原因是
 (氯的化合价为
(氯的化合价为 价),其原理是
价),其原理是
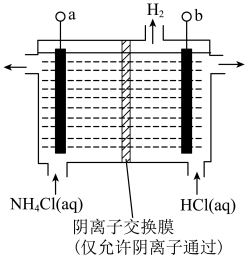
 接电源的
接电源的②阳极反应式是
您最近一年使用:0次
解题方法
3 .  是光电转化材料。利用钛铁矿(主要成分为
是光电转化材料。利用钛铁矿(主要成分为 ,还含有少量
,还含有少量 等杂质)来制备
等杂质)来制备 ,并回收铁制备难溶于水的黄钾铁矾
,并回收铁制备难溶于水的黄钾铁矾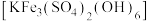 ,制备流程如图,回答下列问题:
,制备流程如图,回答下列问题:
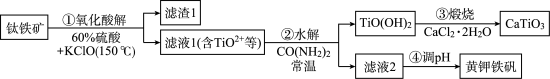
部分原料价格表:
(1) 中Ti的化合价为
中Ti的化合价为_______ 。
(2)步骤①滤渣1的主要成分是_______ ,若氧化酸解的氧化剂用 替代
替代 ,则理论上氧化剂与还原剂物质的量之比为
,则理论上氧化剂与还原剂物质的量之比为_______ ,相同条件下,用 做氧化剂时,其酸解效率较
做氧化剂时,其酸解效率较 低,原因可能是
低,原因可能是_______ 。
(3)已知 在水中能部分水解并有
在水中能部分水解并有 生成,则相关离子方程式为
生成,则相关离子方程式为_______ ;常温下,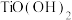
 为
为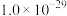 ,滤液1中
,滤液1中 浓度为
浓度为 ,步骤②中要使
,步骤②中要使 水解的转化率达99%,加
水解的转化率达99%,加 时忽略溶液体积变化,则此时溶液的pH应为
时忽略溶液体积变化,则此时溶液的pH应为_______ 。
(4)步骤③反应的化学方程式为_______ ,若在实验室煅烧,用到的实验仪器除了玻璃棒、酒精灯、三脚架及泥三角外,还需要_______ 。
(5)结合信息分析,步骤④调pH最适宜的试剂是_______。
 是光电转化材料。利用钛铁矿(主要成分为
是光电转化材料。利用钛铁矿(主要成分为 ,还含有少量
,还含有少量 等杂质)来制备
等杂质)来制备 ,并回收铁制备难溶于水的黄钾铁矾
,并回收铁制备难溶于水的黄钾铁矾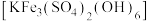 ,制备流程如图,回答下列问题:
,制备流程如图,回答下列问题:
部分原料价格表:
| 物质 | 纯碱(99% ) ) | 氢氧化钾(90% ) ) | 碳酸钾(99% ) ) | 液氨(99.9%) |
| 价格(元/吨) | 1800 | 4000 | 4500 | 25000 |
 中Ti的化合价为
中Ti的化合价为(2)步骤①滤渣1的主要成分是
 替代
替代 ,则理论上氧化剂与还原剂物质的量之比为
,则理论上氧化剂与还原剂物质的量之比为 做氧化剂时,其酸解效率较
做氧化剂时,其酸解效率较 低,原因可能是
低,原因可能是(3)已知
 在水中能部分水解并有
在水中能部分水解并有 生成,则相关离子方程式为
生成,则相关离子方程式为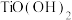
 为
为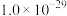 ,滤液1中
,滤液1中 浓度为
浓度为 ,步骤②中要使
,步骤②中要使 水解的转化率达99%,加
水解的转化率达99%,加 时忽略溶液体积变化,则此时溶液的pH应为
时忽略溶液体积变化,则此时溶液的pH应为(4)步骤③反应的化学方程式为
(5)结合信息分析,步骤④调pH最适宜的试剂是_______。
A. | B. | C. | D. |
您最近一年使用:0次
2024-03-28更新
|
111次组卷
|
3卷引用:2024届四川省雅安市高三上学期第一次诊断性考试理综试题
名校
解题方法
4 . 硼化钛强度高、硬度大,广泛应用于机械制造领域;五氟化锑( )是一种高能氟化剂,广泛应用于制药业。工业上以一种含钛的矿渣(主要含
)是一种高能氟化剂,广泛应用于制药业。工业上以一种含钛的矿渣(主要含 、
、 、
、 、
、 、
、 、
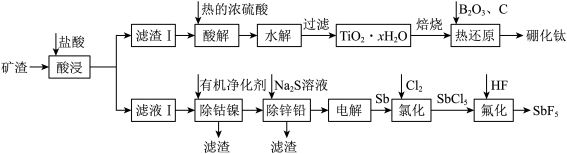
、 )为原料制取硼化钛和五氟化锑的流程如图所示。
)为原料制取硼化钛和五氟化锑的流程如图所示。
已知:① 性质较稳定,加热时可溶于浓硫酸中形成
性质较稳定,加热时可溶于浓硫酸中形成 。
。
②25℃时, 、
、 的
的 分别为
分别为 ,
,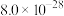 。
。
(1)“水解”步骤中对应的离子方程式为___________ 。为了使水解趋于完全,可采取的措施有___________ 。
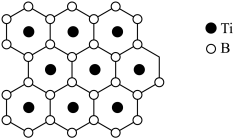
(2)硼化钛有类似石墨的层状结构,硼原子平面和钛原子平面在晶体结构中交替出现,形成二维网状结构,其投影图如下,硼化钛的化学式为___________ 。“热还原”步骤中使用电弧炉高温加热装置(1450~1550℃),每消耗1mol 转移电子数为
转移电子数为___________ 。
(3)“除钴镍”步骤中,有机净化剂的基本组分为大分子立体网格结构的聚合物,其净化原理表示为:
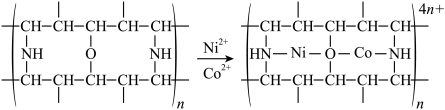
 ,
, 能发生上述转化而
能发生上述转化而 不能,推测可能的原因为
不能,推测可能的原因为___________ 。
(4)已知滤液I中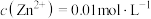 ,
,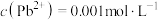 。“除锌铅”步骤中,缓慢滴加稀
。“除锌铅”步骤中,缓慢滴加稀 溶液,先产生的沉淀是(填化学式)
溶液,先产生的沉淀是(填化学式)___________ ;当 、
、 共沉时,先沉淀的物质是否已经沉淀完全(离子浓度
共沉时,先沉淀的物质是否已经沉淀完全(离子浓度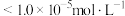 )
)___________ (填“是”或“否”)。
(5)1986年化学家用 和
和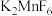 反应,首次实现了用非电解法制取
反应,首次实现了用非电解法制取 ,同时生成
,同时生成 ,已知该过程中
,已知该过程中 接受了一个
接受了一个 的电子对,请写出该反应的化学方程式
的电子对,请写出该反应的化学方程式___________ 。
 )是一种高能氟化剂,广泛应用于制药业。工业上以一种含钛的矿渣(主要含
)是一种高能氟化剂,广泛应用于制药业。工业上以一种含钛的矿渣(主要含 、
、 、
、 、
、 、
、 、
、 )为原料制取硼化钛和五氟化锑的流程如图所示。
)为原料制取硼化钛和五氟化锑的流程如图所示。
已知:①
 性质较稳定,加热时可溶于浓硫酸中形成
性质较稳定,加热时可溶于浓硫酸中形成 。
。②25℃时,
 、
、 的
的 分别为
分别为 ,
,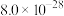 。
。(1)“水解”步骤中对应的离子方程式为
(2)硼化钛有类似石墨的层状结构,硼原子平面和钛原子平面在晶体结构中交替出现,形成二维网状结构,其投影图如下,硼化钛的化学式为
 转移电子数为
转移电子数为
(3)“除钴镍”步骤中,有机净化剂的基本组分为大分子立体网格结构的聚合物,其净化原理表示为:

 ,
, 能发生上述转化而
能发生上述转化而 不能,推测可能的原因为
不能,推测可能的原因为(4)已知滤液I中
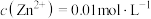 ,
,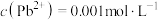 。“除锌铅”步骤中,缓慢滴加稀
。“除锌铅”步骤中,缓慢滴加稀 溶液,先产生的沉淀是(填化学式)
溶液,先产生的沉淀是(填化学式) 、
、 共沉时,先沉淀的物质是否已经沉淀完全(离子浓度
共沉时,先沉淀的物质是否已经沉淀完全(离子浓度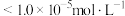 )
)(5)1986年化学家用
 和
和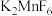 反应,首次实现了用非电解法制取
反应,首次实现了用非电解法制取 ,同时生成
,同时生成 ,已知该过程中
,已知该过程中 接受了一个
接受了一个 的电子对,请写出该反应的化学方程式
的电子对,请写出该反应的化学方程式
您最近一年使用:0次
5 . 低碳经济已成为人们一种新的生活理念,二氧化碳的捕捉和利用是能源领域的一个重要研究方向。回答下列问题:
(1)用 催化加氢可以制取乙烯。
催化加氢可以制取乙烯。 ,该反应体系的能量随反应过程变化关系如图所示,则该反应的
,该反应体系的能量随反应过程变化关系如图所示,则该反应的
_______  (用含a、b的式子表示)。
(用含a、b的式子表示)。

(2)工业上用 和
和 反应合成二甲醚。已知:
反应合成二甲醚。已知:


则
_______  。
。
(3)在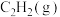 完全燃烧生成
完全燃烧生成 和液态水的反应中,每有
和液态水的反应中,每有 生成时,放出
生成时,放出 的热量,写出
的热量,写出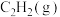 燃烧热的热化学方程式
燃烧热的热化学方程式_______ ;
(4)二氧化碳的捕集、利用是我国能源领域的一个重要战略方向。科学家提出由 制取C的太阳能工艺如图:
制取C的太阳能工艺如图:

①已知“重整系统”发生的反应中 ,则
,则 的化学式为
的化学式为_______ ,“热分解系统”中每转移 电子,需消耗
电子,需消耗
_______ mol。
(5)18-冠-6是冠醚的一种,是有机合成中重要的相转移催化剂,其结构如图A所示,回答下列问题:

18-冠-6中碳原子核外电子有_______ 种不同的空间运动状态,氧原子的杂化类型为_______ 。
(1)用
 催化加氢可以制取乙烯。
催化加氢可以制取乙烯。 ,该反应体系的能量随反应过程变化关系如图所示,则该反应的
,该反应体系的能量随反应过程变化关系如图所示,则该反应的
 (用含a、b的式子表示)。
(用含a、b的式子表示)。
(2)工业上用
 和
和 反应合成二甲醚。已知:
反应合成二甲醚。已知:

则

 。
。(3)在
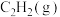 完全燃烧生成
完全燃烧生成 和液态水的反应中,每有
和液态水的反应中,每有 生成时,放出
生成时,放出 的热量,写出
的热量,写出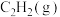 燃烧热的热化学方程式
燃烧热的热化学方程式(4)二氧化碳的捕集、利用是我国能源领域的一个重要战略方向。科学家提出由
 制取C的太阳能工艺如图:
制取C的太阳能工艺如图:
①已知“重整系统”发生的反应中
 ,则
,则 的化学式为
的化学式为 电子,需消耗
电子,需消耗
(5)18-冠-6是冠醚的一种,是有机合成中重要的相转移催化剂,其结构如图A所示,回答下列问题:

18-冠-6中碳原子核外电子有
您最近一年使用:0次
名校
解题方法
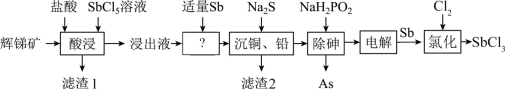
6 . SbCl3用于红外光谱分析以及显像管生产等。工业生产中,以辉锑矿(主要成分为的Sb2S3,还含有As2S3、PbS、CuO和SiO2等)为原料制备SbCl3的工艺流程如下:
②常温下, ,
, ;
;
③溶液中离子浓度小于或等于 mol/L时,认为该离子沉淀完全。
mol/L时,认为该离子沉淀完全。
回答下列问题:
(1)加快辉锑矿“酸浸”的措施有 。
(2)滤渣1中除了S之外,还有__________ 。
(3)浸出液中加入适量Sb的目的是________________________ 。(用化学方程式表示)
(4)已知浸出液中c(Cu2+)=0.01mol/L、c(Pb2+)=0.10mol/L。在沉淀铜、铅过程中,缓慢滴加极稀的硫化钠溶液,先产生的沉淀是__________ (填化学式);常温下,“除铜、铅”时Cu2+和Pb2+均沉淀完全,此时溶液中 不低于
不低于__________ mol/L,Na2S也不宜过多,其原因为__________________ 。
(5)在“除砷”过程中,氧化产物为H3PO4,则该反应中氧化剂、还原剂的物质的量之比为___________ ;已知在“电解”SbCl3溶液时,无气体生成,被氧化的Sb元素与被还原的Sb元素的质量之比为3:2,可在上述流程中循环利用的物质有_________________ 。
②常温下,
 ,
, ;
;③溶液中离子浓度小于或等于
 mol/L时,认为该离子沉淀完全。
mol/L时,认为该离子沉淀完全。回答下列问题:
(1)加快辉锑矿“酸浸”的措施有 。
| A.将辉锑矿粉碎 | B.用酒精灯加热 | C.用玻璃棒搅拌 | D.适当增加酸液浓度 |
(3)浸出液中加入适量Sb的目的是
(4)已知浸出液中c(Cu2+)=0.01mol/L、c(Pb2+)=0.10mol/L。在沉淀铜、铅过程中,缓慢滴加极稀的硫化钠溶液,先产生的沉淀是
 不低于
不低于(5)在“除砷”过程中,氧化产物为H3PO4,则该反应中氧化剂、还原剂的物质的量之比为
您最近一年使用:0次
2024-01-13更新
|
452次组卷
|
5卷引用:2024届四川省成都市第七中学高三上学期一诊模拟考试理科综合试卷
名校
解题方法
7 . 中科院某科研团队发现深海处酸性环境中,在微生物作用下的含硫物质的变化过程如下图所示(已略去部分不含硫物质)。已知: ,下列有关说法错误的是
,下列有关说法错误的是

 ,下列有关说法错误的是
,下列有关说法错误的是
A.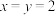 |
B. 中 中 键和 键和 键数目之比为1:2 键数目之比为1:2 |
C.每产生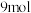  ,步骤④共转移 ,步骤④共转移  |
D.步骤⑥过程可表示为 |
您最近一年使用:0次
2024-01-07更新
|
385次组卷
|
2卷引用:2024届湖南省湘东九校联盟高三上学期第一次联考化学试题
解题方法
8 . 氮化钛(Ti3N4)为金黄色晶体,由于具有令人满意的仿金效果,越来越多地成为黄金的代替品。工业上用钛铁矿(主要成分为FeTiO3,含有少量的SiO2、MgO等杂质)制备氮化钛的工艺流程如下:
部分物质的熔、沸点
请回答下列问题:
(1)滤渣A的主要成分是___________ (化学式)。
(2) 溶液转化为H2TiO3的离子方程式为
溶液转化为H2TiO3的离子方程式为___________ ,加水稀释、加热的目的分别是___________ 。
(3)由滤液丙制备FePO4的过程中,理论上消耗的17%双氧水与H3PO4的质量比是________ 。
(4)TiCl4制取单质Ti涉及的过程中:①由TiCl4→Ti需在严格隔水、Ar气氛围中进行,原因是___________ ;②反应后得到Mg、MgCl2、Ti的混合物,可采用___________ 方法分离得到Ti。
(5)用氧化还原滴定法测定TiOSO4的含量。先取待测钛液10.00mL酸化后加水稀释至100mL,加过量铝粉,充分振荡,使 还原为
还原为 ,发生的离子方程式为
,发生的离子方程式为___________ ;过滤后,取无色滤液20.00mL,向其中滴入2~3滴KSCN溶液作指示剂,用0.1000mol/L 的标准液进行滴定,原理为
的标准液进行滴定,原理为 ,若用去了30.00mL
,若用去了30.00mL 溶液,则待测钛液中TiOSO4的物质的量浓度是
溶液,则待测钛液中TiOSO4的物质的量浓度是___________ mol/L。

部分物质的熔、沸点
| 物质 | TiCl4 | Mg | MgCl2 | Ti |
| 熔点/℃ | -25.0 | 648.8 | 714 | 1667 |
| 沸点/℃ | 136.4 | 1090 | 1412 | 3287 |
(1)滤渣A的主要成分是
(2)
 溶液转化为H2TiO3的离子方程式为
溶液转化为H2TiO3的离子方程式为(3)由滤液丙制备FePO4的过程中,理论上消耗的17%双氧水与H3PO4的质量比是
(4)TiCl4制取单质Ti涉及的过程中:①由TiCl4→Ti需在严格隔水、Ar气氛围中进行,原因是
(5)用氧化还原滴定法测定TiOSO4的含量。先取待测钛液10.00mL酸化后加水稀释至100mL,加过量铝粉,充分振荡,使
 还原为
还原为 ,发生的离子方程式为
,发生的离子方程式为 的标准液进行滴定,原理为
的标准液进行滴定,原理为 ,若用去了30.00mL
,若用去了30.00mL 溶液,则待测钛液中TiOSO4的物质的量浓度是
溶液,则待测钛液中TiOSO4的物质的量浓度是
您最近一年使用:0次
解题方法
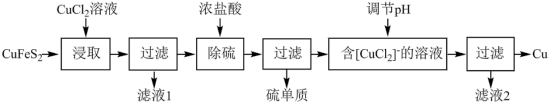
9 . 含铜丰富的自然资源黄铜矿( )冶炼铜的工艺流程如下:
)冶炼铜的工艺流程如下:
已知: 。
。
(1)在元素周期表中,Cu价层电子排布为_______ 。
(2)为提高“浸取”时的反应速率,通常可采用的措施有_______ (答一条即可)。
(3)“除硫”时加入浓盐酸发生反应的离子方程式为_______ 。
(4)调节溶液的pH后,除生成Cu外,还能产生一种金属离子,此金属离子是_______ 。
(5)“滤液2”中可以循环使用的物质为HCl、_______ ,为保持流程持续循环,每生成1molCu,理论上需补充 的物质的量为
的物质的量为_______ 。
 )冶炼铜的工艺流程如下:
)冶炼铜的工艺流程如下:已知:
 。
。
(1)在元素周期表中,Cu价层电子排布为
(2)为提高“浸取”时的反应速率,通常可采用的措施有
(3)“除硫”时加入浓盐酸发生反应的离子方程式为
(4)调节溶液的pH后,除生成Cu外,还能产生一种金属离子,此金属离子是
(5)“滤液2”中可以循环使用的物质为HCl、
 的物质的量为
的物质的量为
您最近一年使用:0次
名校
10 . 已知反应: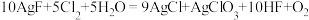 。下列关于该反应的叙述不正确的是
。下列关于该反应的叙述不正确的是
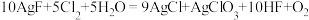 。下列关于该反应的叙述不正确的是
。下列关于该反应的叙述不正确的是| A.该反应中,氧化剂与还原剂的物质的量之比为9:5 |
| B.每产生1mol O2时,被氧元素还原的氯气物质的量为2mol |
| C.当反应中有1mol电子转移时,被还原氯气物质的量为1mol |
D.参加反应的水有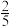 被氧化 被氧化 |
您最近一年使用:0次
2023-12-23更新
|
206次组卷
|
2卷引用:黑龙江省齐齐哈尔市恒昌中学校2023-2024学年高三上学期期中考试化学试题



