解题方法
1 . 金属钛( )密度小,强度高,抗腐蚀性能好。含钛的矿石主要有金红石和铁铁矿。
)密度小,强度高,抗腐蚀性能好。含钛的矿石主要有金红石和铁铁矿。
(1) 元素在周期表中的分区是位于
元素在周期表中的分区是位于___________ 区。基态 原子中含有的未成对电子数是
原子中含有的未成对电子数是___________ 。
(2)金红石主要成分是钛的氧化物,该氧化物的晶胞形状为长方体,边长分别为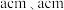 和
和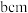 ,结构如下图所示。
,结构如下图所示。___________ , 位于距离最近的
位于距离最近的 构成的
构成的___________ 中心(填字母序号,下同)。
a.三角形 b.四面体 c.六面体 d.八面体
②该氧化物的晶体熔点为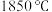 ,其晶体类型
,其晶体类型最不可 能是___________ 。
a.共价晶体 b.离子晶体 c.分子晶体
③若已知 该氧化物晶体体积为
该氧化物晶体体积为 ,则阿伏加德罗常数
,则阿伏加德罗常数 可表示为
可表示为___________  。
。
(3)以钓铁矿 为原料,用美还原法冶炼金属钓的生产流程图如下:
为原料,用美还原法冶炼金属钓的生产流程图如下: 元素在元素周期表中的位置是
元素在元素周期表中的位置是___________ 。
②“高温氯化”时还得到一种可燃性气体,写出反应的化学方程式:___________ 。
③结合流程及下表数据,“分离”时所需控制的最低温度应为___________  。
。
④已知 和
和 的晶胞类型相同,
的晶胞类型相同, 和
和 的离子半径大小相近,解释
的离子半径大小相近,解释 熔点高于
熔点高于 的原因:
的原因:___________ 。
 )密度小,强度高,抗腐蚀性能好。含钛的矿石主要有金红石和铁铁矿。
)密度小,强度高,抗腐蚀性能好。含钛的矿石主要有金红石和铁铁矿。(1)
 元素在周期表中的分区是位于
元素在周期表中的分区是位于 原子中含有的未成对电子数是
原子中含有的未成对电子数是(2)金红石主要成分是钛的氧化物,该氧化物的晶胞形状为长方体,边长分别为
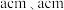 和
和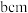 ,结构如下图所示。
,结构如下图所示。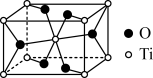
 位于距离最近的
位于距离最近的 构成的
构成的a.三角形 b.四面体 c.六面体 d.八面体
②该氧化物的晶体熔点为
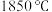 ,其晶体类型
,其晶体类型a.共价晶体 b.离子晶体 c.分子晶体
③若已知
 该氧化物晶体体积为
该氧化物晶体体积为 ,则阿伏加德罗常数
,则阿伏加德罗常数 可表示为
可表示为 。
。(3)以钓铁矿
 为原料,用美还原法冶炼金属钓的生产流程图如下:
为原料,用美还原法冶炼金属钓的生产流程图如下:
 元素在元素周期表中的位置是
元素在元素周期表中的位置是②“高温氯化”时还得到一种可燃性气体,写出反应的化学方程式:
③结合流程及下表数据,“分离”时所需控制的最低温度应为
 。
。 |  |  | |
熔点/ | 1668 | 651 | 714 |
沸点/ | 3287 | 1107 | 1412 |
 和
和 的晶胞类型相同,
的晶胞类型相同, 和
和 的离子半径大小相近,解释
的离子半径大小相近,解释 熔点高于
熔点高于 的原因:
的原因:
您最近一年使用:0次
解题方法
2 . 某化学小组同学对FeCl3溶液与Na2SO3溶液的反应进行探究
(1)请用离子方程式表示Na2SO3溶液显碱性的原因___________ 。
(2)甲同学认为实验①发生了氧化还原,其反应的离子方程式为___________ ,取反应后的溶液中加入K3[Fe(CN)6]溶液,观察到___________ (填现象),证实了此结论。
(3)乙同学检验红褐色沉淀为Fe(OH)3,请用平衡移动原理解释生成沉淀的原因___________ 。
(4)丙组同学检验实验②中无Fe2+,为探究此浓度下是否能发生氧化还原反应,做了如下实验:向U形管的左侧加入___________ ,观察到___________ (填实验现象),证实此浓度下的FeCl3溶液与Na2SO3溶液可以发生氧化还原反应。

(5)查阅资料已知:Fe3+、OH-、SO 可形成难电离的红色配合物:
可形成难电离的红色配合物: 。请解释实验②中无Fe2+生成的原因
。请解释实验②中无Fe2+生成的原因___________ 。
(6)通过以上探究,FeCl3溶液与Na2SO3溶液的反应受___________ 因素影响(至少写出两项)。
| 实验操作 | 现象 | |
| ① |  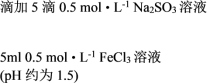 | 溶液由棕黄色变为红色,无沉淀生成。 放置6小时后,溶液变为淡黄色,始终无沉淀生成。 |
② |  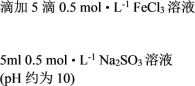 | 溶液由棕黄色变为红色,无沉淀生成。 放置6小时后,生成红褐色沉淀,上层清液为无色。 |
(1)请用离子方程式表示Na2SO3溶液显碱性的原因
(2)甲同学认为实验①发生了氧化还原,其反应的离子方程式为
(3)乙同学检验红褐色沉淀为Fe(OH)3,请用平衡移动原理解释生成沉淀的原因
(4)丙组同学检验实验②中无Fe2+,为探究此浓度下是否能发生氧化还原反应,做了如下实验:向U形管的左侧加入

(5)查阅资料已知:Fe3+、OH-、SO
 可形成难电离的红色配合物:
可形成难电离的红色配合物: 。请解释实验②中无Fe2+生成的原因
。请解释实验②中无Fe2+生成的原因(6)通过以上探究,FeCl3溶液与Na2SO3溶液的反应受
您最近一年使用:0次
3 . 工业上利用软锰矿和菱锰矿联合进行锅炉燃煤烟气脱硫,同时制备重要化工产品MnSO4,工艺流程如下:
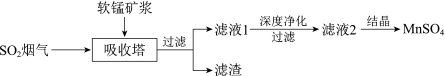
资料:i.软锰矿的主要成分是 MnO2,含少量SiO2、Fe3O4、FeO。
ⅱ.锅炉燃煤过程中空气过量。
ⅲ.该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的pH。
(1)吸收烟气前,软锰矿需研磨后填入吸收塔。研磨的目的是___________ 。
(2)将SO2烟气通入吸收塔中,发生的主要反应的化学方程式是___________ 。
(3)软锰矿浆脱硫过程中,控制流量,每隔3 h监测一次:测定软锰矿浆的pH;同时测定吸收塔入口和出口的SO2含量,计算SO2的吸收率,结果如图所示:
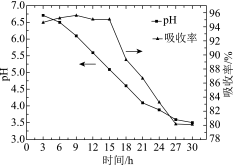
①吸收塔中矿浆pH逐渐下降的原因是________ (用化学用语表示)。
②当SO2吸收率低于95%时,无法实现SO2烟气的达标排放,此时需向吸收塔中加入一定量菱锰矿(主要成分MnCO3)。下列说法中,正确的是_________ (填字母)。
a.吸收塔中吸收率下降的可能原因是pH减小抑制了SO2的溶解
b.菱锰矿调节pH升至5.0以上后,吸收率又可以恢复至95%左右
c.加入菱锰矿能增加矿浆中Mn2+的浓度
(4)经检测发现滤液1中仍含有少量Fe2+,可加入MnO2进行“深度净化”,该过程中反应的离子方程式是___________ 。
(5)产品含量测定方法如下:
I.称取a g晶体,加足量硫酸溶解,将溶液定容于100 mL容量瓶中。
Ⅱ.取25.00 mL 溶液于锥形瓶中,加入少量催化剂和过量 (NH4)2S2O8溶液,加热、充分反应后,煮沸溶液使过量的(NH4)2S2O8分解。
Ⅲ.加入指示剂,用b mol/L (NH4)2Fe(SO4)2溶液滴定,滴定至终点时消耗c mL, 重新变成Mn2+。
重新变成Mn2+。
① 补全步骤Ⅱ中反应的离子方程式:_____ ,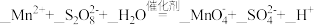 。
。
②产品中MnSO4的质量分数为________ (MnSO4的摩尔质量为151 g/mol)。

资料:i.软锰矿的主要成分是 MnO2,含少量SiO2、Fe3O4、FeO。
ⅱ.锅炉燃煤过程中空气过量。
ⅲ.该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的pH。
| 金属离子 | Fe3+ | Fe2+ | Mn2+ |
| 开始沉淀 | 1.5 | 6.3 | 7.6 |
| 完全沉淀 | 2.8 | 8.3 | 10.2 |
(1)吸收烟气前,软锰矿需研磨后填入吸收塔。研磨的目的是
(2)将SO2烟气通入吸收塔中,发生的主要反应的化学方程式是
(3)软锰矿浆脱硫过程中,控制流量,每隔3 h监测一次:测定软锰矿浆的pH;同时测定吸收塔入口和出口的SO2含量,计算SO2的吸收率,结果如图所示:

①吸收塔中矿浆pH逐渐下降的原因是
②当SO2吸收率低于95%时,无法实现SO2烟气的达标排放,此时需向吸收塔中加入一定量菱锰矿(主要成分MnCO3)。下列说法中,正确的是
a.吸收塔中吸收率下降的可能原因是pH减小抑制了SO2的溶解
b.菱锰矿调节pH升至5.0以上后,吸收率又可以恢复至95%左右
c.加入菱锰矿能增加矿浆中Mn2+的浓度
(4)经检测发现滤液1中仍含有少量Fe2+,可加入MnO2进行“深度净化”,该过程中反应的离子方程式是
(5)产品含量测定方法如下:
I.称取a g晶体,加足量硫酸溶解,将溶液定容于100 mL容量瓶中。
Ⅱ.取25.00 mL 溶液于锥形瓶中,加入少量催化剂和过量 (NH4)2S2O8溶液,加热、充分反应后,煮沸溶液使过量的(NH4)2S2O8分解。
Ⅲ.加入指示剂,用b mol/L (NH4)2Fe(SO4)2溶液滴定,滴定至终点时消耗c mL,
 重新变成Mn2+。
重新变成Mn2+。① 补全步骤Ⅱ中反应的离子方程式:
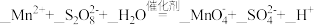 。
。②产品中MnSO4的质量分数为
您最近一年使用:0次
2024-01-19更新
|
226次组卷
|
3卷引用:北京市西城区2023-2024学年高二上学期期末考试化学试题
4 . 高纯硝酸银广泛应用于感光照相、电子浆料、保温瓶胆、制镜等行业。工业上利用粗银粉制备高纯硝酸银的工艺流程如下:

已知:ⅰ.粗 粉中含有
粉中含有 、
、 、
、 、
、 等杂质;
等杂质;
ⅱ.25℃时几种氯化物的溶度积常数如下表:
ⅲ. 在较浓盐酸中,可生成
在较浓盐酸中,可生成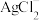 、
、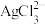 离子。
离子。
(1)酸浸:
①为加快化学反应速率,可采取的措施有_______ (写出一条即可)。
②硝酸与银的反应中,体现了硝酸的_______ 性(填“氧化”或“还原”)。
(2)沉银:在粗 溶液中主要含有
溶液中主要含有 、
、 、
、 、
、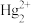 、
、 等离子。向粗
等离子。向粗 溶液中加入盐酸、氯化钠,投加量对
溶液中加入盐酸、氯化钠,投加量对 沉淀率的影响如图。
沉淀率的影响如图。
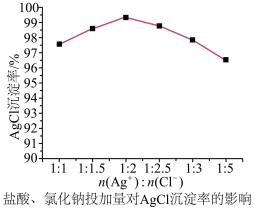
随着氯离子投加量的增加, 的沉淀率出现先增后降的趋势。
的沉淀率出现先增后降的趋势。
①当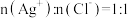 时,
时, 沉淀率并没有达到最高,原因是
沉淀率并没有达到最高,原因是_______ 。
②当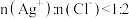 时,
时, 沉淀率降低,原因是
沉淀率降低,原因是_______ 。
(3)还原:精制 被
被 还原时,有
还原时,有 生成。反应的化学方程式为
生成。反应的化学方程式为_______ 。

已知:ⅰ.粗
 粉中含有
粉中含有 、
、 、
、 、
、 等杂质;
等杂质;ⅱ.25℃时几种氯化物的溶度积常数如下表:
| 化学式 |  |  | 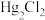 |
 |  |  | 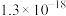 |
 在较浓盐酸中,可生成
在较浓盐酸中,可生成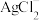 、
、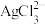 离子。
离子。(1)酸浸:
①为加快化学反应速率,可采取的措施有
②硝酸与银的反应中,体现了硝酸的
(2)沉银:在粗
 溶液中主要含有
溶液中主要含有 、
、 、
、 、
、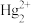 、
、 等离子。向粗
等离子。向粗 溶液中加入盐酸、氯化钠,投加量对
溶液中加入盐酸、氯化钠,投加量对 沉淀率的影响如图。
沉淀率的影响如图。
随着氯离子投加量的增加,
 的沉淀率出现先增后降的趋势。
的沉淀率出现先增后降的趋势。①当
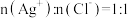 时,
时, 沉淀率并没有达到最高,原因是
沉淀率并没有达到最高,原因是②当
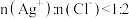 时,
时, 沉淀率降低,原因是
沉淀率降低,原因是(3)还原:精制
 被
被 还原时,有
还原时,有 生成。反应的化学方程式为
生成。反应的化学方程式为
您最近一年使用:0次
2023-01-07更新
|
206次组卷
|
2卷引用:北京市顺义区2022-2023学年高二上学期期末质量检测化学试题
名校
5 . 氯气可用于制取漂白剂和自来水消毒。
(1)下图是实验室制备氯气的制备和除杂装置
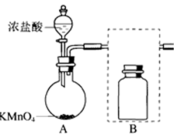
①A为氯气发生装置。A中反应方程式是_______ (锰被还原为 )。
)。
②将除杂装置B补充完整并标明所用试剂_______ 。
(2)“84”消毒液也可用于漂白,其工业制法是控制在常温条件下,将氯气通入NaOH溶液中,反应的离子方程式为_______ 。
(3)同学们探究“84”消毒液在不同pH下使红纸褪色的情况,做了如下实验:
步骤1:将5mL市售“84”消毒液稀释100倍,测得稀释后溶液的 ;
;
步骤2:将稀释后溶液各20mL分别加入3个洁净的小烧杯中;
步骤3:用 溶液将3个烧杯内溶液的pH分别调至10、7和4(溶液体积变化忽略不计)。
溶液将3个烧杯内溶液的pH分别调至10、7和4(溶液体积变化忽略不计)。
步骤4:在3个烧杯中分别放入大小相同的红纸,观察现象,记录如下:
已知,溶液中 、HClO和
、HClO和 物质的量分数
物质的量分数 随溶液pH变化的关系如下图所示:
随溶液pH变化的关系如下图所示:
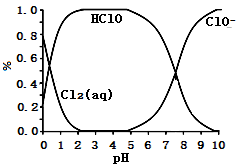
①由实验现象可得以下结论:溶液pH在4~10范围内,pH越大,红纸褪色_______ 。
②结合图像进行分析,b、c两烧杯中实验现象出现差异的原因是_______ 。
(4)由于氯气会与自来水中的有机物发生反应生成对人体有害的物质,人们尝试研究并使用新的自来水消毒剂,如 气体就是一种新型高效含氯消毒剂。
气体就是一种新型高效含氯消毒剂。
①一种制备 的方法是用
的方法是用 通入硫酸酸化的
通入硫酸酸化的 溶液中,反应的离子方程式为
溶液中,反应的离子方程式为_______ 。
②另一种制备 的方法是用
的方法是用 与盐酸反应,同时有
与盐酸反应,同时有 生成,产物中
生成,产物中 体积约占
体积约占 ,每生成
,每生成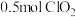 ,转移
,转移_______  。
。
③ 在杀菌消毒过程中会产生副产物亚氯酸盐
在杀菌消毒过程中会产生副产物亚氯酸盐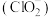 ,需将其转化为
,需将其转化为 除去。下列试剂中,可将
除去。下列试剂中,可将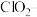 转化为
转化为 的是
的是_______ (填字母序号)。
a. b.
b. c.
c. d.KI
d.KI
(1)下图是实验室制备氯气的制备和除杂装置

①A为氯气发生装置。A中反应方程式是
 )。
)。②将除杂装置B补充完整并标明所用试剂
(2)“84”消毒液也可用于漂白,其工业制法是控制在常温条件下,将氯气通入NaOH溶液中,反应的离子方程式为
(3)同学们探究“84”消毒液在不同pH下使红纸褪色的情况,做了如下实验:
步骤1:将5mL市售“84”消毒液稀释100倍,测得稀释后溶液的
 ;
;步骤2:将稀释后溶液各20mL分别加入3个洁净的小烧杯中;
步骤3:用
 溶液将3个烧杯内溶液的pH分别调至10、7和4(溶液体积变化忽略不计)。
溶液将3个烧杯内溶液的pH分别调至10、7和4(溶液体积变化忽略不计)。步骤4:在3个烧杯中分别放入大小相同的红纸,观察现象,记录如下:
| 烧杯 | 溶液的pH | 现象 |
| a | 10 | 10min后,红纸基本不褪色;4h后红纸褪色 |
| b | 7 | 10min后,红纸颜色变浅;4h后红纸褪色 |
| c | 4 | 10min后,红纸颜色变得更浅;4h后红纸褪色 |
 、HClO和
、HClO和 物质的量分数
物质的量分数 随溶液pH变化的关系如下图所示:
随溶液pH变化的关系如下图所示:
①由实验现象可得以下结论:溶液pH在4~10范围内,pH越大,红纸褪色
②结合图像进行分析,b、c两烧杯中实验现象出现差异的原因是
(4)由于氯气会与自来水中的有机物发生反应生成对人体有害的物质,人们尝试研究并使用新的自来水消毒剂,如
 气体就是一种新型高效含氯消毒剂。
气体就是一种新型高效含氯消毒剂。①一种制备
 的方法是用
的方法是用 通入硫酸酸化的
通入硫酸酸化的 溶液中,反应的离子方程式为
溶液中,反应的离子方程式为②另一种制备
 的方法是用
的方法是用 与盐酸反应,同时有
与盐酸反应,同时有 生成,产物中
生成,产物中 体积约占
体积约占 ,每生成
,每生成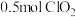 ,转移
,转移 。
。③
 在杀菌消毒过程中会产生副产物亚氯酸盐
在杀菌消毒过程中会产生副产物亚氯酸盐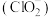 ,需将其转化为
,需将其转化为 除去。下列试剂中,可将
除去。下列试剂中,可将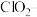 转化为
转化为 的是
的是a.
 b.
b. c.
c. d.KI
d.KI
您最近一年使用:0次
2023-01-07更新
|
447次组卷
|
2卷引用:北京市密云二中2023-2024学年高二上学期10月月考化学试卷
名校
解题方法
6 . 红矾钠 可用于制备制革产业中的铬鞣剂。对含铬污泥进行酸浸处理后,得到浸出液(主要含
可用于制备制革产业中的铬鞣剂。对含铬污泥进行酸浸处理后,得到浸出液(主要含 、
、 、
、 、
、 、
、 和
和 ),经过如下主要流程,可制得红矾钠,实现铬资源的有效循环利用。
),经过如下主要流程,可制得红矾钠,实现铬资源的有效循环利用。

已知:i. 溶液中存在以下平衡:
溶液中存在以下平衡:
ii.相关金属离子形成氢氧化物沉淀的pH范围如下:
(1)Ⅰ中, 溶液呈酸性,结合化学用语说明其原因:
溶液呈酸性,结合化学用语说明其原因:_______ 。
(2)Ⅱ中,加入NaOH调节pH至_______ (填字母序号)。
a.4.3~5.6 b.4.3~7.1 c.5.6~7.1 d.7.1~9.2
(3)Ⅲ中, 氧化
氧化 沉淀的化学方程式为
沉淀的化学方程式为_______ 。
(4)Ⅲ中,在投料比、反应时间均相同时,若温度过高, 的产率反而降低,可能的原因是
的产率反而降低,可能的原因是_______ 。
(5)Ⅳ中,加入 的作用是
的作用是_______ (结合平衡移动原理解释)。
(6)为了测定获得红矾钠( )的纯度,称取上述流程中的产品ag配成100mL溶液,取出25mL放于锥形瓶中,加入稀硫酸和足量的KI溶液,置于暗处充分反应至
)的纯度,称取上述流程中的产品ag配成100mL溶液,取出25mL放于锥形瓶中,加入稀硫酸和足量的KI溶液,置于暗处充分反应至 全部转化为
全部转化为 后,滴入2~3滴淀粉溶液,最后用浓度为
后,滴入2~3滴淀粉溶液,最后用浓度为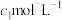 的
的 标准溶液滴定,共消耗
标准溶液滴定,共消耗 。(已知:
。(已知: 。)
。)
①滴定终点的现象为_______ 。
②所得 (摩尔质量为
(摩尔质量为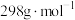 )的纯度的表达式为
)的纯度的表达式为_______ (用质量分数表示)。
 可用于制备制革产业中的铬鞣剂。对含铬污泥进行酸浸处理后,得到浸出液(主要含
可用于制备制革产业中的铬鞣剂。对含铬污泥进行酸浸处理后,得到浸出液(主要含 、
、 、
、 、
、 、
、 和
和 ),经过如下主要流程,可制得红矾钠,实现铬资源的有效循环利用。
),经过如下主要流程,可制得红矾钠,实现铬资源的有效循环利用。
已知:i.
 溶液中存在以下平衡:
溶液中存在以下平衡:
ii.相关金属离子形成氢氧化物沉淀的pH范围如下:
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
 | 4.3 | 5.6 |
 | 7.1 | 9.2 |
 溶液呈酸性,结合化学用语说明其原因:
溶液呈酸性,结合化学用语说明其原因:(2)Ⅱ中,加入NaOH调节pH至
a.4.3~5.6 b.4.3~7.1 c.5.6~7.1 d.7.1~9.2
(3)Ⅲ中,
 氧化
氧化 沉淀的化学方程式为
沉淀的化学方程式为(4)Ⅲ中,在投料比、反应时间均相同时,若温度过高,
 的产率反而降低,可能的原因是
的产率反而降低,可能的原因是(5)Ⅳ中,加入
 的作用是
的作用是(6)为了测定获得红矾钠(
 )的纯度,称取上述流程中的产品ag配成100mL溶液,取出25mL放于锥形瓶中,加入稀硫酸和足量的KI溶液,置于暗处充分反应至
)的纯度,称取上述流程中的产品ag配成100mL溶液,取出25mL放于锥形瓶中,加入稀硫酸和足量的KI溶液,置于暗处充分反应至 全部转化为
全部转化为 后,滴入2~3滴淀粉溶液,最后用浓度为
后,滴入2~3滴淀粉溶液,最后用浓度为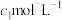 的
的 标准溶液滴定,共消耗
标准溶液滴定,共消耗 。(已知:
。(已知: 。)
。)①滴定终点的现象为
②所得
 (摩尔质量为
(摩尔质量为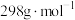 )的纯度的表达式为
)的纯度的表达式为
您最近一年使用:0次
2023-01-06更新
|
923次组卷
|
9卷引用:北京海淀区2022-2023学年高二上学期期末考试化学试题
北京海淀区2022-2023学年高二上学期期末考试化学试题北京一零一中学2022-2023高二上学期期末考试化学试题北京市首都师范大学附属中学2022-2023学年高二上学期期末考试化学试题北京市顺义牛栏山第一中学2023-2024学年高二上学期期中考试化学试题北京市第三十五中学2023-2024学年高二上学期期中考试化学试题 北京市第十一中学2022-2023学年高二上学期期末考试化学试题北京一七一中学2023-2024学年高二上学期12月阶段性诊断化学试题北京交通大学附属中学第二分校2023-2024学年高二上学期12月月考化学试题福建师范大学附属中学2022-2023学年高二下学期开学考试(期末考)化学试卷
名校
解题方法
7 . 已知M2O + 3 S2- + 14H+= 2M 3++ 3S↓+ 7H2O,则M2O
+ 3 S2- + 14H+= 2M 3++ 3S↓+ 7H2O,则M2O 中的M的化合价为
中的M的化合价为
 + 3 S2- + 14H+= 2M 3++ 3S↓+ 7H2O,则M2O
+ 3 S2- + 14H+= 2M 3++ 3S↓+ 7H2O,则M2O 中的M的化合价为
中的M的化合价为| A.+2 | B.+3 | C.+4 | D.+6 |
您最近一年使用:0次
2020-11-25更新
|
1194次组卷
|
57卷引用:北京市第四中学高中化学人教版选修4单元测试题:1.1化学反应及其能量变化
北京市第四中学高中化学人教版选修4单元测试题:1.1化学反应及其能量变化陕西省榆林市第二中学2018-2019学年高二下学期期末考试化学试题福建省福州市八县一中2019-2020学年高二上学期期中考试化学试题(已下线)2010—2011学年黑龙江省大庆中学高一上学期期末考试化学试卷(已下线)2011-2012学年四川省成都七中实验学校高一上学期期中考试化学试卷(已下线)2011-2012学年湖北省荆州中学高一上学期期末考试化学试卷(已下线)2013-2014学年湖北省襄阳市四校高一上学期期中考试化学试卷2015-2016学年河南省许昌、襄城、长葛三校高一上期中测试化学试卷2015-2016学年湖北省宜昌市葛洲坝中学高一上学期期中测试化学试卷2015-2016学年四川省攀枝花十五中高一上期中试卷化学试卷2015-2016学年内蒙古巴彦淖尔一中高一上期中化学试卷2016-2017学年辽宁沈阳东北育才学校高一阶段考一化学卷2016-2017学年安徽省芜湖一中高一上期中考试化学试卷2016-2017学年甘肃省庆阳一中高一上期中化学卷2016-2017学年云南省昆明三中高一上期中化学试卷2017届河北省定州中学高三上期末化学试卷云南省南涧彝族自治县民族中学2017-2018学年高一9月月考化学试题甘肃省天水市第一中学2017-2018学年高一上学期第二学段考试化学试题吉林省长春外国语学校2017-2018学年高一上学期第二次月考化学试题重庆市西北狼联盟2017-2018学年高一上学期第一次联盟考试(12月)化学试题江西省南昌市八一中学2017-2018学年高一1月月考化学试题(已下线)2019高考备考一轮复习精品资料 第二章 化学物质及其变化第4讲 守恒思想在化学中的应用——守恒法解题技巧【押题专练】吉林省长春汽车经济开发区第六中学2017-2018学年高一上学期期中考试化学试题陕西省汉中中学2019届高三上学期第一次月考化学试题(已下线)【走进新高考】(人教版必修一)高一上学期期中复习模拟(A卷)(基础篇)02(已下线)【走进新高考】(人教版必修一)第二章 化学物质及其变化 单元练习01河南省安阳市第二中学2018-2019学年高一上学期期中考试化学试题河南省济源四中2018-2019学年高一上学期期中考试化学试题甘肃省张掖市民乐县第一中学2018-2019学年高一上学期期中考试化学试题广东省揭西县河婆中学2018-2019学年上学期高一期中考试化学试题浙江省金华市东阳中学2019-2020学年高一上学期开学考试化学试题黑龙江省齐齐哈尔市第八中学2019-2020学年高一上学期期中考试化学试题山西省忻州市岢岚县中学2019-2020学年高一上学期期中考试化学试题江西省高安中学2019-2020学年高一上学期期中考试化学(B)试题江苏省苏州市震泽中学2019-2020学年高一上学期第二次月考化学试题吉林省长春市榆树市第一高级中学2019-2020学年高一上学期尖子生考试化学试题安徽省合肥市一六八中2017-2018学年高一上学期期中考试化学试题(已下线)2.3.2 氧化还原反应的应用练习(2)——《高中新教材同步备课》(鲁科版 必修第一册)(已下线)第01章 物质及其变化(B卷能力提高篇)——2020-2021学年高一化学必修第一册同步单元AB卷(新教材人教版)江西省南昌市八一中学、麻丘高级中学等六校2020-2021学年高一上学期期中联考化学试题(已下线)【南昌新东方】10. 2020 高一上 洪八联考 晏梓超河南省三门峡市渑池县第二高级中学2020-2021学年高一上学期第三次月考化学试题江苏省盐城市上冈高级中学2020-2021学年高一上学期第二次学情检测化学试题河北省藁城新冀明中学2020-2021学年高一上学期12月月考化学试题(已下线)1.3.1 氧化还原反应-2021-2022学年高一化学课后培优练(人教版2019必修第一册)广东省揭阳市第一中学2017-2018学年高一上学期期中考试化学试题(已下线)必考点04 氧化还原反应的本质和相关概念-【对点变式题】2021-2022学年高一化学上学期期中期末必考题精准练(人教版2019)宁夏银川一中2021-2022学年高一上学期期中考试化学试题(已下线)第07练 氧化还原反应-2022年【寒假分层作业】高一化学(苏教版2019必修第一册)湖北省随州市第二中学2021-2022学年高一上学期10月月考化学试题江苏省邳州市宿羊山高级中学2021-2022学年高一上学期第二次学情检测化学试题湖北省十堰市联合体2022-2023学年高一上学期10月期中联考化学试题重庆市第八中学校2022-2023学年高一上学期期中考试(半期考试)化学试题四川省达州天立学校2022-2023学年高一上学期11月月考化学试题贵州省三新联盟校2023-2024学年高一上学期10月联考化学试题四川省绵阳中学2023-2024学年高一上学期9月月考化学试题重庆市第一中学校2023-2024学年高一上学期定时练习化学试题
解题方法
8 . 锂电池应用广泛,大致可分为锂金属电池和锂离子电池。锂离子电池工作原理:以石墨/锂钴氧电池为例,其总反应方程式为:LiCoO2+6C Li1-xCoO2+LixC6
Li1-xCoO2+LixC6

试回答下列问题:
(1)连接K1、K2时,a作___ 极。
(2)连接K2、K3时,被还原的物质是___ 。
(3)放电时,负极发生反应的电极反应式是___ 。
(4)锂离子电池的电极废料(含LiCoO2)中的金属可回收利用。
①将电极废料磨碎后用酸浸出,磨碎的目的是___ 。
②将电极废料用盐酸浸出,得到含Li+、Co2+的溶液,并有黄绿色气体生成,则该反应的化学方程式是___ 。
 Li1-xCoO2+LixC6
Li1-xCoO2+LixC6
试回答下列问题:
(1)连接K1、K2时,a作
(2)连接K2、K3时,被还原的物质是
(3)放电时,负极发生反应的电极反应式是
(4)锂离子电池的电极废料(含LiCoO2)中的金属可回收利用。
①将电极废料磨碎后用酸浸出,磨碎的目的是
②将电极废料用盐酸浸出,得到含Li+、Co2+的溶液,并有黄绿色气体生成,则该反应的化学方程式是
您最近一年使用:0次



