名校
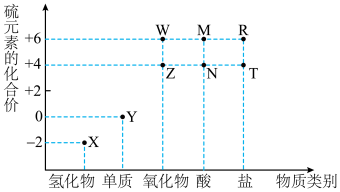
1 . 利用元素的化合价物质类别的坐标系,可以对含某元素的各物质性质有整体的认识。如图是硫元素的常见化合价与部分物质类别的对应关系。______ ;检验其阴离子的方法是______ 。
(2)化石燃料的燃烧可产生 ,在上述图表中它是
,在上述图表中它是______ (图中的字母),为避免过多 进入大气造成酸雨,沿海的火电站可利用天然海水(显弱碱性的微粒主要是
进入大气造成酸雨,沿海的火电站可利用天然海水(显弱碱性的微粒主要是 )吸收该物质,成本低廉。其过程如下。
)吸收该物质,成本低廉。其过程如下。 时,发生的主要反应的离子方程式为
时,发生的主要反应的离子方程式为______ 。
②氧化的目的是将硫元素全部转化为 ,该过程中溶液pH
,该过程中溶液pH______ (填“升高”“不变”或“降低”)。
③排放海水与原海水相比,减少的 与增加的
与增加的 的物质的量之比的为
的物质的量之比的为______ 。
(3) 溶液脱除空气污染物X并再生的原理如图所示。反应I的离子方程式为
溶液脱除空气污染物X并再生的原理如图所示。反应I的离子方程式为______ ;每脱除170kg X,消耗标准状况下 的体积为
的体积为______ L。
(2)化石燃料的燃烧可产生
 ,在上述图表中它是
,在上述图表中它是 进入大气造成酸雨,沿海的火电站可利用天然海水(显弱碱性的微粒主要是
进入大气造成酸雨,沿海的火电站可利用天然海水(显弱碱性的微粒主要是 )吸收该物质,成本低廉。其过程如下。
)吸收该物质,成本低廉。其过程如下。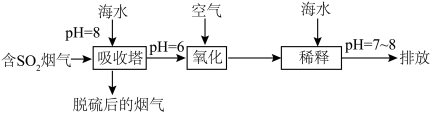
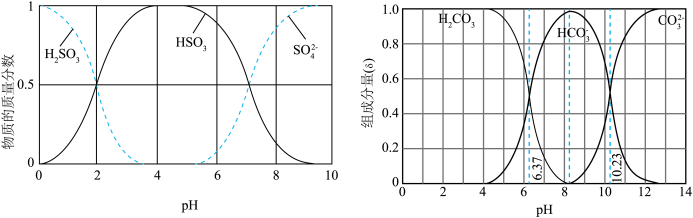
 时,发生的主要反应的离子方程式为
时,发生的主要反应的离子方程式为②氧化的目的是将硫元素全部转化为
 ,该过程中溶液pH
,该过程中溶液pH③排放海水与原海水相比,减少的
 与增加的
与增加的 的物质的量之比的为
的物质的量之比的为(3)
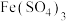 溶液脱除空气污染物X并再生的原理如图所示。反应I的离子方程式为
溶液脱除空气污染物X并再生的原理如图所示。反应I的离子方程式为 的体积为
的体积为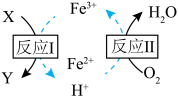
您最近一年使用:0次
2 . 氯的化合物在生活中有着广泛的用途。
(1)二氧化氯(ClO2)的熔点-59℃,沸点11℃,易溶于水,是一种常用的饮用水消毒剂,消毒时会产生Cl-和少量的 ,可利用酸性FeSO4溶液将
,可利用酸性FeSO4溶液将 转化为Cl-除去。
转化为Cl-除去。
①关于二氧化氯的说法不正确的是_______ 。
A.易液化 B.实验室可用排水法收集
C.氯的化合价为+4 D.消毒时利用其强还原性
②FeSO4除去 的离子方程式为
的离子方程式为_______ 。
(2)亚氯酸钠(NaClO2)是一种高效的漂白剂和氧化剂,某种制备亚氯酸钠的反应为:ClO2+H2O2+NaOH=NaClO2+O2+H2O(未配平)。
①ClO2的氧化性_______ H2O2的氧化性(填“大于”或“小于”)。
②为测定产品中NaClO2的纯度,进行如下实验:准确称取1.000g上述产品,溶于水配成100.00mL溶液,取10.00mL待测液,加入过量KI溶液,酸性条件下发生反应: +4I-+4H+=2H2O+2I2+Cl-,杂质不与I-反应。以淀粉作指示剂,再加入0.2000mol/LNa2S2O3溶液,恰好完全反应时消耗的Na2S2O3溶液的体积为20.00mL。(已知:I2+2
+4I-+4H+=2H2O+2I2+Cl-,杂质不与I-反应。以淀粉作指示剂,再加入0.2000mol/LNa2S2O3溶液,恰好完全反应时消耗的Na2S2O3溶液的体积为20.00mL。(已知:I2+2 =2I-+
=2I-+ )。计算该样品的纯度为
)。计算该样品的纯度为_______ 。(写出计算过程)
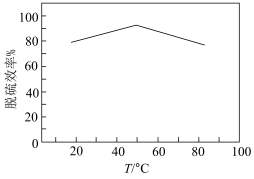
③工业上常用NaClO2溶液对燃煤烟气进行脱硫。已知NaClO2溶液具有强氧化性,酸性条件下NaClO2发生歧化反应生成ClO2,ClO2易溶于水,具有强氧化性,可氧化SO2.在实验室模拟脱硫过程:先加稀硫酸调节NaClO2吸收液的pH为5,再向其中通入含SO2的模拟烟气。测得脱硫反应后,溶液中的阴离子为Cl-,则SO2的氧化产物是_______ 。测得脱硫效率(即SO2的吸收率)随温度变化的曲线如下图所示。_______ 。
(1)二氧化氯(ClO2)的熔点-59℃,沸点11℃,易溶于水,是一种常用的饮用水消毒剂,消毒时会产生Cl-和少量的
 ,可利用酸性FeSO4溶液将
,可利用酸性FeSO4溶液将 转化为Cl-除去。
转化为Cl-除去。①关于二氧化氯的说法不正确的是
A.易液化 B.实验室可用排水法收集
C.氯的化合价为+4 D.消毒时利用其强还原性
②FeSO4除去
 的离子方程式为
的离子方程式为(2)亚氯酸钠(NaClO2)是一种高效的漂白剂和氧化剂,某种制备亚氯酸钠的反应为:ClO2+H2O2+NaOH=NaClO2+O2+H2O(未配平)。
①ClO2的氧化性
②为测定产品中NaClO2的纯度,进行如下实验:准确称取1.000g上述产品,溶于水配成100.00mL溶液,取10.00mL待测液,加入过量KI溶液,酸性条件下发生反应:
 +4I-+4H+=2H2O+2I2+Cl-,杂质不与I-反应。以淀粉作指示剂,再加入0.2000mol/LNa2S2O3溶液,恰好完全反应时消耗的Na2S2O3溶液的体积为20.00mL。(已知:I2+2
+4I-+4H+=2H2O+2I2+Cl-,杂质不与I-反应。以淀粉作指示剂,再加入0.2000mol/LNa2S2O3溶液,恰好完全反应时消耗的Na2S2O3溶液的体积为20.00mL。(已知:I2+2 =2I-+
=2I-+ )。计算该样品的纯度为
)。计算该样品的纯度为③工业上常用NaClO2溶液对燃煤烟气进行脱硫。已知NaClO2溶液具有强氧化性,酸性条件下NaClO2发生歧化反应生成ClO2,ClO2易溶于水,具有强氧化性,可氧化SO2.在实验室模拟脱硫过程:先加稀硫酸调节NaClO2吸收液的pH为5,再向其中通入含SO2的模拟烟气。测得脱硫反应后,溶液中的阴离子为Cl-,则SO2的氧化产物是
您最近一年使用:0次
3 . 氯的化合物在生活中有着广泛的用途。
(1)二氧化氯(ClO2)的熔点-59℃,沸点11℃,易溶于水,是一种常用的饮用水消毒剂,消毒时会产生 和少量的
和少量的 ,可利用酸性FeSO4溶液将
,可利用酸性FeSO4溶液将 转化为
转化为 除去。
除去。
①关于二氧化氯的说法不正确 的是______ 。
A.易液化 B.实验室可用排水法收集
C.氯的化合价为+4 D.消毒时利用其强还原性
②FeSO4除去 的离子方程式为
的离子方程式为______ 。
(2)亚氯酸钠(NaClO2)是一种高效的漂白剂和氧化剂,某种制备亚氯酸钠的反应为: (未配平)。
(未配平)。
①ClO2的氧化性______ H2O2的氧化性(填“大于”或“小于”)。
②当消耗标准状况下2.24 L ClO2时,生成O2的质量为___________ 。
(3)“84”消毒液是一种常用家庭消毒液,其有效成分为NaClO。一种碱性NaClO溶液吸收SO2的过程如下图。

①该过程的总反应的离子方程式是___________ 。
②整个吸收SO2过程中作氧化剂的微粒有___________ 。
(1)二氧化氯(ClO2)的熔点-59℃,沸点11℃,易溶于水,是一种常用的饮用水消毒剂,消毒时会产生
 和少量的
和少量的 ,可利用酸性FeSO4溶液将
,可利用酸性FeSO4溶液将 转化为
转化为 除去。
除去。①关于二氧化氯的说法
A.易液化 B.实验室可用排水法收集
C.氯的化合价为+4 D.消毒时利用其强还原性
②FeSO4除去
 的离子方程式为
的离子方程式为(2)亚氯酸钠(NaClO2)是一种高效的漂白剂和氧化剂,某种制备亚氯酸钠的反应为:
 (未配平)。
(未配平)。①ClO2的氧化性
②当消耗标准状况下2.24 L ClO2时,生成O2的质量为
(3)“84”消毒液是一种常用家庭消毒液,其有效成分为NaClO。一种碱性NaClO溶液吸收SO2的过程如下图。

①该过程的总反应的离子方程式是
②整个吸收SO2过程中作氧化剂的微粒有
您最近一年使用:0次
解题方法
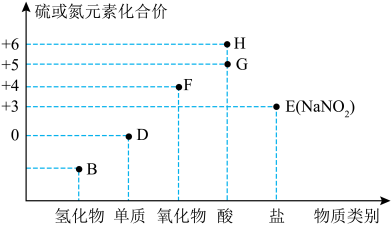
4 . “价—类”二维图是学习元素化合物的一种好方法。硫或氮及其化合物的部分“价—类”二维图如图所示,回答下列问题: ,写出F和G的稀溶液反应生成H的化学方程式(还原产物为+2价氧化物):
,写出F和G的稀溶液反应生成H的化学方程式(还原产物为+2价氧化物):_______ 。
(2)若B为 ,则下列关于氨气的性质和用途描述正确的是_______(填字母)。
,则下列关于氨气的性质和用途描述正确的是_______(填字母)。
(3)在微生物作用下,蛋白质在水中分解产生的氨能够被氧气氧化生成亚硝酸( ),该反应的化学方程式为
),该反应的化学方程式为_______ ;某厂废液中含有2%~5%的 ,直接排放会造成污染,下列试剂能使
,直接排放会造成污染,下列试剂能使 转化为
转化为 的是
的是_______ (填字母)。
A.NaOH B. C.
C. D.浓硫酸
D.浓硫酸
(4)D可以是 ,已知同温同压下,同体积的
,已知同温同压下,同体积的 与
与 (蒸气)的质量比为7:64,则x=
(蒸气)的质量比为7:64,则x=_____ 。
(5) 在空气中易变质,写出检验
在空气中易变质,写出检验 发生变质的实验方法:
发生变质的实验方法:_______ 。
(6)常温下,G的浓溶液可以用干燥的铁或铝制容器盛装,原因是_______ 。
 ,写出F和G的稀溶液反应生成H的化学方程式(还原产物为+2价氧化物):
,写出F和G的稀溶液反应生成H的化学方程式(还原产物为+2价氧化物):(2)若B为
 ,则下列关于氨气的性质和用途描述正确的是_______(填字母)。
,则下列关于氨气的性质和用途描述正确的是_______(填字母)。| A.氨气易液化;液氨可用作制冷剂 | B.可用排水法收集氨气 |
| C.氨气是一种无色、无味的气体 | D.向氨水中滴加酚酞,溶液变红 |
(3)在微生物作用下,蛋白质在水中分解产生的氨能够被氧气氧化生成亚硝酸(
 ),该反应的化学方程式为
),该反应的化学方程式为 ,直接排放会造成污染,下列试剂能使
,直接排放会造成污染,下列试剂能使 转化为
转化为 的是
的是A.NaOH B.
 C.
C. D.浓硫酸
D.浓硫酸(4)D可以是
 ,已知同温同压下,同体积的
,已知同温同压下,同体积的 与
与 (蒸气)的质量比为7:64,则x=
(蒸气)的质量比为7:64,则x=(5)
 在空气中易变质,写出检验
在空气中易变质,写出检验 发生变质的实验方法:
发生变质的实验方法:(6)常温下,G的浓溶液可以用干燥的铁或铝制容器盛装,原因是
您最近一年使用:0次
解题方法
5 . 甲烷既是高效的能源,又是重要的化工原料,在生产、生活中用途广泛。
(1) 燃烧放出大量的热。
燃烧放出大量的热。
常温下,
 在
在 中完全燃烧生成
中完全燃烧生成 和液态水释放出
和液态水释放出 的热量,写出甲烷燃烧的热化学方程式
的热量,写出甲烷燃烧的热化学方程式___________ 。
(2)甲烷—空气质子交换膜燃料电池应用广泛,其结构如图所示。

①a处通入的物质是___________ (填化学式),电极 的电极反应式为
的电极反应式为___________ 。
②若该燃料电池消耗 (标准状况下)
(标准状况下) ,则理论上电路中转移
,则理论上电路中转移___________  电子。
电子。
(3)工业上利用 催化重整制
催化重整制 。
。
在恒容密闭容器中发生反应: 。
。
①在不改变物质浓度的条件下,加快该反应速率的措施有___________ (答出一点即可)。
②下列叙述中能说明该反应已达平衡状态的有___________ (填字母序号)。
A.
B.混合气体的质量不再变化
C.单位时间内生成
 ,同时消耗
,同时消耗

D.混合气体的压强不再变化
(4)高温条件下,利用 还原
还原 的反应过程如图所示。
的反应过程如图所示。

该反应的催化剂是___________ 。写出反应ⅱ的化学方程式___________ 。
(1)
 燃烧放出大量的热。
燃烧放出大量的热。常温下,

 在
在 中完全燃烧生成
中完全燃烧生成 和液态水释放出
和液态水释放出 的热量,写出甲烷燃烧的热化学方程式
的热量,写出甲烷燃烧的热化学方程式(2)甲烷—空气质子交换膜燃料电池应用广泛,其结构如图所示。

①a处通入的物质是
 的电极反应式为
的电极反应式为②若该燃料电池消耗
 (标准状况下)
(标准状况下) ,则理论上电路中转移
,则理论上电路中转移 电子。
电子。(3)工业上利用
 催化重整制
催化重整制 。
。在恒容密闭容器中发生反应:
 。
。①在不改变物质浓度的条件下,加快该反应速率的措施有
②下列叙述中能说明该反应已达平衡状态的有
A.

B.混合气体的质量不再变化
C.单位时间内生成

 ,同时消耗
,同时消耗

D.混合气体的压强不再变化
(4)高温条件下,利用
 还原
还原 的反应过程如图所示。
的反应过程如图所示。
该反应的催化剂是
您最近一年使用:0次
名校
解题方法
6 . 砷及其化合物有着广泛的用途,但也会严重危害环境安全和人体健康。
(1)雌黄( )和雄黄(
)和雄黄( )都是提取砷的主要矿物原料。砷元素有
)都是提取砷的主要矿物原料。砷元素有 、
、 、
、 等常见价态。
等常见价态。
①如图为 分子的空间结构模型。已知
分子的空间结构模型。已知 分子中没有π键,其结构式可表示为
分子中没有π键,其结构式可表示为______ 。

②将含砷废渣(主要成分是 )制成浆料再通入
)制成浆料再通入 氧化,转化为
氧化,转化为 和单质硫,是工业提取砷元素的途径之一、写出
和单质硫,是工业提取砷元素的途径之一、写出 转化为
转化为 的化学方程式
的化学方程式___________ ;该反应需要在加压下进行,原因是___________ 。
(2) 可转化为用于治疗白血病的亚砷酸(
可转化为用于治疗白血病的亚砷酸( )。
)。 在水溶液中存在多种微粒形态,各种微粒的物质的量分数与溶液pH关系如图所示。
在水溶液中存在多种微粒形态,各种微粒的物质的量分数与溶液pH关系如图所示。

① 的电离常数分别为
的电离常数分别为 、
、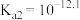 、
、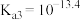 ,则a点
,则a点
___________ 。
②工业含 废水具有剧毒,常用铁盐处理后排放。其原理是:铁盐混凝剂在溶液中产生
废水具有剧毒,常用铁盐处理后排放。其原理是:铁盐混凝剂在溶液中产生 胶粒,其表面带有正电荷,可吸附含砷化合物。不同pH条件下铁盐对水中
胶粒,其表面带有正电荷,可吸附含砷化合物。不同pH条件下铁盐对水中 的去除率如图所示。在
的去除率如图所示。在 溶液中,pH越大,铁盐混凝剂去除水中
溶液中,pH越大,铁盐混凝剂去除水中 的速率越快,原因是
的速率越快,原因是___________ 。

(3)水体中 的毒性远高于
的毒性远高于 且
且 更易除去,常用的处理方法是先将废水中的
更易除去,常用的处理方法是先将废水中的 氧化为
氧化为 ,再通过一定方法除去
,再通过一定方法除去 。
。
① 可被
可被 进一步氧化为
进一步氧化为 。
。 的酸性
的酸性___________  的酸性(填“>”或“<”)。
的酸性(填“>”或“<”)。
②在 的水溶液中,以
的水溶液中,以 为沉淀剂,可将
为沉淀剂,可将 转化为
转化为 沉淀除去,其离子方程式为
沉淀除去,其离子方程式为___________ 。[已知: ,
, ]
]
(1)雌黄(
 )和雄黄(
)和雄黄( )都是提取砷的主要矿物原料。砷元素有
)都是提取砷的主要矿物原料。砷元素有 、
、 、
、 等常见价态。
等常见价态。①如图为
 分子的空间结构模型。已知
分子的空间结构模型。已知 分子中没有π键,其结构式可表示为
分子中没有π键,其结构式可表示为
②将含砷废渣(主要成分是
 )制成浆料再通入
)制成浆料再通入 氧化,转化为
氧化,转化为 和单质硫,是工业提取砷元素的途径之一、写出
和单质硫,是工业提取砷元素的途径之一、写出 转化为
转化为 的化学方程式
的化学方程式(2)
 可转化为用于治疗白血病的亚砷酸(
可转化为用于治疗白血病的亚砷酸( )。
)。 在水溶液中存在多种微粒形态,各种微粒的物质的量分数与溶液pH关系如图所示。
在水溶液中存在多种微粒形态,各种微粒的物质的量分数与溶液pH关系如图所示。
①
 的电离常数分别为
的电离常数分别为 、
、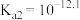 、
、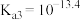 ,则a点
,则a点
②工业含
 废水具有剧毒,常用铁盐处理后排放。其原理是:铁盐混凝剂在溶液中产生
废水具有剧毒,常用铁盐处理后排放。其原理是:铁盐混凝剂在溶液中产生 胶粒,其表面带有正电荷,可吸附含砷化合物。不同pH条件下铁盐对水中
胶粒,其表面带有正电荷,可吸附含砷化合物。不同pH条件下铁盐对水中 的去除率如图所示。在
的去除率如图所示。在 溶液中,pH越大,铁盐混凝剂去除水中
溶液中,pH越大,铁盐混凝剂去除水中 的速率越快,原因是
的速率越快,原因是
(3)水体中
 的毒性远高于
的毒性远高于 且
且 更易除去,常用的处理方法是先将废水中的
更易除去,常用的处理方法是先将废水中的 氧化为
氧化为 ,再通过一定方法除去
,再通过一定方法除去 。
。①
 可被
可被 进一步氧化为
进一步氧化为 。
。 的酸性
的酸性 的酸性(填“>”或“<”)。
的酸性(填“>”或“<”)。②在
 的水溶液中,以
的水溶液中,以 为沉淀剂,可将
为沉淀剂,可将 转化为
转化为 沉淀除去,其离子方程式为
沉淀除去,其离子方程式为 ,
, ]
]
您最近一年使用:0次
2024-01-01更新
|
524次组卷
|
3卷引用:江苏省南京师范大学附属中学2023-2024学年高三上学期期中考试 化学试卷
名校
7 . SO2在生活、生产中有重要用途,使用不当会造成环境污染。
(1)某同学利用图所示装置研究二氧化硫的性质。

①仪器a的名称为_______ 。
②向仪器a中滴加浓硫酸之前,需先通入一段时间N2,此操作的目的是_______ 。
③实验时,装置B中没有明显变化。实验结束后取下装置B,向其中滴加适量氨水,生成的白色沉淀为_______ (填化学式)。
④装置C中出现淡黄色浑浊,说明二氧化硫具有_______ 性。
(2)某兴趣小组用图所示装置模拟空气中二氧化硫含量的测定。当注入标准状况下VmL空气时,酸性KMnO4溶液恰好褪色,停止实验。该空气中二氧化硫的体积分数为_______ (用含V代数式表示)。

(3)某化工厂用图所示工艺流程除去燃煤产生的SO2。
①过程I发生的反应为 ,用双线桥标出该反应电子转移的方向和数目
,用双线桥标出该反应电子转移的方向和数目_______ 。
②过程Ⅱ发生反应的化学方程式为_______ 。

(1)某同学利用图所示装置研究二氧化硫的性质。

①仪器a的名称为
②向仪器a中滴加浓硫酸之前,需先通入一段时间N2,此操作的目的是
③实验时,装置B中没有明显变化。实验结束后取下装置B,向其中滴加适量氨水,生成的白色沉淀为
④装置C中出现淡黄色浑浊,说明二氧化硫具有
(2)某兴趣小组用图所示装置模拟空气中二氧化硫含量的测定。当注入标准状况下VmL空气时,酸性KMnO4溶液恰好褪色,停止实验。该空气中二氧化硫的体积分数为

(3)某化工厂用图所示工艺流程除去燃煤产生的SO2。
①过程I发生的反应为
 ,用双线桥标出该反应电子转移的方向和数目
,用双线桥标出该反应电子转移的方向和数目②过程Ⅱ发生反应的化学方程式为

您最近一年使用:0次
2022-12-18更新
|
380次组卷
|
4卷引用:江苏省靖江高级中学2022-2023学年高一上学期第三次阶段测试化学试题
江苏省靖江高级中学2022-2023学年高一上学期第三次阶段测试化学试题江苏省盐城市阜宁县2022-2023学年高一上学期1月期末考试化学试题(已下线)专题07 硫及含硫化合物 环境保护-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(江苏专用)福建师范大学附属中学2022-2023学年高一下学期开学阶段考试化学试题
名校
解题方法
8 . I.氯元素是中学化学中常见的重要非金属元素之一,氯元素的单质及其化合物在生产与生活中有着重要的用途,依据所学知识完成下列问题:
(1)实验室制备氯气的离子方程式是_____ ;若多余的氯气用氢氧化钠溶液吸收,其离子方程式为_____ 。
II.常温下,二氧化氯(ClO2)是一种黄绿色气体,具有强氧化性,已被联合国世界卫生组织(WHO)列为高效安全消毒剂。常温下,它可用氯酸钠固体与浓盐酸反应制备得到,还有NaCl与Cl2生成。
(2)写出并配平该反应的化学方程式_____ 。
(3)如果反应中生成标准状况下11.2L氯气,则转移电子数为_____ 。
(4)二氧化氯可迅速氧化硫化物(其中还原产物中氯元素为-1价),以除去水中硫化物产生的臭味。取适量ClO2,通入到含有H2S(二元弱酸)的水中,再向其中加入少量氯化钡溶液,发现有白色沉淀生成。写出ClO2与H2S水溶液反应的离子方程式_____ 。
(1)实验室制备氯气的离子方程式是
II.常温下,二氧化氯(ClO2)是一种黄绿色气体,具有强氧化性,已被联合国世界卫生组织(WHO)列为高效安全消毒剂。常温下,它可用氯酸钠固体与浓盐酸反应制备得到,还有NaCl与Cl2生成。
(2)写出并配平该反应的化学方程式
(3)如果反应中生成标准状况下11.2L氯气,则转移电子数为
(4)二氧化氯可迅速氧化硫化物(其中还原产物中氯元素为-1价),以除去水中硫化物产生的臭味。取适量ClO2,通入到含有H2S(二元弱酸)的水中,再向其中加入少量氯化钡溶液,发现有白色沉淀生成。写出ClO2与H2S水溶液反应的离子方程式
您最近一年使用:0次
9 . SO2在生活、生产中有重要用途,使用不当会造成环境污染。
(1)某同学利用图所示装置研究二氧化硫的性质。
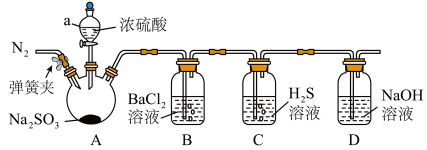
①仪器a的名称为___________ 。
②向仪器a中滴加浓硫酸之前,需先通入一段时间N2,此操作的目的是___________ 。
③实验时,装置B中没有明显变化。实验结束后取下装置B,向其中滴加适量氨水,生成的白色沉淀为___________ (填化学式)。
④装置C中出现淡黄色浑浊,说明二氧化硫具有___________ 性。
(2)某化工厂用图所示工艺流程除去燃煤产生的SO2。
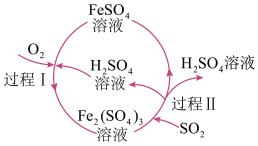
①过程I发生的反应为 ,用双线桥标出该反应电子转移的方向和数目
,用双线桥标出该反应电子转移的方向和数目___________ 。
②过程Ⅱ发生反应的化学方程式为___________ 。
(1)某同学利用图所示装置研究二氧化硫的性质。

①仪器a的名称为
②向仪器a中滴加浓硫酸之前,需先通入一段时间N2,此操作的目的是
③实验时,装置B中没有明显变化。实验结束后取下装置B,向其中滴加适量氨水,生成的白色沉淀为
④装置C中出现淡黄色浑浊,说明二氧化硫具有
(2)某化工厂用图所示工艺流程除去燃煤产生的SO2。

①过程I发生的反应为
 ,用双线桥标出该反应电子转移的方向和数目
,用双线桥标出该反应电子转移的方向和数目②过程Ⅱ发生反应的化学方程式为
您最近一年使用:0次
名校
解题方法
10 . 硫氰化钾(KSCN)是一种用途广泛的化学药品,常用于合成树脂、杀虫杀菌剂等。某化学小组用下图实验装置模拟工业制备硫氰化钾。

已知:①CS2为不溶于水且密度比水大的非极性试剂。
②NH4HS、(NH4)2S 在热水中易分解生成NH3和H2S。
③装置B中,滴液漏斗中装有一定体积5mol/L KOH溶液。
回答下列问题:
(1)制备NH4SCN溶液:
①三颈烧瓶内盛放有76g CS2、水和难溶于水的固体做催化剂。实验开始时,打开K1,水浴加热装置B,发生反应CS2+ 3NH3 NH4SCN + NH4HS, 则装置A中固体a的成分为
NH4SCN + NH4HS, 则装置A中固体a的成分为 _______ 。
②一段时间后,当观察到三颈烧瓶内_______ 时, 停止通入气体,反应完成。关闭K1和K2,将三颈烧瓶继续加热一段时间。
③装置C中用酸性KMnO4溶液吸收尾气后得澄清溶液,H2S所发生反应的离子方程式为_______ 。
(2)制备KSCN晶体:
打开K3,_______ , 干燥,得到硫氰化钾晶体。(须用的试剂:5mol/LKOH、蒸馏水、稀硫酸)
(3)测定产品中KSCN的含量:
称取0.85g样品,配成100mL溶液。量取25.00mL溶液锥形瓶中,加入适量稀硝酸,再加入几滴铁盐溶液作指示剂,用0.1000mol/LAgNO3标准溶液滴定,滴定时发生的反应:SCN—+Ag+=AgSCN↓(白色)。达到滴定终点,三次滴定平均消耗AgNO3标准溶液20.00mL。产品中KSCN的质量分数为_______ 。

已知:①CS2为不溶于水且密度比水大的非极性试剂。
②NH4HS、(NH4)2S 在热水中易分解生成NH3和H2S。
③装置B中,滴液漏斗中装有一定体积5mol/L KOH溶液。
回答下列问题:
(1)制备NH4SCN溶液:
①三颈烧瓶内盛放有76g CS2、水和难溶于水的固体做催化剂。实验开始时,打开K1,水浴加热装置B,发生反应CS2+ 3NH3
 NH4SCN + NH4HS, 则装置A中固体a的成分为
NH4SCN + NH4HS, 则装置A中固体a的成分为 ②一段时间后,当观察到三颈烧瓶内
③装置C中用酸性KMnO4溶液吸收尾气后得澄清溶液,H2S所发生反应的离子方程式为
(2)制备KSCN晶体:
打开K3,
(3)测定产品中KSCN的含量:
称取0.85g样品,配成100mL溶液。量取25.00mL溶液锥形瓶中,加入适量稀硝酸,再加入几滴铁盐溶液作指示剂,用0.1000mol/LAgNO3标准溶液滴定,滴定时发生的反应:SCN—+Ag+=AgSCN↓(白色)。达到滴定终点,三次滴定平均消耗AgNO3标准溶液20.00mL。产品中KSCN的质量分数为
您最近一年使用:0次
2022-04-20更新
|
459次组卷
|
4卷引用:江苏省南通市海门区2022届高三下学期阶段检测化学试题
江苏省南通市海门区2022届高三下学期阶段检测化学试题(已下线)考点51 物质的制备-备战2023年高考化学一轮复习考点帮(全国通用)江西省重点校联盟2022-2023学年高三上学期10月联考化学试题新疆乌鲁木齐市第101中学2023-2024学年高三上学期8月月考化学试题



