1 . 过二硫酸钾( )是一种白色结晶性粉末,溶于水、不溶于乙醇,具有强氧化性,加热至100℃时会完全分解。某学习小组拟探究过二硫酸钾的性质。
)是一种白色结晶性粉末,溶于水、不溶于乙醇,具有强氧化性,加热至100℃时会完全分解。某学习小组拟探究过二硫酸钾的性质。
实验(一):探究过二硫酸钾的强氧化性。
探究 溶液与
溶液与 溶液反应,实验操作与现象如下:
溶液反应,实验操作与现象如下:
(1)同学甲用碰撞理论分析,实验Ⅰ中 和
和 反应很慢的主要原因是
反应很慢的主要原因是___________
(2)同学乙猜想实验Ⅱ中 起催化作用,其总反应分两步进行:
起催化作用,其总反应分两步进行:
(ⅰ)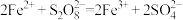 ;(ⅱ)___________。
;(ⅱ)___________。
①补充反应(ⅱ):___________ 。
②请你设计实验证明同学乙的猜想:___________ 。
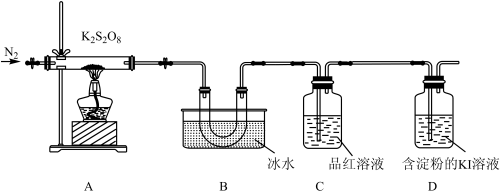
(3)查阅文献知,氧化性: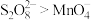 。在稀硫酸酸化的
。在稀硫酸酸化的 溶液中滴加1滴
溶液中滴加1滴 溶液作催化剂,再滴加
溶液作催化剂,再滴加 溶液,实验现象是
溶液,实验现象是___________ ,该反应的离子方程式为___________ 。
实验(二):探究过二硫酸钾的热稳定性。
已知几种气体的熔点、沸点如下表所示:
取适量的 装入硬质玻璃管中,加热,将分解产物依次通过装置B、C、D。实验中发现B中U形管内产生无色液体,接着无色液体慢慢变成固体,C中溶液颜色无明显变化,D中溶液逐渐变蓝色。
装入硬质玻璃管中,加热,将分解产物依次通过装置B、C、D。实验中发现B中U形管内产生无色液体,接着无色液体慢慢变成固体,C中溶液颜色无明显变化,D中溶液逐渐变蓝色。
(4)加热之前,先通入一段时间 ,当观察到D中
,当观察到D中___________ (填实验现象)时点燃酒精灯。
(5)B中U形管收集的物质是___________ (填化学式)。
(6)当A中硬质玻璃管中固体完全分解,停止加热,残留的固体产物只有一种。待冷却至室温时取少量残留固体于试管,加入蒸馏水,溶解后滴加BaCl2溶液和盐酸,产生白色沉淀。A中 完全分解发生反应的化学方程式为
完全分解发生反应的化学方程式为___________ 。
 )是一种白色结晶性粉末,溶于水、不溶于乙醇,具有强氧化性,加热至100℃时会完全分解。某学习小组拟探究过二硫酸钾的性质。
)是一种白色结晶性粉末,溶于水、不溶于乙醇,具有强氧化性,加热至100℃时会完全分解。某学习小组拟探究过二硫酸钾的性质。实验(一):探究过二硫酸钾的强氧化性。
探究
 溶液与
溶液与 溶液反应,实验操作与现象如下:
溶液反应,实验操作与现象如下:| 实验 | 操作 | 现象 |
| Ⅰ | 在10L含淀粉的 的 的 溶液中滴加 溶液中滴加   溶液 溶液 | 一段时间后,溶液缓慢变蓝 |
| Ⅱ | 在 含淀粉的 含淀粉的 的 的 溶液中先滴几滴 溶液中先滴几滴 的 的 溶液,再滴加 溶液,再滴加   溶液 溶液 | 溶液迅速变蓝 |
 和
和 反应很慢的主要原因是
反应很慢的主要原因是(2)同学乙猜想实验Ⅱ中
 起催化作用,其总反应分两步进行:
起催化作用,其总反应分两步进行:(ⅰ)
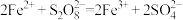 ;(ⅱ)___________。
;(ⅱ)___________。①补充反应(ⅱ):
②请你设计实验证明同学乙的猜想:
(3)查阅文献知,氧化性:
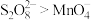 。在稀硫酸酸化的
。在稀硫酸酸化的 溶液中滴加1滴
溶液中滴加1滴 溶液作催化剂,再滴加
溶液作催化剂,再滴加 溶液,实验现象是
溶液,实验现象是实验(二):探究过二硫酸钾的热稳定性。
已知几种气体的熔点、沸点如下表所示:
| 气体 |  |  |  |
| 熔点/℃ | 16.8 | -72.7 | -218.4 |
| 沸点/℃ | 44.8 | -10 | -182.9 |
 装入硬质玻璃管中,加热,将分解产物依次通过装置B、C、D。实验中发现B中U形管内产生无色液体,接着无色液体慢慢变成固体,C中溶液颜色无明显变化,D中溶液逐渐变蓝色。
装入硬质玻璃管中,加热,将分解产物依次通过装置B、C、D。实验中发现B中U形管内产生无色液体,接着无色液体慢慢变成固体,C中溶液颜色无明显变化,D中溶液逐渐变蓝色。
(4)加热之前,先通入一段时间
 ,当观察到D中
,当观察到D中(5)B中U形管收集的物质是
(6)当A中硬质玻璃管中固体完全分解,停止加热,残留的固体产物只有一种。待冷却至室温时取少量残留固体于试管,加入蒸馏水,溶解后滴加BaCl2溶液和盐酸,产生白色沉淀。A中
 完全分解发生反应的化学方程式为
完全分解发生反应的化学方程式为
您最近一年使用:0次
2022-04-13更新
|
533次组卷
|
5卷引用:陕西省榆林市2022届高三第二次联考化学试题
陕西省榆林市2022届高三第二次联考化学试题(已下线)秘籍21 性质探究实验-备战2022年高考化学抢分秘籍(全国通用)甘肃省平凉市2022届高三下学期第二次模拟考试理科综合化学试题甘肃省兰州第一中学2022-2023学年高三上学期期中考试化学试题热点1物质性质探究类实验
名校
解题方法
2 . 二氧化铈(CeO2)是一种重要的稀土氧化物,平板电视显示屏生产过程中产生大量的废玻璃粉末(含SiO2、Fe2O3、CeO2、FeO等物质),某课题组以此粉末为原料,设计如图工艺流程对资源进行回收,得到纯净的CeO2和硫酸亚铁铵晶体。
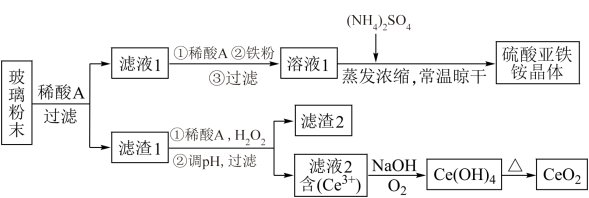
已知:CeO2不溶于稀硫酸,也不溶于NaOH溶液。
(1)Fe元素在元素周期表中的位置___________ 。
(2)稀酸A的分子式是___________ ;滤液1中加入铁粉的目的是___________ 。
(3)设计实验证明滤液l中含有Fe2+:___________ 。
(4)由滤渣1生成Ce3+的化学方程式为___________ 。
(5)硫酸铁铵晶体[Fe2(SO4)3·2(NH4)2SO4·3H2O]广泛用于水的净化处理,但其在去除酸性废水中的悬浮物时效率降低,其原因是___________ 。

已知:CeO2不溶于稀硫酸,也不溶于NaOH溶液。
(1)Fe元素在元素周期表中的位置
(2)稀酸A的分子式是
(3)设计实验证明滤液l中含有Fe2+:
(4)由滤渣1生成Ce3+的化学方程式为
(5)硫酸铁铵晶体[Fe2(SO4)3·2(NH4)2SO4·3H2O]广泛用于水的净化处理,但其在去除酸性废水中的悬浮物时效率降低,其原因是
您最近一年使用:0次
名校
解题方法
3 . 每年夏天是菠萝上市的季节,有不少的消费者因为菠萝“扎嘴”的口感而放弃这一酸酸甜甜独具风味的水果。菠萝“扎嘴”的原因之一是菠萝中含有一种难溶于水的草酸钙针晶。隔绝空气条件下,16.4g草酸钙晶体(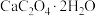 )受热分解过程的热重曲线(剩余固体质量随温度变化的曲线)如图所示,下列说法错误的是
)受热分解过程的热重曲线(剩余固体质量随温度变化的曲线)如图所示,下列说法错误的是
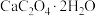 )受热分解过程的热重曲线(剩余固体质量随温度变化的曲线)如图所示,下列说法错误的是
)受热分解过程的热重曲线(剩余固体质量随温度变化的曲线)如图所示,下列说法错误的是
| A.草酸钙晶体中碳元素的化合价为+3价 |
B.物质M的化学式为 |
C.温度由200~520℃阶段,反应的化学方程式为 |
| D.温度高于940℃,所得物质X的俗名为熟石灰 |
您最近一年使用:0次
2023-10-08更新
|
183次组卷
|
3卷引用:陕西省榆林市靖边县靖边中学、绥德中学、府谷中学联考2023-2024学年高三上学期10月月考化学试题
名校
解题方法
4 . 以太阳能为热源分解 ,铁氧化合物循环分解水制
,铁氧化合物循环分解水制 的过程如图所示。下列说法错误的是
的过程如图所示。下列说法错误的是
 ,铁氧化合物循环分解水制
,铁氧化合物循环分解水制 的过程如图所示。下列说法错误的是
的过程如图所示。下列说法错误的是
| A.过程Ⅰ、Ⅱ发生的反应均属于氧化还原反应 |
| B.该制氢过程中,固体的颜色不会发生变化 |
C.过程Ⅰ中每消耗116g ,理论上转移2mol电子 ,理论上转移2mol电子 |
D.过程Ⅱ的化学方程式为 |
您最近一年使用:0次
2023-12-31更新
|
133次组卷
|
2卷引用:陕西省榆林市十校联考2023-2024学年高一上学期12月月考化学试题
解题方法
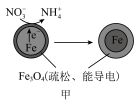
5 . 用零价铁去除酸性水体中的 是地下水修复研究的热点之一、下列说法错误的是
是地下水修复研究的热点之一、下列说法错误的是
 是地下水修复研究的热点之一、下列说法错误的是
是地下水修复研究的热点之一、下列说法错误的是
|
|
|
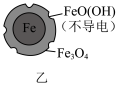
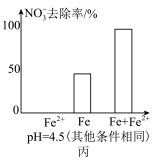
铁粉还原水体中 的反应原理示意图(已知:形成了原电池) 的反应原理示意图(已知:形成了原电池) | 足量铁粉还原水体中的 后,铁表面最终的形态示意图 后,铁表面最终的形态示意图 | 初始 的水体中,分别加入 的水体中,分别加入 、Fe(足量)、Fe(足量)和 、Fe(足量)、Fe(足量)和 时 时 去除率(%)的对比图像 去除率(%)的对比图像 |
| A.图甲中电极Fe发生氧化反应 |
B.图甲中正极发生的电极反应式为 |
C.当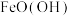 附着在Fe表面后会阻碍零价铁还原水体中的 附着在Fe表面后会阻碍零价铁还原水体中的 |
D.由图丙可知,去除 时,若只加入适量 时,若只加入适量 ,就可直接还原 ,就可直接还原 ,从而提高 ,从而提高 的去除率 的去除率 |
您最近一年使用:0次
解题方法
6 . 一种锂离子电池的正极材料中含钴酸锂( )。某离子反应涉及
)。某离子反应涉及 、
、 、
、 、
、 、
、 、
、 等微粒,溶液中
等微粒,溶液中 、
、 的粒子数目随时间变化的曲线如图所示。下列说法错误的是
的粒子数目随时间变化的曲线如图所示。下列说法错误的是
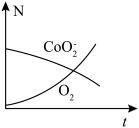
 )。某离子反应涉及
)。某离子反应涉及 、
、 、
、 、
、 、
、 、
、 等微粒,溶液中
等微粒,溶液中 、
、 的粒子数目随时间变化的曲线如图所示。下列说法错误的是
的粒子数目随时间变化的曲线如图所示。下列说法错误的是
A.反应中的还原剂是 |
B.氧化性: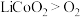 |
| C.反应配平后氧化剂与还原剂的化学计量数之比为2:1 |
D.每生成2分子 转移8个电子 转移8个电子 |
您最近一年使用:0次
解题方法
7 . 四氯化硅( )是制造半导体材料硅的中间产物,在空气中容易吸收水蒸气生成原硅酸(
)是制造半导体材料硅的中间产物,在空气中容易吸收水蒸气生成原硅酸(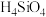 )和
)和 而产生白色烟雾,下列说法不正确的是
而产生白色烟雾,下列说法不正确的是
 )是制造半导体材料硅的中间产物,在空气中容易吸收水蒸气生成原硅酸(
)是制造半导体材料硅的中间产物,在空气中容易吸收水蒸气生成原硅酸(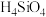 )和
)和 而产生白色烟雾,下列说法不正确的是
而产生白色烟雾,下列说法不正确的是A.由 转化为 转化为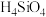 的过程中,硅元素化合价没有发生改变 的过程中,硅元素化合价没有发生改变 |
B.原硅酸中氢、氧元素的质量比为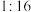 |
| C.四氯化硅由一个硅原子和四个氯原子构成 |
| D.四氯化硅应密封保存 |
您最近一年使用:0次
名校
8 . 以氯酸钠等为原料制备亚氯酸钠的工艺流程如下,下列说法错误的是
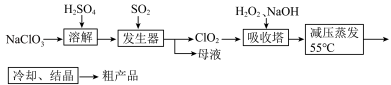

| A.NaClO3在发生器中作氧化剂 |
| B.吸收塔中1mol H2O2得到2mol电子 |
| C.吸收塔中温度不宜过高,会导致H2O2的分解 |
| D.从“母液”中可回收的主要物质是Na2SO4 |
您最近一年使用:0次
2019-03-16更新
|
1055次组卷
|
9卷引用:【市级联考】陕西省榆林市2019届高三下学期模拟考试化学试题