解题方法
1 .  具有耐高温的惰性,高活性,可广泛应用于制作各种塑料、橡胶、陶瓷、耐火材料等。工业上以油页岩灰渣(主要成分为
具有耐高温的惰性,高活性,可广泛应用于制作各种塑料、橡胶、陶瓷、耐火材料等。工业上以油页岩灰渣(主要成分为 、
、 ,含少量
,含少量 、
、 、
、 和其他不溶于酸、碱的杂质)为原料制备纳米
和其他不溶于酸、碱的杂质)为原料制备纳米 的流程如下。已知:
的流程如下。已知: 熔点高,硬度大,不溶于酸、碱;常温下,
熔点高,硬度大,不溶于酸、碱;常温下, 、
、 、
、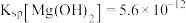 ;溶液中离子的浓度小于
;溶液中离子的浓度小于 时可视为该离子沉淀完全。请回答下列问题:
时可视为该离子沉淀完全。请回答下列问题:___________ ;加入 的目的是
的目的是___________ 。
(2)滤渣1的主要成分为___________ 、___________ 及不溶于酸、碱的杂质;加入 调节溶液的
调节溶液的 为13后,溶液中的
为13后,溶液中的
___________ 。
(3)若通入过量 ,发生的主要反应的离子方程式为
,发生的主要反应的离子方程式为___________ 。
(4)写出洗去固体A表面杂质的简要操作:___________ 。
(5)“煅烧”固体A反应的化学方程式为___________ 。
 具有耐高温的惰性,高活性,可广泛应用于制作各种塑料、橡胶、陶瓷、耐火材料等。工业上以油页岩灰渣(主要成分为
具有耐高温的惰性,高活性,可广泛应用于制作各种塑料、橡胶、陶瓷、耐火材料等。工业上以油页岩灰渣(主要成分为 、
、 ,含少量
,含少量 、
、 、
、 和其他不溶于酸、碱的杂质)为原料制备纳米
和其他不溶于酸、碱的杂质)为原料制备纳米 的流程如下。已知:
的流程如下。已知: 熔点高,硬度大,不溶于酸、碱;常温下,
熔点高,硬度大,不溶于酸、碱;常温下, 、
、 、
、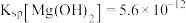 ;溶液中离子的浓度小于
;溶液中离子的浓度小于 时可视为该离子沉淀完全。请回答下列问题:
时可视为该离子沉淀完全。请回答下列问题:
 的目的是
的目的是(2)滤渣1的主要成分为
 调节溶液的
调节溶液的 为13后,溶液中的
为13后,溶液中的
(3)若通入过量
 ,发生的主要反应的离子方程式为
,发生的主要反应的离子方程式为(4)写出洗去固体A表面杂质的简要操作:
(5)“煅烧”固体A反应的化学方程式为
您最近半年使用:0次
2024-04-25更新
|
166次组卷
|
3卷引用:2024届陕西省榆林市高三上学期第一次模拟检测理综试题-高中化学
解题方法
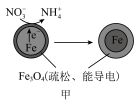
2 . 用零价铁去除酸性水体中的 是地下水修复研究的热点之一、下列说法错误的是
是地下水修复研究的热点之一、下列说法错误的是
 是地下水修复研究的热点之一、下列说法错误的是
是地下水修复研究的热点之一、下列说法错误的是
|
|
|
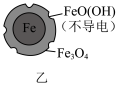
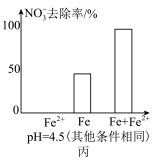
铁粉还原水体中 的反应原理示意图(已知:形成了原电池) 的反应原理示意图(已知:形成了原电池) | 足量铁粉还原水体中的 后,铁表面最终的形态示意图 后,铁表面最终的形态示意图 | 初始 的水体中,分别加入 的水体中,分别加入 、Fe(足量)、Fe(足量)和 、Fe(足量)、Fe(足量)和 时 时 去除率(%)的对比图像 去除率(%)的对比图像 |
| A.图甲中电极Fe发生氧化反应 |
B.图甲中正极发生的电极反应式为 |
C.当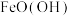 附着在Fe表面后会阻碍零价铁还原水体中的 附着在Fe表面后会阻碍零价铁还原水体中的 |
D.由图丙可知,去除 时,若只加入适量 时,若只加入适量 ,就可直接还原 ,就可直接还原 ,从而提高 ,从而提高 的去除率 的去除率 |
您最近半年使用:0次
解题方法
3 . 铋酸钠( ,难溶于水)是一种新型光催化剂,也被广泛应用于制药业。以辉铋矿(主要成分为
,难溶于水)是一种新型光催化剂,也被广泛应用于制药业。以辉铋矿(主要成分为 ,含
,含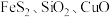 等杂质)为原料制备
等杂质)为原料制备 的工艺流程如图。
的工艺流程如图。
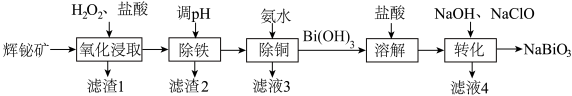
已知:“氧化浸取”时,铋元素转化为 ,硫元素转化为硫单质。回答下列问题:
,硫元素转化为硫单质。回答下列问题:
(1) 中铋元素的化合价为
中铋元素的化合价为___________ 价;“氧化浸取”时温度不能过高的原因是___________ ;“氧化浸取”时 发生反应的化学方程式为
发生反应的化学方程式为___________ 。
(2)“滤渣1”的主要成分为硫单质和___________ (写化学式)。
(3)“除铜”时,发生反应 ,该反应的平衡常数
,该反应的平衡常数
___________ 。{已知
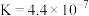 }
}
(4)在酸性介质中, 可将
可将 氧化为
氧化为 ,反应后
,反应后 元素呈
元素呈 价,则向足量稀硫酸和
价,则向足量稀硫酸和 稀溶液的混合溶液中加入
稀溶液的混合溶液中加入 时,反应中n(氧化剂):n(还原剂)=
时,反应中n(氧化剂):n(还原剂)=___________ 。
(5)“转化”时生成 反应的离子方程式为
反应的离子方程式为___________ 。
 ,难溶于水)是一种新型光催化剂,也被广泛应用于制药业。以辉铋矿(主要成分为
,难溶于水)是一种新型光催化剂,也被广泛应用于制药业。以辉铋矿(主要成分为 ,含
,含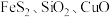 等杂质)为原料制备
等杂质)为原料制备 的工艺流程如图。
的工艺流程如图。
已知:“氧化浸取”时,铋元素转化为
 ,硫元素转化为硫单质。回答下列问题:
,硫元素转化为硫单质。回答下列问题:(1)
 中铋元素的化合价为
中铋元素的化合价为 发生反应的化学方程式为
发生反应的化学方程式为(2)“滤渣1”的主要成分为硫单质和
(3)“除铜”时,发生反应
 ,该反应的平衡常数
,该反应的平衡常数

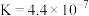 }
}(4)在酸性介质中,
 可将
可将 氧化为
氧化为 ,反应后
,反应后 元素呈
元素呈 价,则向足量稀硫酸和
价,则向足量稀硫酸和 稀溶液的混合溶液中加入
稀溶液的混合溶液中加入 时,反应中n(氧化剂):n(还原剂)=
时,反应中n(氧化剂):n(还原剂)=(5)“转化”时生成
 反应的离子方程式为
反应的离子方程式为
您最近半年使用:0次
解题方法
4 .  是一种强氧化剂,具有高效、广谱、安全的杀菌消毒能力。但是液体
是一种强氧化剂,具有高效、广谱、安全的杀菌消毒能力。但是液体 具有强烈刺激性、不稳定性、高浓度易爆等特点,可通过如图(加热及夹持装置已省略)装置制备稳定性
具有强烈刺激性、不稳定性、高浓度易爆等特点,可通过如图(加热及夹持装置已省略)装置制备稳定性 。回答下列问题:
。回答下列问题:
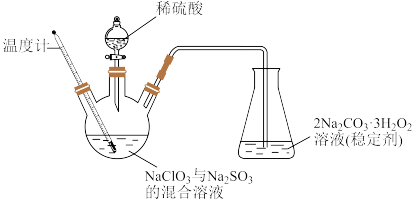
(1)盛装稀硫酸的仪器名称为___________ ;控制温度为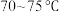 ,缓慢滴加稀硫酸,则该过程中适宜的加热方式为
,缓慢滴加稀硫酸,则该过程中适宜的加热方式为___________ ;写出生成 反应的化学方程式:
反应的化学方程式:___________ 。
(2)长导管的作用为___________ 。
(3)使用过碳酸钠( ,在水中转化为
,在水中转化为 和
和 )溶液作稳定剂时,
)溶液作稳定剂时, 被还原成较稳定的
被还原成较稳定的 ,可较长时间保存,写出锥形瓶中
,可较长时间保存,写出锥形瓶中 与
与 反应的离子方程式:
反应的离子方程式:___________ 。
(4)稳定液中的 并不能起到杀菌的作用,因此在实际应用中,必须对其进行活化,使
并不能起到杀菌的作用,因此在实际应用中,必须对其进行活化,使 转化成
转化成 释放出来。
释放出来。 活化率与不同活化剂(浓度均为
活化率与不同活化剂(浓度均为 )用量的关系如表。
)用量的关系如表。
①请分析盐酸活化效果最好的原因:___________ 。
②使用盐酸作活化剂时发生反应的离子方程式为___________ 。
 是一种强氧化剂,具有高效、广谱、安全的杀菌消毒能力。但是液体
是一种强氧化剂,具有高效、广谱、安全的杀菌消毒能力。但是液体 具有强烈刺激性、不稳定性、高浓度易爆等特点,可通过如图(加热及夹持装置已省略)装置制备稳定性
具有强烈刺激性、不稳定性、高浓度易爆等特点,可通过如图(加热及夹持装置已省略)装置制备稳定性 。回答下列问题:
。回答下列问题:
(1)盛装稀硫酸的仪器名称为
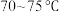 ,缓慢滴加稀硫酸,则该过程中适宜的加热方式为
,缓慢滴加稀硫酸,则该过程中适宜的加热方式为 反应的化学方程式:
反应的化学方程式:(2)长导管的作用为
(3)使用过碳酸钠(
 ,在水中转化为
,在水中转化为 和
和 )溶液作稳定剂时,
)溶液作稳定剂时, 被还原成较稳定的
被还原成较稳定的 ,可较长时间保存,写出锥形瓶中
,可较长时间保存,写出锥形瓶中 与
与 反应的离子方程式:
反应的离子方程式:(4)稳定液中的
 并不能起到杀菌的作用,因此在实际应用中,必须对其进行活化,使
并不能起到杀菌的作用,因此在实际应用中,必须对其进行活化,使 转化成
转化成 释放出来。
释放出来。 活化率与不同活化剂(浓度均为
活化率与不同活化剂(浓度均为 )用量的关系如表。
)用量的关系如表。活化剂用量 活化率 活化剂 | 5mL | 10mL | 15mL | 20mL | 25mL |
盐酸 | 29.32% | 58.02% | 86.91% | 99.57% | 100.00% |
醋酸 | 26.75% | 55.52% | 79.01% | 97.22% | 97.53% |
柠檬酸 | 20.03% | 41.22% | 52.13% | 53.76% | 59.80% |
②使用盐酸作活化剂时发生反应的离子方程式为
您最近半年使用:0次
2024-03-31更新
|
95次组卷
|
2卷引用:2024届陕西省榆林市高三上学期第一次模拟检测理综试题-高中化学
解题方法
5 . 一种锂离子电池的正极材料中含钴酸锂( )。某离子反应涉及
)。某离子反应涉及 、
、 、
、 、
、 、
、 、
、 等微粒,溶液中
等微粒,溶液中 、
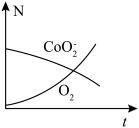
、 的粒子数目随时间变化的曲线如图所示。下列说法错误的是
的粒子数目随时间变化的曲线如图所示。下列说法错误的是
 )。某离子反应涉及
)。某离子反应涉及 、
、 、
、 、
、 、
、 、
、 等微粒,溶液中
等微粒,溶液中 、
、 的粒子数目随时间变化的曲线如图所示。下列说法错误的是
的粒子数目随时间变化的曲线如图所示。下列说法错误的是
A.反应中的还原剂是 |
B.氧化性: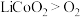 |
| C.反应配平后氧化剂与还原剂的化学计量数之比为2:1 |
D.每生成2分子 转移8个电子 转移8个电子 |
您最近半年使用:0次
6 . 以某工厂矿渣(主要含有 、
、 、
、 、
、 及少量
及少量 、
、 )为原料制备金属银及
)为原料制备金属银及 的工艺流程如图所示{已知:
的工艺流程如图所示{已知: }。
}。
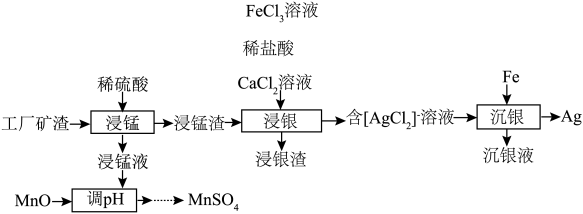
回答下列问题:
(1)“浸锰”时,发生反应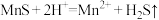 、
、 与
与 反应生成
反应生成 、
、 、
、 ,
, 残留于浸锰渣中。
残留于浸锰渣中。
①为了提高“浸锰”速率,可采取的措施为_______ (任写一种)。
② 发生反应时,消耗的
发生反应时,消耗的 与
与 物质的量之比为
物质的量之比为_______ 。
(2)“浸银”时,使用过量 、
、 和
和 的混合液作为浸出剂,将
的混合液作为浸出剂,将 中的银以
中的银以 的形式浸出。
的形式浸出。
①“浸银渣”的主要成分是_______ (填化学式)。
②配平“浸银”反应的离子方程式:_______ 。
_______ _______
_______ _______
_______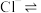 _______
_______ _______
_______ _______S。
_______S。
③结合平衡移动原理,解释浸出剂中 的作用:
的作用:_______ 。
(3)一定温度下,“沉银”时Ag的沉淀率随反应时间的变化如图所示。
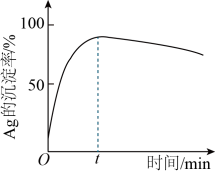
① 参加反应的离子方程式为
参加反应的离子方程式为_______ 。
②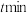 后Ag的沉淀率逐渐减小的原因可能是
后Ag的沉淀率逐渐减小的原因可能是_______ 。
 、
、 、
、 、
、 及少量
及少量 、
、 )为原料制备金属银及
)为原料制备金属银及 的工艺流程如图所示{已知:
的工艺流程如图所示{已知: }。
}。
回答下列问题:
(1)“浸锰”时,发生反应
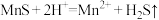 、
、 与
与 反应生成
反应生成 、
、 、
、 ,
, 残留于浸锰渣中。
残留于浸锰渣中。①为了提高“浸锰”速率,可采取的措施为
②
 发生反应时,消耗的
发生反应时,消耗的 与
与 物质的量之比为
物质的量之比为(2)“浸银”时,使用过量
 、
、 和
和 的混合液作为浸出剂,将
的混合液作为浸出剂,将 中的银以
中的银以 的形式浸出。
的形式浸出。①“浸银渣”的主要成分是
②配平“浸银”反应的离子方程式:
_______
 _______
_______ _______
_______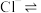 _______
_______ _______
_______ _______S。
_______S。③结合平衡移动原理,解释浸出剂中
 的作用:
的作用:(3)一定温度下,“沉银”时Ag的沉淀率随反应时间的变化如图所示。

①
 参加反应的离子方程式为
参加反应的离子方程式为②
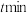 后Ag的沉淀率逐渐减小的原因可能是
后Ag的沉淀率逐渐减小的原因可能是
您最近半年使用:0次
7 . 铵铁蓝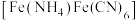 主要用于涂料和油墨工业等,工业上制备铵铁蓝的步骤如下:
主要用于涂料和油墨工业等,工业上制备铵铁蓝的步骤如下:
步骤1:在45℃左右条件下,将 、
、 与
与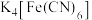 溶于水,用稀硫酸调节混合液的
溶于水,用稀硫酸调节混合液的 ,反应生成白色沉淀
,反应生成白色沉淀 ,用
,用 溶液检验
溶液检验 是否完全沉淀;
是否完全沉淀;
步骤2:过滤后加入稀硫酸和 ,加热条件下反应,经洗涤、干燥得
,加热条件下反应,经洗涤、干燥得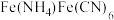 。回答下列问题:
。回答下列问题:
(1)“步骤1”的装置如图所示(加热装置已省略)。
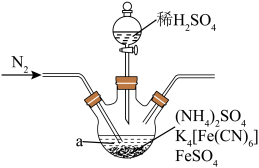
①仪器a的名称为_______ 。
②不断的通入 的目的为
的目的为_______ 。
③反应完成时溶液中,若 、
、 、
、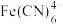 的浓度分别为
的浓度分别为 、
、 、
、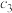 ,则
,则
_______ 。
(2)“步骤2”反应生成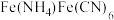 的化学方程式为
的化学方程式为_______ ;“洗涤”时,检验产品是否洗涤干净的试剂为_______ 。
(3)实验室制取并配制 溶液,用以检验
溶液,用以检验 是否完全沉淀:将
是否完全沉淀:将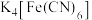 的饱和溶液在60℃以下进行电解,生成
的饱和溶液在60℃以下进行电解,生成 及副产品
及副产品 。待电解液中
。待电解液中 含量达
含量达 时开始冷却结晶、分离、干燥,制得
时开始冷却结晶、分离、干燥,制得 ,配制
,配制 的
的 溶液。
溶液。
① 中Fe元素的化合价为
中Fe元素的化合价为_______ 。
②电解时,阴极的电极反应为_______ ,“分离”时玻璃棒的作用为_______ 。
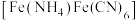 主要用于涂料和油墨工业等,工业上制备铵铁蓝的步骤如下:
主要用于涂料和油墨工业等,工业上制备铵铁蓝的步骤如下:步骤1:在45℃左右条件下,将
 、
、 与
与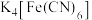 溶于水,用稀硫酸调节混合液的
溶于水,用稀硫酸调节混合液的 ,反应生成白色沉淀
,反应生成白色沉淀 ,用
,用 溶液检验
溶液检验 是否完全沉淀;
是否完全沉淀;步骤2:过滤后加入稀硫酸和
 ,加热条件下反应,经洗涤、干燥得
,加热条件下反应,经洗涤、干燥得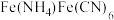 。回答下列问题:
。回答下列问题:(1)“步骤1”的装置如图所示(加热装置已省略)。

①仪器a的名称为
②不断的通入
 的目的为
的目的为③反应完成时溶液中,若
 、
、 、
、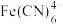 的浓度分别为
的浓度分别为 、
、 、
、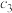 ,则
,则
(2)“步骤2”反应生成
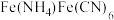 的化学方程式为
的化学方程式为(3)实验室制取并配制
 溶液,用以检验
溶液,用以检验 是否完全沉淀:将
是否完全沉淀:将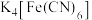 的饱和溶液在60℃以下进行电解,生成
的饱和溶液在60℃以下进行电解,生成 及副产品
及副产品 。待电解液中
。待电解液中 含量达
含量达 时开始冷却结晶、分离、干燥,制得
时开始冷却结晶、分离、干燥,制得 ,配制
,配制 的
的 溶液。
溶液。①
 中Fe元素的化合价为
中Fe元素的化合价为②电解时,阴极的电极反应为
您最近半年使用:0次
解题方法
8 . 羰基硫( ,沸点:
,沸点: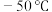 )又称氧硫化碳,其结构与
)又称氧硫化碳,其结构与 类似.回答下列问题:
类似.回答下列问题:
(1)实验室中通常用粉状硫氰化钾、水和浓硫酸反应制备 ,同时生成两种硫酸氢盐。写出该反应的化学方程式:
,同时生成两种硫酸氢盐。写出该反应的化学方程式:__________________________________ .
(2)以 为原料制备其他含硫物质的流程如下(部分产物已略去):
为原料制备其他含硫物质的流程如下(部分产物已略去):
 溶液
溶液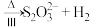
①反应Ⅰ中另一种产物是_____________ 。
②写出反应Ⅲ的离子方程式:_____________________________________________ 。
(3) 和
和 反应是制备
反应是制备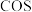 的另一种方法。恒温下,向体积为
的另一种方法。恒温下,向体积为 密闭容器中分别充入
密闭容器中分别充入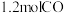 和
和 ,发生反应:
,发生反应: 后达到平衡状态,测得混合体系中含
后达到平衡状态,测得混合体系中含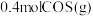 。
。
①平衡时, 的浓度为
的浓度为_____________  ;
; 内用
内用 表示的化学反应速率
表示的化学反应速率_____________  。
。
②下列描述中能说明上述反应已达平衡状态的是_____________ (填字母)。
a.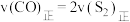
b.容器中气体的平均相对分子质量不随时间而变化
c.容器中气体的密度不随时间而变化
d.容器内气体压强保持不变
 ,沸点:
,沸点: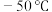 )又称氧硫化碳,其结构与
)又称氧硫化碳,其结构与 类似.回答下列问题:
类似.回答下列问题:(1)实验室中通常用粉状硫氰化钾、水和浓硫酸反应制备
 ,同时生成两种硫酸氢盐。写出该反应的化学方程式:
,同时生成两种硫酸氢盐。写出该反应的化学方程式:(2)以
 为原料制备其他含硫物质的流程如下(部分产物已略去):
为原料制备其他含硫物质的流程如下(部分产物已略去): 溶液
溶液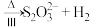
①反应Ⅰ中另一种产物是
②写出反应Ⅲ的离子方程式:
(3)
 和
和 反应是制备
反应是制备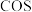 的另一种方法。恒温下,向体积为
的另一种方法。恒温下,向体积为 密闭容器中分别充入
密闭容器中分别充入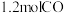 和
和 ,发生反应:
,发生反应: 后达到平衡状态,测得混合体系中含
后达到平衡状态,测得混合体系中含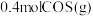 。
。①平衡时,
 的浓度为
的浓度为 ;
; 内用
内用 表示的化学反应速率
表示的化学反应速率 。
。②下列描述中能说明上述反应已达平衡状态的是
a.
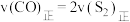
b.容器中气体的平均相对分子质量不随时间而变化
c.容器中气体的密度不随时间而变化
d.容器内气体压强保持不变
您最近半年使用:0次
名校
解题方法
9 . 以太阳能为热源分解 ,铁氧化合物循环分解水制
,铁氧化合物循环分解水制 的过程如图所示。下列说法错误的是
的过程如图所示。下列说法错误的是
 ,铁氧化合物循环分解水制
,铁氧化合物循环分解水制 的过程如图所示。下列说法错误的是
的过程如图所示。下列说法错误的是
| A.过程Ⅰ、Ⅱ发生的反应均属于氧化还原反应 |
| B.该制氢过程中,固体的颜色不会发生变化 |
C.过程Ⅰ中每消耗116g ,理论上转移2mol电子 ,理论上转移2mol电子 |
D.过程Ⅱ的化学方程式为 |
您最近半年使用:0次
2023-12-31更新
|
130次组卷
|
2卷引用:陕西省榆林市十校联考2023-2024学年高一上学期12月月考化学试题
名校
解题方法
10 . 写出下列化学反应方程
(1)氢气在氧气中燃烧___________ ;
(2)过氧化氢在二氧化锰的催化下分解___________ ;
(3)锌和硫酸反应制取氢气的反应方程式___________ 。
(1)氢气在氧气中燃烧
(2)过氧化氢在二氧化锰的催化下分解
(3)锌和硫酸反应制取氢气的反应方程式
您最近半年使用:0次