解题方法
1 . 物质分类与转化是学习化学的基石,如图为氯及其化合物的“价-类”二维图,请正确回答下列问题:
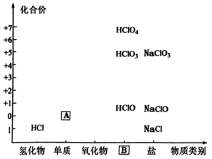
(1)填写二维图缺失的内容:化学式A__________ ;类别B__________ 。
(2)A可与热的 浓溶液反应生成
浓溶液反应生成 和
和 ,写出反应的化学方程式
,写出反应的化学方程式__________ 。
(3)关于盐酸与 反应,同学们有不同意见,甲同学认为发生反应:
反应,同学们有不同意见,甲同学认为发生反应: ,该反应属于
,该反应属于__________ 反应类型(填四大基本反应类型);乙同学认为发生氧化还原反应,因为他曾经看到一篇报道称:某家庭主妇在清洗卫生间时,因混合使用“洁厕灵”(主要成分是稀盐酸)与“84”消毒液(主要成分是 )而发生氯气中毒事件。请写出反应方程式
)而发生氯气中毒事件。请写出反应方程式__________ ,该反应从化合价角度体现了盐酸具有__________ 性。

(1)填写二维图缺失的内容:化学式A
(2)A可与热的
 浓溶液反应生成
浓溶液反应生成 和
和 ,写出反应的化学方程式
,写出反应的化学方程式(3)关于盐酸与
 反应,同学们有不同意见,甲同学认为发生反应:
反应,同学们有不同意见,甲同学认为发生反应: ,该反应属于
,该反应属于 )而发生氯气中毒事件。请写出反应方程式
)而发生氯气中毒事件。请写出反应方程式
您最近一年使用:0次
名校
解题方法
2 . 为纪念元素周期表诞生150周年,IUPAC等向世界介绍了118位优秀青年化学家,并形成一张“青年化学家元素周期表”。中国学者雷晓光、姜雪峰、刘庄分别成为“ ,
, 、
、 ”元素的代言人。回答下列问题:
”元素的代言人。回答下列问题:
(1)根据汞的原子结构示意图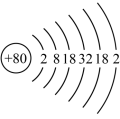 判断,汞在第
判断,汞在第___________ 周期。工业上冶炼金属汞的方法为___________ 。
(2)硒(Se)与硫位于同一主族,均是生命必需元素。下列推断不正确的是___________ 。
A.硒元素的最低负化合价为 价
价
B.还原性: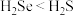
C.二氧化硒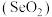 具有还原性
具有还原性
(3)氮是自然界各种生物体生命活动不可缺少的重要元素,磷(P)、砷(As)也是氮族元素。
①砷有多种同位素原子,其中稳定的核素是 ,它的中子数为
,它的中子数为___________ 。
②已知 与
与 的性质相似,则对
的性质相似,则对 性质的推测正确的是
性质的推测正确的是___________ 。
A.含有离子键和共价键
B.能与 溶液反应
溶液反应
C.加热充分分解时与 分解产物的种类完全一样
分解产物的种类完全一样
③下列关于第ⅤA族元素及其化合物的说法正确的是___________ 。
A.热稳定性:
B.As的氧化物的水化物是强碱
C.简单离子半径随原子序数递增而增大
(4)砷酸 可用于制造杀虫剂、药物等。
可用于制造杀虫剂、药物等。 溶于稀硝酸中可得砷酸,此反应的化学方程式为
溶于稀硝酸中可得砷酸,此反应的化学方程式为___________ 。
 ,
, 、
、 ”元素的代言人。回答下列问题:
”元素的代言人。回答下列问题:(1)根据汞的原子结构示意图
 判断,汞在第
判断,汞在第(2)硒(Se)与硫位于同一主族,均是生命必需元素。下列推断不正确的是
A.硒元素的最低负化合价为
 价
价B.还原性:
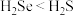
C.二氧化硒
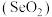 具有还原性
具有还原性(3)氮是自然界各种生物体生命活动不可缺少的重要元素,磷(P)、砷(As)也是氮族元素。
①砷有多种同位素原子,其中稳定的核素是
 ,它的中子数为
,它的中子数为②已知
 与
与 的性质相似,则对
的性质相似,则对 性质的推测正确的是
性质的推测正确的是A.含有离子键和共价键
B.能与
 溶液反应
溶液反应C.加热充分分解时与
 分解产物的种类完全一样
分解产物的种类完全一样③下列关于第ⅤA族元素及其化合物的说法正确的是
A.热稳定性:

B.As的氧化物的水化物是强碱
C.简单离子半径随原子序数递增而增大
(4)砷酸
 可用于制造杀虫剂、药物等。
可用于制造杀虫剂、药物等。 溶于稀硝酸中可得砷酸,此反应的化学方程式为
溶于稀硝酸中可得砷酸,此反应的化学方程式为
您最近一年使用:0次
2024-02-11更新
|
136次组卷
|
3卷引用:山东省东明县第一中学2023-2024学年高一下学期4月第一次月考化学试题
名校
3 . 现有以下物质:① ②Cu③
②Cu③ ④
④ 胶体⑤
胶体⑤ 溶液⑥干冰⑦稀硝酸⑧乙醇⑨熔融碳酸钠。回答下列问题:
溶液⑥干冰⑦稀硝酸⑧乙醇⑨熔融碳酸钠。回答下列问题:
(1)以上物质中属于电解质的是_______ (填序号,下同);上述状态下能导电的是________ 。
(2)①的电离方程式为___________ 。
(3)向④中逐滴滴加⑦,可观察到的现象是___________ 。
(4)⑤中混有少量①,除杂过程中选用的试剂为___________ 。
(5)③可发生如下反应 (未配平);配平该反应并用双线桥法分析电子转移的情况:
(未配平);配平该反应并用双线桥法分析电子转移的情况:________ ;每生成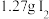 ,反应中转移电子的物质的量为
,反应中转移电子的物质的量为________ 。
 ②Cu③
②Cu③ ④
④ 胶体⑤
胶体⑤ 溶液⑥干冰⑦稀硝酸⑧乙醇⑨熔融碳酸钠。回答下列问题:
溶液⑥干冰⑦稀硝酸⑧乙醇⑨熔融碳酸钠。回答下列问题:(1)以上物质中属于电解质的是
(2)①的电离方程式为
(3)向④中逐滴滴加⑦,可观察到的现象是
(4)⑤中混有少量①,除杂过程中选用的试剂为
(5)③可发生如下反应
 (未配平);配平该反应并用双线桥法分析电子转移的情况:
(未配平);配平该反应并用双线桥法分析电子转移的情况: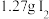 ,反应中转移电子的物质的量为
,反应中转移电子的物质的量为
您最近一年使用:0次
解题方法
4 . 图示分析是学习化学的一种重要方法,结合所给图示回答相关问题。
(1)下图是氮及其化合物的“价—类”二维图部分信息。

①X的化学式为________ 。
②图中关于 和
和 的相互转化,下列说法正确的是
的相互转化,下列说法正确的是________ (填标号)。
a.由 转化为
转化为 ,实现了氮的固定
,实现了氮的固定
b.工业上利用 与
与 反应制取
反应制取
c.不加入还原剂,也可实现 转化为
转化为
d.由硝酸转化成等物质的量的 时,消耗碳单质和铜单质的物质的量相同
时,消耗碳单质和铜单质的物质的量相同
(2) 、
、 是大气污染物的主要成分,
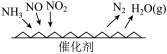
是大气污染物的主要成分, 催化还原氮氧化物是目前应用最广泛的烟气氮氧化物脱除技术,反应原理如图所示。若处理的污染物中
催化还原氮氧化物是目前应用最广泛的烟气氮氧化物脱除技术,反应原理如图所示。若处理的污染物中 与
与 的物质的量之比为1:1,则相应的化学方程式为
的物质的量之比为1:1,则相应的化学方程式为________ 。
(3)在微生物的作用下实现 转化,称为硝化过程。在碱性条件下,
转化,称为硝化过程。在碱性条件下, 被氧气氧化成
被氧气氧化成 的总反应的离子方程式为
的总反应的离子方程式为________ 。
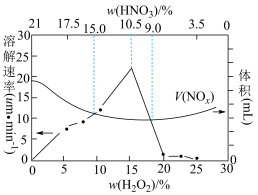
(4)硝酸可用作金属溶解剂。在不同浓度的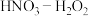 混合溶液中,金属溶解速率和生成
混合溶液中,金属溶解速率和生成 ,体积的变化如图。据图分析,混合溶液中
,体积的变化如图。据图分析,混合溶液中 的质量分数最佳为
的质量分数最佳为________ %,理由是________ 。
(1)下图是氮及其化合物的“价—类”二维图部分信息。

①X的化学式为
②图中关于
 和
和 的相互转化,下列说法正确的是
的相互转化,下列说法正确的是a.由
 转化为
转化为 ,实现了氮的固定
,实现了氮的固定b.工业上利用
 与
与 反应制取
反应制取
c.不加入还原剂,也可实现
 转化为
转化为
d.由硝酸转化成等物质的量的
 时,消耗碳单质和铜单质的物质的量相同
时,消耗碳单质和铜单质的物质的量相同(2)
 、
、 是大气污染物的主要成分,
是大气污染物的主要成分, 催化还原氮氧化物是目前应用最广泛的烟气氮氧化物脱除技术,反应原理如图所示。若处理的污染物中
催化还原氮氧化物是目前应用最广泛的烟气氮氧化物脱除技术,反应原理如图所示。若处理的污染物中 与
与 的物质的量之比为1:1,则相应的化学方程式为
的物质的量之比为1:1,则相应的化学方程式为
(3)在微生物的作用下实现
 转化,称为硝化过程。在碱性条件下,
转化,称为硝化过程。在碱性条件下, 被氧气氧化成
被氧气氧化成 的总反应的离子方程式为
的总反应的离子方程式为(4)硝酸可用作金属溶解剂。在不同浓度的
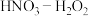 混合溶液中,金属溶解速率和生成
混合溶液中,金属溶解速率和生成 ,体积的变化如图。据图分析,混合溶液中
,体积的变化如图。据图分析,混合溶液中 的质量分数最佳为
的质量分数最佳为
您最近一年使用:0次
名校
5 .  分子曾因污染空气而臭名昭著,但随着“扩张血管、免疫、增强记忆”功能的发现,现在成为当前生命科学研究中的“明星分子”,回答下列问题:
分子曾因污染空气而臭名昭著,但随着“扩张血管、免疫、增强记忆”功能的发现,现在成为当前生命科学研究中的“明星分子”,回答下列问题:
(1)汽车燃料中一般不含氮元素,尾气中所含的 是如何产生的?请用化学方程式解释相关原因
是如何产生的?请用化学方程式解释相关原因___________ 。
(2)在含有 的酶的活化中心,亚硝酸根离子(
的酶的活化中心,亚硝酸根离子( )可转化为
)可转化为 ,写出
,写出 和
和 在酸性溶液中转化为
在酸性溶液中转化为 的离子方程式
的离子方程式___________ 。
(3)一定条件下 可转化为
可转化为 和另一种红棕色气体,方程式为
和另一种红棕色气体,方程式为___________ 。
(4)镁铁混合物 ,溶解在过量的某浓度的稀硝酸中,完全反应后得到标准状况下
,溶解在过量的某浓度的稀硝酸中,完全反应后得到标准状况下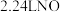 气体。若向反应后的溶液中加入足量的烧碱,则可生成沉淀的质量是
气体。若向反应后的溶液中加入足量的烧碱,则可生成沉淀的质量是___________ 。
 分子曾因污染空气而臭名昭著,但随着“扩张血管、免疫、增强记忆”功能的发现,现在成为当前生命科学研究中的“明星分子”,回答下列问题:
分子曾因污染空气而臭名昭著,但随着“扩张血管、免疫、增强记忆”功能的发现,现在成为当前生命科学研究中的“明星分子”,回答下列问题:(1)汽车燃料中一般不含氮元素,尾气中所含的
 是如何产生的?请用化学方程式解释相关原因
是如何产生的?请用化学方程式解释相关原因(2)在含有
 的酶的活化中心,亚硝酸根离子(
的酶的活化中心,亚硝酸根离子( )可转化为
)可转化为 ,写出
,写出 和
和 在酸性溶液中转化为
在酸性溶液中转化为 的离子方程式
的离子方程式(3)一定条件下
 可转化为
可转化为 和另一种红棕色气体,方程式为
和另一种红棕色气体,方程式为(4)镁铁混合物
 ,溶解在过量的某浓度的稀硝酸中,完全反应后得到标准状况下
,溶解在过量的某浓度的稀硝酸中,完全反应后得到标准状况下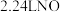 气体。若向反应后的溶液中加入足量的烧碱,则可生成沉淀的质量是
气体。若向反应后的溶液中加入足量的烧碱,则可生成沉淀的质量是
您最近一年使用:0次
6 .  为白色立方结晶或白色粉末,难溶于水,露置于空气中易被氧化为绿色的碱式氯化铜。以工业废铜泥为原料制备
为白色立方结晶或白色粉末,难溶于水,露置于空气中易被氧化为绿色的碱式氯化铜。以工业废铜泥为原料制备 的流程如下图(工业废铜泥的主要成分为
的流程如下图(工业废铜泥的主要成分为 、
、 、
、 还含有Fe等金属杂质)
还含有Fe等金属杂质)

下列说法错误的是
 为白色立方结晶或白色粉末,难溶于水,露置于空气中易被氧化为绿色的碱式氯化铜。以工业废铜泥为原料制备
为白色立方结晶或白色粉末,难溶于水,露置于空气中易被氧化为绿色的碱式氯化铜。以工业废铜泥为原料制备 的流程如下图(工业废铜泥的主要成分为
的流程如下图(工业废铜泥的主要成分为 、
、 、
、 还含有Fe等金属杂质)
还含有Fe等金属杂质)
下列说法错误的是
A.“灼烧”不充分会降低 的产率 的产率 |
| B.溶液1经处理后可循环使用 |
| C.“除杂”步骤中,应加过量的氢氧化钠溶液 |
| D.为了保证产品纯度,应采用减压过滤及真空干燥的方式 |
您最近一年使用:0次
名校
7 . 按要求完成下列填空:
(1)写出 在水中的电离方程式
在水中的电离方程式___________ 。
(2)向新制氯水中滴加石蕊试液,溶液变红,起作用的微粒是___________ ;然后又褪色,起作用的微粒是___________ 。
(3)实验证明铜、不能在低温下与 反应,也不能与稀
反应,也不能与稀 共热发生反应,但工业上却是将废铜屑倒入热的稀
共热发生反应,但工业上却是将废铜屑倒入热的稀 中并通入空气来制备
中并通入空气来制备 溶液的。铜屑在此状态下被溶解的化学方程式为
溶液的。铜屑在此状态下被溶解的化学方程式为___________ 。
(4)过量铁粉与稀硝酸反应方程式为: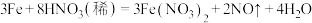 此反应中,被还原和未被还原的硝酸的物质的量之比为
此反应中,被还原和未被还原的硝酸的物质的量之比为___________ 。当产生 气体在标况下体积为
气体在标况下体积为 时,转移电子
时,转移电子___________  ,被还原的硝酸的物质的量为
,被还原的硝酸的物质的量为___________  。
。
(5)漂白粉是常用的消毒剂。漂白粉的有效成分是(填化学式)___________ 。
(1)写出
 在水中的电离方程式
在水中的电离方程式(2)向新制氯水中滴加石蕊试液,溶液变红,起作用的微粒是
(3)实验证明铜、不能在低温下与
 反应,也不能与稀
反应,也不能与稀 共热发生反应,但工业上却是将废铜屑倒入热的稀
共热发生反应,但工业上却是将废铜屑倒入热的稀 中并通入空气来制备
中并通入空气来制备 溶液的。铜屑在此状态下被溶解的化学方程式为
溶液的。铜屑在此状态下被溶解的化学方程式为(4)过量铁粉与稀硝酸反应方程式为:
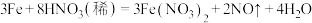 此反应中,被还原和未被还原的硝酸的物质的量之比为
此反应中,被还原和未被还原的硝酸的物质的量之比为 气体在标况下体积为
气体在标况下体积为 时,转移电子
时,转移电子 ,被还原的硝酸的物质的量为
,被还原的硝酸的物质的量为 。
。(5)漂白粉是常用的消毒剂。漂白粉的有效成分是(填化学式)
您最近一年使用:0次
名校
8 . 元素周期表与元素周期律在化学学习研究中有很重要的作用。如表是元素周期表的一部分,回答下列问题(用相关化学用语回答)。
(1)③、⑥、⑨的简单离子半径由小到大的顺序___________ (用离子符号表示)。
(2)写出元素⑪的单质与水反应的化学方程式___________ 。
(3)元素③、④、⑩的简单气态氢化物的稳定性最强的是___________ (用化学式表示)。
(4)配制0.1mol/L500mL元素⑤的氢氧化物溶液,需用托盘天平称取该氢氧化物的质量是___________ g。
(5)⑤2⑨③3在加热条件下发生分解反应生成两种盐,其中氧化产物与还原产物的物质的量之比为3:1,该反应的化学方程式:___________ 。
(6)欲比较④和⑨两种元素的非金属性强弱,可以作为验证的证据是___________(填字母)。
| 族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ||
| 四 | ⑪ |
(2)写出元素⑪的单质与水反应的化学方程式
(3)元素③、④、⑩的简单气态氢化物的稳定性最强的是
(4)配制0.1mol/L500mL元素⑤的氢氧化物溶液,需用托盘天平称取该氢氧化物的质量是
(5)⑤2⑨③3在加热条件下发生分解反应生成两种盐,其中氧化产物与还原产物的物质的量之比为3:1,该反应的化学方程式:
(6)欲比较④和⑨两种元素的非金属性强弱,可以作为验证的证据是___________(填字母)。
| A.比较这两种元素单质的沸点 |
| B.比较这两种元素单质与氢气化合的难易 |
| C.比较这两种元素的最高价氧化物对应水化物的酸性强弱 |
| D.比较这两种元素的单质与酸或碱反应的难易程度 |
您最近一年使用:0次
解题方法
9 . 某化学学习小组同学用如下实验探究 的性质。请回答下列问题:
的性质。请回答下列问题:
(1)甲组分别取一定量氯化铁、氯化亚铁固体,均配制成 的溶液。在
的溶液。在  溶液中加入少量铁屑,其目的是
溶液中加入少量铁屑,其目的是___________ 。
(2)乙组同学取 溶液,加入几滴氯水,再加入1滴
溶液,加入几滴氯水,再加入1滴  溶液,溶液变红,说明
溶液,溶液变红,说明 可将
可将  氧化。
氧化。  溶液与氯水反应的离子方程式为:
溶液与氯水反应的离子方程式为:___________ 。
(3)丙组同学认为乙组的实验不够严谨,该组同学在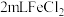 溶液中先加入
溶液中先加入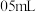 煤油,再于液面下依次加入几滴氯水和1滴
煤油,再于液面下依次加入几滴氯水和1滴  溶液,溶液变红,煤油的作用是
溶液,溶液变红,煤油的作用是___________ 。
(4)丁组同学探究证实了 沉淀易被
沉淀易被  氧化,写出该反应的化学方程式
氧化,写出该反应的化学方程式___________ 。
(5)戊组同学模拟工业上用 氧化酸性
氧化酸性  废液制备
废液制备  。
。
①若酸性 废液中:
废液中: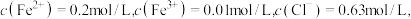 则该溶液的
则该溶液的
___________ 。
②完成 氧化酸性
氧化酸性  的离子方程式 (“□ ”中填离子或分子的化学式):
的离子方程式 (“□ ”中填离子或分子的化学式):___________
___________ +___________
+___________ ___________=___________
___________=___________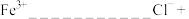 ___________。
___________。
 的性质。请回答下列问题:
的性质。请回答下列问题:(1)甲组分别取一定量氯化铁、氯化亚铁固体,均配制成
 的溶液。在
的溶液。在  溶液中加入少量铁屑,其目的是
溶液中加入少量铁屑,其目的是(2)乙组同学取
 溶液,加入几滴氯水,再加入1滴
溶液,加入几滴氯水,再加入1滴  溶液,溶液变红,说明
溶液,溶液变红,说明 可将
可将  氧化。
氧化。  溶液与氯水反应的离子方程式为:
溶液与氯水反应的离子方程式为:(3)丙组同学认为乙组的实验不够严谨,该组同学在
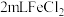 溶液中先加入
溶液中先加入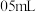 煤油,再于液面下依次加入几滴氯水和1滴
煤油,再于液面下依次加入几滴氯水和1滴  溶液,溶液变红,煤油的作用是
溶液,溶液变红,煤油的作用是(4)丁组同学探究证实了
 沉淀易被
沉淀易被  氧化,写出该反应的化学方程式
氧化,写出该反应的化学方程式(5)戊组同学模拟工业上用
 氧化酸性
氧化酸性  废液制备
废液制备  。
。①若酸性
 废液中:
废液中: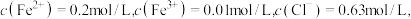 则该溶液的
则该溶液的
②完成
 氧化酸性
氧化酸性  的离子方程式 (“□ ”中填离子或分子的化学式):
的离子方程式 (“□ ”中填离子或分子的化学式):___________
 +___________
+___________ ___________=___________
___________=___________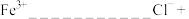 ___________。
___________。
您最近一年使用:0次
名校
解题方法
10 . 一种以镉废渣(含CdO及少量ZnO、CuO和FeO)为原料制备镉(Cd)的流程如下:
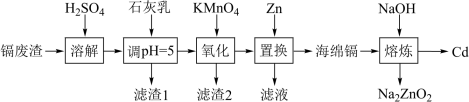
已知: 在酸性环境中被还原为
在酸性环境中被还原为 ,在弱酸性、弱碱性溶液中被还原为
,在弱酸性、弱碱性溶液中被还原为 ,在碱性环境中被还原为
,在碱性环境中被还原为 ;部分阳离子以氢氧化物形式沉淀时溶液pH如下。
;部分阳离子以氢氧化物形式沉淀时溶液pH如下。
下列说法正确的是

已知:
 在酸性环境中被还原为
在酸性环境中被还原为 ,在弱酸性、弱碱性溶液中被还原为
,在弱酸性、弱碱性溶液中被还原为 ,在碱性环境中被还原为
,在碱性环境中被还原为 ;部分阳离子以氢氧化物形式沉淀时溶液pH如下。
;部分阳离子以氢氧化物形式沉淀时溶液pH如下。 |  |  | |
| 开始沉淀时的pH | 2.7 | 6.3 | 3.8 |
| 完全沉淀时的pH | 3.2 | 8.3 | 5.0 |
| A.“调pH=5”可除去Fe和Cu等杂质 |
B.滤渣2的成分中含有 |
C.“置换”后滤液溶质主要成分是 和 和 |
| D.“熔炼”过程中有气体产生 |
您最近一年使用:0次



