名校
1 . 实现碳达峰、碳中和是党中央做出的重大战略决策。恒压、  时,
时, 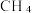 和
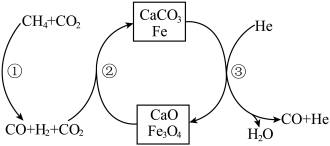
和  按物质的量之比1:3 投料,反应经如下流程(主要产物已标出)可实现
按物质的量之比1:3 投料,反应经如下流程(主要产物已标出)可实现 高效转化。下列说法正确的是
高效转化。下列说法正确的是
 时,
时, 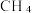 和
和  按物质的量之比1:3 投料,反应经如下流程(主要产物已标出)可实现
按物质的量之比1:3 投料,反应经如下流程(主要产物已标出)可实现 高效转化。下列说法正确的是
高效转化。下列说法正确的是
A.过程②中  的吸收,不利于CO还原 的吸收,不利于CO还原  的平衡正向移动 的平衡正向移动 |
B.过程③中通入 He 的作用是催化剂,加快  分解 分解 |
| C.过程①、②、③均涉及到了氧化还原反应 |
D. 可循环利用,而 CaO不可循环利用 可循环利用,而 CaO不可循环利用 |
您最近一年使用:0次
2 . 回答下列问题:
(1)中国古代著作中有“银针验毒”的记录,其原理为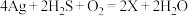 ,则X的化学式是
,则X的化学式是_______ ,其中 在该反应中
在该反应中_______ (填标号)。
A.作氧化剂 B.作还原剂
C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂
(2)按如图所示操作,充分反应后:
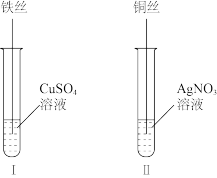
①Ⅱ中铜丝上观察到的现象是_______ 。
②结合Ⅰ、Ⅱ实验现象可知 、
、 、
、 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为_______ 。
(3)已知 可发生反应:
可发生反应: 。
。
①该反应中被还原的元素是_______ (填化学式,下同),氧化产物是_______ 。
②某温度下,将 通入
通入 溶液中,反应后得到
溶液中,反应后得到 、
、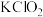 、
、 的混合溶液,经测定
的混合溶液,经测定 与
与 的数目之比为1:2,该反应的化学反应方程式为
的数目之比为1:2,该反应的化学反应方程式为_______ 。
(1)中国古代著作中有“银针验毒”的记录,其原理为
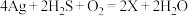 ,则X的化学式是
,则X的化学式是 在该反应中
在该反应中A.作氧化剂 B.作还原剂
C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂
(2)按如图所示操作,充分反应后:

①Ⅱ中铜丝上观察到的现象是
②结合Ⅰ、Ⅱ实验现象可知
 、
、 、
、 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为(3)已知
 可发生反应:
可发生反应: 。
。①该反应中被还原的元素是
②某温度下,将
 通入
通入 溶液中,反应后得到
溶液中,反应后得到 、
、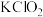 、
、 的混合溶液,经测定
的混合溶液,经测定 与
与 的数目之比为1:2,该反应的化学反应方程式为
的数目之比为1:2,该反应的化学反应方程式为
您最近一年使用:0次
2023-10-15更新
|
0次组卷
|
3卷引用:陕西省汉中市南郑区铁佛中学2023-2024学年高一上学期12月月考化学试题
3 . 高锰酸钾是一种典型的强氧化剂。
Ⅰ.用 酸性溶液处理
酸性溶液处理 和CuS的混合物时,发生如下反应:
和CuS的混合物时,发生如下反应:
①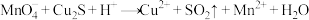 (未配平)
(未配平)
②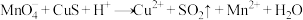 (未配平)
(未配平)
(1)反应①中被氧化的元素是__________ ,氧化剂与还原剂的物质的量之比为__________ 。
(2)当反应①中转移0.8mol电子,生成 的体积为
的体积为__________ L(标准状况下)。
(3)配平并用单线桥法标出反应②中电子转移的方向和数目______________ 。
Ⅱ.在稀硫酸中, 和
和 能发生氧化还原反应:
能发生氧化还原反应:
氧化反应:
还原反应:
(4)写出该氧化还原反应的离子方程式______________________________ 。
(5)反应中若有 参加此反应,转移电子的个数为
参加此反应,转移电子的个数为__________ 。
(6)由上述反应得出物质氧化性强弱的结论是
__________ (填“>”或“<”) 。
。
(7)实验中发现,当加入的少量 完全反应后,
完全反应后, 仍能发生反应放出气体,其原因可能是
仍能发生反应放出气体,其原因可能是__________ 。
Ⅰ.用
 酸性溶液处理
酸性溶液处理 和CuS的混合物时,发生如下反应:
和CuS的混合物时,发生如下反应:①
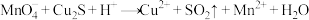 (未配平)
(未配平)②
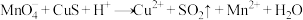 (未配平)
(未配平)(1)反应①中被氧化的元素是
(2)当反应①中转移0.8mol电子,生成
 的体积为
的体积为(3)配平并用单线桥法标出反应②中电子转移的方向和数目
Ⅱ.在稀硫酸中,
 和
和 能发生氧化还原反应:
能发生氧化还原反应:氧化反应:

还原反应:

(4)写出该氧化还原反应的离子方程式
(5)反应中若有
 参加此反应,转移电子的个数为
参加此反应,转移电子的个数为(6)由上述反应得出物质氧化性强弱的结论是

 。
。(7)实验中发现,当加入的少量
 完全反应后,
完全反应后, 仍能发生反应放出气体,其原因可能是
仍能发生反应放出气体,其原因可能是
您最近一年使用:0次
解题方法
4 . 下列离子反应方程式的书写错误的是
| A.AgCl浊液中通入H2S,变黑:2AgCl+H2S=Ag2S+2H++2Cl- |
B.用亚硫酸钠溶液吸收少量氯气:3SO +Cl2+H2O=2HSO +Cl2+H2O=2HSO +2Cl-+SO +2Cl-+SO |
| C.醋酸除去水垢中的碳酸钙:CaCO3+2H+=Ca2++CO2↑+H2O |
| D.氯化铁溶液腐蚀电路板:2Fe3++Cu=2Fe2++Cu2+ |
您最近一年使用:0次
名校
解题方法
5 . 已知Mn2O 与S2-在酸性溶液中能发生反应: Mn2O
与S2-在酸性溶液中能发生反应: Mn2O +3S2-+14H+=2Mn3++3S↓+7H2O,则Mn2O
+3S2-+14H+=2Mn3++3S↓+7H2O,则Mn2O 中锰元素的化合价是
中锰元素的化合价是
 与S2-在酸性溶液中能发生反应: Mn2O
与S2-在酸性溶液中能发生反应: Mn2O +3S2-+14H+=2Mn3++3S↓+7H2O,则Mn2O
+3S2-+14H+=2Mn3++3S↓+7H2O,则Mn2O 中锰元素的化合价是
中锰元素的化合价是| A.+2 | B.+4 | C.+3 | D.+6 |
您最近一年使用:0次
2022-02-28更新
|
853次组卷
|
36卷引用:陕西省汉中市龙岗学校2019-2020学年高一上学期期末考试化学试题
陕西省汉中市龙岗学校2019-2020学年高一上学期期末考试化学试题河南省安阳市第三十六中学2017-2018学年高一上学期期中考试化学试题安徽省阜阳市第三中学2018-2019学年高一下学期开学考试化学试题夯基提能2020届高三化学选择题对题专练——氧化还原反应的实际应用广东省2020年普通高中学业水平考试化学合格性考试模拟试题(七)(已下线)【南昌新东方】江西省九江一中2013-2014学年高一上学期期中考试化学试题广东省珠海市第二中学2019-2020学年高一上学期期中考试化学试题广东省中山纪念中学2019-2020学年高一上学期第二次段考化学试题山东省济宁市邹城兖矿一中2020-2021学年度高一9月月考化学试题吉林公主岭范家屯一中2020-2021学年高一上学期期中考试化学试题(已下线)【浙江新东方】30湖南省岳阳市楚雄中学2020-2021学年高一上学期期中考试化学试题广东省湛江市第四中学2020-2021学年高一上学期期中考试化学试题北京市铁路第二中学2020-2021学年高一上学期期中考试化学试题(已下线)【南昌新东方】9. 2020 高一上 铁路一中 刘惠文 钟欣(已下线)【浙江新东方】双师 (55)宁夏青铜峡市高级中学2020-2021学年高一12月月考化学试题河北衡水市第十四中学2020-2021学年高一上学期三调考试化学试题天津市滨海新区2020-2021学年高一上学期期末考试化学试题河北省衡水市武邑武罗学校2020-2021学年高一上学期期中考试化学试题新疆巴音郭楞蒙古自治州第二中学2021届高三上学期第一次摸底考试化学试题河北省衡水市武强中学2020-2021学年高一上学期第一次月考化学试题云南省玉溪市江川区第二中学2020-2021学年高一下学期竞赛化学试题黑龙江省鸡西市第一中学2020-2021学年高一上学期第一次月考化学试题四川省成都市第七中学2021-2022学年高一上学期期中考试化学试题四川省攀枝花市第十五中学校2021-2022学年高一上学期期中考试化学试题安徽省安庆市第十中学2021-2022学年高一上学期10月月考化学试题江苏省宿迁市泗阳县实验高级中学2021-2022学年高一上学期第二次调研测试化学试题广东省梅州市兴宁市叶塘中学2021-2022学年高一上学期摸底考试化学试题浙江省绿谷联盟2022-2023学年高一上学期10月份考试化学试题 黑龙江省鹤岗市第一中学2022-2023学年高一上学期10月月考化学试题山西省晋城市第一中学校2022-2023学年高一上学期第二次调研考试化学试题四川省仁寿县铧强中学2021-2022学年高一上学期半期考试化学试题云南省昆明市第八中学2020-2021学年高一上学期期中考试化学试题(已下线)专题七 氧化还原反应天津市宁河区2023-2024学年高一上学期期末考试化学试题
名校
6 . KI淀粉溶液在酸性条件下能与氧气反应。现有以下实验记录:
回答下列问题:
(1)该反应的离子方程式为___________ 。
(2)该实验的目的是___________ 。
(3)实验试剂除了1 KI溶液、0.1
KI溶液、0.1 H2SO4溶液外,还需要的试剂是
H2SO4溶液外,还需要的试剂是___________ ,实验现象为___________ 。
(4)实验操作中除了需要上述条件外,还必须控制___________ (填字母)不变。
A.温度B.试剂的用量(体积)C.试剂添加的顺序
(5)由上述实验记录可得出的结论是___________ 。
(6)若要进行溶液酸性强弱对反应速率影响的探究实验,你会采取的实验方案是___________ 。
| 实验编号 | ① | ② | ③ | ④ | ⑤ |
| 温度/℃ | 30 | 40 | 50 | 60 | 70 |
| 显色时间/s | 160 | 80 | 40 | 20 | 10 |
(1)该反应的离子方程式为
(2)该实验的目的是
(3)实验试剂除了1
 KI溶液、0.1
KI溶液、0.1 H2SO4溶液外,还需要的试剂是
H2SO4溶液外,还需要的试剂是(4)实验操作中除了需要上述条件外,还必须控制
A.温度B.试剂的用量(体积)C.试剂添加的顺序
(5)由上述实验记录可得出的结论是
(6)若要进行溶液酸性强弱对反应速率影响的探究实验,你会采取的实验方案是
您最近一年使用:0次
2021-10-19更新
|
147次组卷
|
21卷引用:陕西省汉中市五校2020-2021学年高二上学期第一次月考化学试题
陕西省汉中市五校2020-2021学年高二上学期第一次月考化学试题(已下线)2013-2014学年广东省执信中学高二上学期期中考试理科化学试卷2015-2016学年安徽师大附中高二下期中化学试卷江西省赣县三中2018-2019学年高二上学期9月月考化学试题【校级联考】安徽省定远重点中学2018-2019学年高二下学期开学考试化学试题广东省揭阳市惠来县第一中学2019-2020学年高二上学期第一次阶段考试化学试题2019年10月21日《每日一题》2019-2020学年高二化学人教选修4——化学反应速率的实验探究山西省阳泉市2019-2020学年高二上学期期末考试化学试题(已下线)2.2+影响化学反应速率的因素-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)云南省新平县一中2020-2021学年高二下学期期中考试化学试题(已下线)考向21 化学反应速率及影响因素-备战2022年高考化学一轮复习考点微专题福建省福州格致中学2021-2022学年高二上学期第一阶段测试化学试题(10月)四川省凉山宁南中学2019-2020学年高二上学期第一次月考化学试题云南省丘北县第一中学2021-2022学年高二下学期3月份考试 化学试题云南省玉龙县第一中学2021-2022学年高二下学期3月份考试化学试题(已下线)2.3.3 化学反应速率综合分析-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修1)四川省广元市八二一中学2021-2022学年高二上学期期中考试化学试题云南省广南县二中2021-2022年学年高二下学期开学考试化学试题云南省楚雄第一中学2022-2023学年高二下学期期末考试化学试题安徽省滁州市定远县第三中学等2校2022-2023学年高二上学期12月月考化学试题(已下线)专题03 化学反应速率及影响因素、活化能【考题猜想】(9大题型)-2023-2024学年高二化学期中考点大串讲(人教版2019选择性必修1)
名校
解题方法
7 . 化学社的同学查阅资料发现,工业上曾经通过反应“3Fe+4NaOH Fe3O4↑+2H2↑+4Na”生产金属钠。下列说法正确的是
Fe3O4↑+2H2↑+4Na”生产金属钠。下列说法正确的是
 Fe3O4↑+2H2↑+4Na”生产金属钠。下列说法正确的是
Fe3O4↑+2H2↑+4Na”生产金属钠。下列说法正确的是A.还原产物是钠Na和 |
B.用磁铁可以将Fe与 分离 分离 |
| C.将生成的气体在空气中冷却可获得钠 |
D.每生成1molH2,该反应转移的电子数约为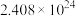 |
您最近一年使用:0次
2021-03-18更新
|
179次组卷
|
8卷引用:陕西省汉中市汉中中学2020-2021学年高一上学期期中考试化学试题
名校
解题方法
8 . 已知M2O + 3 S2- + 14H+= 2M 3++ 3S↓+ 7H2O,则M2O
+ 3 S2- + 14H+= 2M 3++ 3S↓+ 7H2O,则M2O 中的M的化合价为
中的M的化合价为
 + 3 S2- + 14H+= 2M 3++ 3S↓+ 7H2O,则M2O
+ 3 S2- + 14H+= 2M 3++ 3S↓+ 7H2O,则M2O 中的M的化合价为
中的M的化合价为| A.+2 | B.+3 | C.+4 | D.+6 |
您最近一年使用:0次
2020-11-25更新
|
1194次组卷
|
57卷引用:陕西省汉中中学2019届高三上学期第一次月考化学试题
陕西省汉中中学2019届高三上学期第一次月考化学试题(已下线)2010—2011学年黑龙江省大庆中学高一上学期期末考试化学试卷(已下线)2011-2012学年四川省成都七中实验学校高一上学期期中考试化学试卷(已下线)2011-2012学年湖北省荆州中学高一上学期期末考试化学试卷(已下线)2013-2014学年湖北省襄阳市四校高一上学期期中考试化学试卷2015-2016学年河南省许昌、襄城、长葛三校高一上期中测试化学试卷2015-2016学年湖北省宜昌市葛洲坝中学高一上学期期中测试化学试卷2015-2016学年四川省攀枝花十五中高一上期中试卷化学试卷2015-2016学年内蒙古巴彦淖尔一中高一上期中化学试卷2016-2017学年辽宁沈阳东北育才学校高一阶段考一化学卷2016-2017学年安徽省芜湖一中高一上期中考试化学试卷2016-2017学年甘肃省庆阳一中高一上期中化学卷2016-2017学年云南省昆明三中高一上期中化学试卷2017届河北省定州中学高三上期末化学试卷云南省南涧彝族自治县民族中学2017-2018学年高一9月月考化学试题甘肃省天水市第一中学2017-2018学年高一上学期第二学段考试化学试题吉林省长春外国语学校2017-2018学年高一上学期第二次月考化学试题重庆市西北狼联盟2017-2018学年高一上学期第一次联盟考试(12月)化学试题江西省南昌市八一中学2017-2018学年高一1月月考化学试题(已下线)2019高考备考一轮复习精品资料 第二章 化学物质及其变化第4讲 守恒思想在化学中的应用——守恒法解题技巧【押题专练】吉林省长春汽车经济开发区第六中学2017-2018学年高一上学期期中考试化学试题(已下线)【走进新高考】(人教版必修一)高一上学期期中复习模拟(A卷)(基础篇)02(已下线)【走进新高考】(人教版必修一)第二章 化学物质及其变化 单元练习01河南省安阳市第二中学2018-2019学年高一上学期期中考试化学试题河南省济源四中2018-2019学年高一上学期期中考试化学试题甘肃省张掖市民乐县第一中学2018-2019学年高一上学期期中考试化学试题广东省揭西县河婆中学2018-2019学年上学期高一期中考试化学试题陕西省榆林市第二中学2018-2019学年高二下学期期末考试化学试题浙江省金华市东阳中学2019-2020学年高一上学期开学考试化学试题黑龙江省齐齐哈尔市第八中学2019-2020学年高一上学期期中考试化学试题山西省忻州市岢岚县中学2019-2020学年高一上学期期中考试化学试题江西省高安中学2019-2020学年高一上学期期中考试化学(B)试题江苏省苏州市震泽中学2019-2020学年高一上学期第二次月考化学试题吉林省长春市榆树市第一高级中学2019-2020学年高一上学期尖子生考试化学试题安徽省合肥市一六八中2017-2018学年高一上学期期中考试化学试题福建省福州市八县一中2019-2020学年高二上学期期中考试化学试题北京市第四中学高中化学人教版选修4单元测试题:1.1化学反应及其能量变化(已下线)2.3.2 氧化还原反应的应用练习(2)——《高中新教材同步备课》(鲁科版 必修第一册)(已下线)第01章 物质及其变化(B卷能力提高篇)——2020-2021学年高一化学必修第一册同步单元AB卷(新教材人教版)江西省南昌市八一中学、麻丘高级中学等六校2020-2021学年高一上学期期中联考化学试题(已下线)【南昌新东方】10. 2020 高一上 洪八联考 晏梓超河南省三门峡市渑池县第二高级中学2020-2021学年高一上学期第三次月考化学试题江苏省盐城市上冈高级中学2020-2021学年高一上学期第二次学情检测化学试题河北省藁城新冀明中学2020-2021学年高一上学期12月月考化学试题(已下线)1.3.1 氧化还原反应-2021-2022学年高一化学课后培优练(人教版2019必修第一册)广东省揭阳市第一中学2017-2018学年高一上学期期中考试化学试题(已下线)必考点04 氧化还原反应的本质和相关概念-【对点变式题】2021-2022学年高一化学上学期期中期末必考题精准练(人教版2019)宁夏银川一中2021-2022学年高一上学期期中考试化学试题(已下线)第07练 氧化还原反应-2022年【寒假分层作业】高一化学(苏教版2019必修第一册)湖北省随州市第二中学2021-2022学年高一上学期10月月考化学试题江苏省邳州市宿羊山高级中学2021-2022学年高一上学期第二次学情检测化学试题湖北省十堰市联合体2022-2023学年高一上学期10月期中联考化学试题重庆市第八中学校2022-2023学年高一上学期期中考试(半期考试)化学试题四川省达州天立学校2022-2023学年高一上学期11月月考化学试题贵州省三新联盟校2023-2024学年高一上学期10月联考化学试题四川省绵阳中学2023-2024学年高一上学期9月月考化学试题重庆市第一中学校2023-2024学年高一上学期定时练习化学试题
解题方法
9 . 李克强总理在《2018年国务院政府工作报告》中强调“今年二氧化硫、氮氧化物排放量要下降3%。”因此,研究烟气的脱硝(除NOx)、脱硫(除SO2)技术有着积极的环保意义。
Ⅰ.(1)工业煤干馏得到的产品有_______ 、_______ 、焦炉煤气、粗氨水等。
(2)在煤燃烧前需对煤进行脱硫处理。煤的某种脱硫技术的原理如下所示。FeS2 Fe2++
Fe2++
 Fe3+,这种脱硫技术称为微生物脱硫技术。该技术的第一步反应的离子方程式为
Fe3+,这种脱硫技术称为微生物脱硫技术。该技术的第一步反应的离子方程式为_______ 。
Ⅱ.制备乙炔的电石渣对环境污染极为严重,因此需要对水体进行净化处理。现取500mL电石渣废水(阳离子主要为Ca2+),测定水质的数据如下表所示。
注:SS表示固体悬浮物。模拟工业处理流程如图1。


已知:ⅰ.常温时CaSO4微溶于水;ⅱ.溶解度:CaSO4>Fe(OH)2>FeS。
(1)①滤渣A的主要成分有SS和_______ 。
②采用20%的硫酸对废水进行预中和处理,pH变化如图2所示。硫酸的用量和废水中固体悬浮物(SS)含量的关系是_______ 。
(2)根据表中数据,回答下列问题。
熟石灰能促进FeS沉淀的生成,结合离子方程式,从平衡角度分析其原因是_______ 。
(3)用臭氧进一步处理废水中的氰化物和残留硫化物,若将500mL废水中的CN-完全氧化成N2和CO2,转移_______ mol e-。
Ⅰ.(1)工业煤干馏得到的产品有
(2)在煤燃烧前需对煤进行脱硫处理。煤的某种脱硫技术的原理如下所示。FeS2
 Fe2++
Fe2++
 Fe3+,这种脱硫技术称为微生物脱硫技术。该技术的第一步反应的离子方程式为
Fe3+,这种脱硫技术称为微生物脱硫技术。该技术的第一步反应的离子方程式为Ⅱ.制备乙炔的电石渣对环境污染极为严重,因此需要对水体进行净化处理。现取500mL电石渣废水(阳离子主要为Ca2+),测定水质的数据如下表所示。
项目 | pH | S2−(mg/L) | CN-(mg/L) | SS(mg/L) |
平均 | 14 | 1000 | 5.2 | 2500 |


已知:ⅰ.常温时CaSO4微溶于水;ⅱ.溶解度:CaSO4>Fe(OH)2>FeS。
(1)①滤渣A的主要成分有SS和
②采用20%的硫酸对废水进行预中和处理,pH变化如图2所示。硫酸的用量和废水中固体悬浮物(SS)含量的关系是
(2)根据表中数据,回答下列问题。
不同熟石灰投加量下的废水处理效果 | ||||
加试剂量(g) | 分析结果 | |||
FeSO4 | Ca(OH)2 | pH | S2−(mg/L) | SS(mg/L) |
4.8 | 0.50 | 5.5 | 15 | >250 |
0.85 | 6.8 | 3.0 | <50 | |
1.15 | 9.3 | 0.95 | <50 | |
1.25 | 10.5 | 0.85 | <50 | |
(3)用臭氧进一步处理废水中的氰化物和残留硫化物,若将500mL废水中的CN-完全氧化成N2和CO2,转移
您最近一年使用:0次
名校
10 . 化学社的同学在实验时不小心沾了一些KMnO4在皮肤上,产生的黑斑很久才能消除,如果用草酸的稀溶液洗涤马上可以复原,其离子方程式为: +H2C2O4+H+→CO2↑+Mn2++____(未配平)。关于此反应的叙述正确的是
+H2C2O4+H+→CO2↑+Mn2++____(未配平)。关于此反应的叙述正确的是
 +H2C2O4+H+→CO2↑+Mn2++____(未配平)。关于此反应的叙述正确的是
+H2C2O4+H+→CO2↑+Mn2++____(未配平)。关于此反应的叙述正确的是| A.从反应中看出草酸性质很不稳定 | B.1mol 在反应中失去5mol电子 在反应中失去5mol电子 |
| C.该反应右横线上的产物是H2O | D.配平该反应后,H+的计量数是3 |
您最近一年使用:0次
2020-09-03更新
|
155次组卷
|
4卷引用:陕西省汉中市汉中中学2020-2021学年高一上学期期中考试化学试题



