名校
1 . 下列指定反应的离子方程式书写正确的是
A.NO2与水反应: |
B.氨水吸收足量SO2的反应: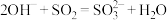 |
C.过量Fe和稀HNO3的反应: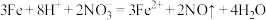 |
D.向 溶液中通入少量SO2: 溶液中通入少量SO2: |
您最近一年使用:0次
名校
2 . 二氧化硫对环境有一定的负面影响,对 的处理和利用是科学研究的重要课题之一。
的处理和利用是科学研究的重要课题之一。
 .用石灰石、氨水等脱硫。以硫酸工业的二氧化硫尾气、氨水、石灰石、碳酸氢铵和氯化钾等为原料,可以制备有重要应用价值的硫酸钾、亚硫酸铵等物质,制备流程如下:
.用石灰石、氨水等脱硫。以硫酸工业的二氧化硫尾气、氨水、石灰石、碳酸氢铵和氯化钾等为原料,可以制备有重要应用价值的硫酸钾、亚硫酸铵等物质,制备流程如下: 的一种常用方法,其总反应的化学方程式为
的一种常用方法,其总反应的化学方程式为___________ 。
②研究发现,pH和温度对石灰石浆液的脱硫效率有一定影响。当烟气通入速度一定时,石灰石浆液的脱硫率与浆液pH的关系如图所示。___________ 。
a.烟气通入石灰石浆液时的温度越高,吸收越快,吸收率越高
b.反应时需鼓入足量的空气以保证 被充分氧化生成
被充分氧化生成
c.将脱硫后的气体通入 溶液,可粗略判断烟气脱硫效率
溶液,可粗略判断烟气脱硫效率
d.石灰石浆液pH>5.7烟气脱硫效果降低,是因为石灰石的溶解程度增大
(2)生产中,需要向反应的溶液中加入适量强还原剂,其目的是___________ 。
(3)反应 所得的滤液中所含阳离子的电子式为
所得的滤液中所含阳离子的电子式为___________ ,检验该滤液中所含阴离子的方法是:取少量滤液于试管中,___________ 。
(4) 可用于电厂等烟道气中脱氮。将氮氧化物转化为氮气,同时生成一种氨肥。写出用
可用于电厂等烟道气中脱氮。将氮氧化物转化为氮气,同时生成一种氨肥。写出用 溶液吸收NO的离子方程式
溶液吸收NO的离子方程式___________ 。
 .
. 还原法也是处理硫酸厂废气的方法之一、400℃时,将
还原法也是处理硫酸厂废气的方法之一、400℃时,将 和含
和含 的尾气按一定比例混合,以一定流速通过装有
的尾气按一定比例混合,以一定流速通过装有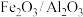 的负载型催化剂(
的负载型催化剂( 为催化剂,
为催化剂, 为载体),发生反应。
为载体),发生反应。
(5)该反应生成s单质和水,其中氧化剂和还原剂的物质的量之比为___________ 。
 的处理和利用是科学研究的重要课题之一。
的处理和利用是科学研究的重要课题之一。 .用石灰石、氨水等脱硫。以硫酸工业的二氧化硫尾气、氨水、石灰石、碳酸氢铵和氯化钾等为原料,可以制备有重要应用价值的硫酸钾、亚硫酸铵等物质,制备流程如下:
.用石灰石、氨水等脱硫。以硫酸工业的二氧化硫尾气、氨水、石灰石、碳酸氢铵和氯化钾等为原料,可以制备有重要应用价值的硫酸钾、亚硫酸铵等物质,制备流程如下:
 的一种常用方法,其总反应的化学方程式为
的一种常用方法,其总反应的化学方程式为②研究发现,pH和温度对石灰石浆液的脱硫效率有一定影响。当烟气通入速度一定时,石灰石浆液的脱硫率与浆液pH的关系如图所示。

a.烟气通入石灰石浆液时的温度越高,吸收越快,吸收率越高
b.反应时需鼓入足量的空气以保证
 被充分氧化生成
被充分氧化生成
c.将脱硫后的气体通入
 溶液,可粗略判断烟气脱硫效率
溶液,可粗略判断烟气脱硫效率d.石灰石浆液pH>5.7烟气脱硫效果降低,是因为石灰石的溶解程度增大
(2)生产中,需要向反应的溶液中加入适量强还原剂,其目的是
(3)反应
 所得的滤液中所含阳离子的电子式为
所得的滤液中所含阳离子的电子式为(4)
 可用于电厂等烟道气中脱氮。将氮氧化物转化为氮气,同时生成一种氨肥。写出用
可用于电厂等烟道气中脱氮。将氮氧化物转化为氮气,同时生成一种氨肥。写出用 溶液吸收NO的离子方程式
溶液吸收NO的离子方程式 .
. 还原法也是处理硫酸厂废气的方法之一、400℃时,将
还原法也是处理硫酸厂废气的方法之一、400℃时,将 和含
和含 的尾气按一定比例混合,以一定流速通过装有
的尾气按一定比例混合,以一定流速通过装有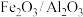 的负载型催化剂(
的负载型催化剂( 为催化剂,
为催化剂, 为载体),发生反应。
为载体),发生反应。(5)该反应生成s单质和水,其中氧化剂和还原剂的物质的量之比为
您最近一年使用:0次
解题方法
3 . 在生活中亚硝酸钠 应用十分广泛,它是一种白色固体,外观与NaCl极其相似;少量可做食品的护色剂,可防止肉毒杆菌在肉类食品中生长。某化学兴趣小组查阅资料得知
应用十分广泛,它是一种白色固体,外观与NaCl极其相似;少量可做食品的护色剂,可防止肉毒杆菌在肉类食品中生长。某化学兴趣小组查阅资料得知 ,该学习小组利用下列装置制备干燥的亚硝酸钠(夹持及加热装置略去,部分仪器可重复使用)。
,该学习小组利用下列装置制备干燥的亚硝酸钠(夹持及加热装置略去,部分仪器可重复使用)。
②酸性高锰酸钾溶液可将 氧化成
氧化成 。
。
回答下列问题:
Ⅰ. 的制备:
的制备:
(1)装置A中的仪器名称分别是______ ,仪器按气流方向连接顺序为b→______ 。
(2)反应开始前打开止水夹a,通入过量氮气的目的是______ ;反应结束后打开止水夹a,再通入过量氮气的目的是______ 。
(3)装置D的作用是______ 。
(4)判断 已被NO反应完全的现象是
已被NO反应完全的现象是______ 。
Ⅱ.
(5)写出实验室制氨气的化学方程式______ 。
Ⅲ.测定的纯度(假设杂质不与反应):
(6)准确称取反应后的固体3.000g于烧杯中,加入蒸馏水溶解,配成250mL的溶液;取出25.00mL的溶液于锥形瓶中,滴入 的酸性
的酸性 溶液至恰好完全反应,用去16mL的酸性
溶液至恰好完全反应,用去16mL的酸性 溶液。固体中
溶液。固体中 的纯度为
的纯度为______ %。
 应用十分广泛,它是一种白色固体,外观与NaCl极其相似;少量可做食品的护色剂,可防止肉毒杆菌在肉类食品中生长。某化学兴趣小组查阅资料得知
应用十分广泛,它是一种白色固体,外观与NaCl极其相似;少量可做食品的护色剂,可防止肉毒杆菌在肉类食品中生长。某化学兴趣小组查阅资料得知 ,该学习小组利用下列装置制备干燥的亚硝酸钠(夹持及加热装置略去,部分仪器可重复使用)。
,该学习小组利用下列装置制备干燥的亚硝酸钠(夹持及加热装置略去,部分仪器可重复使用)。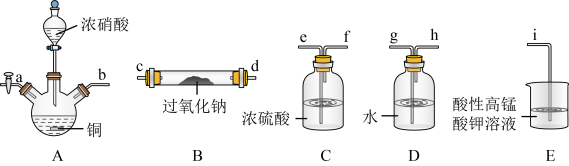
②酸性高锰酸钾溶液可将
 氧化成
氧化成 。
。回答下列问题:
Ⅰ.
 的制备:
的制备:(1)装置A中的仪器名称分别是
(2)反应开始前打开止水夹a,通入过量氮气的目的是
(3)装置D的作用是
(4)判断
 已被NO反应完全的现象是
已被NO反应完全的现象是Ⅱ.
(5)写出实验室制氨气的化学方程式
Ⅲ.测定的纯度(假设杂质不与反应):
(6)准确称取反应后的固体3.000g于烧杯中,加入蒸馏水溶解,配成250mL的溶液;取出25.00mL的溶液于锥形瓶中,滴入
 的酸性
的酸性 溶液至恰好完全反应,用去16mL的酸性
溶液至恰好完全反应,用去16mL的酸性 溶液。固体中
溶液。固体中 的纯度为
的纯度为
您最近一年使用:0次
名校
解题方法
4 . 亚硝酰氯(NOCl,熔点:-64.5℃,沸点:-5.5℃)是一种黄色气体,遇水易水解。可用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与一氧化氮在常温常压下合成。
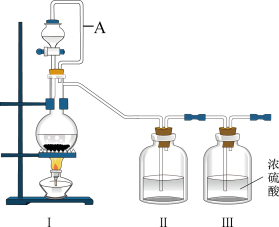
(1)甲组同学拟用同一装置Ⅰ、Ⅱ、Ⅲ分别制备纯净干燥的NO和
_______ 。写出该装置制备氯气的离子方程式:_______ 。
(2)乙组同学利用甲组制得的NO和 制备NOCl,装置如图所示:
制备NOCl,装置如图所示:________ 。
②装置连接顺序为a→________ (按气流自左向右方向,用小写字母表示)。
③装置Ⅷ中吸收尾气时,NOCl发生反应的化学方程式为_______ 。
(3)丙组同学查阅资料,查得王水是浓硝酸与浓盐酸的混酸,一定条件下混酸可生成亚硝酰氯和氯气,该反应的化学方程式为______ 。
(4)丁组同学用以下方法测定亚硝酰氯(NOCl)纯度:取Ⅷ中所得液体m克溶于水,配制成250mL溶液,取出25.00 mL,用c mol/L 溶液反应,消耗
溶液反应,消耗 溶液的体积为bmL。亚硝酰氯(NOCl)的质量分数为
溶液的体积为bmL。亚硝酰氯(NOCl)的质量分数为________ (用代数式表示即可)。
(1)甲组同学拟用同一装置Ⅰ、Ⅱ、Ⅲ分别制备纯净干燥的NO和

(2)乙组同学利用甲组制得的NO和
 制备NOCl,装置如图所示:
制备NOCl,装置如图所示: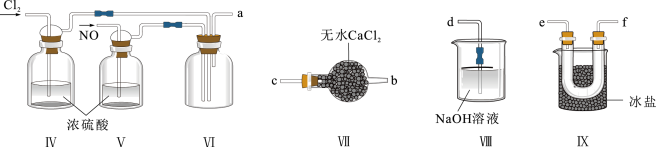
②装置连接顺序为a→
③装置Ⅷ中吸收尾气时,NOCl发生反应的化学方程式为
(3)丙组同学查阅资料,查得王水是浓硝酸与浓盐酸的混酸,一定条件下混酸可生成亚硝酰氯和氯气,该反应的化学方程式为
(4)丁组同学用以下方法测定亚硝酰氯(NOCl)纯度:取Ⅷ中所得液体m克溶于水,配制成250mL溶液,取出25.00 mL,用c mol/L
 溶液反应,消耗
溶液反应,消耗 溶液的体积为bmL。亚硝酰氯(NOCl)的质量分数为
溶液的体积为bmL。亚硝酰氯(NOCl)的质量分数为
您最近一年使用:0次
名校
解题方法
5 . I.某化学自主实验小组利用如图所示装置探究 能否被
能否被 还原
还原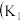 、
、 为止水夹,夹持固定装置略去)。
为止水夹,夹持固定装置略去)。________ 。 装置发生的化学反应方程式为
装置发生的化学反应方程式为_________ 。
(2)甲、乙分别是___________  填标号
填标号 。
。
a.硫酸、浓硫酸 b.碱石灰、无水氯化钙 c.碱石灰、碱石灰 d.五氧化二磷、五氧化二磷
(3)若 能够被
能够被 还原,写出发生反应的化学方程式:
还原,写出发生反应的化学方程式:___________ 。
(4)此实验装置存在一个明显的缺陷是___________ 。
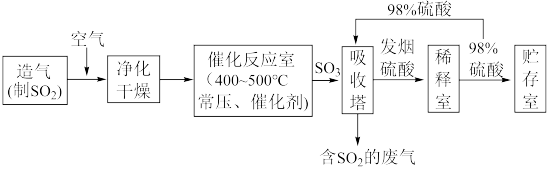
II.硫酸可用于生产化肥、农药、炸药、染料和盐类等。工业生产硫酸的流程图如下: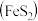 为原料来制备SO2,将黄铁矿粉碎的原因是:
为原料来制备SO2,将黄铁矿粉碎的原因是:___________ 。
(6)写出催化反应室中SO2被氧化为SO3的化学方程式___________ 。
(7)硫酸工业的尾气中含有少量SO2,若直接排放会污染空气,并导致硫酸型酸雨,可用___________ 吸收。
 能否被
能否被 还原
还原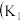 、
、 为止水夹,夹持固定装置略去)。
为止水夹,夹持固定装置略去)。
 装置发生的化学反应方程式为
装置发生的化学反应方程式为(2)甲、乙分别是
 填标号
填标号 。
。a.硫酸、浓硫酸 b.碱石灰、无水氯化钙 c.碱石灰、碱石灰 d.五氧化二磷、五氧化二磷
(3)若
 能够被
能够被 还原,写出发生反应的化学方程式:
还原,写出发生反应的化学方程式:(4)此实验装置存在一个明显的缺陷是
II.硫酸可用于生产化肥、农药、炸药、染料和盐类等。工业生产硫酸的流程图如下:
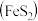 为原料来制备SO2,将黄铁矿粉碎的原因是:
为原料来制备SO2,将黄铁矿粉碎的原因是:(6)写出催化反应室中SO2被氧化为SO3的化学方程式
(7)硫酸工业的尾气中含有少量SO2,若直接排放会污染空气,并导致硫酸型酸雨,可用
您最近一年使用:0次
2024-02-24更新
|
716次组卷
|
4卷引用:广东省广州市黄广中学2023-2024学年高一下学期3月月考化学试题
名校
解题方法
6 . 84消毒液是一种常见的含氯消毒剂,广泛用于家庭、医院的消毒。某兴趣小组对84 消毒液的组成、性质与使用进行探究。所用试剂:84消毒液(含 )、医用酒精(乙醇体积分数为70~75%)
)、医用酒精(乙醇体积分数为70~75%)
Ⅰ.探究84消毒液的成分
(1)实测该84消毒液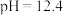 ,能使
,能使 试纸先变
试纸先变___________ 色后褪色,因此其成分中,除了 、
、 ,还含有少量
,还含有少量___________ (填化学式)。
(2)84消毒液露置于空气中,消毒效果先增强,而再将其光照后消毒效果又降低。消毒效果降低的原因是(用化学方程式表示)___________ 。
Ⅱ.探究84消毒液的性质与使用
(3)84消毒液具有氧化性,预测的依据是___________ 。巴西奥运会期间,由于工作人员将84消毒液与双氧水混用,导致游泳池藻类快速生长,池水变绿。一种可能的原因是 与
与 反应产生
反应产生 促进藻类快速生长该反应的化学方程式为
促进藻类快速生长该反应的化学方程式为___________ 。
Ⅲ.84消毒液能否与医用酒精混用实验装置如图所示
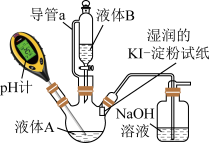
已知: 是常见的还原剂;单质碘(
是常见的还原剂;单质碘( )遇淀粉变蓝。
)遇淀粉变蓝。
(4)判断实验②中生成了 的依据是
的依据是___________ 。
(5)图中 溶液的作用是
溶液的作用是___________ 。
(6)实验过程中混合溶液的 逐渐增大至13.1,预测酒精与
逐渐增大至13.1,预测酒精与 反应还可能生成
反应还可能生成 ,但得补充以下实验③,才能说明反应中有
,但得补充以下实验③,才能说明反应中有 生成。填写表中空白完成实验设计。
生成。填写表中空白完成实验设计。
结论:医用酒精可与84消毒液发生反应,二者不可混用。
 )、医用酒精(乙醇体积分数为70~75%)
)、医用酒精(乙醇体积分数为70~75%)Ⅰ.探究84消毒液的成分
(1)实测该84消毒液
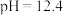 ,能使
,能使 试纸先变
试纸先变 、
、 ,还含有少量
,还含有少量(2)84消毒液露置于空气中,消毒效果先增强,而再将其光照后消毒效果又降低。消毒效果降低的原因是(用化学方程式表示)
Ⅱ.探究84消毒液的性质与使用
(3)84消毒液具有氧化性,预测的依据是
 与
与 反应产生
反应产生 促进藻类快速生长该反应的化学方程式为
促进藻类快速生长该反应的化学方程式为Ⅲ.84消毒液能否与医用酒精混用实验装置如图所示

已知:
 是常见的还原剂;单质碘(
是常见的还原剂;单质碘( )遇淀粉变蓝。
)遇淀粉变蓝。| 序号 | 液体A | 液体B | 现象 |
| ① |  ( (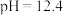 )的84消毒液 )的84消毒液 |  蒸馏水 蒸馏水 | 溶液中无明显现象;溶液 变为12.0;淀粉- 变为12.0;淀粉- 试纸在 试纸在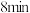 时变蓝, 时变蓝, 时蓝色完全褪去 时蓝色完全褪去 |
| ② |  ( (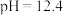 )的84消毒液 )的84消毒液 |  医用酒精 医用酒精 | 产生气泡,颜色无明显变化;溶液 升高到13.1,淀粉- 升高到13.1,淀粉- 试纸在 试纸在 时变蓝, 时变蓝,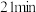 时蓝色完全褪去 时蓝色完全褪去 |
(4)判断实验②中生成了
 的依据是
的依据是(5)图中
 溶液的作用是
溶液的作用是(6)实验过程中混合溶液的
 逐渐增大至13.1,预测酒精与
逐渐增大至13.1,预测酒精与 反应还可能生成
反应还可能生成 ,但得补充以下实验③,才能说明反应中有
,但得补充以下实验③,才能说明反应中有 生成。填写表中空白完成实验设计。
生成。填写表中空白完成实验设计。| 序号 | 液体A | 液体B | 现象 |
| ③ |  ( (  溶液 溶液 |  医用酒精 医用酒精 | 溶液 升高到12.6 升高到12.6 |
您最近一年使用:0次
名校
解题方法
7 . 硝酸厂烟气中的大量NO经还原法可转化为无害物质。常温下,将NO与 的混合气体通入
的混合气体通入 与
与 的混合溶液中,其转化过程如图所示。下列说法错误的是
的混合溶液中,其转化过程如图所示。下列说法错误的是
 的混合气体通入
的混合气体通入 与
与 的混合溶液中,其转化过程如图所示。下列说法错误的是
的混合溶液中,其转化过程如图所示。下列说法错误的是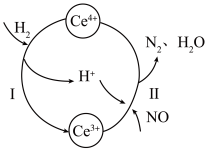
A.该转化过程的实质为NO被 还原 还原 |
| B.反应I中氧化剂与还原剂的物质的量之比为1∶2 |
C.反应II的离子反应方程式为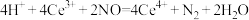 |
D.反应过程中混合溶液内 和 和 的总数不变 的总数不变 |
您最近一年使用:0次
2023-11-29更新
|
671次组卷
|
5卷引用:广东省深圳市南头中学2023-2024学年高一上学期期末调研考试(模拟)化学试题
名校
解题方法
8 . 某同学类比镁在二氧化碳中的燃烧反应,认为钠和二氧化碳也可以发生反应,他在实验室中选择以下装置对该反应能否发生进行了实验探究。
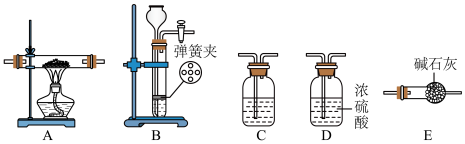
依据要求回答问题:
(1)二氧化碳的发生装置应选用上述装置___________ (填装置下方对应字母),反应的化学方程式为___________ 。
(2)装置 C所装的试剂是___________ ,发生的反应为(用离子方程式表示)___________ 。
(3)为达到实验目的,选择上图中的装置,其连接顺序为:按二氧化碳的发生装置→___________ 。(按气流方向,填写装置的大写字母)。
(4)操作中通空气和加热的先后顺序为___________ 。
(5)该同学在制取 的过程中,向装置B中加入某酸后,发现固体与酸没有接触,为使反应顺利进行,下列可再加入的试剂是___________。
的过程中,向装置B中加入某酸后,发现固体与酸没有接触,为使反应顺利进行,下列可再加入的试剂是___________。
(6)若反应过程中 足量,反应结束后,该同学对硬质玻璃管中生成的固体提出了以下猜想:①生成的固体物质为
足量,反应结束后,该同学对硬质玻璃管中生成的固体提出了以下猜想:①生成的固体物质为 ;②生成的固体物质为
;②生成的固体物质为 和C的混合物③生成的固体物质为
和C的混合物③生成的固体物质为 和
和 的混合物;④生成的固体物质为
的混合物;④生成的固体物质为 和C的混合物。报告给老师后,老师认为可以排除其中的3种情况,老师排除的理由是
和C的混合物。报告给老师后,老师认为可以排除其中的3种情况,老师排除的理由是___________ ;则钠与 反应的化学方程式为
反应的化学方程式为___________ 。
(7)该同学经过反思,认为上述实验设计中存在缺陷。他查阅资料后得知, 溶液可以吸收
溶液可以吸收 ,同时得到黑色的
,同时得到黑色的 和一种酸。于是他在装置后加装一个盛
和一种酸。于是他在装置后加装一个盛 溶液的吸收装置,该装置中发生反应的化学方程式为
溶液的吸收装置,该装置中发生反应的化学方程式为___________ 。

依据要求回答问题:
(1)二氧化碳的发生装置应选用上述装置
(2)装置 C所装的试剂是
(3)为达到实验目的,选择上图中的装置,其连接顺序为:按二氧化碳的发生装置→
(4)操作中通空气和加热的先后顺序为
(5)该同学在制取
 的过程中,向装置B中加入某酸后,发现固体与酸没有接触,为使反应顺利进行,下列可再加入的试剂是___________。
的过程中,向装置B中加入某酸后,发现固体与酸没有接触,为使反应顺利进行,下列可再加入的试剂是___________。| A.稀硝酸 | B. 溶液 溶液 |
| C.煤油 | D. (无色有机溶剂,与水互不相溶,密度比水大) (无色有机溶剂,与水互不相溶,密度比水大) |
(6)若反应过程中
 足量,反应结束后,该同学对硬质玻璃管中生成的固体提出了以下猜想:①生成的固体物质为
足量,反应结束后,该同学对硬质玻璃管中生成的固体提出了以下猜想:①生成的固体物质为 ;②生成的固体物质为
;②生成的固体物质为 和C的混合物③生成的固体物质为
和C的混合物③生成的固体物质为 和
和 的混合物;④生成的固体物质为
的混合物;④生成的固体物质为 和C的混合物。报告给老师后,老师认为可以排除其中的3种情况,老师排除的理由是
和C的混合物。报告给老师后,老师认为可以排除其中的3种情况,老师排除的理由是 反应的化学方程式为
反应的化学方程式为(7)该同学经过反思,认为上述实验设计中存在缺陷。他查阅资料后得知,
 溶液可以吸收
溶液可以吸收 ,同时得到黑色的
,同时得到黑色的 和一种酸。于是他在装置后加装一个盛
和一种酸。于是他在装置后加装一个盛 溶液的吸收装置,该装置中发生反应的化学方程式为
溶液的吸收装置,该装置中发生反应的化学方程式为
您最近一年使用:0次
2023-11-28更新
|
127次组卷
|
2卷引用:广东省广州市第二中学教育集团联考2023-2024学年高一上学期11月期中考试化学试题
名校
解题方法
9 . 运用氧化还原反应和离子反应知识回答下列问题:
Ⅰ.将H2S和空气的混合气体通入FeCl3、FeCl2和CuCl2的混合溶液中回收S,其转化如图所示(CuS不溶于水)。
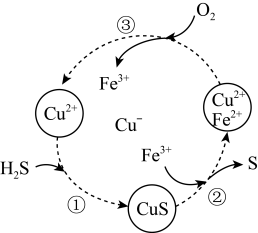
(1)写出过程②和过程中③发生反应的离子方程式:
i.过程②___________ 。
ii.过程③___________ 。
iii.整个转化过程中可以循环使用的离子是___________ 。
Ⅱ.新型纳米材料氧缺位铁酸盐(MFe2Ox,3<x<4,M=Mn、Zn、Ni,且均为+2价,下同)是由铁酸盐MFe2O4经过高温反应得到的。
(2)将纳米材料氧缺位铁酸盐分散在蒸馏水中,所形成的分散系属于___________ 。
(3)MFe2O4中Fe元素的化合价为___________ 。
(4)在酸性条件下,Fe2O 容易转化为Fe2+,某反应体系中共存在下列6种粒子:Fe2O
容易转化为Fe2+,某反应体系中共存在下列6种粒子:Fe2O 、Fe2+、H+、H2O、Cu2O、Cu2+,则Fe2O
、Fe2+、H+、H2O、Cu2O、Cu2+,则Fe2O 转化为Fe2+的离子方程式
转化为Fe2+的离子方程式___________ 。
(5)已知As2O3与Zn可以发生如下反应:As2O3+6Zn+6H2SO4=2AsH3↑+6ZnSO4+3H2O(反应前后H元素化合价未发生变化),请用单线桥法标出电子转移的方向和数目___________ 。
Ⅰ.将H2S和空气的混合气体通入FeCl3、FeCl2和CuCl2的混合溶液中回收S,其转化如图所示(CuS不溶于水)。

(1)写出过程②和过程中③发生反应的离子方程式:
i.过程②
ii.过程③
iii.整个转化过程中可以循环使用的离子是
Ⅱ.新型纳米材料氧缺位铁酸盐(MFe2Ox,3<x<4,M=Mn、Zn、Ni,且均为+2价,下同)是由铁酸盐MFe2O4经过高温反应得到的。
(2)将纳米材料氧缺位铁酸盐分散在蒸馏水中,所形成的分散系属于
(3)MFe2O4中Fe元素的化合价为
(4)在酸性条件下,Fe2O
 容易转化为Fe2+,某反应体系中共存在下列6种粒子:Fe2O
容易转化为Fe2+,某反应体系中共存在下列6种粒子:Fe2O 、Fe2+、H+、H2O、Cu2O、Cu2+,则Fe2O
、Fe2+、H+、H2O、Cu2O、Cu2+,则Fe2O 转化为Fe2+的离子方程式
转化为Fe2+的离子方程式(5)已知As2O3与Zn可以发生如下反应:As2O3+6Zn+6H2SO4=2AsH3↑+6ZnSO4+3H2O(反应前后H元素化合价未发生变化),请用单线桥法标出电子转移的方向和数目
您最近一年使用:0次
解题方法
10 . 亚氯酸钠(NaClO2)和ClO2都是重要的漂白剂。
(1)草酸(H2C2O4)是一种弱酸,利用硫酸酸化的草酸还原NaClO3,可较安全地生成ClO2,反应的离子方程式为_______ 。
(2)自来水用ClO2处理后,有少量ClO2残留在水中,可用碘量法做如下检测(已知ClO2存在于pH为4~6的溶液中,ClO 存在于中性溶液中):
存在于中性溶液中):
①取0.50 L水样,加入一定量的碘化钾,用氢氧化钠溶液调至中性,再加入淀粉溶液,溶液变蓝。写出ClO2与碘化钾反应的化学方程式:_______ 。
②已知:2Na2S2O3+I2=Na2S4O6+2NaI,向①所得溶液中滴加5.00×10-4 mol·L-1的Na2S2O3溶液至恰好反应,消耗Na2S2O3溶液20.00 mL。该水样中ClO2的浓度是_______ mg·L-1。
(3)某学习小组设计如下装置制取亚氯酸钠(NaClO2)。
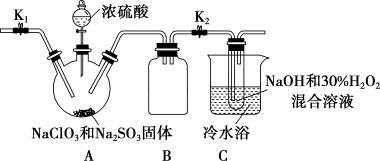
①装置A中产生的ClO2气体,在装置C中反应生成NaClO2,写出生成NaClO2的化学方程式:_______ 。
②将NaClO2溶液在一定条件下处理即可得到NaClO2晶体。装置B的作用是_______ 。
(1)草酸(H2C2O4)是一种弱酸,利用硫酸酸化的草酸还原NaClO3,可较安全地生成ClO2,反应的离子方程式为
(2)自来水用ClO2处理后,有少量ClO2残留在水中,可用碘量法做如下检测(已知ClO2存在于pH为4~6的溶液中,ClO
 存在于中性溶液中):
存在于中性溶液中):①取0.50 L水样,加入一定量的碘化钾,用氢氧化钠溶液调至中性,再加入淀粉溶液,溶液变蓝。写出ClO2与碘化钾反应的化学方程式:
②已知:2Na2S2O3+I2=Na2S4O6+2NaI,向①所得溶液中滴加5.00×10-4 mol·L-1的Na2S2O3溶液至恰好反应,消耗Na2S2O3溶液20.00 mL。该水样中ClO2的浓度是
(3)某学习小组设计如下装置制取亚氯酸钠(NaClO2)。

①装置A中产生的ClO2气体,在装置C中反应生成NaClO2,写出生成NaClO2的化学方程式:
②将NaClO2溶液在一定条件下处理即可得到NaClO2晶体。装置B的作用是
您最近一年使用:0次



