解题方法
1 . S2O82-具有强氧化性,其还原产物为SO42-,硫酸锰(MnSO4)和过硫酸钾(K2S2O8)两种盐溶液在银离子催化下可发生反应,得到紫红色溶液。请写出此反应的化学方程式:__ 。
您最近一年使用:0次
解题方法
2 . 在氯氧化法处理CN-的废水过程中,液氯在碱性条件下可以将氰化物氧化成氰酸盐(其毒性仅为氰化物的千分之一),氰酸盐进一步被氧化为无毒物质。
⑴某厂废水中含KCN(N为-3价,KOCN也是),其浓度为650mg·L-1。现用氯碱法处理,发生如下反应:KCN+2KOH+Cl2=KOCN+2KCl+H2O,被氧化的元素是_______ 。
⑵投入过量的液氯,可以将氰酸盐进一步氧化为N2,化学方程式为2KOCN+4KOH+3Cl2=N2↑+2CO2↑+6KCl+2H2O,若处理上述废水20L,使KCN完全转化为无毒物质,计算需要液氯的质量。___________ 若将所需液氯换成氯气,则所需氯气在标准状况下的体积为多少?______________
⑴某厂废水中含KCN(N为-3价,KOCN也是),其浓度为650mg·L-1。现用氯碱法处理,发生如下反应:KCN+2KOH+Cl2=KOCN+2KCl+H2O,被氧化的元素是
⑵投入过量的液氯,可以将氰酸盐进一步氧化为N2,化学方程式为2KOCN+4KOH+3Cl2=N2↑+2CO2↑+6KCl+2H2O,若处理上述废水20L,使KCN完全转化为无毒物质,计算需要液氯的质量。
您最近一年使用:0次
名校
3 . 水热法制备 纳米颗粒的反应为
纳米颗粒的反应为 ,下列说法中不正确的是
,下列说法中不正确的是
 纳米颗粒的反应为
纳米颗粒的反应为 ,下列说法中不正确的是
,下列说法中不正确的是A.每生成1mol  转移4mol电子 转移4mol电子 |
B.该反应中 和 和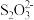 都是还原剂 都是还原剂 |
C.3mol  被氧化时有 被氧化时有 被还原 被还原 |
D.反应方程式中化学计量数 |
您最近一年使用:0次
2020-02-05更新
|
134次组卷
|
4卷引用:夯基提能2020届高三化学选择题对题专练——氧化还原反应的综合分析(强化练习)
名校
解题方法
4 . 配平下列方程式:
(1)___ Mg3N2+___ H2O——___ Mg(OH)2+___ NH3
(2)___ Ag+___ HNO3(稀)——___ AgNO3+___ NO+___ H2O
(3)___ Cl2+___ KOH——___ KC1+___ KC1O3+___ H2O
(4)___ NO3-+___ Zn+___ OH-+___ H2O——___ NH3+___ Zn(OH)42-
(1)
(2)
(3)
(4)
您最近一年使用:0次
2020-01-31更新
|
235次组卷
|
3卷引用:广东省揭阳普宁市2019-2020学年高一上学期期末考试化学试题
广东省揭阳普宁市2019-2020学年高一上学期期末考试化学试题(已下线)第三节 氧化还原反应(一)-2020-2021学年高一化学必修第一册课时同步练(新人教)山西省芮城中学2021-2022学年高一上学期阶段性月考化学试题
解题方法
5 . 铜在自然界多以+1价存在于矿石中,在固态特别是高温下,+1价铜的化合物比+2价稳定。用辉铜矿(Cu2S)炼铜的方法如下:
(1)将辉铜矿在空气中高温焙烧,生成两种氧化物,反应的化学方程式是_____________ 。
(2)向焙烧得到的矿石中,再加上原矿石一半质量的未经焙烧过的矿石,混合后隔绝空气进行高温煅烧,得到金属铜和一种具有刺激性气味的气体,反应的化学方程式是____________ 。
(1)将辉铜矿在空气中高温焙烧,生成两种氧化物,反应的化学方程式是
(2)向焙烧得到的矿石中,再加上原矿石一半质量的未经焙烧过的矿石,混合后隔绝空气进行高温煅烧,得到金属铜和一种具有刺激性气味的气体,反应的化学方程式是
您最近一年使用:0次
解题方法
6 . 氮元素的单质和常见的化合物在工、农业生产中用途广泛.
(1)工业上利用分离空气的方法得到氮气.空气各主要成分的沸点如下:
现将空气深度冷却液化,然后缓慢升温,则最先分离出来的气体是____________ 。
(2)雷雨时空气中的N2转化为NO,生成物NO是______ 色的气体,________ (填“易”或“难”)溶于水;NO在空气中很容易被氧化成NO2,NO2能与水发生化学反应。NO2与水反应的化学方程式为_______________________________ 。
(1)工业上利用分离空气的方法得到氮气.空气各主要成分的沸点如下:
| N2 | O2 | Ar | CO2 |
| -196℃ | -183℃ | -186℃ | -78℃ |
现将空气深度冷却液化,然后缓慢升温,则最先分离出来的气体是
(2)雷雨时空气中的N2转化为NO,生成物NO是
您最近一年使用:0次
2020-01-29更新
|
206次组卷
|
2卷引用:新人教版必修2同步测试:5.2.1一氧化氮和二氧化氮
解题方法
7 . 已知稀硝酸和铜能发生反应,生成硝酸铜、一氧化氮气体和水。
(1)请写出该反应的化学方程式,并用双线桥法标出反应中电子转移的方向和数目。________
(2)一次实验中,某同学用过量的稀硝酸(其密度为1.08 g·mL-1,HNO3的质量分数为12%)跟一定量的铜片反应,产生了标准状况下0.56 L的一氧化氮。试计算(简要写出计算过程):
①该稀硝酸的物质的量浓度(结果保留小数点后一位);______________
②被还原的HNO3的物质的量。________________
(1)请写出该反应的化学方程式,并用双线桥法标出反应中电子转移的方向和数目。
(2)一次实验中,某同学用过量的稀硝酸(其密度为1.08 g·mL-1,HNO3的质量分数为12%)跟一定量的铜片反应,产生了标准状况下0.56 L的一氧化氮。试计算(简要写出计算过程):
①该稀硝酸的物质的量浓度(结果保留小数点后一位);
②被还原的HNO3的物质的量。
您最近一年使用:0次
2020-01-29更新
|
149次组卷
|
3卷引用:人教版高中化学必修一第四章《非金属及其化合物》测试卷
8 . 我国广泛采用将干燥空气稀释的氯气通入填有固体亚氯酸钠(NaClO2)的柱内制得ClO2,用其取代氯气对自来水消毒,从而降低自来水中的氯残留对人体健康的影响。
(1)在ClO2分子中氯元素的化合价是______________ 。
(2)表示这一反应的化学方程式是________________________________ ,和欧洲的方法相比,我国这一方法的主要优点是生产出的ClO2中不含Cl2杂质。
(3)在酸性溶液中,用草酸钠(Na2C2O4)还原NaClO3也可制得ClO2,表示这一反应的化学方程式是________________________________ ,此法的优点是ClO2可被CO2稀释(Na2C2O4的氧化产物是CO2)。
(4)根据上述原理,北京绿先锋环保科技有限责任公司生产的“绿先锋消毒剂”是由两组固体试剂组成的。其使用方法见下图:
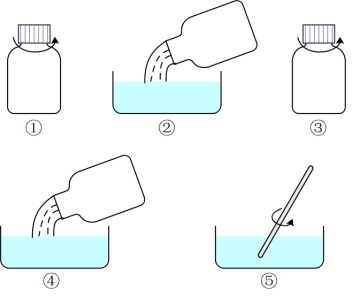
小瓶内盛的白色固体是________________ ,瓶胆内盛的白色固体是______________ 。
(1)在ClO2分子中氯元素的化合价是
(2)表示这一反应的化学方程式是
(3)在酸性溶液中,用草酸钠(Na2C2O4)还原NaClO3也可制得ClO2,表示这一反应的化学方程式是
(4)根据上述原理,北京绿先锋环保科技有限责任公司生产的“绿先锋消毒剂”是由两组固体试剂组成的。其使用方法见下图:

小瓶内盛的白色固体是
您最近一年使用:0次
9 . MnO2是一种重要的无机功能材料,可由MnSO4和NaClO3溶液反应制得,反应原理为: MnSO4+ NaClO3+ H2O Cl2↑ + Na2SO4 + MnO2 ↓+ (未配平),则关于此反应的叙述不正确的是
Cl2↑ + Na2SO4 + MnO2 ↓+ (未配平),则关于此反应的叙述不正确的是
 Cl2↑ + Na2SO4 + MnO2 ↓+ (未配平),则关于此反应的叙述不正确的是
Cl2↑ + Na2SO4 + MnO2 ↓+ (未配平),则关于此反应的叙述不正确的是| A.NaClO3中Cl的化合价为+5 |
| B.每生成8.7 g氧化产物,反应中转移的电子数约为0.2×6.02×1023 |
| C.NaClO3的氧化性强于MnO2的氧化性 |
| D.该反应右边方框内的产物是NaOH |
您最近一年使用:0次
2020-01-19更新
|
364次组卷
|
2卷引用:甘肃省武威第六中学2020届高三上学期第六次诊断考试化学试题
解题方法
10 . 有关系式:有机物X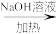 A
A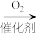 B
B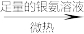 Ag若该有机物X与析出的银的物质的量之比为1∶4,则该有机物X可能是
Ag若该有机物X与析出的银的物质的量之比为1∶4,则该有机物X可能是
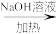 A
A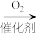 B
B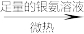 Ag若该有机物X与析出的银的物质的量之比为1∶4,则该有机物X可能是
Ag若该有机物X与析出的银的物质的量之比为1∶4,则该有机物X可能是| A.CH3Cl | B.CH3CH2Br | C.CH3CHBrCH3 | D.CH3CH2CH2Cl |
您最近一年使用:0次
2020-01-18更新
|
391次组卷
|
2卷引用:云南省陆良县第八中学2019-2020学年高二上学期期末考试化学试题



