解题方法
1 . “神舟六号”宇宙飞船是靠长征Ⅱ(F)型运载火箭发射升空的。该火箭所用的燃料是偏二甲肼[(CH3)2NNH2],氧化剂是N2O4,产物是氮气、二氧化碳和水。
(1)火箭点火瞬间,逸出的红棕色气体是________ ,产生该气体的化学反应方程式为________________________________ 。
(2)偏二甲肼在N2O4中燃烧的化学方程式为____________________ ,当有1 mol 偏二甲肼燃烧时,转移电子的物质的量为________________________________ 。
(1)火箭点火瞬间,逸出的红棕色气体是
(2)偏二甲肼在N2O4中燃烧的化学方程式为
您最近一年使用:0次
2 . 写出下列变化的文字表达式并在括号内注明反应的基本类型。
①硫在氧气中燃烧________ ;
②在二氧化锰的催化下加热氯酸钾制氧气________ 。
①硫在氧气中燃烧
②在二氧化锰的催化下加热氯酸钾制氧气
您最近一年使用:0次
名校
3 . 某研究小组制备氯气并对产生氯气的条件进行探究。___________ (填“氧化性”或“还原性”)。
(2)A中产生的气体不纯,含有的杂质可能是___________ 。
(3)B用于收集Cl2,请完善装置B并用箭头标明进出气体方向。___________
(4)C用于吸收多余的Cl2,C中发生反应的离子方程式是___________ 。
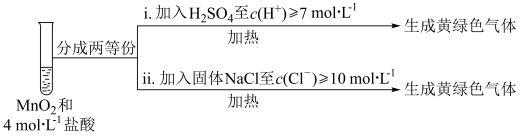
(5)该小组欲研究盐酸的浓度对制Cl2的影响,设计实验进行如下探究。
①已知MnO2呈弱碱性。I中溶液呈浅棕色是由于MnO2与浓盐酸发生了复分解反应,化学方程式是___________ 。
②II中发生了分解反应,反应的化学方程式是___________ 。
③III中无明显现象的原因,可能是c(H+)或c(Cl-)较低,设计实验IV进行探究:___________ ;将i、ii作对比,得出的结论是___________ 。
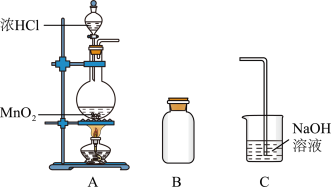
(2)A中产生的气体不纯,含有的杂质可能是
(3)B用于收集Cl2,请完善装置B并用箭头标明进出气体方向。
(4)C用于吸收多余的Cl2,C中发生反应的离子方程式是
(5)该小组欲研究盐酸的浓度对制Cl2的影响,设计实验进行如下探究。
| 实验 | 操作 | 现象 |
| I | 常温下将MnO2和12 mol·L-1浓盐酸混合 | 溶液呈浅棕色,略有刺激性气味 |
| II | 将I中混合物过滤,加热滤液 | 生成大量黄绿色气体 |
| III | 加热MnO2和4 mol·L-1稀盐酸混合物 | 无明显现象 |
②II中发生了分解反应,反应的化学方程式是
③III中无明显现象的原因,可能是c(H+)或c(Cl-)较低,设计实验IV进行探究:
您最近一年使用:0次
名校
解题方法
4 . 欲降低废水中重金属元素铬的毒性,可将 转化为Cr(OH)3沉淀除去。几种金属离子生成沉淀的pH如下表。
转化为Cr(OH)3沉淀除去。几种金属离子生成沉淀的pH如下表。
(1)某含铬废水处理的主要流程如下图所示:

①初沉池中加入明矾作沉降剂,其作用的原理是(用离子方程式表示)______________________________ 。
②请补充并配平以下反应池中发生主要反应的离子方程式:____  +____
+____ +____===____Cr3++____
+____===____Cr3++____ +____H2O。
+____H2O。
③根据“沉淀法”和“中和法”的原理,向沉淀池中加入NaOH溶液,此过程中发生主要反应的离子方程式是:H++OH-===H2O和_______________________________ 。证明Cr3+沉淀完全的方法是_____________________________________________________________ 。
(2)工业可用电解法来处理含 的废水。实验室利用如图模拟处理含
的废水。实验室利用如图模拟处理含 的废水,阳极反应是Fe-2e-===Fe2+,阴极反应式是2H++2e-===H2↑。
的废水,阳极反应是Fe-2e-===Fe2+,阴极反应式是2H++2e-===H2↑。

①Fe2+与酸性溶液中的 反应的离子方程式是
反应的离子方程式是______________________________ 。
② 若溶液中含有0.01 mol ,则阳离子全部生成的沉淀的物质的量是
,则阳离子全部生成的沉淀的物质的量是______ mol。
 转化为Cr(OH)3沉淀除去。几种金属离子生成沉淀的pH如下表。
转化为Cr(OH)3沉淀除去。几种金属离子生成沉淀的pH如下表。 | 阳离子 | Fe3+ | Fe2+ | Al3+ | Cr3+ |
| 开始沉淀时的pH | 1.9 | 7.0 | —— | —— |
| 沉淀完全时的pH | 3.2 | 9.0 | 9(>9溶解) | 8 |
(1)某含铬废水处理的主要流程如下图所示:

①初沉池中加入明矾作沉降剂,其作用的原理是(用离子方程式表示)
②请补充并配平以下反应池中发生主要反应的离子方程式:
 +____
+____ +____===____Cr3++____
+____===____Cr3++____ +____H2O。
+____H2O。③根据“沉淀法”和“中和法”的原理,向沉淀池中加入NaOH溶液,此过程中发生主要反应的离子方程式是:H++OH-===H2O和
(2)工业可用电解法来处理含
 的废水。实验室利用如图模拟处理含
的废水。实验室利用如图模拟处理含 的废水,阳极反应是Fe-2e-===Fe2+,阴极反应式是2H++2e-===H2↑。
的废水,阳极反应是Fe-2e-===Fe2+,阴极反应式是2H++2e-===H2↑。
①Fe2+与酸性溶液中的
 反应的离子方程式是
反应的离子方程式是② 若溶液中含有0.01 mol
 ,则阳离子全部生成的沉淀的物质的量是
,则阳离子全部生成的沉淀的物质的量是
您最近一年使用:0次
2018-06-25更新
|
473次组卷
|
2卷引用:辽宁省沈阳铁路实验中学2017-2018学年高二6月月考化学试题
9-10高三·湖南·阶段练习
名校
5 . 氧化还原反应广泛应用于金属的冶炼。下列说法不正确的是
| A.电解熔融NaCl制取金属钠的反应中,钠离子被还原,氯离子被氧化 |
| B.湿法炼铜与火法炼铜的反应中,铜元素都发生还原反应 |
| C.用磁铁矿炼铁的反应中,1 mol Fe3O4被CO还原成Fe,转移9 mol e− |
| D.铝热法还原铁的反应中,放出的热量能使铁熔化 |
您最近一年使用:0次
2018-06-11更新
|
334次组卷
|
10卷引用:炎德?英才大联考三湘名校2010届高三月考试卷(一)
(已下线)炎德?英才大联考三湘名校2010届高三月考试卷(一)(已下线)2018年5月21日 金属的冶炼原理与方法——《每日一题》2017-2018学年高一化学人教必修2(已下线)2019年5月13日 《每日一题》人教必修2——金属的冶炼原理与方法内蒙古开来中学2018-2019学年高一下学期期末考试化学试题云南省通海县三中2019-2020学年高二9月份(开学考试)化学试题2019-2020人教版高中化学必修2第四章《化学与自然资源开发利用》测试卷四川省泸州市泸县第二中学2019-2020学年高一下学期第一次在线月考化学试题四川省阆中中学2019-2020学年高一(仁智班)下学期开学考试化学试题内蒙古巴彦淖尔市乌拉特前旗第一中学2020-2021学年高二下学期期中考试化学试题9.1.2金属的冶炼(课后)-2019苏教版必修2课前课中课后
名校
6 . 近年来,我国在超导研究方面居世界领先地位,铊(Tl)是超导体的组成成分之一,铊位于第6周期ⅢA族,下列对铊的性质推导可能正确的是( )
①铊是易导电的银白色金属
②Tl(OH)3是两性氢氧化物
③Tl3+的氧化能力比Al3+的强
④单质能跟稀HNO3反应生成硝酸盐
①铊是易导电的银白色金属
②Tl(OH)3是两性氢氧化物
③Tl3+的氧化能力比Al3+的强
④单质能跟稀HNO3反应生成硝酸盐
| A.①④ | B.②③ | C.只有① | D.只有④ |
您最近一年使用:0次
2018-04-07更新
|
477次组卷
|
9卷引用:山东省寿光现代中学2017-2018学年高一4月月考化学试题
山东省寿光现代中学2017-2018学年高一4月月考化学试题福建省德化县第一中学、永安市第一中学、漳平市第一中学2017--2018学年高一年第一次联考(4月)化学试题(已下线)4.2.2 元素周期表和元素周期律的应用练习(1)——《高中新教材同步备课》(人教版 必修第一册)(已下线)练习15 元素周期表的应用-2020-2021学年【补习教材·寒假作业】高一化学(鲁科版2019)专题5 本专题复习提升-高中化学苏教2019版必修第一册江西省抚州市南城一中2020-2021学年高一下学期4月月考化学试题山东省泰安市2020-2021学年高一下学期期末考试化学试题(已下线)5.1.4 元素周期表的应用(备作业)-【上好课】2021-2022学年高一化学同步备课系列(苏教版2019必修第一册)山东省泰安市东平高级中学2021-2022学年高一上学期期中考试化学试题
名校
7 . 中国科学院官方微信于2017年3月发表《灰霾专题》,提出灰霾中细颗粒物的成因,部分分析如下图所示。

(1)根据上图信息可以看出,下列哪种气体污染物不是 由机动车行驶造成的_______________ 。
a.SO2 b.NOx c.VOCs d. NH3
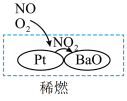
(2)机动车大量行驶是污染源之一。汽车发动机废气稀燃控制系统主要工作原理如图所示;写出稀燃过程中NO发生的主要反应的方程式_______________ 。
(3)科学家经过研究发现中国霾呈中性,其主要原因如下图所示:

请判断A的化学式并说明判断理由:_____________________________________________ 。
(4)煤燃烧排放的烟气含有SO2和NOx,采用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝。将含有SO2和NOx的烟气通入盛有NaClO2溶液的反应器中,反应一段时间后,测得溶液中离子浓度的有关数据如下(其他离子忽略不计):
①SO2和NaClO2溶液反应的离子方程式是________________________________________ 。
②表中y =_______________ 。

(1)根据上图信息可以看出,下列哪种气体污染物
a.SO2 b.NOx c.VOCs d. NH3
(2)机动车大量行驶是污染源之一。汽车发动机废气稀燃控制系统主要工作原理如图所示;写出稀燃过程中NO发生的主要反应的方程式

(3)科学家经过研究发现中国霾呈中性,其主要原因如下图所示:

请判断A的化学式并说明判断理由:
(4)煤燃烧排放的烟气含有SO2和NOx,采用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝。将含有SO2和NOx的烟气通入盛有NaClO2溶液的反应器中,反应一段时间后,测得溶液中离子浓度的有关数据如下(其他离子忽略不计):
| 离子 | Na+ | SO42− | NO3− | H+ | Cl− |
| 浓度/(mol·L−1) | 5.5×10−3 | 8.5×10−4 | y | 2.0×10−4 | 3.4×10−3 |
②表中y =
您最近一年使用:0次
2018-03-13更新
|
226次组卷
|
2卷引用:黑龙江省大庆实验中学2017-2018学年高一下学期开学考试化学试题
名校
解题方法
8 . “绿水青山就是金山银山”。近年来,绿色发展、生态保护成为中国展示给世界的一张新“名片”。
(1)硫酸工业排出的尾气(主要含SO2)有多种处理方式。
①写出用过量氨水吸收尾气的离子方程式:___________________ 。
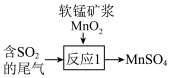
②尾气也可用软锰矿浆(MnO2)吸收,写出如图所示“反应1”的化学方程式:___________________ 。
(2)治理汽车尾气中NO和CO的方法之一是在汽车的排气管上装一个催化转化装置,使NO和CO在催化剂作用下转化为大气成分排出。写出该反应的化学方程式:___________________ 。
(3)某工厂拟综合处理含NH 废水和工业废气(主要含N2、Cl2、NO),设计了如下流程:
废水和工业废气(主要含N2、Cl2、NO),设计了如下流程:
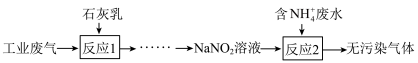
①“反应1”用于吸收Cl2,“反应1”的化学方程式为___________________ 。
② “反应2”的离子方程式为___________________ 。
(1)硫酸工业排出的尾气(主要含SO2)有多种处理方式。
①写出用过量氨水吸收尾气的离子方程式:
②尾气也可用软锰矿浆(MnO2)吸收,写出如图所示“反应1”的化学方程式:

(2)治理汽车尾气中NO和CO的方法之一是在汽车的排气管上装一个催化转化装置,使NO和CO在催化剂作用下转化为大气成分排出。写出该反应的化学方程式:
(3)某工厂拟综合处理含NH
 废水和工业废气(主要含N2、Cl2、NO),设计了如下流程:
废水和工业废气(主要含N2、Cl2、NO),设计了如下流程: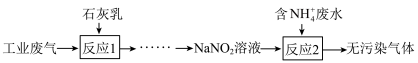
①“反应1”用于吸收Cl2,“反应1”的化学方程式为
② “反应2”的离子方程式为
您最近一年使用:0次
2018-02-25更新
|
969次组卷
|
6卷引用:江苏省如皋市2017-2018学年高一上学期期末考试化学试题
9 . 空气的主要污染物为硫的氧化物和氮的氧化物。研究人员设计了同时净化废气中二氧化硫和氮的氧化物的方法,将其转化为硫酸和硝酸,工艺流程如下:
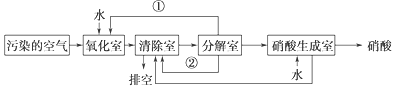
各室中发生的反应如下:
氧化室:NO2+SO2+H2O==H2SO4+NO
清除室:NO+NO2==N2O3、N2O3+2H2SO4==2NOHSO4(固体)+H2O
分解室:4NOHSO4(固体)+O2+2H2O==4H2SO4+4NO2
(1)物质①和②分别为(填化学式)________ 、__________ 。
(2)写出SO2、O2与H2O反应生成H2SO4的化学方程式:_____________________ 。

各室中发生的反应如下:
氧化室:NO2+SO2+H2O==H2SO4+NO
清除室:NO+NO2==N2O3、N2O3+2H2SO4==2NOHSO4(固体)+H2O
分解室:4NOHSO4(固体)+O2+2H2O==4H2SO4+4NO2
(1)物质①和②分别为(填化学式)
(2)写出SO2、O2与H2O反应生成H2SO4的化学方程式:
您最近一年使用:0次
10 . 下列说法正确的是( )
| A.欲使1.6 g氧化铁完全被还原,需要CO的体积为672 mL |
| B.直接加热CuO可以得到Cu单质 |
| C.用磁铁矿炼铁的反应中,1 mol Fe3O4被CO还原成Fe,转移9 mol e- |
| D.工业上用电解法制铝,加入冰晶石是为了使氧化铝熔化的温度降低 |
您最近一年使用:0次



