名校
解题方法
1 . 下列有关反应涉及的离子方程式不正确的是
A.酸性碘化钾溶液中滴加适量双氧水: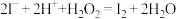 |
B.加入 将污水中的 将污水中的 氧化成 氧化成 : :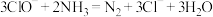 |
C.实验室用 和氨水制取氢氧化铝: 和氨水制取氢氧化铝: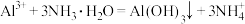 |
D. 溶液与足量 溶液与足量 溶液混合: 溶液混合: |
您最近一年使用:0次
2 .  、
、 、
、 是氧元素的3种核素,其中
是氧元素的3种核素,其中 常用作示踪原子;1mol
常用作示踪原子;1mol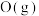 得到电子生成1mol
得到电子生成1mol ,吸收752kJ的热量;钾的含氧化合物有
,吸收752kJ的热量;钾的含氧化合物有 、
、 、
、 等,
等, 和
和 常用于潜水时的供氧剂。常温下,S在潮湿的空气中可以被缓慢氧化成
常用于潜水时的供氧剂。常温下,S在潮湿的空气中可以被缓慢氧化成 ,下列化学反应表示正确的是
,下列化学反应表示正确的是
 、
、 、
、 是氧元素的3种核素,其中
是氧元素的3种核素,其中 常用作示踪原子;1mol
常用作示踪原子;1mol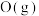 得到电子生成1mol
得到电子生成1mol ,吸收752kJ的热量;钾的含氧化合物有
,吸收752kJ的热量;钾的含氧化合物有 、
、 、
、 等,
等, 和
和 常用于潜水时的供氧剂。常温下,S在潮湿的空气中可以被缓慢氧化成
常用于潜水时的供氧剂。常温下,S在潮湿的空气中可以被缓慢氧化成 ,下列化学反应表示正确的是
,下列化学反应表示正确的是A.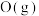 得到电子生成 得到电子生成 : :  |
B. 与水的反应: 与水的反应: |
C.S在潮湿的空气中氧化成 的反应: 的反应: |
D.酸性 溶液与 溶液与 反应: 反应: |
您最近一年使用:0次
名校
3 . SO2直接排放会造成环境污染,可用浓溴水等物质进行回收再利用。单质Se是半导体材料,Se可通过SO2还原H2SeO3获得。K2O2和KO2常用于潜水时的供氧剂。下列化学反应表示正确的是
| A.SO2与溴水反应:SO2+Br2+2H2O=H2SO3+HBr+HBrO |
| B.SO2还原H2SeO3:H2O+2SO2+H2SeO3=Se+2H2SO4 |
| C.KO2与水的反应:KO2+H2O=KOH+O2 |
| D.酸性KMnO4溶液与H218O2反应:2KMnO4+H2l8O2+3H2SO4=K2SO4+MnSO4+318O2↑+4H2O |
您最近一年使用:0次
2024-01-18更新
|
157次组卷
|
2卷引用:江苏省镇江市2023-2024学年高一上学期期末考试化学试题
名校
解题方法
4 . 铋酸钠(NaBiO3)在酸性条件下可将Mn2+氧化成MnO ,在钢铁工业中可用于锰元素的分析测定。NaBiO3的制备过程为:①将试剂级Bi(NO3)3溶解于稀HNO3溶液中,滤去不溶物;②依次加入水和30%的NaOH溶液至溶液呈中性;③再依次加入30%的NaOH溶液和NaClO溶液,加热至95℃并维持1h;④反应结束后,静置冷却,分去上层清液,用水洗涤沉淀至洗涤液中不含Cl-,在80℃下干燥,即得成品。下列说法正确的是
,在钢铁工业中可用于锰元素的分析测定。NaBiO3的制备过程为:①将试剂级Bi(NO3)3溶解于稀HNO3溶液中,滤去不溶物;②依次加入水和30%的NaOH溶液至溶液呈中性;③再依次加入30%的NaOH溶液和NaClO溶液,加热至95℃并维持1h;④反应结束后,静置冷却,分去上层清液,用水洗涤沉淀至洗涤液中不含Cl-,在80℃下干燥,即得成品。下列说法正确的是
 ,在钢铁工业中可用于锰元素的分析测定。NaBiO3的制备过程为:①将试剂级Bi(NO3)3溶解于稀HNO3溶液中,滤去不溶物;②依次加入水和30%的NaOH溶液至溶液呈中性;③再依次加入30%的NaOH溶液和NaClO溶液,加热至95℃并维持1h;④反应结束后,静置冷却,分去上层清液,用水洗涤沉淀至洗涤液中不含Cl-,在80℃下干燥,即得成品。下列说法正确的是
,在钢铁工业中可用于锰元素的分析测定。NaBiO3的制备过程为:①将试剂级Bi(NO3)3溶解于稀HNO3溶液中,滤去不溶物;②依次加入水和30%的NaOH溶液至溶液呈中性;③再依次加入30%的NaOH溶液和NaClO溶液,加热至95℃并维持1h;④反应结束后,静置冷却,分去上层清液,用水洗涤沉淀至洗涤液中不含Cl-,在80℃下干燥,即得成品。下列说法正确的是| A.常温下,NaBiO3和Bi(NO3)3均可溶于水 |
B.制备NaBiO3的化学方程式为Bi(NO3)3+4NaOH+NaClO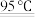 NaBiO3↓+NaCl+3NaNO3+2H2O NaBiO3↓+NaCl+3NaNO3+2H2O |
| C.将Bi(NO3)3溶解于稀HNO3溶液中的目的是增强酸性 |
| D.用NaBiO3分析测定锰元素的过程中,NaBiO3发生氧化反应 |
您最近一年使用:0次
2023-08-15更新
|
469次组卷
|
3卷引用:河北省保定市定州中学2023届高三下学期模拟考试化学试题
5 . 根据表中信息,判断下列叙述中正确的是
| 序号 | 氧化剂 | 还原剂 | 其他反应物 | 氧化产物 | 还原产物 |
| ① | Cl2 | FeBr2 | / | Cl- | |
| ② | KClO3 | 浓盐酸 | / | Cl2 | |
| ③ | KMnO4 | H2O2 | H2SO4 | O2 | Mn2+ |
| A.表中①组的反应只可能有一种元素被氧化和一种元素被还原 |
| B.氧化性强弱的比较: KClO3>Fe3+>Cl2>Br2 |
| C.由表中①②组反应推测:ClO3-、Br-、H+、Fe2+不能在浓溶液中大量共存 |
| D.表中③组反应的离子方程式为:2MnO4-+ 3H2O2+ 6H+=2Mn2++ 4O2↑+ 6H2O |
您最近一年使用:0次
解题方法
6 . 下列反应的离子方程式,能正确表示化学反应的是
A. 能使溴水褪色: 能使溴水褪色: |
B.向 溶液中滴加过量氨水: 溶液中滴加过量氨水: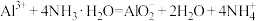 |
C. 溶于HI溶液: 溶于HI溶液: |
D.乙醇被酸性 溶液氧化成乙酸: 溶液氧化成乙酸: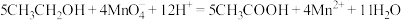 |
您最近一年使用:0次
7 . 习近平总书记视察赣州时强调,稀土是重要的战略资源,也是不可再生资源。钪(Sc)是一种稀土金属,从钛白酸性废水(主要含有 、
、 ,还含有微量
,还含有微量 )中富集钪,并制备氧化钪(
)中富集钪,并制备氧化钪( )的工艺流程如图所示[已知:
)的工艺流程如图所示[已知: 、
、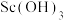 均难溶于水]。下列说法错误的是
均难溶于水]。下列说法错误的是

 、
、 ,还含有微量
,还含有微量 )中富集钪,并制备氧化钪(
)中富集钪,并制备氧化钪( )的工艺流程如图所示[已知:
)的工艺流程如图所示[已知: 、
、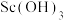 均难溶于水]。下列说法错误的是
均难溶于水]。下列说法错误的是
A.酸洗时加入 的目的是将 的目的是将 氧化为 氧化为 |
| B.实验室进行“操作Ⅰ”需要的玻璃仪器有烧杯、玻璃棒、漏斗 |
C.“滤渣Ⅰ”的成分是 、 、 |
D.草酸钪焙烧时反应的化学方程式: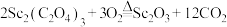 |
您最近一年使用:0次
解题方法
8 . 宏观辨识与微观探析是化学学科核心素养之一。下列事实与对应离子方程式均正确的是
| 选项 | 事实 | 离子方程式 |
| A | 用酸性高锰酸钾溶液滴定草酸 | 2MnO +6H++5H2C2O4=2Mn2++10CO2↑+8H2O +6H++5H2C2O4=2Mn2++10CO2↑+8H2O |
| B | H2SO3酸性强于HClO | SO2+H2O+2ClO-=2HClO+SO |
| C | 铁盐净水 | Fe3++3H2O=Fe(OH)3↓+3H+ |
| D | Na2O2与H2O反应,可用作供氧剂 | Na2O2+H2O=2Na++2OH-+O2↑ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2014·河北唐山·一模
名校
9 . 根据表中信息判断,下列选项正确的是
| 序号 | 反应物 | 产物 |
| ① | KMnO4,H2O2,H2SO4 | K2SO4、MnSO4……… |
| ② | Cl2、FeBr2 | FeCl3、FeBr3 |
| ③ | MnO4-………… | Cl2、Mn2+ |
| A.第①组反应的其余产物为H2O |
| B.第②组反应中Cl2与FeBr2的物质的量之比小于或等于1 : 2 |
| C.第③组反应中生成1 mol Cl2,转移电子5 mol |
| D.氧化性由强到弱的顺序为MnO4->Cl2>Fe3+>Br2 |
您最近一年使用:0次
2014-04-02更新
|
1191次组卷
|
7卷引用:2014届河北省唐山市高三第一次模拟考试理综化学试卷
10 . 某酸性工业废水中含有K2Cr2O7.光照下,草酸(H2C2O4)能将其中的Cr2O 转化为Cr3+。某课题组研究发现,少量铁明矾[Al2Fe(SO4)4·24H2O]即可对该反应起催化作用。为进一步研究有关因素对该反应速率的影响,探究如下:在25°C下,控制光照强度、废水样品初始浓度和催化剂用量相同,调节不同的初始pH和一定浓度草酸溶液用量,作对比实验,完成以下实验设计表。
转化为Cr3+。某课题组研究发现,少量铁明矾[Al2Fe(SO4)4·24H2O]即可对该反应起催化作用。为进一步研究有关因素对该反应速率的影响,探究如下:在25°C下,控制光照强度、废水样品初始浓度和催化剂用量相同,调节不同的初始pH和一定浓度草酸溶液用量,作对比实验,完成以下实验设计表。
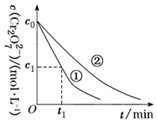
测得实验①和②溶液中的Cr2O 浓度随时间变化关系如图所示。下列叙述
浓度随时间变化关系如图所示。下列叙述不正确 的是:
 转化为Cr3+。某课题组研究发现,少量铁明矾[Al2Fe(SO4)4·24H2O]即可对该反应起催化作用。为进一步研究有关因素对该反应速率的影响,探究如下:在25°C下,控制光照强度、废水样品初始浓度和催化剂用量相同,调节不同的初始pH和一定浓度草酸溶液用量,作对比实验,完成以下实验设计表。
转化为Cr3+。某课题组研究发现,少量铁明矾[Al2Fe(SO4)4·24H2O]即可对该反应起催化作用。为进一步研究有关因素对该反应速率的影响,探究如下:在25°C下,控制光照强度、废水样品初始浓度和催化剂用量相同,调节不同的初始pH和一定浓度草酸溶液用量,作对比实验,完成以下实验设计表。
| 实验编号 | 初始pH | 废水样品 体积mL | 草酸溶液 体积mL | 蒸馏水体 积mL |
| ① | 4 | 60 | 10 | 30 |
| ② | 5 | 60 | 10 | 30 |
| ③ | 5 | 60 | a | b |
 浓度随时间变化关系如图所示。下列叙述
浓度随时间变化关系如图所示。下列叙述| A.上述反应后草酸被氧化为CO2 |
| B.实验③中a和b如果是20和20,则反应速率③﹥② |
C.由曲线①可知,0~t1时间段反应速率v(Cr3+)= mol·L-1·min-1 mol·L-1·min-1 |
| D.实验①和②的结果表明,其他条件相同时,pH越小,该反应速率越快 |
您最近一年使用:0次



