名校
解题方法
1 . 探究亚硝酸钠( NaNO2 )的化学性质,实验如下:
资料: AgNO2是淡黄色难溶于水的固体;由上述实验所得结论不正确的是
| 实验 | 装置 | 试剂a | 现象 |
| ① | 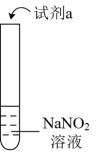 | 酚酞溶液 | 无色溶液变红 |
| ② | AgNO3溶液 | 产生淡黄色沉淀 | |
| ③ | 淀粉KI溶液+稀硫酸 | 无 色溶液立即变蓝 | |
| ④ | 酸性K2Cr2O7溶液 | 无色溶液变为绿色 |
| A.NaNO2溶液显碱性 |
B.NaNO2可与某些盐发生复分解反应: +Ag+= AgNO2↓ +Ag+= AgNO2↓ |
C.NaNO2有氧化性: 2I- +2H++2 =I2+2NO2 ↑+H2O =I2+2NO2 ↑+H2O |
D.NaNO2有还原性: +3 +3 +8H+=3 +8H+=3 +2Cr3++4H2O +2Cr3++4H2O |
您最近半年使用:0次
2022-05-25更新
|
325次组卷
|
6卷引用:北京市北京中国人民大学附属中学2022届高三10月检测化学试卷
2 . 向2 mL 1 mol/L淀粉KI溶液中通入SO2再加入1 mL 1mol/L盐酸,溶液迅速变黄,塞紧胶塞静置一段时间,溶液变成乳黄色。
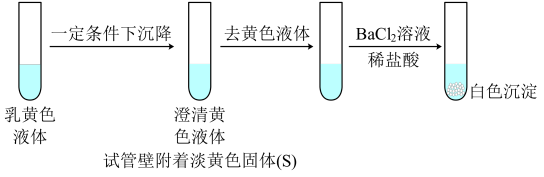
下列说法中不正确 的是
资料:SO2+4I-+4H+=S↓+2I2+2H2O

下列说法中
资料:SO2+4I-+4H+=S↓+2I2+2H2O
| A.整个反应过程中,KI可能起到了催化剂的作用 |
| B.该反应能够证明SO2既有氧化性又有还原性。 |
| C.改变c(H+)对反应速率没有影响 |
| D.结合实验现象可以证明SO2与I-的反应速率小于SO2与I2的反应 |
您最近半年使用:0次
2021-04-04更新
|
242次组卷
|
3卷引用:北京市丰台区2021届高三一模化学试题
名校
3 . 已知HNO2在低温下较稳定,是比醋酸略强的弱酸,既有氧化性又有还原性,其氧化产物、还原产物与溶液pH的关系如表。下列有关说法错误的是
| pH范围 | >7 | <7 |
| 产物 |  | NO、N2O、N2中的一种 |
A.碱性条件下,NaNO2与NaClO反应的离子方程式为NO +ClO-=NO +ClO-=NO +Cl- +Cl- |
| B.向冷的NaNO2溶液中加入滴有淀粉的氢碘酸(HI溶液),溶液变蓝色 |
| C.低温时不用其它试剂即可区分HNO2溶液与Na2CO3溶液 |
| D.HNO2可以利用强酸制弱酸原理,通过加热NaNO2溶液与H2SO4溶液混合溶液制得 |
您最近半年使用:0次
4 . 已知HNO2在低温下较稳定,酸性比醋酸略强,既有还原性又有氧化性,其氧化产物、还原产物与溶液pH的关系如下表。下列有关说法错误的是
| pH范围 | >7 | <7 |
| 产物 |  | NO、N2O、N2中的一种 |
A.碱性条件下,NaNO2与NaClO反应的离子方程式为 + ClO- = + ClO- = +Cl- +Cl- |
| B.向冷的NaNO2溶液中加入滴有淀粉的氢碘酸,若溶液变蓝色,则证明氧化性:HNO2>I2 |
| C.向冷的NaNO2溶液中通入SO2最终可得到HNO2 |
| D.低温时不用其他试剂即可区分HNO2溶液与Na2CO3溶液 |
您最近半年使用:0次
2022-01-22更新
|
132次组卷
|
2卷引用: 山西省太原市2021-2022学年高三上学期期末考试化学试题
名校
解题方法
5 . 已知 在低温下较稳定,酸性比醋酸略强,既有氧化性又有还原性,其氧化产物、还原产物与溶液pH的关系如下表。下列有关说法错误的是
在低温下较稳定,酸性比醋酸略强,既有氧化性又有还原性,其氧化产物、还原产物与溶液pH的关系如下表。下列有关说法错误的是
 在低温下较稳定,酸性比醋酸略强,既有氧化性又有还原性,其氧化产物、还原产物与溶液pH的关系如下表。下列有关说法错误的是
在低温下较稳定,酸性比醋酸略强,既有氧化性又有还原性,其氧化产物、还原产物与溶液pH的关系如下表。下列有关说法错误的是| pH范围 | >7 | <7 |
| 产物 |  | NO、 、 、 中的一种 中的一种 |
A.碱性条件下, 与NaClO反应的离子方程式为 与NaClO反应的离子方程式为 |
B.向冷的 溶液中加入滴有淀粉的氢碘酸,溶液变蓝色 溶液中加入滴有淀粉的氢碘酸,溶液变蓝色 |
C.向冷的 溶液中通入 溶液中通入 可得到 可得到 |
D.低温时不用其它试剂即可区分 溶液与 溶液与 溶液 溶液 |
您最近半年使用:0次
2021-10-28更新
|
84次组卷
|
8卷引用:河北省石家庄二中2018届高三上学期期中考试化学试题
名校
解题方法
6 . 利用下列实验探究亚硝酸钠(NaNO2)的化学性质(AgNO2是淡黄色近白色难溶于水的固体),对现象的描述或解释有错误的是
| 实验 | 装置 | 试剂a | 现象 |
| ① | 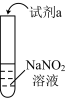 | 酚酞 | 无色溶液变红 |
| ② | AgNO3溶液 | 产生淡黄色近白色沉淀 | |
| ③ | 淀粉KI 溶液+稀硫酸 | 无色溶液立即变蓝 | |
| ④ | 酸性K2Cr2O7溶液 | 溶液变为绿色 |
A.NaNO2溶液呈碱性:NO +H2O ⇌HNO2+OH- +H2O ⇌HNO2+OH- |
B.NaNO2可与某些盐发生复分解反应:NO +Ag+=AgNO2↓ +Ag+=AgNO2↓ |
C.NaNO2具有氧化性:2I-+2H++2NO =I2+2NO2↑+H2O =I2+2NO2↑+H2O |
D.NaNO2具有还原性:Cr2O +3NO +3NO +8H+=3NO +8H+=3NO +2Cr3++4H2O +2Cr3++4H2O |
您最近半年使用:0次
2021-01-12更新
|
574次组卷
|
12卷引用:2020届高三化学海淀区高三第一学期期中练习
2020届高三化学海淀区高三第一学期期中练习北京市海淀区2019-2020学年高三期中考试化学试题重庆南开中学高2020届高三11月月考理综化学试题山西省长治市第二中学2019-2020学年高二上学期12月月考化学试题(已下线)考点24 元素与理论综合——《备战2020年高考精选考点专项突破题集》重庆市南开中学2020届高三年级网课学习能力自测理科综合化学试题浙江省诸暨市2019-2020学年高二上学期期末考试化学试题天津市第四十七中学2020~2021学年高三模拟考试化学试题四川省成都市第七中学2023届高三上学期零诊模拟考试化学试题北京师范大学附属中学2023-2024学年高三上学期10月月考化学试题北京市中国人民大学附属中学2023-2024学年高三上学期期中考试前练习化学试题天津北京师范大学静海附属学校 (天津市静海区北师大实验学校)2023-2024学年高三上学期第二次阶段检测(期中)化学试题
名校
7 . 几种离子在水溶液(溶液酸碱性可调节)中有如下转化关系。下列说法正确的是
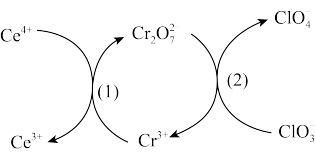

A.氧化性: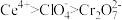 |
B.反应(1)生成 转移3mol电子 转移3mol电子 |
C.将反应(2)设计成原电池, 一定向负极迁移 一定向负极迁移 |
D.由图推知可以发生反应: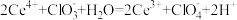 |
您最近半年使用:0次
名校
解题方法
8 . 高铜酸钾(KCuO2)是一种难溶于水的黑色粉末状固体,与高铁酸钾(K2FeO4)性质相似,可以由四羟基合铜酸钾和次溴酸在冰水浴中合成:①K2[Cu(OH)4]+HBrO→KCuO2+KBr+KBrO+H2O(未配平)。高铜酸钾在酸性条件下不稳定:②KCuO2+H2SO4→O2↑+CuSO4+H2O+K2SO4(未配平)。下列说法错误的是
| A.①中参与反应的还原剂和氧化剂的物质的量之比为1∶2 |
| B.②若有8gO2生成,则转移电子的物质的量为1mol |
| C.②中KCuO2既表现氧化性,又表现还原性 |
| D.由①、②可知氧化性强弱顺序为HBrO>KCuO2>O2 |
您最近半年使用:0次
2023-11-07更新
|
92次组卷
|
2卷引用:甘肃省兰州第一中学2023-2024学年高一上学期11月期中考试化学试题
名校
9 . 高铜酸钾(KCuO2)是一种难溶于水的黑色粉末状固体(其中氧元素的化合价为-2价),与高铁酸钾(K2FeO4)性质相似,可以由四羟基合铜酸钾和次溴酸在冰水浴中合成:①K2[Cu(OH)4]+HBrO→KCuO2+KBr+KBrO+H2O(未配平)。高铜酸钾在酸性条件下不稳定:②KCuO2+H2SO4→O2↑+CuSO4+H2O+K2SO4(未配平)。下列说法错误的是
| A.①中还原剂和氧化剂的数量之比为2:1 |
| B.②若有32gO2生成,则生成72gH2O |
| C.②中KCuO2既表现氧化性,又表现还原性 |
| D.由①、②可知氧化性强弱顺序为HBrO>KCuO2>O2 |
您最近半年使用:0次
名校
解题方法
10 . 已知 Co2O3、Cl2、FeCl3和 I2的氧化性依次减弱。在酸性溶液中,Co2O3发生氧化还原反应时其还原产物为
 下列说法正确的是
下列说法正确的是

 下列说法正确的是
下列说法正确的是| A.酸性溶液中Co2O3与KI发生反应时,氧化产物与还原产物的物质的量之比为2∶1 |
B.向 FeCl3溶液中滴加 KI溶液,可发生反应: |
| C.Co2O3与浓盐酸反应时,HCl只 体现还原性 |
| D.向酸性FeCl2溶液中加入足量Co₂O₃,仅Cl⁻被氧化 |
您最近半年使用:0次
2023-11-17更新
|
266次组卷
|
2卷引用:河南省八市2023~2024学年高一上学期期中学业质量检测化学试题



